消化道磁懸浮膠囊機器人模型及控制系統
鄭齊,馮久奎
1 福州大學至誠學院 (福建福州 350002);2 福州大學物理與信息工程學院 (福建福州350108); 3 銳捷網絡股份有限公司 (福建福州 350002)
目前我國慢性消化系統疾病發病率為24.9%,其中消化道腫瘤是高發病種。《柳葉刀》上的報告顯示2010—2014年中、日、韓3國胃癌患者5年生存率分別為35.9%、60.3%、68.9%,我國胃癌患者5年生存率遠低于周邊國家。消化系統疾病的篩查工作不便開展,其主要因素是傳統插管式胃鏡檢查讓患者痛苦不堪。膠囊內窺鏡可大幅度減少消化道檢查引起的不適感,但普通膠囊內窺鏡不適用于胃部檢查,漏檢率較高。本研究設計的磁懸浮微型機器人定點釋藥導航系統適用于胃部、小腸等消化道疾病的檢查及治療。
1 研究現狀
2000年在美國加利福尼亞圣地亞哥的消化疾病周會議上,來自以色列的Given Imaging公司,宣布研制了世界上第一個無創可吞咽膠囊式腸鏡拍攝檢查系統“M2A”[1],可實現小腸 “無痛”檢查。但是胃腸道梗阻患者使用該膠囊內窺鏡時存在膠囊滯留現象。膠囊滯留是指膠囊在胃腸道內滯留時間長達2周以上[2],小腸膠囊內窺鏡的滯留率為1.4%~2.6%[3]。因此Given Imaging公司開發了一種能夠自我分解的膠囊AgileTM Patency System用于小腸檢測[4]。2004年重慶金山科技集團開發出國內第一款小腸膠囊內窺鏡“OMOM”,并于2005年3月獲得原國家食品藥品監督管理局頒發的醫療器械注冊證。2006年日本奧林巴斯公司發布了一款小腸膠囊內窺鏡,具有0~20 mm的景深和自動照明亮度控制功能,可持續工作8 h,每秒可實時發送2張圖像到體外采集器上。SmartPill公司推出一款可檢測pH、溫度和壓力的膠囊內窺鏡,并于2006年獲得美國食品藥品管理局(U.S. Food and Drug Administration,FDA)批準上市。2009年杭州華沖科技有限公司在國家“863計劃”的支持下,用自主知識產權專用芯片開發出膠囊內窺鏡,并于2011年獲得原國家食品藥品監督管理局頒發的醫療器械注冊證。圖1為目前市場常見的幾種膠囊內窺鏡,主要分為可控和不可控兩大類。膠囊內窺鏡可一次拍攝幾萬張消化道照片,醫師需花費大量時間仔細對比,查找可疑病灶圖像,嚴重影響工作效率,導致檢查的時間成本增加,且與傳統軟管式胃腸鏡對比,膠囊內窺鏡無法進行活檢取樣等操作。

圖1 市場常見的幾種膠囊內窺鏡
當前,膠囊內窺鏡的智能驅動已經成為一個熱門研究課題。2003年日本東北大學Sendoh和Ishiyama[5]提出一種類似三軸亥姆霍茲線圈提供旋轉空間磁場,使膠囊能夠旋轉起來,依靠膠囊表面設計的螺旋紋結構推動旋進。2004年奧林巴斯公司提出由3對電磁鐵構建一個均勻的電磁場驅動膠囊內窺鏡旋轉,借助外表面螺紋結構,實現膠囊的前進后退,同時內置了無線能量傳輸技術[6]。日本長野縣RF SYSTEM實驗室的Norika團隊提出一款具有無線充電、活檢采樣倉、定點釋藥倉、無線圖像傳輸、可變波長發光二極管(LED)等技術的磁控膠囊,外部3個方向的磁場變化可帶動膠囊做類似電機內轉子的旋轉運動,實現膠囊的旋轉運動[7],目前該方案僅是構想,未實現商業化。2010年Gao等[8]設計、構造了一種多自由度磁場驅動膠囊內窺鏡推進系統,采用一個永磁鐵柱狀外殼包覆膠囊表面,通過兩組釹鐵硼永磁鐵提供的磁場驅動膠囊內窺鏡,每組包含1個矩形和1個圓柱形永磁鐵,應用有限元方法仿真磁場分布和力學特性,并通過試驗模擬膠囊在腸道內運動,表明了該方法的可行性。安翰科技(武漢)股份有限公司開發出一款Navicam磁控膠囊胃鏡檢查系統,可通過控制C型機械臂實現膠囊旋轉、翻轉[9-10],并于2013年獲得原國家食品藥品監督管理總局三類醫療器械注冊證。2015年徐建省等[11]采用電機帶動螺旋槳的驅動方式,由外部3對亥姆霍茲線圈產生指定大小和方向的導向磁場,實現了對膠囊運動方向的控制。趙振亮等[12]于2018年提出一種采用復合磁場的閉環主動控制方法,將霍爾傳感器放置于膠囊內部,通過無線通信方式,將膠囊內部磁場傳感器測量到的信號發送給外部控制設備,進而調節磁場,實現閉環控制。上述國內外研究成果推動了膠囊內窺鏡的發展,并為該領域研究提供了重要的借鑒和指導。然而這些驅動方式還存在著控制精確度差、空間狀態鎖定及無法實施活檢取樣等方面的不足。
2 膠囊磁懸浮系統設計
2.1 膠囊設計
目前的膠囊內窺鏡普遍存在以下不足:(1)操控精度較低;(2)續航受限;(3)功能單一;(4)無法定點釋藥和活檢取樣等。
為解決以上問題,現提出一款上推式磁懸浮膠囊機器人,其內部結構如圖2所示。該膠囊由具有生物相容性的透明有機材料制成,膠囊內部主要由攝像頭、可調波長照明LED、超級電容、無線電發射電路、活檢取樣裝置、藥倉、永磁體、無線供電線圈等組成。永磁體設計成類半球體形狀,使整個膠囊的重心靠近膠囊垂直方向的底部,受重力作用,膠囊在沒有其他外力作用下可保持豎立狀態。
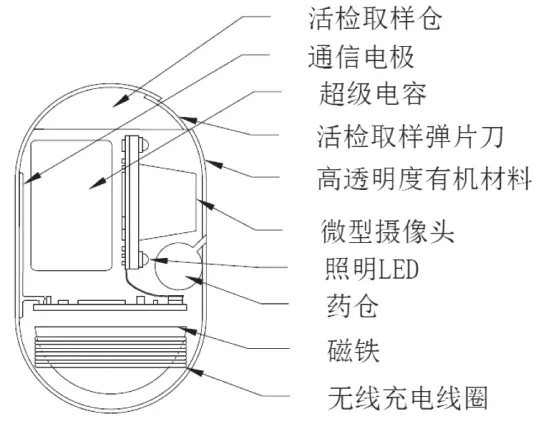
圖2 上推式磁懸浮膠囊機器人內部結構
底部安裝無線充電感應線圈,用于接收來自懸浮底座的無線能量傳輸,整流穩壓后存儲于膠囊內的超級電容,供攝像頭、LED、給藥器、取樣裝置、無線圖傳電路等使用;永磁鐵采用釹鐵硼永磁材料,置于重心位置,外形經過設計可產生特定的磁場配合上推電磁鐵,同時鎖定永磁鐵的空間位置,使其保持固定,保證攝像清晰、穩定;藥倉采用電控微閥門設計,內部氣壓高于外界,當微閥門打開時內部的藥劑便會噴射、粘附于患處;照明采用可調節波長的發光二極管,以擴展檢測范圍,提高病變檢出率;通信電極由兩片環繞膠囊的金屬環構成,用于數據通信傳輸及體內電刺激治療;活檢取樣裝置采取電控微彈片刀結構,當外界發送控制信號時,緊貼患病部位的微彈片瞬間切取小塊病變組織,并收入活檢取樣倉。
2.2 檢測平臺設計
檢測平臺如圖3、4所示。磁懸浮底座安裝在平臺底部的機械臂上,平臺呈弧形結構貼合人體,縮短磁懸浮控制底座與體內膠囊的距離。該平臺通過中間的支撐軸可實現水平方向旋轉和垂直方向位移,同時還可實現前后滑動,用于調節膠囊在人體內的縱向位置。磁懸浮控制底座在多軸機械臂的控制下可進行平移和多角度旋轉運動,配合平臺的簡單平行運動可實現體內膠囊不同空間狀態的控制,并可采集消化道內各視角的圖像,任意調節膠囊的角度和距離,均可保證圖像的清晰度。
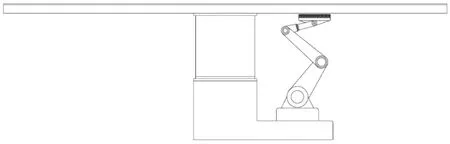
圖3 平臺正視圖
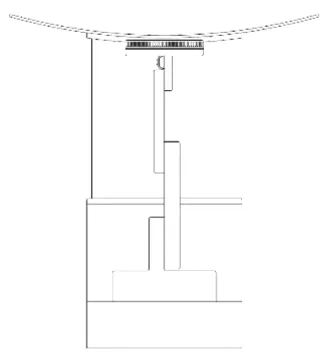
圖4 平臺左視圖
2.3 磁懸浮控制底座設計
磁懸浮控制底座內部結構如圖5所示。中間安裝1個高精度三維磁敏霍爾傳感器,霍爾傳感器采用基準恒流源提供偏置電流。在膠囊內永磁鐵的磁場作用下,霍爾傳感器輸出端產生微弱的電勢,經放大器放大后送至AD采樣電路,高精度傳感器產生的電勢轉換為對應的磁感應強度,從而可判斷膠囊的實時相對位置。霍爾傳感器的8個方向上各安裝1個電磁鐵,可根據膠囊實時位置調節電磁鐵中的電流,控制電磁鐵產生的磁場,推動膠囊懸浮在目標位置。
膠囊的磁懸浮控制系統是一個不穩定的非線性系統,線性化擬合數學模型的建立較為困難,因此采用PID算法,聯合python語言編寫的神經網絡算法進行PID參數整定,通過霍爾傳感器檢測信號換算成位置信息,實現閉環控制,具有較強的魯棒性和良好的動靜態性能。磁懸浮控制底座的結構設計保證了膠囊受力平衡、懸浮穩定。磁懸浮控制底座安裝于機械臂上,機械臂由連接計算機的操縱搖桿進行控制,可實現磁懸浮控制底座的移動和旋轉。
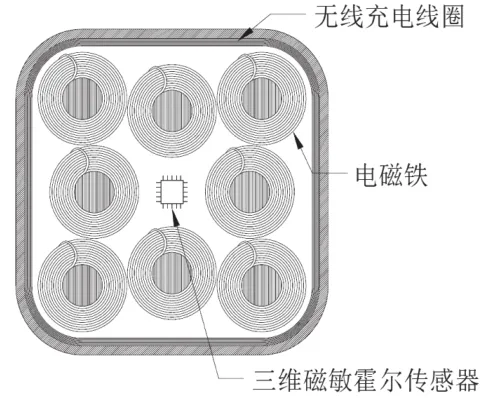
圖5 磁懸浮控制底座內部結構
2.4 磁懸浮控制流程
膠囊磁懸浮控制流程如圖6所示。膠囊與磁懸浮控制底座的相對位置及空間狀態由計算機設置、鎖定;膠囊相對人體的傾斜角度由機械臂旋轉進行控制;膠囊與磁懸浮控制底座的距離微調可通過調節電磁鐵的電流實現。
當膠囊進入人體內時,緩慢移動磁懸浮底座,實時監測霍爾傳感器采集到的電壓信號,確定膠囊在體內的空間位置及狀態。由于膠囊內部的重心設計,在有足夠空間的器官內,膠囊受重力作用始終處于豎直狀態;通過觀察膠囊傳送回的圖像,可確認膠囊的位置;計算機自動運算并輸出控制信號到功率放大器,以控制電磁鐵校準膠囊空間位置至平衡狀態。
操作搖桿時,計算機通過計算搖桿的輸入信號判斷水平、垂直方向的位移量,進而控制平臺可進行相應的水平移動、垂直升降;當需要膠囊傾斜旋轉時,平臺下方的機械臂根據計算機計算結果,可進行相應角度的傾斜、旋轉。
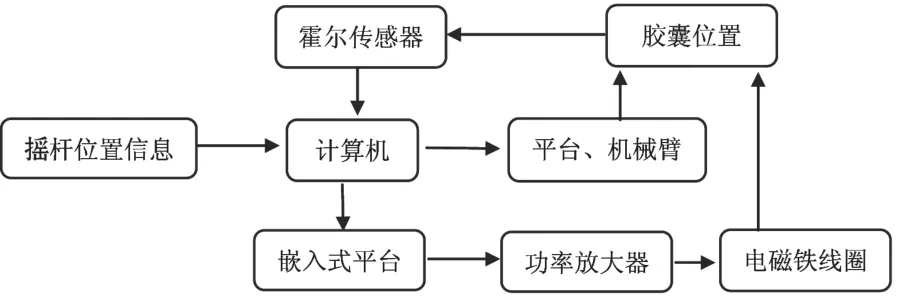
圖6 膠囊磁懸浮控制流程
3 結語
目前膠囊機器人的能耗、精確控制成為其功能拓展的瓶頸。更低的能耗可帶來更多的功能,同時可節省電池占用空間,增加更多的裝置。例如提高CMOS相機的像素以及拍攝的幀率,清晰的圖像有利于醫師快速定位和后期圖像的人工智能篩檢、分析;改進為可變波長的LED照明裝置,可用于特殊檢查;增加膠囊體內精確定位裝置;設計活檢取樣裝置進行病變部位樣本采集;增加釋藥倉用于體內定點釋藥等。本系統可解決能耗及精確運動控制問題,相信在不久的將來,這款多功能膠囊機器人的普及可以讓廣大患者更加舒適地體檢,并可應用于臨床體內微創治療等。

