康柏西普輔助玻璃體切除聯合人工晶體植入手術與序貫手術治療增殖性糖尿病視網膜病變對比研究
儲昭節,王 彤,潘小燕,尹 妮,范晶晶
西安市第一醫院眼科(西安市眼科醫院·陜西省眼科研究所)(西安710002)
增殖性糖尿病視網膜病變(Proliferative diabetic retinopathy,PDR)是一種嚴重的致盲性眼病。常表現為玻璃體積血,玻璃體視網膜增殖,牽拉性視網膜脫離等[1-2]。流行病學研究發現糖尿病患者白內障發病提前,白內障加重[3]。
睫狀體平坦部玻璃體切除術(Pars plana vitrectomy ,PPV)是治療PDR常見的手術方式。由于PDR患者常并發不同程度的白內障,玻璃體切除術也可加速白內障的形成[4],術者的手術設計需考慮行PPV聯合白內障超乳人工晶體植入或行單純玻璃體切除術,后續行白內障手術。但兩種手術選擇仍存在爭論,國內外研究也有不一致的報道。
抗血管內皮生長因子(Vascular endothelial growth factor,VEGF)藥物已廣泛應用于PDR患者,可明顯縮短玻璃體切除手術時間以及減少手術并發癥[5]。本研究回顧分析康柏西普輔助下玻切聯合白內障手術與序貫手術治療PDR的臨床資料,對比治療效果和并發癥情況。
對象和方法
1 研究對象 本研究為回顧性病例研究。2017年3月至2018年6月就診于西安市第一醫院眼科診斷為PDR的患者共48例56眼納入本研究。疾病診斷標準依據我國1984年DR分期,手術前眼底不清患者以手術中所見為準。所有患者均合并不同程度的白內障,晶狀體核硬度(按照Emery硬度分級標準)均為 Ⅱ~Ⅲ級核。Ⅳ級核及以上排除。排除外傷性白內障,葡萄膜炎并發白內障等,排除糖尿病視網膜病變以外的眼底病變繼發的玻璃體積血、牽拉性視網膜脫離等。所有患者術前1周行玻璃體注射康柏西普注射液0.05 ml。其中28例32眼行玻璃體切除聯合白內障超聲乳化人工晶狀體(IOL)植入術,稱A組;其中20例24眼行1期玻璃體切除術,2期行白內障超聲乳化IOL植入,或聯合硅油取出,稱B組。兩組患者的臨床資料(表1),年齡、糖尿病病程、糖尿病視網膜病變分期及晶狀體核硬化程度比較,差異無統計學意義(P>0.05)。本研究經醫院倫理委員會批準,患者均簽署知情同意書。
2 術前準備及手術
2.1 術前準備:眼部檢查:患者術前常規行裂隙燈、眼底檢查,眼部B超,A超(或IOLmaster),角膜內皮,眼底照相,驗光檢查,部分患者行FFA檢查。術前行常規心電圖,血壓,血糖,肝腎功,出凝血檢查。排除嚴重影響手術的全身疾病。術前控制血糖、血壓。
2.2 手術方法:所有患者術前一周行玻璃體腔注射康柏西普注射液,注射嚴格按內眼手術準備,常規消毒后上方角膜緣后4 mm,注入康柏西普0.05 ml。

表1兩組患者的臨床資料比較
A組:玻璃體切除術聯合白內障超聲乳化:采取23G微創玻璃體切除術,設備為:Alcon Constallation玻切超乳一體機,非接觸眼底廣角成像系統。常規局部麻醉,聚維酮碘結膜囊消毒后,11:00位3.2 ml透明角膜切口,3:00位輔助側切口,前房粘彈劑填充后行連續環形撕囊,囊環直徑約5 mm,水分離、水分層,轉核,囊袋內超聲乳化吸出晶狀體核,I/A抽吸晶狀體皮質。睫狀體平坦部穿刺行標準三通道玻璃體切除,助手頂壓徹底清除周邊基底部玻璃體,小心分離、剝離或切除增殖膜,升高灌注壓或電凝輔助止血。全視網膜光凝。部分患者行重水置換,氣液交換、玻璃體腔硅油填充,7-0可吸收線縫合鞏膜切口。玻璃體手術完成后行人工晶狀體植入,根據病情術后3~6個月行硅油取出。B組:玻璃體切除方法同A組。部分患者為水眼,術后3~6個月行白內障超聲乳化,植入人工晶狀體,術中采取后節輔助。部分患者為硅油眼行白內障超聲乳化人工晶體植入聯合硅油取出。白內障超聲乳化同前,睫狀體平坦部穿刺,建立灌注和硅油抽吸通道。徹底清除玻璃體腔硅油,檢查視網膜后縫合鞏膜切口。
2.3 術后處理及隨訪:術后常規抗生素眼液、非甾體抗炎眼液、激素類眼液局部用藥4~6周,部分患者使用睫狀體麻痹劑防止瞳孔粘連。術后隨訪時間為6~9個月。定期記錄最佳矯正視力,眼壓,并發癥情況等。術后根據病情行熒光素眼底血管造影(FFA)檢查,視網膜光凝或抗VEGF治療。最佳矯正視力(BCVA)提高大于等于2行表示視力改善。
3 統計學方法 采用SPSS20.0統計學軟件分析數據,計量資料采用t檢驗,計數資料及組間率的比較采用卡方檢驗,P<0.05表示差異有統計學意義。
結 果
1 兩組視力改善情況比較 最后一次隨訪的最佳矯正視力,A組視力改善情況為62.5%(20/32);B組為66.7%(18/24)。
2 兩組術中情況比較 術中所有患者均行視網膜光凝,部分患者根據病情行電凝止血、重水置換、硅油填充或灌注液填充。兩組比較差異無統計學意義(P>0.05),見表2 。
3 術后并發癥 A組前房滲出反應發生率為25%(8/32),B組為0;A組新生血管性青光眼(Neovascular glaucoma,NVG)的發生率為15.6%(5/32),B組為0。兩組比較差異有統計學意義(P>0.05),A組前房滲出反應和NVG的發生較B組高。兩組一過性高眼壓分別為9例和 3例、黃斑水腫7例和 4例、術后再發玻璃體積血3例和 2例,后發性白內障4例和 2例,兩組比較差異無統計學意義(P>0.05)。
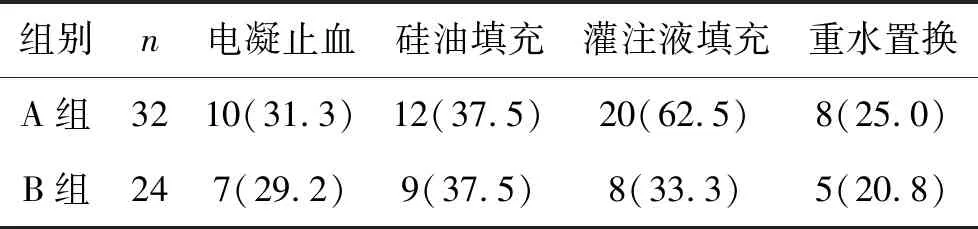
表2兩組術中情況[例(%)]
討 論
PPV是治療PDR的有效手段。PDR患者常并發白內障,且玻切術后白內障可能會加速形成。隨著微創玻璃體視網膜手術和白內障手術設備和技術的不斷提高,國內外不少研究者采取行PPV聯合白內障超乳人工晶體植入,并獲得了良好的治療效果[6-9]。聯合手術的優點有:同期摘除晶狀體,可明顯改善屈光間質,有利于充分處理玻璃體基底部和周邊網膜病變,有利于術中行充分周邊部視網膜光凝;減少了手術次數,減輕患者負擔、降低費用;手術同期植入人工晶狀體有利于快速恢復視力。可能存在的缺點:手術炎癥反應較重,前房滲出反應,NVG的發生率較高。
序貫玻璃體切除術和白內障超聲乳化人工晶狀體植入術也是PDR手術的另一種路徑[9]。可能的優點有:減輕玻璃體手術的炎癥反應和并發癥;有利于術后周邊部視網膜光凝的補充。缺點有:玻璃體切除術后白內障手術難度增加,懸韌帶損傷,后囊破裂,晶狀體核墜入玻璃體腔的風險增加;增加患者負擔。
目前兩種手術路徑各有利弊,仍存在爭論。我國PDR患者病情普遍較重,血糖、血壓控制較差,術后用藥、隨訪依從性較差。相關的研究及手術對比缺乏。康柏西普廣泛應用于PDR患者,研究提示能顯著縮短手術時間,減少術中出血及術后并發癥[10]。本組研究中納入的PDR患者病情普遍較重,均采取康柏西普玻璃體切除術前一周眼內注射; 患者的術后BCVA改善無明顯差異,兩組分別有62.5%、66.7%視力得到改善。說明聯合手術或序貫手術均能有效改善患者的視功能,與文獻報道類似的研究一致[6,9]。
A組的前房炎癥反應較重,術后患者存在虹膜后粘連,可能的原因為A組的手術時間更長,超乳常無紅光反射輔助,Yang的研究也有類似的結果[9]。聯合手術可能影響了血視網膜、血-房水屏障,相關的炎癥因子分泌增加,形成虹膜粘連。但一過性高眼壓發生率兩組無明顯差異。
PDR玻切術后NVG的發生率在2%~18%,本組研究顯示A組為15.6%;B組未發生。目前PDR玻切術后繼發NVG的確切原因尚不清楚,研究報道相關的危險因素有前后聯合手術,術前存在的虹膜、房角新生血管,男性,術后視網膜脫離等[10-13]。 A組的NVG的發生較多,可能的原因有手術造成的VEGF等因子的生成增加,促進新生血管生成。既往有研究發現術后存在NVG或玻璃體出血的眼內VEGF水平明顯升高[14]。序貫手術炎癥反應輕,可能會減少VEGF以及其他炎癥因子的釋放。 筆者認為術后視網膜激光補充不足,患者全身情況等也可能造成NVG的發生。另外,部分研究提示術前抗VEGF治療可能減少NVG的發生。但本組患者仍較多發生NVG,NVG的相關危險因素仍待進一步研究。
兩組患者術中使用電凝、激光、重水置換、硅油填充的比例無明顯差異,分析可能本研究中兩組玻璃體視網膜病變嚴重程度的患者比例相仿,PDR玻切術中,一些嚴重患者繼發牽拉性視網膜脫離、視網膜裂孔等常使用重水置換及硅油填充。
術后并發癥如再次玻璃體出血,兩組分別為9.4 %和8.3%,發生無明顯差異。文獻提示PDR玻切術后玻璃體積血(VH)發生率為10.8%~32.4% ,PDR患者VEGF表達明顯升高,聯合抗VEGF能減少術后VH[15],與本組資料符合。術后黃斑水腫的發生率,以及后發性白內障均無明顯差異。分析原因可能與患者PDR病情相關。
總之,本研究采取康柏西普術前用藥,兩種手術方式均能有效改善患者視力,聯合手術較序貫手術的前房滲出反應和NVG較高。聯合手術可能引起更多的炎癥反應,在實際工作中如何采取手術方式尚需更多大樣本量的病例對照研究。

