伊立替康聯合替莫唑胺治療兒童難治性、復發性髓母細胞瘤療效觀察
劉晶晶,孫艷玲,杜淑旭,李春德,武萬水,孫黎明
(1首都醫科大學附屬北京世紀壇醫院,北京100038;2 首都醫科大學附屬北京天壇醫院)
髓母細胞瘤(MB)是兒童最常見的腦惡性腫瘤,約占兒童中樞神經系統惡性腫瘤的20%[1]。研究[2]結果顯示,MB約占所有后顱窩腫瘤的40%,3歲以下者占兒童MB的25%~30%。MB以手術、放療、化療等綜合治療為主,經綜合治療,其5年總體生存率(OS)已提高至80%以上。難治性MB是指經一線標準化療方案治療2個療程后腫瘤增大25%以上或出現新病灶者;復發性MB是指經綜合治療取得完全緩解1個月后再復發者。武萬水等[3]研究發現,雖然MB的5年OS較高,但對于兒童難治性、復發性MB的治療并不樂觀。本研究采用伊立替康聯合替莫唑胺(IT)治療兒童難治性、復發性MB,療效較好,現報告如下。
1 資料與方法
1.1 臨床資料 選取2015年7月~2017年12月在北京世紀壇醫院兒科住院并使用IT治療的難治性、復發性MB患兒27例,全部患兒經病理組織學檢查確診。納入標準:①患兒入院后均完善相關檢查。血紅蛋白>80 g/L,中性粒細胞計數>1.5×109/L,血小板計數>80×109/L,其余血常規檢查及X線、腹部超聲、常規心電圖、心臟超聲等影像學檢查結果均正常;膽紅素小于正常值的1.5倍,丙氨酸氨基轉移酶小于正常值的2.5倍。②左心室射血分數>50%。③接受過放化療,但化療方案中不包括伊立替康和替莫唑胺。27例患兒中,男22例、女5例,中位發病年齡為7(3~11)歲,其中難治性MB患兒17例、復發性MB患兒10例,腫瘤位于第四腦室者15例、位于小腦蚓部者9例、位于后顱窩者2例、多發占位者1例。國際上常用Change后顱窩MB分期系統對MB患者進行分期:M0期指無腫瘤轉移者,M1期為僅腦脊液中有腫瘤細胞,M2期為僅腦部MRI發現腫瘤轉移灶,M3期為脊髓MRI發現腫瘤轉移灶,M4期為神經系統外發現腫瘤轉移灶。本研究27例患兒中,初診斷時臨床分期M0期5例、M1期8例、M2期3例、M3期11例。本研究獲醫院醫學倫理委員會批準,患兒監護人均簽署知情同意書。
1.2 IT治療方法 伊立替康總量300 mg/m2,靜脈滴注,分2 d完成;替莫唑胺150 mg/(m2·d),口服,連用5 d;每4周為1個化療周期。每2~3個周期復查全腦全脊髓MRI,治療過程中監測患兒的血常規、肝腎功能、心肌酶等指標。患兒用藥后耐受良好,且復查影像學檢查無進展者,方可進行下一周期的治療,否則更換為其他治療方案。所有患兒用藥期間常規應用保肝藥、止吐藥及地塞米松預防藥物過敏,并給予充足的水化治療,未常規使用抗生素。若患兒出現白細胞減少、粒細胞減少或血小板減少時,分別給予相應的集落刺激因子藥物,出現嚴重骨髓抑制時給予輸血治療。
1.3 觀察方法 27例患兒均接受隨訪,隨訪至2018年10月,觀察并記錄患兒的無進展生存期、無進展生存率(PFS)、OS,根據患兒的臨床表現、影像學檢查結果對所有患兒進行療效評價。療效評價標準:MRI檢查結果顯示腫瘤信號完全消失為完全緩解(CR),MRI檢查結果顯示腫瘤病灶減少≥50%為部分緩解(PR),MRI檢查結果顯示腫瘤減小或者增大0~<25%為疾病穩定(SD),MRI檢查結果顯示腫瘤增大≥25%或出現明顯的腫瘤繼發的神經系統后遺癥為疾病進展(PD)[4]。其中CR+PR為化療有效,CR+PR+SD為疾病控制。IT化療時,最常見的不良反應為骨髓抑制(白細胞減少、粒細胞減少、貧血、血小板減少)、消化道反應(腹瀉、嘔吐)、發熱、肝功能損傷等。按美國國家癌癥研究所的不良事件通用術語標準,記錄27例患兒的不良反應及其占比。
2 結果
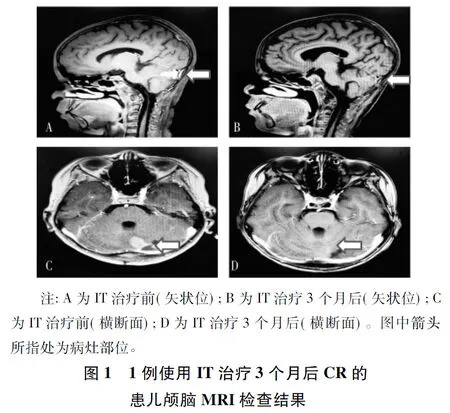
截止到2018年10月,27例患兒共接受IT治療140個周期,平均5.5(1~12)個周期,中位隨訪時間7(3~15)個月。27例患兒中,CR 2例、PR 5例、SD 10例、PD 10例,化療有效率為25.9%,疾病控制率為62.9%。1例患兒因治療過程中出現PD而放棄治療;1例患兒因病情進展迅速,接受2個周期治療后死亡。圖1為1例使用IT治療3個月后CR的患兒前后頭部MRI檢查結果。
截止到2018年10月,27例患兒的中位無進展生存期為6(1~12)個月, 6個月、10個月PFS分別為74%、66.7%,1年、2年OS分別為95%、87%。27例患兒中,腹瀉發生率為29.6%,3~4級骨髓抑制發生率為18.5%(粒細胞減少發生率為14.8%、血小板下降發生率為7.4%)。腹瀉患兒給予膜固思達、易蒙停聯合治療,多數腹瀉患兒于化療停止后5 d內恢復正常,腹瀉發生時無聯合使用抗生素者。大部分出現骨髓抑制的患兒給予對癥處理后逐漸升至正常,2例患兒因化療后出現嚴重骨髓抑制而減量治療。沒有患兒因化療不良反應死亡。
3 討論
目前MB的治療主要包括手術、全腦全脊髓放療、化療等,可使標危患兒的5年OS達70%以上[5]。在過去的20年里,經過對各種治療方法的探索以及新藥的研發、聯合治療的應用等,MB的治療效果及5年OS都在逐漸上升[6]。研究[7]發現,IT治療實體瘤如尤文氏肉瘤、橫紋肌肉瘤以及MB都取得了較好的效果。除此之外,伊立替康和替莫唑胺還沒有重疊的不良反應,伊立替康的不良反應主要為腹瀉,而替莫唑胺的不良反應主要為骨髓抑制。
伊立替康是半合成喜樹堿類衍生物,為拓撲異構酶I(TOPO I)抑制劑,可通過與TOPO-DNA復合物共價形成TOPO-藥物-DNA復合物,阻斷DNA復制,從而誘導腫瘤細胞凋亡。Houghton等[8]研究發現,伊立替康連續給藥5 d,每2周為1個周期,其療效較連續給藥2周更好。已有研究[7]表明,伊立替康50 mg/(m2·d)聯合替莫唑胺150 mg/(m2·d)應用5 d,每3~4周為1個治療周期,在治療神經母細胞瘤中療效較好。
替莫唑胺是一種新型的二代烷化劑,口服后吸收迅速,透過血腦屏障較好,生物利用率高。替莫唑胺主要通過誘導腫瘤細胞凋亡而發揮抗腫瘤活性,但其化療的有效率不足50%。替莫唑胺化療失敗的主要原因是其耐藥性,故替莫唑胺通常選擇與其他藥物聯用,以增強抗腫瘤活性并減少耐藥的發生[9]。替莫唑胺的傳統給藥模式一般為放療同步替莫唑胺化療,自放療第1天起至放療結束,劑量為75 mg/(m2·d),放療結束后再給予6個周期的替莫唑胺輔助化療,劑量為(150~200) mg/(m2·d),第1~5天,28天為1個周期。
本研究納入的27例患兒均為難治性、復發性MB,在應用IT治療方案前,已接受過環磷酰胺、甲氨蝶呤、順鉑、長春新堿等藥物的聯合治療。兒童腫瘤用藥相對局限,在上述藥物治療效果欠佳的情況下可供選擇的治療藥物并不多,可用于兒童并能發揮療效的藥物更少。Casey等[10]研究提示,IT可用于治療兒童復發性或進展性尤文氏肉瘤,且患兒耐受性良好,20例患兒的中位生存時間為8.3個月。Bagatell等[11]研究顯示,IT治療神經母細胞瘤時,其化療有效率為15%,疾病控制率為52.7%,2年PFS和OS分別為13%和30%。本研究結果顯示,IT方案治療難治性、復發性MB的化療有效率為25.9%,疾病控制率為62.9%,中位無進展生存期為6個月。本研究化療有效率和疾病控制率與相關研究結果一致,2年PFS和OS均高于神經母細胞瘤患者,可能與神經母細胞瘤本身預后不佳有關,其10年生存率僅為1.5%~2%[12]。
雖然IT治療效果較好,但其不良反應也不容忽視,常見的不良反應包括:神經認知功能的損害、聽力損傷、內分泌紊亂以及繼發惡性腫瘤[13]。Casey等[10,14]研究結果顯示,在IT治療尤文氏肉瘤時,最常見不良反應為腹瀉、結腸炎和骨髓抑制(包括粒細胞減少和血小板減少)。Bagatell等[11]研究中,IT治療神經母細胞瘤,大部分患者耐受良好,不到6%的患者出現腹瀉;約20%的患者出現中性粒細胞減少,僅有不到10%的粒細胞減少患者出現感染;約15%的患者出現3~4級骨髓抑制;約10%的患者出現低鉀血癥。本研究腹瀉發生率為29.6%,高于相關研究結果,但均為輕中度腹瀉,可能與本研究用藥前未使用頭孢克肟/頭孢泊肟預防有關。本研究骨髓抑制發生率為18.5%,與前述研究相近。聽力損傷、內分泌紊亂、繼發腫瘤等不良反應未觀察到,可能與病例數較少有關。
綜上,IT治療兒童難治性、復發性MB表現出較理想的治療反應和順應性,少有嚴重不良反應事件發生,可作為兒童難治性或復發性MB的治療方案之一。但由于本研究樣本量不足,隨訪時間尚短,故暫時無法觀測其對患兒長時間OS的有效性,需要更大的樣本量及更長的隨訪時間,以進一步明確該聯合方案的遠期療效。

