電場增強錳摻雜硫化鋅量子點室溫磷光的肝素鈉多糖檢測
鄧茗月,葉翆紅,鄒文生,李衛華
(1.安徽建筑大學 環境與能源工程學院,安徽 合肥 230601;2.安徽建筑大學 材料與化學工程學院,安徽 合肥 230601)
0 引言
肝素鈉是帶負電荷最多、由三磺酸二糖重復單元組成的線性多糖,主要用作抗凝劑[1]。過量的肝素鈉會誘導大出血和血小板減少[2],因此,對肝素鈉的檢測顯得十分必要。迄今,發展簡單、可靠的生物流體中肝素鈉檢測方法已經引起了相當大的關注[3-6]。除了傳統的激活凝血時間法與活化凝結時間法等,由于具有操作方便與成本低廉的優勢,光學傳感器包括熒光法[7-9]、光散射法[10-12]和比色法[2,8-9],目前已得到很大發展。這些傳感器的設計原理均基于帶正電的有機染料與帶負電的肝素鈉之間的靜電作用[7-13]。南開大學的王荷芳教授[14]發展了一種聚乙烯亞胺包裹的Mn摻雜ZnS量子點(Mn-ZnS QDs)檢測肝素鈉技術,由于肝素鈉荷負電引起了荷正點的Mn-ZnS QDs的點間聚集,肝素鈉負電荷產生的電場誘導了Mn-ZnS QDs的RTP增強,根據RTP的強度變化與肝素鈉濃度的關系,達到了檢測肝素鈉的目的。由于磷光的長發射壽命能夠很容易地避免體系的自熒光與散射光[15],在很多摻雜半導體體系中研究了主體半導體與摻雜劑的室溫磷光(Room-temperature phosphorescence,RTP)[16-21]。Mn-ZnS QDs用作室溫磷光探針,已經廣泛應用于傳感與分析領域[22-25]。
本文報道了一種基于Mn-ZnS QDs的RTP方法檢測肝素鈉。合成了荷正電的八胺丙基寡聚硅(OA-POSS)與荷負電的半胱氨酸包裹的Mn-ZnS QDs。當OA-POSS加入到半胱氨酸包裹的Mn-ZnS QDs的溶液中,由于靜電作用使Mn-ZnS QDs發生點間聚集,形成OA-POSS與Mn-ZnS QDs聚集復合物,OA-POSS的電場誘導了RTP的增強。當荷更高負電的肝素鈉加入到上述體系中,由于肝素鈉與OA-POSS間更強的靜電作用,使OA-POSS從聚集復合物中剝離,形成新的OA-POSS與肝素鈉聚集復合物,舊的聚集復合物的破壞使Mn-ZnS QDs的RTP逐漸衰減,這種衰減的RTP信號被用來檢測肝素鈉。衰減的RTP強度(ΔP)和肝素鈉濃度在2.5 μM到70 μM范圍內存在著很好的線性相關關系(R=0.991),檢測限為2.0 μM。重要的是,Mn-ZnS QDs應用于環境流體中肝素鈉的檢測,有效消除了背景熒光與散射光的干擾,且作為肝素鈉的傳感平臺具有很好的應用前景。
與Mn-ZnS QDs荷相反電荷的物質能夠誘導Mn-ZnS QDs靜電組裝,從而縮短QDs間距離并形成更大的粒子,依次導致了下面三個結果:(1)單個Mn-ZnS QDs上的缺陷可以被臨近QDs修復;(2)由于組裝提的形成,相當于QDs表面的Mn2+分布重排到內部,導致更高的Mn2+發射[26];(3)QDs周圍增強的定域電場增加了QDs間的庫侖作用,能夠更有效地誘導QDs的激發[14,27]。上述的每一個方面都有助于Mn-ZnS QDs發射的增強。每個OA-POSS分子帶八個正電荷,而先前工作中合成的半胱氨酸包裹的Mn-ZnS QDs帶負電(約-32mV)[28],那么可以設想:當OA-POSS與半胱氨酸包裹的Mn-ZnS QDs發生靜電自組裝,由于靜電作用使Mn-ZnS QDs發生點間聚集,就會產生上述三種作用,從而誘導Mn-ZnS QDs的RTP的增強。此外,當荷更高負電的肝素鈉(約-60mV)加入到上述體系中,發生三組分競爭,由于肝素鈉與OAPOSS間更強的靜電作用,剝離促使Mn-ZnS QDs發生聚集的OA-POSS,形成新的OA-POSS與肝素鈉聚集復合物,使Mn-ZnS QDs增強的RTP逐漸衰減,這種衰減的RTP信號可用來檢測肝素鈉,見下圖1。為了證明上述設想的科學性,我們就Mn-ZnS QDs與OA-POSS間的作用,以及由此產生的光譜信號變化進行了研究。
1 實驗部分
1.1 材料
氨丙基三乙氧基硅烷(APTES)、半胱氨酸和肝素鈉均購自上海阿拉丁生化科技股份有限公司。ZnSO4·7H2O、MnCl2·2H2O 和 Na2S·9H2O 等購自國藥集團。其它試劑均為分析試劑級。實驗用水均為超純水。
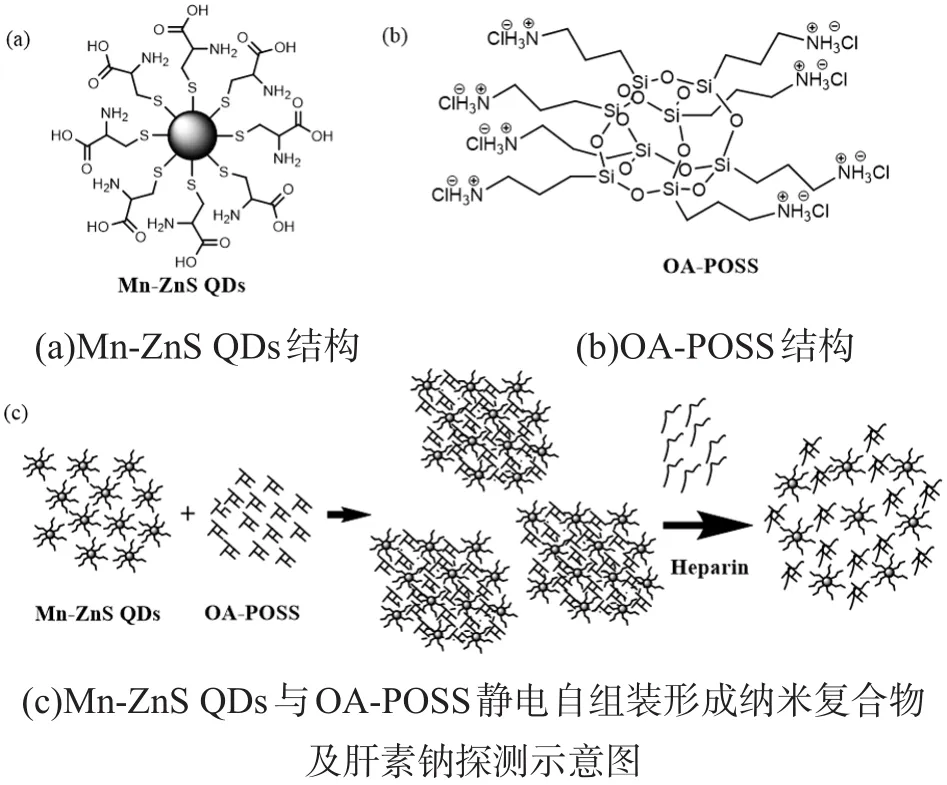
圖1 結構示意圖
1.2 儀器
分別用F-4600(日立,日本東京)和日立紫外UV-2910紫外-可見分光光度計記錄熒光光譜和紫外-可見吸收光譜。在Nicolet-6700分光光度計(Nicolet,Madison,WI,USA)上,用 KBR 窗口測量了傅里葉變換紅外光譜(FT-IR)。在JEL-200CX(JEOL,日本東京)顯微鏡上對透射電子顯微鏡(TEM)進行了表征,加速電壓200 kV。利用Al Ka X射線源(1486.6eV)用XPS儀器(美國熱ESCALAB 250)進行了X射線光電子能譜(XPS)測試。在島津XRD-6000型衍射儀上,用Cu KA射線衍射儀測定了粉末X射線衍射譜。酸度用SartoriusPB-10 pH 計測定(Sartorius,Diatekon,瑞士)。以氫燈為光源,365 nm為激發波長,在愛丁堡譜儀F 900上記錄了熒光壽命的測量結果。
1.3 Mn-ZnS QDs的合成
量取 5.0 mL ZnSO4·7H2O(0.1 M)和 30 mg 半胱氨酸于燒杯中,用超純水溶解并稀釋到50 mL,將體系的pH調整為11.0,將溶液轉移到圓底燒瓶中攪拌 20 min后,注入 1.5 mL MnCl2·2H2O(0.01M),30 min 后注入 5 mL Na2S(0.1M),繼續攪拌30 min,上述過程全程充氮除氧。將溶液加熱到50°C,在有氧環境下陳化2 h后,自然冷卻至室溫,轉移至燒杯中,加入2倍體積乙醇后靜置1天,3000轉速下離心10 min,將得到的沉淀儲存于4°C冰箱中備用。
1.4 OA-POSS的合成
在典型的合成中,氨丙基三乙氧基硅烷作為溶膠-凝膠法的先驅被使用。取20 mL氨丙基三乙氧基硅烷(APTES)和160 mL甲醇于燒杯中,攪拌混合。在混合后的混合物中加入27 mL 0.1M的鹽酸,混合液攪拌一個星期直至OA-POSS白色粉末沉淀物出現,該沉淀即為OA-POSS。
1.5 樣品分析
實驗用水樣取自合肥污水廠,水樣通過0.45 μM微孔濾膜過濾,并將pH調整為7.4,儲存于4℃的冰箱中備用。
2 結果與討論
2.1 Mn-ZnSQDs與OA-POSS間的自組裝
量子點是最具吸引力的納米粒子之一,與有機染料相比有著很多優勢,比如可調發射和高量子產率等。Mn-ZnS QDs近年來被用作為室溫磷光探針[22-25]。這種類型的量子點可以通過靜電組裝形成聚集體而增強RTP發射,還可以有效避免散射光和自熒光。OA-POSS分子是八個APTES聚合的,八個角上的胺基容易結合質子,形成荷八個正電荷的寡聚硅。兩種荷相反電荷的材料在同一體系中容易發生靜電自組裝作用。量子點的ζ電位被檢測為6.42mV,量子點帶正電荷,表明此測試方法是基于OA-POSS和半胱氨酸包裹的Mn-ZnS QDs之間的靜電作用[29]。
如圖2所示,Mn-ZnS QDs和OA-POSS形成的納米復合物的RTP光譜展示了此QDs的發射峰位于576 nm處。對于50 mg/L的Mn-ZnS QDs溶液中,隨著加入的OA-POSS的濃度從0逐漸增加時,QDs的RTP發射強度隨之增強。當加入的OA-POSS的濃度為75 μM時,RTP強度達到最大值,而后隨著OA-POSS的繼續加入,RTP開始衰減。此外,QDs和OA-POSS形成的納米復合物的磷光強度在pH為7.0時能夠保持穩定,且可以維持80 min以上,表明了此納米復合物結構的穩定性。
利用UV-vis光譜研究了不同組分間的相互作用。如圖2b所示,檢測了OA-POSS(曲線1)、肝素鈉(曲線 2)和 Mn-ZnS QDs(曲線 3)從 200到 500 nm的吸收光譜。當OA-POSS加入到QDs的溶液中,導致了QDs的吸光度的增強(曲線4)。QDs和OA-POSS形成的納米粒子溶液中加入肝素鈉會致使其吸收度的增大(曲線5)。如圖2c所示,肝素鈉的吸光度隨著加入的OA-POSS濃度的增大而增強,這是由于肝素鈉與OA-POSS之間形成了緊湊的光散射粒子。同樣地,隨著加入的肝素鈉濃度的增強,QDs和OA-POSS形成的納米復合物的吸光度也隨之增大(見圖2d)。上述現象表明了QDs與OA-POSS之間發生了相互作用,且肝素鈉與QDs和OA-POSS形成的納米復合物之間也存在著相互作用。透射電鏡成像亦用于研究OA-POSS與Mn-ZnS QDs之間以及OA-POSS與肝素鈉之間的相互作用。如圖3(a)所示,OA-POSS加入到Mn-ZnS QDs溶液中,由于荷相反電荷,兩者間通過靜電自組裝成納米復合物。同樣地,將OA-POSS加入到肝素鈉溶液中,也會形成納米復合物,如圖3(b)。
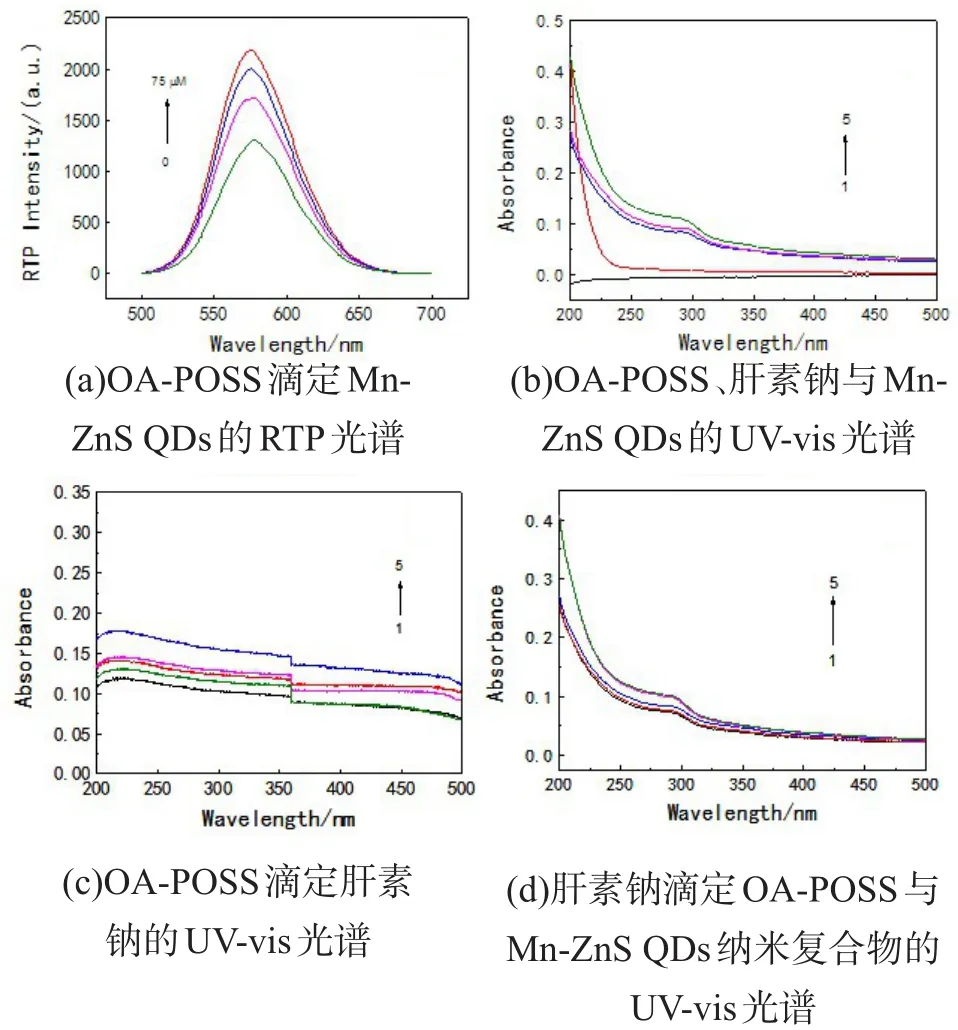
圖2 RTP及UV-vis光譜圖
2.2 肝素鈉滴定OA-POSS與Mn-ZnS QDs納米復合物的RTP光譜
肝素鈉可以誘導PEI包裹的Mn-ZnS QDs之間的發生靜電聚集而縮短點間距離,促使QDs間形成更大的粒子[14]。為了證實Mn-ZnS QDs與OA-POSS之間形成的納米復合物探測肝素鈉的可能性,我們研究了肝素鈉對納米復合物的RTP的影響。如圖4所示,QDs與OA-POSS形成的納米復合物的增強的RTP隨著肝素鈉的加入而逐漸衰減,表明QDs與OA-POSS形成的納米復合物與肝素鈉之間存在著相互作用,這可能是由于肝素鈉的荷電更負,奪取了QDs與OA-POSS納米復合物中的OA-POSS,導致了納米復合物的解組裝,電場破壞以后,由電場引起的RTP增強隨之衰減,并接近原始強度。反之,當肝素鈉加入到Mn-ZnS QDs溶液中(不存在OA-POSS)中,QDs的磷光發射強度幾乎沒有改變,這是由于兩者荷負電引起的。以上的光譜變化表明QDs與OA-POSS形成的納米復合物的RTP發射強度的衰減起因于OA-POSS和肝素鈉之間的相互作用。也研究了肝素鈉滴定前后的Mn-ZnS QDs的壽命變化,6.3毫秒左右的壽命符合靜態猝滅規律,說明了靜電作用的存在。

圖3 透射電鏡(TEM)成像圖
2.3 肝素鈉的RTP檢測和條件優化
Mn-ZnS QDs與OA-POSS形成的納米復合物的在576 nm處的RTP發射用于肝素鈉的檢測,目的在于評估此納米復合物的肝素鈉定量的潛在可行性。如圖5所示,猝滅的磷光強度(ΔP)和肝素鈉濃度在2.5到70 μM范圍內存在著很好的線性相關關系(R=0.991),檢測限為2.0 μM,且5次測量的相對標準偏差(RSD)為6.9%。
考察了作用時間對光譜測量的影響,如圖6所示,上述的RTP強度的衰減受反應時間的影響。對于不同的肝素鈉的加入量,QDs與OA-POSS形成的納米復合物與肝素鈉之間的競爭相互作用在經過了大約40 min后保持持穩定。因此,本研究選擇40 min作為實驗的反應時間。

圖4 滴定RTP光譜圖

圖5 使用Mn-ZnSQDs與OA-POSS納米復合物作RTP探針的肝素鈉檢測校正曲線
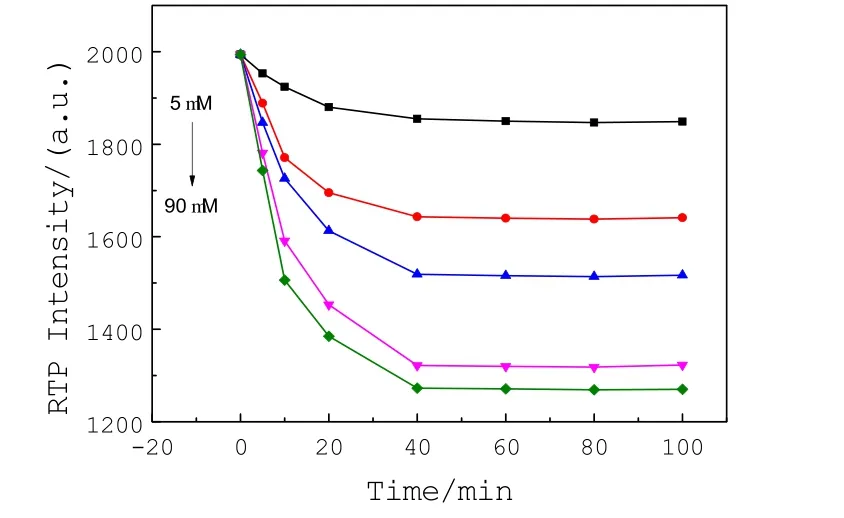
圖6 不同肝素鈉濃度滴定Mn-ZnSQDs與OA-POSS納米復合物的時間依賴性RTP光譜
2.4 基質干擾
環境樣品中共存的主要的金屬離子、大分子和小分子可能對肝素鈉的檢測存在干擾。為了考察Mn-ZnS QDs與OA-POSS納米復合物RTP探針的對肝素鈉的選擇性,對可能共存的過量的金屬離子(如 K+、Na+、Ca2+、Mg2+、Fe3+、Zn2+、Mn2+和 Cu2+)、葡萄糖及腐殖酸等加入到含1 μM的肝素鈉的Mn-ZnS QDs與OA-POSS納米復合物體系中,檢測干擾物質加入前后的RTP光譜。結果如表1所示,各種過量的干擾物質的加入對RTP強度產生的影響在±5%的范圍內。此外,腐殖酸作為有機復合物的代表物,在pH為7.0的溶液中,也同樣對肝素鈉的檢測無干擾。上述結果表明Mn-ZnS QDs與OA-POSS納米復合物RTP探針可用于選擇性肝素鈉的檢測。
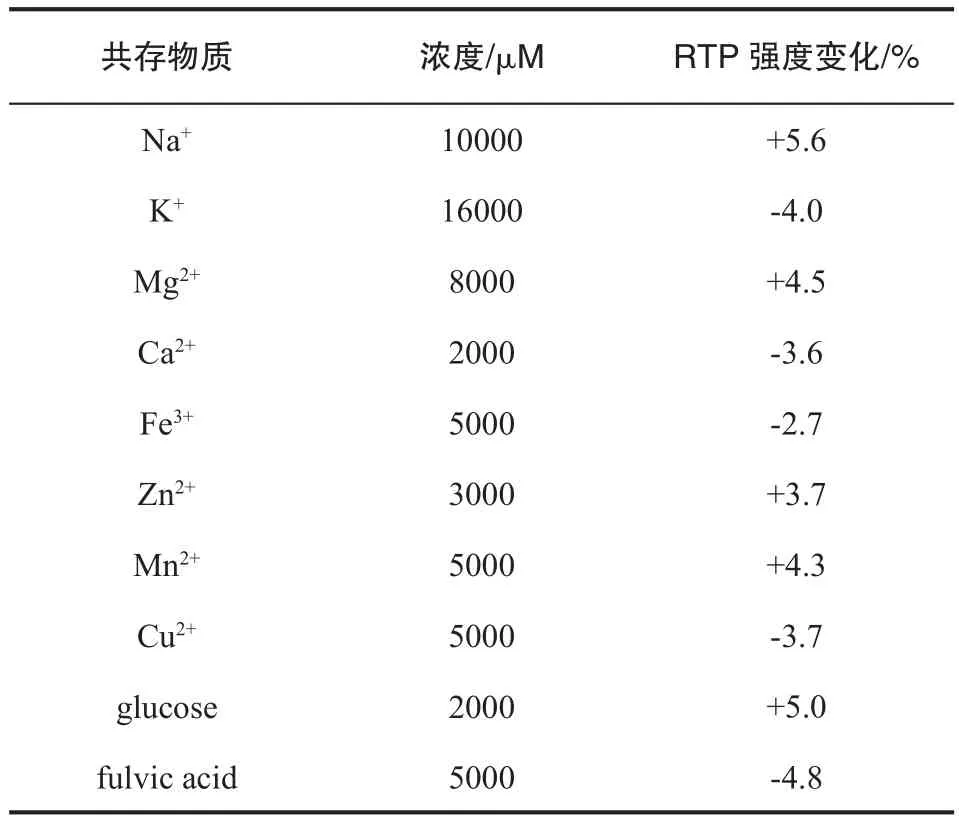
表1 各種共存基質對Mn-ZnSQDs與OA-POSS納米復合物RTP探針檢測肝素鈉的影響
2.5 實際樣品分析
為了論證Mn-ZnS QDs與OA-POSS納米復合物RTP探針的適用性,污水廠尾水被用于肝素鈉的分析檢測。如表2所示,尾水樣品經過適當稀釋后加入標準的肝素鈉后,能夠獲得好的定量回收率(95~101%),且可以使用一個簡單的標準溶液來精確定量肝素鈉。
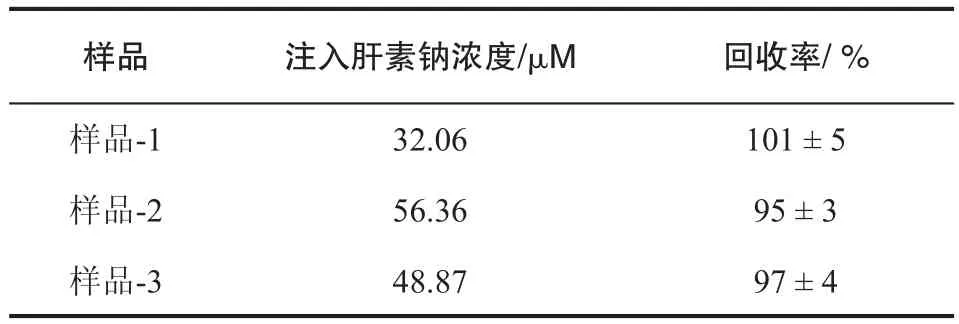
表2 實際水樣品中肝素鈉探測的三次測定回收率
3 結論
總之,荷正電的OA-POSS與荷負電的半胱氨酸包裹的Mn-ZnS QDs在溶液中由于靜電作用發生點間聚集,形成OA-POSS與Mn-ZnS QDs納米復合物,OA-POSS的電場誘導了RTP的增強。當荷更高負電的肝素鈉加入到上述體系中,肝素鈉與QDs競爭,使得舊的納米復合物解體,新的OAPOSS與肝素鈉納米復合物形成。舊的納米復合物的解體使Mn-ZnS QDs的RTP逐漸衰減,并應用于復雜樣品中肝素鈉的選擇性檢測,這已經被證實是一種有效且實用的技術。

