腦血流自動調節:從理論到臨床轉化及檢查流程的標準化
韓珂,胡漢華
腦血流(cerebral blood flow,CBF)存在于人腦中一個約600 km長,具備協同作用且相互連接的血管網內。在此血管網系統中,腦動脈、小動脈和毛細血管為大腦提供O2、能量和營養,而腦靜脈將CO2和代謝廢物從大腦中排出。腦幾乎沒有能量儲備,必須通過血流持續供應O2和能量。
腦血管的適應性調節機制有助于保證腦在各種條件下均可獲得充足且適當的血液供應。包括:平均動脈血壓(arterial blood pressure,ABP)在一定范圍內變動時,保持腦灌注穩定能力的CA;腦內動脈PaCO2/pH改變時,保持腦灌注穩定的血流動力學反應的腦血管運動(舒縮)反應性(cerebral vasomotor reactivity,VMR)。以上2種調節機制針對的是靜息狀態的腦血流調控。此外,細胞活性增加時,CBF通常也會增加,這是通過神經血管耦聯(neurovascular coupling,NVC)調整腦灌注以適應大腦活動增強時細胞功能增加的高代謝需求,又被稱為功能性充血,目前是一個比較活躍的研究領域。
上述3種腦血管的適應性調節機制均通過神經血管單元(neurovascular unit,NVU)起作用。傳統NVU位于腦循環的末段,由小動脈、微血管、壁細胞如血管平滑肌細胞和周細胞、內皮細胞、星形膠質細胞、神經元及小靜脈構成。上述結構不但在神經血管耦聯中各司其職(如壁細胞具有收縮性,能夠直接調控血管的直徑和血流),而且與動脈、小動脈和腦微循環毛細血管段的神經元之間相互作用;同時通過介導腦血管擴張和收縮的細胞信號通路進而調控CBF使其增加和減少[1-3]。在許多神經系統疾病的早期階段,當CBF調節的細胞和分子機制異常,CBF、O2輸送和神經元活動不匹配,出現神經血管功能連接中斷,神經血管將失耦聯[4-5]。近年來,NVU的概念逐漸擴展為更大范圍的“血管神經網絡”[6-8],包括在生理和病理條件下維持腦血流所需的全部細胞及結構,除了傳統的毛細血管內皮細胞、周細胞和被星形細胞端足包裹的基底層、內皮細胞、神經元和星形膠質細胞,還包括平滑肌細胞、非毛細血管內皮細胞、血管周圍神經、成纖維細胞、平滑肌祖細胞和免疫系統細胞及側支血管、血管周圍神經和靜脈。正是依賴于這個血管神經網絡的精細和復雜的協同合作,才實現了腦血流的精確調控,支持了大腦正常的穩態和功能。
TCD可以同步動態監測顱內血管的血流速度(cerebral blood flow velocity,CBFV)。假設顱內血管的直徑不變,血流速度可以代表腦血流。通過TCD監測顱內血管的血流速度,得以實現實時同步監測生理或病理條件下由外部或者內部刺激誘發的NVU的變化和反應,進而分析這些機制調控下的腦血流改變。
由于人體研究更適合闡述CA的機制,本文結合團隊多年的臨床研究積累的經驗,主要關注的是人體CA的生理和臨床轉化應用,包括CA檢查流程的的標準化。
1 腦血流自動調節的生理
CA的概念由Lassen等在1959年首次提出,是當ABP在60~150 mm Hg之間波動時,CBF保持穩定的能力。CA保護腦,避免低血壓導致的腦灌注不足,或高血壓導致的腦充血、過度灌注[9]。
CA的基礎是通過小動脈和毛細血管括約肌調節腦血管的阻力(cerebrovascular resistance,CVR)。關于機制,主要是4種學說,包括肌源性、神經源性、內皮性和代謝反應機制。肌源性張力是壓力增高時小動脈及其平滑肌收縮,壓力降低時舒張[10]。跨壁壓力快速變化(ΔP=10~25 mm Hg/s)將觸發血管直徑的即時變化[11]。跨壁刺激開始和血管機械應答開始之間的潛伏期通常<250 ms[12]。代謝機制發生在較小的血管,局部微環境的變化會影響血管舒縮反應,例如,低于自動調節下限的低血壓導致了腦血流降低,進而導致CO2蓄積,由于調節存在則小血管擴張,PaCO2每增加1 mm Hg,腦血流增加近4%。相反,高于CA上限的高血壓導致高灌注和CO2減少,相應地血管收縮,PaCO2每降低1 mm Hg,腦血流減少4%[13]。該反應已經被歸因于腦血管平滑肌對H+的反應[14]。神經源性機制也被稱為“神經血管耦聯”,包括對中、小直徑血管的控制。神經元分泌具有血管活性的神經遞質,如血管擴張劑乙酰唑胺、NO及血管收縮劑5-羥色胺和神經肽Y[15]。通過紅外視頻顯微技術觀察大鼠的神經元之間和鄰近的微血管,發現微血管對神經元間去極化的反應是收縮[16]。內皮性機制是指內皮細胞產生了多種信號,如內皮細胞分泌血管擴張劑NO等,以及血管收縮劑如內皮素-1、血栓素A2等,影響正常和疾病狀態下腦血管的張力[17]。
CA分為2種類型:靜態的自動調節和動態的自動調節。sCA是調整腦血流適應在數分鐘或者數小時內緩慢/漸進改變的血壓,是在TCD技術應用臨床之前,因無法實現同步,故記錄的是滯后的數據。TCD問世后,由于具有高時間分辨率,可以實現即時同步,故dCA可以在數秒鐘內對血壓的即時變化做出反應,允許持續測量CA,實現對血流動力學的逐波分析。
CA及腦血流與晝夜、運動、強迫呼吸(伴隨著動脈血PaCO2的變化)、體位和功能活動均有關,飲食、月經周期的激素改變、麻醉劑也是影響因素。所以,在隊列研究(在相同條件下評估每例患者)或者個體前、后比較的縱斷面研究中,進行CA實驗時,必須要考慮這些波動因素的影響,以便實現標準化操作,提高該檢查的可重復性及多中心之間比較結果。
2 腦血流自動調節的檢查方法
動物研究發表始于20世紀60年代。與爬行動物比較,人類更易受直立重力影響,因此,關于CA的機制可能不同。而且隨著TCD的引入,直接無創地研究人體受試者已經成為可能。CA的檢查方法分類見表1。
sCA是通過藥物干預實現腦灌注(血)壓的變化。
dCA包括外界誘發血壓或者自發血壓波動2種類型。其中外界誘發的dCA是通過刺激-反應的方法,分析血壓快速下降之后,腦血流速度的動態變化(直到腦血流速度再次達到穩定)。簡而言之,是給予無創的即時或者周期性的刺激。方法主要如下:①下肢袖帶釋放實驗,用血壓袖帶阻斷雙下肢近端(大于收縮期血壓)2~3 min,然后快速放氣[18]。由于誘發了收縮期血壓快速下降(大約20 mm Hg),正常情況下,腦血流速度將每秒上升達20%。下肢袖帶釋放實驗禁忌證是下肢血管病或者下肢骨折[19]。該刺激不能代表日常生活中的生理狀況(如體位變化或者藥物刺激)。下肢袖帶釋放實驗是在仰臥位進行的,因此,臥床的患者也適用。②頸動脈壓迫實驗或者短暫充血反應實驗,指在盡量靠近頸部的位置壓迫頸總動脈(注意:壓迫實驗有效的標準是頸總動脈血流速度至少下降30%~50%),3 s后再解除壓迫[20]。由于壓迫引起了小動脈的代償性舒張,誘發了短暫的充血反應(transient hyperemic response,THR),計算公式為:THR系數(transient hyperemic response ratio,THRR)=充血時血流速度/基線血流速度,其中充血時血流速度=壓迫解除后2個收縮期血流速度的均值;基線血流速度=壓迫前5個收縮期血流速度的均值。正常值是1.105~1.29。壓頸動作有產生栓子的風險,且患者不舒服,限制了該方法的重復應用。③瓦氏動作(valsalva maneuver,VM)持續用力吹氣,維持在30~40 mm Hg,持續15 s能引起血壓變化及相應的CA反應[21]。但是,胸膜腔內壓的增高也會導致顱內壓增高,進一步降低灌注壓,及存在呼氣末PaCO2增高的可能,是影響CA的干擾因素。④規律的緩慢呼吸是另一個有效的方法,但同樣的,也存在增加潮氣量及誘發測試期間低碳酸血癥的風險[22]。⑤“坐-立位實驗”模擬生理狀態下的血壓下降,受試者坐位持續5 min(下肢抬高90°),轉為立位持續1 min,5 min后再重復一遍坐位和立位[23]。該方法與下肢袖帶釋放實驗的結果類似,已被證實是有效的[24]。⑥其他誘發血壓波動的方法,如周期性蹲坐、被動抬頭直立傾斜實驗、等長握力練習(需要患者配合)及冷壓實驗,其中一個較復雜的技術是下肢負壓實驗,將雙下肢置于呈正弦波的負壓艙(桶)中,實現血壓的周期性變化,該負壓導致下肢血流的重新分布和血壓下降[25]。但這個過程可使肥胖者不適,也不太可能被實現,更被批評可能導致損傷CA本身。
與外界誘發的CA方法不同,自發的dCA是記錄血壓和腦血流的自發的波動。該方法始于20世紀90年代,由于不需要受試者配合任何誘發動作,簡單易行,在臨床應用廣泛,目前是CA的主流檢查方法[26-28]。但由于之后處理的分析方法不同,對檢查數據設置的要求也不同,而且數據的分析方法較復雜。
3 腦血流自動調節的分析方法
基于血流、血壓呈線性關系的假設,分析數據的常用指標如下:腦血管阻力(cerebrovascular resistance,CVR)=均值BP/均值CBF(單位:mm Hg·mL-1·min-1)[29]。在TCD的研究中,CVR指數(CVR index,CVRi)=均值BP/均值CBFV(單位:mm Hg·cm-1·s-1)。搏動指數(pulsatility index,PI)=(收縮期峰值血流速度-舒張期末血流速度)/均值血流速度。PI值是量化微小血管收縮、舒張阻力的常用工具,它與穩定條件下的CVR的意義不同,在描述CA的特征時PI似乎沒那么有用,因為條件改變時,PI并不總是以與CVR相同的方式做出反應[30]。另一個量化CA的方式是當腦血流接近0時的BP值即為臨界關閉壓(critical closing pressure,CrCP,單位:mm Hg)。

表1 CA的檢查方法
更復雜的分析d C A特性的是時域分析和頻域分析[26-28,31-35]。自動調節指數(autoregulation index,ARI)可用于時域分析[31]。應用該指數的技術背景是假設腦血流速度被動隨血壓下降,利用計算機構建了ABP驟降后,CBFV變化的10個(0~9)標準應答模型曲線。如果被評估的曲線符合這個模型且ARI=0,則代表無CA,ARI=9,則代表CA最佳,故ARI 0~ARI 9,代表對血壓下降的調節能力越來越強。這種分析方法最初針對的是下肢袖帶釋放實驗,也被廣泛用于其他檢查方法[24]。而自動調節斜率指數(autoregulatory slope index)作為ARI的替代,評估CA響應斜率的陡度,顯示出與ARI良好的相關性。恢復率(the rate of recovery,ROR)=[(CVR指數的差值/時間差)/平均ABP的差值]×(腦血流速度/s),是通過分析血壓下降刺激腦血流速度的恢復時間,評估CA的有效性。
另一個在時域內評估CA的分析方法是血壓和腦血流速度之間的相關系數(the correlation coefficient,Mx),或者皮爾森相關系數[32]。每5 s的平均值為一個單位,再以每3 min為單位(共36個單位時間)計算均值,然后將所得數值進行灌注壓與平均腦血流速度的相關性分析,這個相關系數被定義為平均速度指數,若為0或負值,提示CBFV和CPP之間無關或負相關,即血壓與腦血流速度之間存在時間差,并非完全同步變化,故CA未受損,調控正常;若為正值,提示CBFV和CPP之間正相關,即完全同步變化,故CA受損。Mx是CA隨時間變化的一個新的持續監測的指標。與傳遞函數分析不同的是,當線性關系不存在時Mx仍然有效。
傳遞函數分析(transfer function analysis,TFA)是評估頻域的方法,用于分析逐波的血壓和腦血流之間的關系[26-28,30,35]。簡言之,通過分析輸入信號血壓和輸出信號腦血流之間的即時變化,量化CA[30]。該分析方法的參數是3個:增益(或振幅),相位差,一致性函數(簡稱一致性)。有效的CA使增益衰減,因此,低增益代表CA存在,而高增益提示CA的有效性減弱。CA存在時血壓和血流之間的相位差是正值,當CA能力下降時,則伴隨著相位差消失,轉化為時域,相位差為0(血壓和血流振蕩之間無時間延遲)代表CA消失[30,36]。一致性描述的是血壓和血流之間的線性關系,一致性高提示呈線性關系,而一致性接近0提示無線性關系。不同頻段內各個參數的值和意義不同,需要進行區分,低頻振蕩(也稱為M波)可能反映了交感神經張力的變化,這是由平均ABP的自發變化引起的,而極低頻振蕩(也稱為B波)似乎反映了顱內壓的自發振蕩,并由其他機制觸發。CA的分析方法見表2。
4 自發的動態腦血流自動調節標準化方案的探討
針對諸多的CA的檢查方法,對應的CA的分析方法也諸多,但至今無公認的金標準。CA的概念代表了BP(刺激或輸入信號)和CBF(反應或輸出信號)之間的動態關系,假設CA被簡化為一個線性控制系統,由于臨床廣泛采用的檢查方法是自發動態的CBFV與BP波動法,那么基于BP自發波動的TFA是目前研究中常用的分析方法。其理論基礎是TFA可獲取頻率依賴的增益和相位評估,而且還能根據一致性函數評估這些數據的可靠性,所以《傳遞函數分析dCA:源于國際CA研究網絡的白皮書》推薦了TFA的參數和設置,旨在完善和標準化dCA,使檢測結果更穩定、更可靠[35]。本團隊自1998年首次發表應用頻域方法分析自發dCA的研究以來,在臨床研究中積累了關于儀器設備的選擇、操作步驟、檢查參數、報告內容及臨床解讀的豐富的實踐經驗[26]。
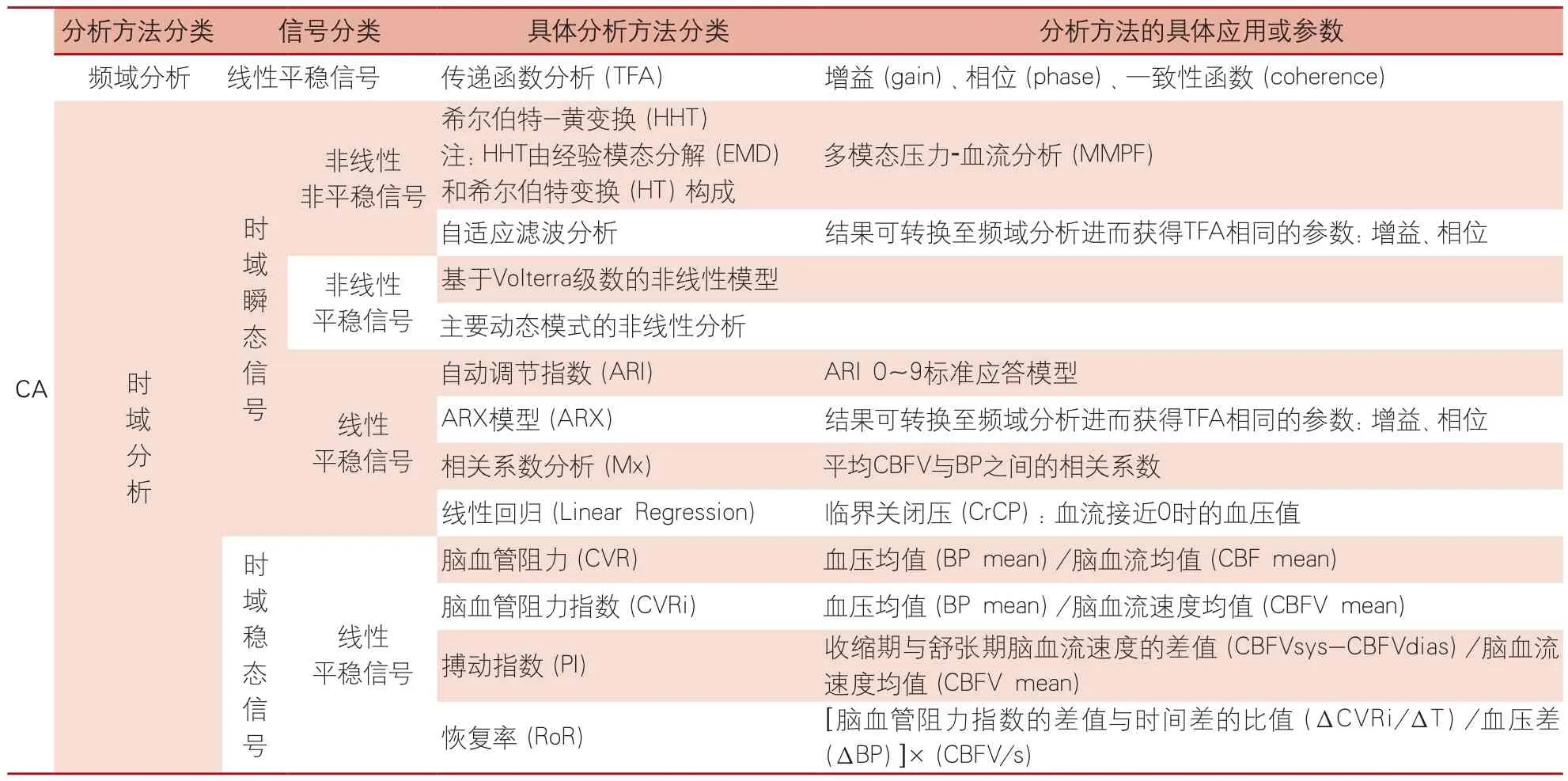
表2 CA的分析方法
4.1 儀器設備 以TFA分析方法為例,臨床應用中的常規配置:①TCD儀。是無創的檢查設備。配備2.0/1.6 MHz監護探頭及監護頭架,或者選配4.0/8.0 MHz探頭及其配套的監護頭架(目前深圳市德力凱醫療設備股份有限公司可定制)。需要配備實時的血流監護軟件。②無創性連續逐波血壓監測儀。此儀器是無創的檢查設備。配備手指動脈容積夾(即指套,此為消耗品),容積夾按照尺寸分大、中、小規格,分別匹配不同粗細的手指。配備校正血壓用的袖帶血壓。③呼氣末CO2分析儀(或模塊)。此儀器是無創的檢查設備。常采用紅外線法或者質譜儀法測定呼氣末CO2。配備規格相同的鼻導管(一次性的消耗品)。④連續心電監測儀。此儀器是無創的檢查設備。選配。目前大多數儀器通過CBFV的波形可以間接算出心率,但一些專業軟件需要配備連續心電監測。⑤數據整合設備。選配。是整合以上多個數據達到同步輸入、輸出的設備(如多功能數據采集卡)。⑥選配其他設備。根據臨床研究的需要,監測參數不同,選擇有創或者無創的檢查設備,如近紅外光譜儀(near-infrared spectroscopy,NIRS),用于無創測量局部腦氧飽和度;腦組織血氧監測儀,用于無創測量局部組織氧分壓;腦血氧和血流監測一體機,屬新型設備,是以色列Ornim醫療有限公司的CerOx(將近紅外與局部低功率超聲結合,配無創探頭);顱內壓監測儀,配顱內導管,用于有創測量顱內壓;腦血流和無創連續血壓監測一體機,是新型設備,深圳市德力凱醫療設備股份有限公司的EMS-9D Pro(實現了腦血流及無創連續逐波血壓監測的同步輸入輸出,配無創自動監護探頭、壓力感應指套等)。⑦專業分析軟件。包括離線分析和在線即時分析軟件。
4.2 操作步驟
①對檢測環境及受試者的一般要求。檢測需要在有空調的環境中,理想溫度是22~24 ℃。如果檢測靜息狀態下自發的CA(基線),應該盡量避免干擾,如視覺或者聽覺刺激(包括人員進出的干擾)。由于晝夜節律的變化,推薦在相似的時間段檢測,以保證可重復性。
受試者檢查前至少4 h避免飲用含咖啡因的飲料、巧克力和難消化食物,還須在檢查前至少12 h避免運動和攝入酒精。保健品和各種藥物也能影響分析結果(如TFA),需要根據實驗目的酌情考慮。受試者應休息15 min(確保血壓、心率和心搏量穩定)后,取仰臥位(需同時記錄頭的位置)或者坐位(需雙下肢不交叉)檢測。
②選擇腦血流速度信號。記錄MCA血流速度之前,先戴監護頭架,固定好探頭,將TCD機器調為雙通道單深度模式,監測雙側MCA,深度分別為50~65 mm,取樣容積10~15 mm3,增益的調整以血流速度頻譜的包絡線平滑,無毛刺樣改變為宜(在臨床工作中發現,DWL TCD機器增益調整為38或者52時,其頻譜包絡的平滑效果最佳;而德力凱TCD機器對增益無特殊要求)。
雙側顳窗穿透不良者,可嘗試監測雙側PCA,深度分別為60~70 mm,取樣容積10~15 mm3,鑒于CA評估對腦血流速度包絡線平滑度的要求比較高,在MCA獲取失敗的條件下,PCA的失敗率也較高。本團隊嘗試應用4~8 MHz探頭及頭架(自行研制)監測雙側ICA顱外段評估CA,與同側MCA比較,也是一個有效的選擇,盡管ICA和MCA的調節結果存在差異[37]。
③選擇血壓信號。記錄連續逐波血壓之前,需要高度校準器對戴指套側的手指與心臟的高度差進行校準,避免手的位置的高低對準確性的影響。需要同時用袖帶血壓校正逐波血壓的準確性。后期的數據分析需要保持血壓信號的連續性,故建議校正完成后,關閉血壓的自動校正功能。
④選擇呼氣末CO2信號。記錄CO2波形之前,先將鼻導管的鼻子端放到鼻孔下邊,另一端的采樣管經過濾器連接到CO2儀器的進氣口。CO2波形的高度代表CO2濃度。由于吸氣中無CO2,呼氣中出現CO2,正常情況下,吸氣期間CO2波形是逐漸下降,呼氣期間逐漸上升。波形出現的頻率是呼吸頻率。監測CO2信號,用于判斷自主呼吸,以便調整呼吸維持穩定,避免過度通氣或者通氣不足。因CO2會顯著影響CBF,故應記錄和重視任何明顯的PaCO2波動(如>1 mm Hg)。
⑤調試不同設備的信號使之同步化。是否同步化對CA參數的差異性很大(尤其對相位的干擾),所以要特別注意不同設備的信號是否存在延遲輸出的問題。
⑥記錄時間。因TFA分析要求至少是連續5 min的BP和CBFV數據,所以至少連續監測5 min,要求是在生理條件穩定,BP和CBFV的自發波動不間斷的數據。由于Finapres的BP設備存在“physiocals”功能,會造成BP缺失的短片段,建議BP校正后關掉該功能,從而避免影響數據分析。
實踐中,鑒于臨床采集數據的可用性,建議連續監測10 min。本團隊比較了5 min和10 min的數據分析結果,雖然兩者的有效性是一致的[38],但考慮到多中心的可比性,建議還是標準化分析5 min數據。
4.3 參數的預設 僅以TFA分析方法為例,該參數預設為TFA分析前的數據準備。
①采樣頻率。推薦BP和CBFV連續信號進行模擬-數字轉換時最小采樣頻率為50 Hz(即≥50 Hz)。實踐中,考慮到設備及數據存儲的可行性,通常推薦設置較Nyquist頻率高4~5倍。
②數據的格式。BP和CBFV信號的記錄采用2種格式,原始波形和(每搏心跳時的)平均BP和平均CBFV。2種格式的相關性很好,但相比較而言,原始波形更易被偽跡等干擾所影響,故推薦采用每搏心跳數據,即將BP舒張值的時間作為每個心動周期的起點、終點,根據波形曲線下面積計算每個心動周期的平均BP和CBFV。
③檢查數據是否可用。分析BP和CBFV數據之前,首先檢查信號是否存在偽跡,如偽跡連續存在超過3個心動周期,可以由線性插值插補,不會影響分析結果。如果偽跡等干擾持續時間過長則應刪除該段數據。但關于通過線性插值的插補而刪除的異位搏動的最大個數,一般認為0.03~0.07 Hz頻率范圍插補的缺失<10 s不會影響分析結果,而0.07~0.5 Hz頻率范圍每50 s內缺失達5 s,則分析結果不可靠,該數據應棄之。
④缺失數據的處理。通常采用插值法,包括線性插值和仿樣插值,推薦采用仿樣插值(即三階多項式)。
⑤為了推進標準化,推薦如下設置,最小的再采樣頻率4 Hz,去趨勢(無),正態化(無),濾波(無),防漏窗(Hanning取樣窗),窗長(≥100 s),窗的疊加度(50%),平滑化[用系數為(1/4,1/2,1/4)三角形平均窗],一致性臨界值(95%CI,基于自由度或者Monte Carlo模擬)。
備注:關于設置④~⑤建議感興趣者查閱英文原文或中文譯文[35,39]。
⑥參數單位的選擇。一致性函數無單位。相位的單位用角度(α0)或者弧度(αrad),兩者可以直接換算[公式α0=(αrad/π)×180]。增益的單位用絕對值(cm·s-1·mm Hg-1)或百分比(%·mm Hg-1)。
4.4 報告 以TFA分析方法的結果為例。
4.4.1 報告內容 需要描述特定頻帶范圍內的一致性、增益、相位的均值。具體包括3部分:①頻率的范圍。頻率的范圍為0.02~0.5 Hz,最常用的頻帶分段如下:極低頻0.02~0.07 Hz,低頻0.07~0.2 Hz,高頻0.2~0.5 Hz。②每個頻率范圍內的參數。包括一致性、增益、相位(即時間差)。③對應參數的平均值及標準差。報告內容是低、中、高頻段分別對應的一致性、增益、相位的均值和標準差。
備注:如果可能,還需要提供每個頻段內BP和CBFV的功率譜密度,以及BP和CBFV的均值和自身的變異度。由于低于0.02 Hz頻率的BP和CBFV的相位和增益不可信,所以頻率的下限為0.02 Hz。如果數據的頻譜分辨率高且數據長超過5 min,可以嘗試分析頻率低于0.02 Hz(如0.008 Hz)的數據,但需附加說明相關細節。
4.4.2 報告解讀 結合了近年臨床研究的實踐。
參考值:一致性(極低頻:0.51;低頻:0.62;高頻:0.57);增益(單位:cm·s-1·mm Hg-1,極低頻:0.68,低頻:0.96,高頻:1.20);相位(單位:角度,極低頻:53.0,低頻:25.4,高頻9.38)(備注:考慮到白皮書中的數據未統一標準校正,故此參考值中的相位值偏低。)
一致性,正常情況下在0~1之間變化,表示CBFV隨BP變化而變化,通常應>0.4。如果太小,提示CBFV隨BP變化呈非線性關系,可靠性差,則該數據不適于TFA分析。如果等于1,提示CBFV隨BP變化而完全同步變化,正常情況下呈線性關系的CBFV隨BP的變化是存在時間差的,雖然貌似可靠性好,但是代表調節消失。通常在高頻段內一致性高,接近1;低頻段內一致性相對低,故認為CA主要在低頻段內發揮作用。
相位差,通常在0°~90°變化,表示調節能力從差到好,通常在高頻段內幾乎為0°,表示CBFV隨BP同步變化,提示CA差;低頻段內是60°左右,提示CA好。
增益,通常>1或者<1之間變化。通常在高頻段內>1,表示BP無衰減的傳遞到CBFV,提示CA差;低頻段內<1,表示BP傳遞到CBFV有衰減,提示CA好。
備注:在輸入、輸出數據呈線性關系的前提下,“相位”參數較其他TFA的參數更穩定。
5 腦血流自動調節的應用
已知某些臨床情況,包括腦外傷、蛛網膜下腔出血、急性腦出血、急性呼吸窘迫綜合征、重癥監護室的敗血癥和相關譫妄患者、重度急性腦炎、缺血性卒中(包括ICA狹窄,MCA狹窄等血管狹窄)、糖尿病、血管迷走神經性暈厥、神經退行性病變(如癡呆)、嚴重的高血壓、進行外科手術的患者等,尤其是在重癥監護條件下,CA對于維持穩定的腦灌注非常重要。本文針對臨床的關注度,重點介紹個體化最佳血壓/灌注壓的調控、急性缺血性卒中、AD的CA的應用現狀。
5.1 個體化平均動脈壓的調控 目前CA監測的最新應用是,通過監測CA,估算每個個體的最佳平均ABP和最佳腦灌注壓,并明確床邊CA監測的可行性。Lucia Rivera-Lara等[40]的綜述總結了成人和兒童的觀察性研究是通過個體的CA曲線,估算不同人群的最佳腦灌注壓和最佳平均ABP,且評估高于或者低于最佳腦灌注壓或者平均ABP與預后之間的關系。研究表明,腦灌注壓或者平均ABP與CA監測確定的最佳值有顯著差異者,更易預后不良,而且在床邊連續監測CA是可行的,并且有望被直接用于調控急性期的血壓,具有潛在的指導個體化血壓管理的應用價值。
有4項研究調查了成人的急性腦外傷,以自動調節監測的最佳ABP為基線,評估其高血壓和(或)低血壓與功能預后的相關性。其中一項收集了327例患者的用“壓力反應指數”評估最佳腦灌注壓的研究發現,過低的腦灌注壓增加了致命性結局的發生率,而過高的腦灌注壓與嚴重殘疾比例增加相關[41]。與該研究結果相似,一項用“低頻CA指數”評估最佳腦灌注壓的55例患者的隊列研究發現,實際的腦灌注壓接近低頻自動調節指數(基于最佳腦灌注壓)與生存率增加相關,而多變量模型發現,實際的腦灌注壓和最佳腦灌注壓之間的平均絕對差值是死亡率增加的獨立相關因素[42]。另一項對18例患者的隊列研究發現,用“壓力反應指數”估算最佳腦灌注壓,實際腦灌注壓和最佳腦灌注壓之間存在較大差異(>10 mm Hg)的患者,更易預后不良[43]。與上述研究相反,一項用新參數“低頻樣本壓力反應指數”的研究,則未發現最佳腦灌注壓與死亡或重度殘障之間的相關性,但該指數本身對結局和最佳腦灌注壓的估算的預測價值也很低[44]。
針對腦出血(n=25)和動脈瘤性蛛網膜下腔出血(n=38)的研究分別顯示,用“壓力反應指數”評估最佳腦灌注壓和預后的關系,未發現兩者之間有顯著的相關性[45-46]。而對121例心臟手術患者的觀察性研究發現,基于“腦血氧定量指數”預估的低血壓,與腦細胞損傷及神經膠質纖維酸性蛋白增高(血清中腦損傷的特征性的生物標記物)相關[47]。
兒童的觀察性研究是通過床邊監測CA評估最佳平均ABP[48-50]。28例新生兒缺氧缺血性腦病的研究用“血紅蛋白容積指數”評估低于最佳平均ABP的血壓及與21~32個月后存在運動和認知障礙即預后不良之間的相關性,發現低溫治療復溫期間血壓嚴重低于最佳平均動脈血壓的新生兒的預后差[50]。另一項納入30例6個月~16歲的創傷性腦外傷兒童的隊列研究也報告了類似的結果,腦灌注壓與最佳腦灌注壓之間的差異中負偏差的持續時間和波幅的大小與預后不良(GCS評分≥4分)是相關的[48]。
值得注意的是,不同人群和可能存在并發癥的患者,估算的最佳平均ABP或者最佳腦灌注壓的平均值或者中位數是不同的。例如,腦出血患者的平均最佳腦灌注壓(85 mm Hg)比腦外傷患者(75 mm Hg)高,動脈瘤性蛛網膜下腔出血伴血管痙攣者其最佳腦灌注壓(98 mm Hg)比無血管痙攣者(78 mm Hg)高。與最佳腦灌注壓相比,腦外傷的血壓過高或過低均與嚴重殘疾有關,而在接受心臟手術的患者中,僅僅動脈壓過低與腦細胞損傷有關,考慮在嚴重的急性腦損傷、顱內壓增高和腦順應性差的患者中,可能部分是由于腦灌注壓過大,靜水壓力增高導致腦水腫惡化,從而使顱內壓進一步增高[41]。
目前關于指南中推薦的血壓管理的目標值是非個體化的,遺留了許多疑問,如長期高血壓者的最佳血壓是多少?相對于無腦損傷的患者,急性腦損傷和顱內壓增高患者的腦灌注壓的下、上限有不同嗎?上述研究通過CA的調控實現的個體化的最佳血壓,由于其為腦及其他器官提供了最佳的灌注,故與臨床結局預后改善密切相關,說明了實現個體化血壓管理的重要性。利用CA實現評估最佳腦灌注壓或者血壓是一個值得重點關注的領域。目前存在的問題是該項新技術缺乏隨機對照實驗數據來確定以最佳血壓或最佳腦灌注壓為基礎進行治療的臨床療效。未來,有望以自動調節為導向,通過前瞻性、大規模、隨機對照臨床研究評估,實現個體化血壓的調控。
5.2 缺血性卒中 另一個重點關注的領域是急性缺血性卒中。Marcel J.H. Aries等[29]發表的系統綜述,總結了23項研究(其中16項針對急性卒中,7項針對慢性卒中)。討論了3個問題:①CA受損了?為什么?CA受損似乎與缺血后血管內皮和平滑肌的功能喪失相關。②受損的范圍多大?不僅較大的梗死,而且腔隙性梗死患者的CA也受損。另一方面,CA受損發生在雙側半球,不局限于癥狀側。但是,由于缺乏縱斷面研究,腔隙性梗死的CA受損是由慢性小血管病引起的,還是由急性梗死引起的,目前尚不清楚。一項小型研究證實了急性缺血性卒中者雙側大腦半球的CA受損,與皮層下卒中相比,皮層卒中的CA受損略明顯,而不是顯著差異。③時間進程是什么?隨訪調查研究顯示,最初幾天內CA的受損惡化,較大卒中患者2周后仍持續存在,而小卒中患者,2周后受損會恢復。據報道,恢復期會持續3個月。慢性卒中患者,因為惡性高血壓患者的CA受損,卒中后慢性期CA持續受損時,其動脈高壓可能扮演了一個角色。而在微血管病的患者中,也發現了CA受損,并且與慢性白質病變的嚴重程度顯著相關。除了慢性高血壓的CA受損,CA的相位的界值移向血壓較高側。這似乎是有意義的,因為大腦可以更好地被保護去預防高血壓。但是,在全身低血壓的情況下,大腦可能更易受到低灌注的影響。最近,一些研究者假設,對于老年高血壓患者,藥物降低血壓可能改變CA,從而導致認知功能損傷。
CA也已經被用于評估ICA狹窄血流動力學改變的嚴重度和缺血性卒中的風險。側支循環是重要因素之一,但是,通過小動脈舒張降低腦灌注的完整的CA的代償可能也扮演了一個角色[51-52]。研究發現,一般說來,與對側比較,患側動脈至少達到70%的狹窄,才能引起狹窄側血管的CA降低。盡管對此存在爭議,但與CA未受影響側比較,調節受損側的卒中風險高,受損的CA本身代表了一個獨立的危險因素[53]。頸動脈手術中評估CA,發現術后CA功能的整體(部分)有恢復[54-56]。關于MCA重度狹窄者的研究顯示,CA受損出現在狹窄側。雙側ICA重度狹窄/閉塞者其CA也下降。對比而言,PCA中度狹窄者,未發現CA的顯著改變,潛在的原因可能是狹窄程度低。
5.3 癡呆 這是一個新興的領域,由于在AD小鼠模型中,CA受損嚴重,因此假設受損的CA在AD的病程進展中起作用(如未保護腦免受血壓波動的影響,因此導致了短暫的低灌注或者高灌注)。但人類研究的初步數據未證實CA對AD的影響[57]。然而,腦小血管病占全世界癡呆癥的40%左右,包括AD,而且最近的流行病學、臨床、病理學和實驗研究累積的數據表明AD與早期神經血管功能障礙是有關的,有待于進一步的研究來闡明AD與CA之間的聯系[58-66]。
總之,結合臨床研究的實踐,在白皮書的基礎上,細化了CA的標準化方案,包括檢查方法(推薦:記錄自發的動態的血壓、血流及呼氣末CO2的數據)和分析方法(推薦:TFA分析),為臨床科研及進一步開展臨床日常診療工作提供了可能,助力于相關醫院轉化應用參考。期待未來更多的中心借助CA的研究解決更多的臨床問題,如對血壓/灌注壓的個體化調控,對癡呆的早期篩查和干預等熱點問題。

