奧拉西坦對癲癇模型大鼠的治療效果及對大鼠Caspase-3 Hcy水平的影響
于海燕 閔連秋 王東玉 包翠芳
1)錦州市中心醫院神經內科,遼寧 錦州 121000 2)錦州醫科大學附屬第一醫院神經內科,遼寧 錦州 121000
癲癇是一種常見的神經系統疾病,會嚴重影響患者的生活質量,增加家庭負擔。許多抗癲癇類藥物都會對患者的認知功能產生不同程度的損傷,所以尋求一種既能有效抑制癲癇發作,又能保護神經功能的抗癲癇藥物成為了當下治療癲癇的重要課題[1-2]。奧拉西坦是一種用于腦損傷以及神經功能缺失的藥物,相關研究表明[3-4],奧拉西坦能夠有效抑制癲癇患者的癲癇發作癥狀,并且對損傷神經組織進行組織和重建。蛋白酶Caspase-3和同型半胱氨酸(Hcy)作為兩種常用的神經功能檢測指標,可能參與了癲癇疾病的發病過程,并起重要的調控作用[5-6]。本文使用奧拉西坦對癲癇大鼠模型進行干預治療,旨在探究奧拉西坦對癲癇的作用效果以及對Caspase-3、Hcy兩種指標的影響。
1 材料與方法
1.1實驗動物選取40只SD大鼠,由錦州醫科大學實驗動物中心提供,雄性,年齡3~6(3.8±1.5)個月,體質量200~250(220±7.9)g。所有大鼠均養殖在干凈籠子里,室溫在(22.1±1.8)℃,相對濕度35%~40%,光照12 h/d,喂飲純凈水,飼養時間為1周。2組大鼠在年齡、體質量上差異均無統計學意義。所做實驗均獲得我院倫理會批準。
主要試劑:兔抗大鼠Caspase-3抗體(均由根生化科技有限公司提供);小鼠抗大鼠Hcy、Cx43抗體(北京中杉金橋生物技術有限公司);戊四氮、奧拉美唑、氯化鋰(上海國藥集團化學試劑有限公司);PCR緩沖液、MgCl2溶液(北京中杉金橋生物技術有限公司);魯米諾發光底液、MgCl2溶液(武漢博士德生物工程有限公司);Cx43 mRNA引物(Invitrogen公司);TUNEL細胞凋亡檢測試劑盒(Sigma公司)。
1.2方法
1.2.1 建模:將40只大鼠隨機分為4組,各10只。對其中3組大鼠腹腔注射127 mg/kg的氯化鋰,24 h后腹腔注射戊四氮(35 mg/kg)。給予另一組大鼠腹腔注射同體積的無菌生理鹽水。PNASANI等[7]在注射戊四氮30 min后,觀察大鼠出現的面肌抽動、咀嚼點頭、前肢陣攣、站立、后肢陣攣以及跌倒等癥狀。根據Racine分級評價的標準分為[8]:Ⅰ級面部出現陣攣;Ⅱ級析出現節律性點頭;Ⅲ級出現單側前肢抽搐;Ⅳ級出現雙前肢抽搐;Ⅴ級出現四肢抽搐以及失去平衡、跳躍并跌倒等。癲癇持續狀態定義是Ⅳ級以上癇性發作并且能夠持續30 min。如大鼠在建模過程中持續出現Ⅳ~Ⅴ級表現,說明建模成功,最終建模成功24只。
1.2.2 分組處理:將24只癲癇模型大鼠分為模型組、奧拉西坦低劑量組和奧拉西坦高劑量組各8只,另10只大鼠為正常組。低劑量組大鼠給予奧拉西坦射液的劑量為30 mL/(kg·d),高劑量組大鼠給予奧拉西坦射液的劑量為50 mL/(kg·d);正常組和模型組大鼠,給予腹腔注射等體積的生理鹽水。連續給藥處理7 d。給藥處理過程中,注意觀察大鼠的體溫變化,各大鼠在給藥處理期間均可以自由飲食。
1.2.3 學習記憶能力測試:GRABENSTATTER等[9]使用Morris水迷宮對4組大鼠學習記憶能力進行測試,建造直徑1.25 m,高0.5 m的圓形水池,水深為0.3 m,水溫保持在(26.5±0.8)℃。在池壁上設置四個不同的標志點,在水池中央設置一直徑9 cm,高28 cm的深色平臺,平臺頂部位于水面下1.5 cm處。訓練測試期間水迷宮外參照物不變。訓練過程持續5 d,以四個標志點作為入水點,將大鼠放入池中,記錄所有大鼠游至平臺所用時長,若2 min內未找到平臺,將其引至平臺,潛伏期記為120 s。所有大鼠上臺后均停留30 s,隨后將其從不同的標志點放入水中再次檢測。連續測試4 d,第5天撤去水中平臺,將大鼠從池壁放入水中,記錄1 min內大鼠穿越原平臺位置次數。
1.2.4 癲癇發作情況:對3組癲癇模型大鼠進行觀察,記錄3組大鼠驚厥潛伏期、癲癇發作頻率以及每次發作持續時間,并進行組間比較。
1.2.5 大鼠海馬區形態學觀察檢測:所有大鼠樣本在實驗及各項目檢測完成后均斷頭取腦,冠狀切取視交叉4 mm腦組織,使用濃度為4%的多聚甲醛固定2 d,用石蠟包埋,然后常規腦組織切片,切片厚度約為5 μm,通過硫堇染色對大鼠的海馬區形態進行觀察,并用高倍的光學顯微鏡對海馬CA1、CA3區每1 mm段內的胞核飽滿、細胞膜完整、核仁清晰的錐體細胞情況進行觀察統計。
1.2.6 標本采集及大鼠海馬組織Caspase-3、Hcy水平檢測:用手術刀割取所研究大鼠海馬區組織,大小為1 cm×1 cm,保存在-50 ℃的冰箱中。使用前1 d取出,在5 ℃的環境中冰浴3 min后,用離心機以2 500 r/min的轉速分離,取上清液,保存至-50 ℃的冰箱中。采用高效液相色譜法,將待測的標本注入在色譜柱中,在壓力下進行固定相移動,經過固定相與待測標本中不同物質相互作用,物質會依次的離開色譜柱,應用檢測器捕捉物質信號,嚴格按照高效液相色譜儀說明書上的操作步驟進行,對比分析所測的Caspase-3、Hcy水平。
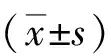
2 結果
2.1癲癇模型建立情況使用30只大鼠進行建模,建模成功24只,癲癇發作期間表現為陣發性肢體震顫、呼吸深且快,出現濕狗狀抖動,站立不穩,并伴隨陣發性抽搐、口吐白沫,興奮性極高。
2.2大鼠行為學觀察
2.2.1 4組大鼠空間學習記憶能力比較:如表1所示,模型組大鼠逃避潛伏期時長明顯長于正常組、奧拉西坦低劑量組及奧拉西坦高劑量組,且奧拉西坦高劑量組大鼠逃避潛伏期時長短于奧拉西坦低劑量組,差異有統計學意義(P<0.05);模型組大鼠穿越平臺次數明顯少于正常組、奧拉西坦低劑量組及奧拉西坦高劑量組,且奧拉西坦高劑量組大鼠穿越平臺次數多于奧拉西坦低劑量組,差異有統計學意義(P<0.05)。
2.2.2 3組癲癇大鼠驚厥潛伏期及癇樣發作情況比較:如表2所示,模型組大鼠驚厥潛伏期明顯短于奧拉西坦低劑量組及奧拉西坦高劑量組,且奧拉西坦高劑量組大鼠驚厥潛伏期明顯長于奧拉西坦低劑量組,差異有統計學意義(P<0.05);模型組模型大鼠癲癇持續時間及發作頻率均顯著高于奧拉西坦低劑量組及奧拉西坦高劑量組,且奧拉西坦高劑量組大鼠癲癇持續時間及發作頻率均低于奧拉西坦低劑量組,差異有統計學意義(P<0.05)。
2.3大鼠海馬結構形態學觀察如圖1所示,正常組和奧拉西坦高劑量組大鼠對側海馬無明顯損傷,海馬CA1、CA3區及齒狀回細胞無缺失現象,形態完整,排列整齊,胞核飽滿,核仁清晰,細胞有凸起且齒狀回神經元呈帶狀分布,無苔狀纖維發芽情況;模型組大鼠海馬區域均可見較明顯的組織損傷,海馬CA1、CA3區及齒狀回排列紊亂、細胞疏松、細胞形態由正常的多角形變為三角形或者不規則圖形,殘留錐體細胞周圍能夠見到較多的細胞碎片,且伴有膠質細胞浸潤,苔狀纖維發芽明顯;低劑量奧拉西坦組大鼠海馬區損傷明顯少于模型組,排列較為緊密有序,且齒狀回無明顯神經元缺失狀況,有輕微苔狀纖維發芽情況。
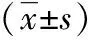
表1 4組大鼠空間學習記憶能力比較
注:與正常組相比,△P<0.05;與模型組相比,*P<0.05;與奧拉西坦低劑量組相比,#P<0.05
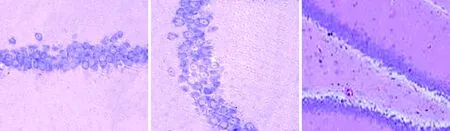
正常組C1區 正常組C3區 正常組齒狀回
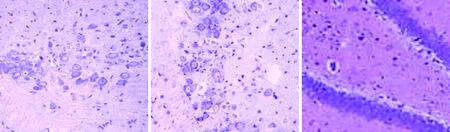
模型組C1區 模型組C3區 模型組齒狀回
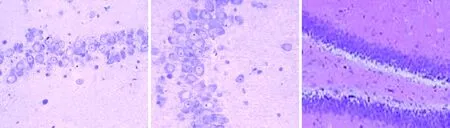
低劑量組C1區 低劑量組C3區 低劑量組齒狀回
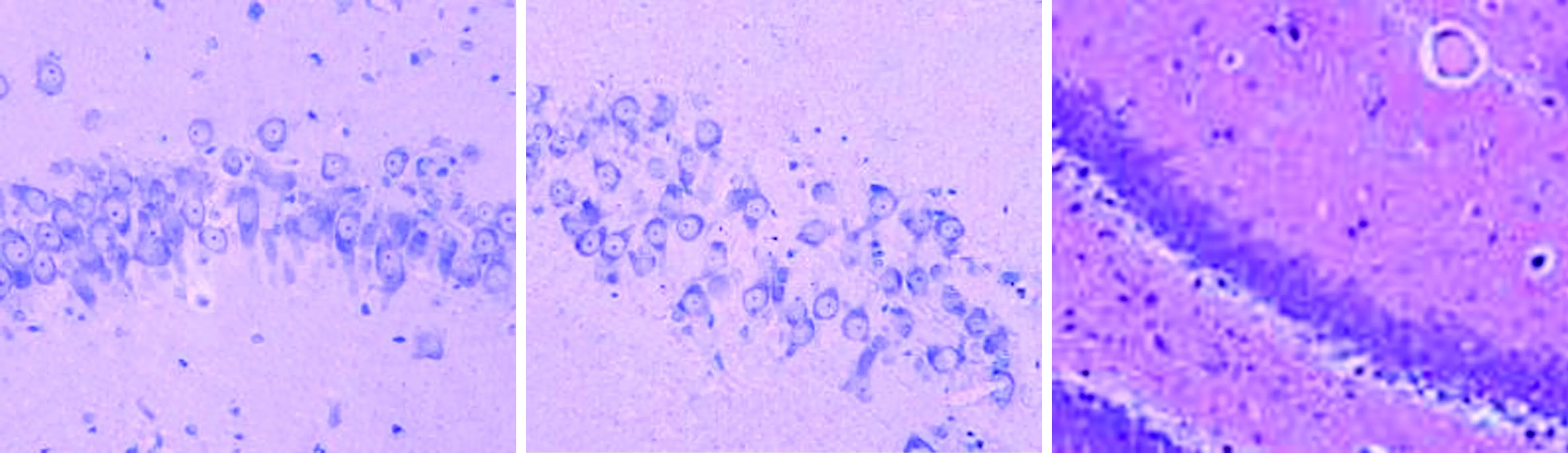
高劑量組C1區 高劑量組C3區 高劑量組齒狀回圖1 不同組別大鼠海馬結構形態學觀察(×200)Figure 1 Morphological observation of hippocampal formation in different groups of rats(×200)
2.4奧拉西坦對癲癇模型大鼠Caspase-3、Hcy水平的影響如表3所示,3組癲癇模型大鼠Caspase-3、Hcy水平與正常組相比,差異有統計學意義(P<0.05)。正常組大鼠Caspase-3、Hcy水平顯著低于模型組和奧拉西坦組,模型組Caspase-3、Hcy水平顯著高于奧拉西坦2組,差異有統計學意義(P<0.05);奧拉西坦高劑量組Caspase-3、Hcy水平低于奧拉西坦低劑量組,差異有統計學意義(P<0.05)。
3 討論
癲癇是一種慢性神經系統疾病,具有長期反復發作的特點,由于機體大腦神經元的異常突發性放電所導致的短暫性大腦功能障礙,同時也是人體發作性意識喪失的原因[10-11]。患有癲癇的患者在一定程度上會伴認知功能障礙,但造成這種認知功能障礙的原因目前還無準確性的研究結論[12-13]。
一直以來,人們對于癲癇發病機制的研究一直使用動物模型進行實驗,戊四氮(PTZ)是一種中樞神經系統興奮藥物,依據戊四氮的藥代動力學特點,可在短時間內使動物產生抽搐,而且這種抽搐的持續時間比較短,還可以自動停止,但能迅速使癲癇狀態達到高峰[14-15]。用戊四氮作為一種致癇藥物,使機體在導致癲癇后不會對自身的局部腦部組織造成破壞,而且還不會造成神經元的損傷和壞死,有利于對癲癇腦組織形態學的觀察,所以采用戊四氮致癇的動物模型是非常理想的動物實驗模型[16-17]。
本研究對癲癇大鼠采用奧拉西坦進行治療取得較好抗癲癇效果。奧拉西坦是一種合成的羥基氨基丁酸環狀衍生物,臨床中主要適用于腦損傷以及腦損傷引起的記憶功能障礙和神經功能缺失等[18-19]。奧拉西坦能夠穿過血腦屏障,能夠分布在機體的海馬區、紋狀體、中隔區以及皮層區中,主要作用于門冬氨酸受體,可以通過膽堿能系統對蛋白激酶C產生激動作用,發揮改善腦組織能量代謝的作用,對神經功能缺損機體的定向力、大腦認知、記憶力以及抽象概括力作出有效改善[20-21]。奧拉西坦可以聚集未受損的腦組織進行重新組織和重建,從而恢復機體神經功能[22]。本研究通過Morris水迷宮對癲癇大鼠學習記憶能力進行測試,結果顯示,在奧拉西坦作用下,癲癇大鼠學習記憶能力有顯著增強,且隨著奧拉西坦劑量的增加,增強效果更明顯。本研究還對癲癇大鼠驚厥潛伏期、持續時間以及發作頻率進行檢測,結果顯示,在奧拉西坦的作用下,癲癇大鼠驚厥潛伏期明顯較短,發生頻率以及持續時間更少,而且隨著奧拉西坦劑量的增加,癲癇大鼠的發作潛伏期延長,發生頻率以及持續時間明顯減少,說明奧拉西坦對大鼠癲癇癥狀具有一定的抑制作用。
同型半胱氨酸(Hcy)屬于一種興奮性氨基酸[23],同型半胱氨酸由于過度的聚集會引起神經細胞興奮性增加,對機體神經細胞造成損害,且同型半胱氨酸在癲癇疾病的發病中發揮非常重要的作用。同型半胱氨酸作為一種興奮性物質[24],能夠刺激N-甲基-D-天門冬氨酸受體,使神經元發揮毒性作用,造成機體神經功能的損害[25-26]。同型半胱氨酸不僅可以引起多系統的代謝毒作用,還以對癲癇癥狀起到加重的作用[27-28]。動物實驗表明,同型半胱氨酸能夠活化致癲灶[29],致使局灶性的癲癇發作,且同型半胱氨酸的高水平表達能夠改變皮層腦電圖,導致機體全身抽搐[30-31]。本研究中,癲癇大鼠模型在經過治療后的同型半胱氨酸水平明顯降低,而高劑量的用藥治療方式能夠更加顯著地對其水平產生抑制作用,說明在經過奧拉西坦治療后,癲癇大鼠本身的同型半胱氨酸水平從高水平降低,減少了神經功能的損傷,改善了癲癇癥狀的產生,且用藥的使用劑量可以稍微增加以提高治療效果,與其他學者[32-33]的研究結果一致。Caspase-3是Caspase家族一種核心蛋白酶[34],能夠介導細胞凋亡,也稱死亡蛋白酶,在哺乳動物細胞凋亡中起到關鍵作用[35]。激活Caspase-3能夠使細胞質、細胞核以及細胞骨架中的重要蛋白質降解失活,使蛋白酶級聯反應被放大,從而引起細胞的凋亡[36]。相關研究表明,采用抗癲癇藥物對癲癇對象進行干預后,Caspase-3的表達水平明顯下降,說明Caspase-3在癲癇過程中起重要作用[37]。本研究中,經奧拉西坦治療后的大鼠Caspase-3水平降低,說明奧拉西坦對Caspase-3的功能產生較為明顯抑制作用,減少了神經細胞的凋亡,與丁緒平等[19]研究結論一致。
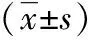
表2 3組癲癇模型大鼠驚厥潛伏期及癇樣發作情況比較
注:與模型組相比,*P<0.05;與奧拉西坦低劑量組相比,#P<0.05
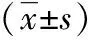
表3 4組大鼠Caspase-3、Hcy水平比較
注:與正常組相比,△P<0.05;與模型組相比,*P<0.05;與奧拉西坦低劑量組相比,#P<0.05
奧拉西坦能夠對癲癇起到很好的抑制作用,延長癲癇的發作時間,減少發病次數,且能夠降低Hcy和Caspase-3的表達水平,保護機體神經功能不受損傷。

