2016-2018年廣州市H6亞型禽流感病毒外環(huán)境分離株HA基因遺傳特征分析
曹 藍(lán),李魁彪,魯恩潔,陳藝韻,劉艷慧,夏 丹,狄 飚
禽流感病毒屬于正粘病毒科流感病毒屬A型流感病毒,根據(jù)病毒表面抗原血凝素(HA)和神經(jīng)氨酸酶(NA)的不同,分為不同亞型:H1~H16,N1~N9[1]。H6亞型禽流感病毒屬于低致病性禽流感病毒,禽類感染后常表現(xiàn)為輕微臨床癥狀或無臨床癥狀。1965年首次從火雞體內(nèi)分離到H6亞型禽流感病毒以來,該亞型病毒不斷地在野禽和家禽體內(nèi)分離到。研究顯示,我國早期H6亞型禽流感病毒主要為H6N1和H6N2[2],近期主要流行亞型為H6N6和H6N2[3],同時(shí)其流行和傳播呈上升趨勢(shì),是我國南方地區(qū)家禽常見的禽流感病毒亞型之一[4]。一方面H6亞型禽流感病毒可以為人感染H5亞型禽流感病毒提供基因骨架,進(jìn)而增加禽流感病毒跨物種傳播風(fēng)險(xiǎn)[5],另一方面H6亞型禽流感病毒可以直接感人,具有突破種間屏障而感染哺乳動(dòng)物甚至感染人的潛能[6]。當(dāng)前我國家禽中H6與H5、H7、H9亞型共流行,增加了不同禽流感病毒重組的復(fù)雜性。研究發(fā)現(xiàn),HA蛋白受體結(jié)合位點(diǎn)變異在禽流感病毒跨宿主傳播中發(fā)揮了重要作用[6]。本研究以廣州地區(qū)2016-2018年外環(huán)境監(jiān)測(cè)分離的H6亞型禽流感病毒為研究對(duì)象,分析HA基因變異和進(jìn)化特點(diǎn),進(jìn)而監(jiān)測(cè)廣州地區(qū)H6亞型禽流感病毒跨物種傳播風(fēng)險(xiǎn)。
1 材料與方法
1.1樣本來源 根據(jù)廣州市外環(huán)境禽流感病毒監(jiān)測(cè)方案,在禽類生鮮市場(chǎng)、活禽肉菜市場(chǎng)、批發(fā)市場(chǎng)、家禽規(guī)模養(yǎng)殖場(chǎng)(戶)或散養(yǎng)戶集中地區(qū)和野生禽鳥棲息地等五類場(chǎng)所中,隨機(jī)選取糞便、飲水、污水、籠具、刀具、地面、稱、脫毛機(jī)等不同類型外環(huán)境標(biāo)本并于4 ℃保存,在24 h內(nèi)送至實(shí)驗(yàn)室于-80 ℃冰箱保存?zhèn)溆谩?016-2018年的監(jiān)測(cè)標(biāo)本中有6份標(biāo)本經(jīng)熒光定量RT-PCR檢測(cè)為A型、H6亞型禽流感病毒陽性,H5、H7和H9亞型禽流感病毒陰性,檢測(cè)試劑盒購于江蘇碩世生物科技股份有限公司。
1.2病毒分離 陽性標(biāo)本進(jìn)行10 000 g離心2 min后取上清,抗生素處理后接種9~10 d齡SPF雞胚。37 ℃培養(yǎng)2~3 d后,收獲接胚尿囊液,通過血凝實(shí)驗(yàn)記錄病毒滴度,血凝陽性毒株再一次經(jīng)熒光定量RT-PCR檢測(cè)為A型、H6亞型禽流感病毒陽性,H5、H7和H9亞型禽流感病毒陰性。
1.3序列測(cè)定 應(yīng)用Oligo 6軟件設(shè)計(jì)H6亞型禽流感病毒HA基因全長擴(kuò)增引物,引物由華大基因合成。通過RT-PCR方法擴(kuò)增HA基因,將陽性鑒定產(chǎn)物送至廣州華大基因公司,通過ABI 3730進(jìn)行病毒基因一代測(cè)序。
1.4序列分析 以2013年臺(tái)灣分離的人源毒株A/Taiwan/2/2013(H6N1)和近年H6亞型病毒流行株HA基因作為比較基因,應(yīng)用DNA Star7.1軟件拼接HA基因序列并對(duì)序列進(jìn)行同源性分析,用MegAlign軟件比對(duì)受體結(jié)合位點(diǎn)和糖基化位點(diǎn)變異情況。使用MEGA 4.0軟件,以HA基因ORF(Open Reading Frame)為基本單元,從GISAID(Global Initiative on Sharing All Influenza Data)數(shù)據(jù)庫下載相關(guān)參考序列,繪制HA基因系統(tǒng)進(jìn)化樹。繪制方法為Neighbor-joining法(參數(shù)設(shè)置為1 000 replications)及Maximum composite likelihood model比對(duì)核苷酸序列。
2 結(jié) 果
2.1同源性分析 6株病毒HA基因核苷酸同源性在81.0%~99.1%之間,分離株HA蛋白氨基酸同源性在81.3%~99.4%之間,分離株核苷酸最大相似性毒株見表1。
表1 2016-2018年廣州H6亞型禽流感病毒HA基因最大相似性毒株
Tab.1 Viruses of maximum similarity with HA gene of H6 subtype avian influenza viruses in Guangzhou from 2016 to 2018

毒株名稱最大相似性毒株相似度/%A/environment/2016B1395/2016A/duck/Jiangxi/262/2013(mixed)97A/environment/2017NX25557/2017A/duck/Ganzhou/GZ151/2016(H6N6)99A/environment/2018XN03891/2018A/duck/Ganzhou/GZ151/2016(H6N6)98A/environment/20180467/2018A/duck/Ganzhou/GZ151/2016(H6N6)98A/environment/20180518/2018A/duck/Ganzhou/GZ151/2016(H6N6)98A/environment/2018XN13565/2018A/pigeon/Guangxi/158/2014(H6N2)97
2.2分子特征分析 有研究表明,HA裂解位點(diǎn)附近具有4個(gè)以上連續(xù)的堿性氨基酸插入是高致病性禽流感病毒重要的分子標(biāo)志[7],本研究的6株毒株的裂解位點(diǎn)位于第345位和第346位氨基酸之間,且裂解位點(diǎn)序列相對(duì)保守,沒有出現(xiàn)變異,只在第345位有1個(gè)堿性氨基酸,呈現(xiàn)為低致病性禽流感病毒分子特點(diǎn)。HA蛋白第226位和228位是禽流感病毒重要的受體結(jié)合位點(diǎn),本研究中6株毒株均為226Q和228G,即傾向與禽類呼吸道細(xì)胞受體結(jié)合,此外A/environment/2018XN13565/2018毒株出現(xiàn)E190T變異。H6亞型禽流感病毒HA蛋白共有8個(gè)糖基化位點(diǎn),其中A/environment/2016B1395/2016毒株在183位出現(xiàn)糖基化位點(diǎn)缺失,詳見表2。
表2 2016-2018年廣州H6亞型禽流感病毒HA基因分子特征
Tab.2 Molecular characteristics of HA gene of H6 subtype avian influenza viruses in Guangzhou from 2016 to 2018
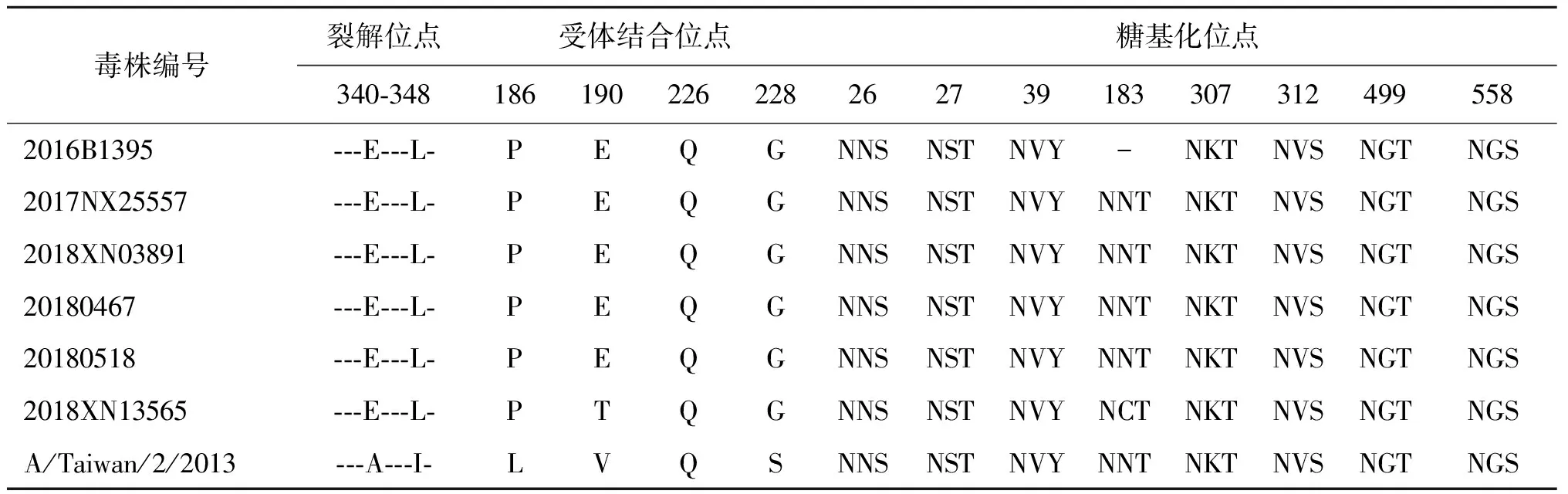
毒株編號(hào)裂解位點(diǎn)受體結(jié)合位點(diǎn)糖基化位點(diǎn)340-3481861902262282627391833073124995582016B1395---E---L-PEQGNNSNSTNVY-NKT NVSNGTNGS2017NX25557---E---L-PEQGNNSNSTNVYNNTNKT NVSNGTNGS2018XN03891---E---L-PEQGNNSNSTNVYNNTNKT NVSNGTNGS20180467---E---L-PEQGNNSNSTNVYNNTNKT NVSNGTNGS20180518---E---L-PEQGNNSNSTNVYNNTNKT NVSNGTNGS2018XN13565---E---L-PTQGNNSNSTNVYNCTNKT NVSNGTNGSA/Taiwan/2/2013---A---I- LVQSNNSNSTNVYNNTNKT NVSNGTNGS
2.3遺傳進(jìn)化分析 本研究中2016-2018年5株毒株歸屬于歐亞譜系內(nèi)的ST2853-like分支,該分支內(nèi)流行毒株分離地的不同,又形成2個(gè)小分支,其中A/environment/2016B1395/2016毒株與華東地區(qū)流行毒株親緣關(guān)系相近,其余4株毒株與華南地區(qū)流行毒株親緣關(guān)系相近。而2018年另有一毒株(A/environment/2018XN13565/2018)歸屬于歐亞譜系內(nèi)的ST339-like分支,見圖1。
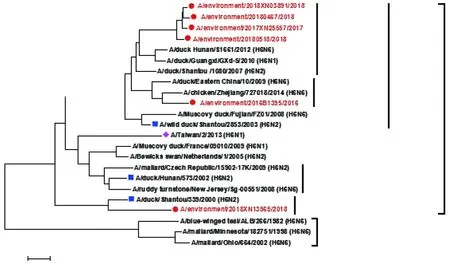
注:“●”代表2016-2018年廣州外環(huán)境分離株;“■”代表不同進(jìn)化分支代表株;“◆”代表人源毒株圖1 2016-2018年廣州H6亞型禽流感病毒HA基因遺傳進(jìn)化分析Fig.1 Genetic evolution analysis of HA gene of H6 subtype avian influenza viruses in Guangzhou from 2016 to 2018
3 討 論
1997年出現(xiàn)首例人感染H5N1禽流感病例,研究發(fā)現(xiàn)H6N1的7個(gè)基因片段與該H5N1病毒高度同源,推測(cè)H6N1是H5N1的前體病毒,而同樣在2014年我國四川出現(xiàn)的首例人感染H5N6禽流感病例中發(fā)現(xiàn),H5N6病毒NA基因即是與H6N6病毒重組而來[8],提示說明H6亞型禽流感病毒可以通過重組而增加病毒的跨物種傳播風(fēng)險(xiǎn),以及H6亞型禽流感病毒與H5亞型禽流感病毒之間發(fā)生自然重組的普遍性,推測(cè)H5Nx流行株的 NA亞型與H6Nx的NA亞型流行有關(guān)。因此當(dāng)前流行的H5N6病毒,是否會(huì)繼續(xù)以H6Nx為病毒骨架,進(jìn)一步重組產(chǎn)生新型H5Nx病毒,需要特別關(guān)注。活禽市場(chǎng)是禽流感病毒流行和傳播的重要場(chǎng)所,Peng等[9]監(jiān)測(cè)研究顯示,2012-2016年我國家禽中H6亞型禽流感病毒的流行呈上升趨勢(shì)。因此開展H6亞型禽流感病毒流行情況及其NA亞型分布情況監(jiān)測(cè),對(duì)監(jiān)測(cè)新型H5Nx的出現(xiàn)及禽流感病毒跨種間傳播具有一定的預(yù)警意義。
早在2009年的研究報(bào)道顯示,H6亞型禽流感病毒可以人工感染小鼠和雪貂[10-11],2011年我國廣東分離到豬源H6N6禽流感病毒[12],特別是2013年臺(tái)灣報(bào)道了首例人感染H6N1禽流感病毒病例[13],血清學(xué)研究也顯示,2007年在廣西健康人群中檢測(cè)到了H6亞型禽流感病毒抗體[14],上述研究均提示H6亞型禽流感病毒具有突破種間屏障直接感染哺乳動(dòng)物甚至感染人的潛能,這對(duì)公共衛(wèi)生構(gòu)成嚴(yán)重威脅。進(jìn)一步研究顯示,HA蛋白G228S突變?cè)黾恿薍6N1禽流感病毒與人唾液酸受體的結(jié)合能力,這是H6亞型禽流感病毒感染人的重要分子基礎(chǔ)[6],此外也與HA蛋白受體結(jié)合位點(diǎn)P186L突變有關(guān)。本研究中,2016-2018年分離株HA基因與人源A/Taiwan/2/2013(H6N1)毒株同源性差異較大(核苷酸同源性在82.8%~83.4%之間),基因比對(duì)顯示大部分分離株與廣東地區(qū)H6N6亞型禽源病毒基因相似度最高。但2016-2018年廣州分離株之間同源性差異也變化較大,最大同源性高達(dá)99.1%,最小同源性僅為81.0%,說明雖然近年來廣州地區(qū)H6毒株尚為禽源本地化病毒,也未監(jiān)測(cè)到與2013年臺(tái)灣人源H6N1病毒基因同源的相似病毒存在,但HA基因已出現(xiàn)較大變異,提示持續(xù)開展H6亞型禽流感病毒基因進(jìn)化監(jiān)測(cè)的必要性。
進(jìn)化分析上,廣州H6亞型禽流感病毒環(huán)境分離株與人源A/Taiwan/2/2013(H6N1)位于不同進(jìn)化分支。2018年之前廣州分離株遺傳進(jìn)化上相對(duì)單一,均屬于ST-2853 like流行分支,與以往報(bào)道一致[15-16],但由于禽流感病毒基因變異較快,在ST-2853 like分支內(nèi),2016年毒株與華東地區(qū)流行毒株親緣較近,2017-2018年毒株與華南地區(qū)流行毒株親緣較近,出現(xiàn)一定的進(jìn)化差異。從2018年開始,廣州分離株保持在ST2853-like分支繼續(xù)進(jìn)化的基礎(chǔ)上,又出現(xiàn)ST339-like新流行分支病毒。
基因分子變異上,H6亞型禽流感病毒HA蛋白只有1個(gè)堿性氨基酸插入,屬于低致病性禽流感病毒,雖對(duì)禽類呈現(xiàn)低致病性,但臨床癥狀上難于發(fā)現(xiàn),更有利于病毒的潛在傳播,提示未來一段時(shí)間H6亞型禽流感病毒仍然是活禽市場(chǎng)常見流行的禽流感病毒亞型之一。本研究毒株中HA蛋白受體結(jié)合位點(diǎn)相對(duì)保守,尚未出現(xiàn)重要變異,為典型的禽類受體位點(diǎn)特點(diǎn),推測(cè)發(fā)生跨種間傳播的風(fēng)險(xiǎn)較低。
利益沖突:無

