精準脾切除術在乙肝肝硬化、肝豆狀核變性合并脾功能亢進治療中的應用觀察
胡高斌,于慶生,2,潘晉方,2,沈毅,2,張琦,2,王振,2
(1安徽中醫藥大學第一附屬醫院,合肥230031;2安徽中醫藥科學院中醫外科研究所)
脾是一種淋巴器官,在先天和后天的免疫中都發揮著至關重要作用[1]。脾切除術廣泛應用于脾破裂、游走脾(異位脾)、脾局部感染或腫瘤、囊腫、肝內型門靜脈高壓癥合并脾功能亢進等引起充血性脾腫大等疾病。傳統脾切除術對腹腔干擾較大,術后腸道功能恢復慢,并且術后切口疼痛明顯,各類型并發癥發生率較高。近年,隨著手術技術的提高以及臨床影像技術的增強,精準外科理念在臨床應用中越來越受到重視。據文獻[2]報道,精準脾切除術可以明顯減少術中出血的危險,改善患者的生存質量,是一種安全且效果良好的手術,但其對術后并發癥、術前準備、術后處理方面沒有進行詳細描述。本研究中,我們秉承著精準外科的理念,在傳統脾切除的基礎上,創新性地應用精準脾切除術治療乙肝肝硬化、肝豆狀核變性合并脾功能亢進患者105例,取得較好效果,現報告如下。
1 資料與方法
1.1 臨床資料 選擇2005年1月~2018年7月安徽中醫藥大學第一附屬醫院普外科住院的乙肝肝硬化、肝豆狀核變性合并脾功能亢進患者177例。納入標準:肝功能Child-Pugh分級A~B級,非手術治療無效,無其他系統嚴重疾病,無手術禁忌證者;排除標準: 臨床資料不全,凝血功能嚴重障礙,肝功能Child-Pugh分級為C級者。根據脾切除的術式分為精準組和傳統組。精準組105例,男61例、女44例,年齡10~69(32.18±13.73)歲,肝豆狀核變性[3]84例、乙肝肝硬化23例,肝功能分級[4]Child-Pugh A級68例、Child-Pugh B級37例,脾功能亢進分級[5]輕度13例、中度27例、重度65例。傳統組72例,男50例、女22例,年齡10~58(25.78±12.17)歲,肝豆狀核變性56例、乙肝肝硬化16例,肝功能分級Child-Pugh A級55例、Child-Pugh B級17例,脾功能亢進分級:輕度3例、中度27例、重度42例。兩組基線資料有可比性。
1.2 脾切除方法 精準組采用精準脾切除術:術前準備:肝功能準備:應用青霉胺和二巰基丙磺酸鈉強力驅銅6個療程(6 d為一個療程);應用極化液、支鏈氨基酸等保肝藥物,根據肝功能情況再酌情應用異甘草酸鎂、谷胱甘肽、多烯磷脂酰膽堿和門冬氨酸鳥氨酸等藥物。凝血功能準備:術前1周補充維生素K1,酌情應用血漿調節凝血功能至正常或接近正常水平,對于經術前準備凝血功能仍不正常者,術前30 min靜注凝血酶原復合物300~500 U。手術方法:首先結扎脾動脈,并應用脾血回輸技術使脾臟處于無血狀態;然后在無血狀態下逐一結扎脾臟2~3級血管,以期減少術中創傷和出血,術后門靜脈系統血栓形成、發熱、胰漏等并發癥發生。具體步驟如下:先小切口進腹,進腹后探查脾臟,根據脾臟大小適當延長切口;分離胃結腸和胃脾韌帶,顯露和結扎脾動脈;自體脾血回輸:脾動脈結扎以遠脾動脈內注入生理鹽水500 mL,再注射腎上腺1 mg;拖出脾臟;無血狀態下逐一結扎脾臟上下端2~3級血管;銳性游離脾腎韌帶背葉,鈍性分離出胰腺尾部;銳性游離脾腎韌帶前葉,分別結扎動、靜脈2級分支,切除脾臟;切除創面止血和漿膜化縫合。術后密切監測患者各項指標,及時處理脾切除術后各項并發癥。傳統組采用傳統脾切除術:完善各種常規術前準備,達到手術指征后手術。常規開腹,先盡量游離、切斷脾胃韌帶和脾結腸韌帶, 脾動脈若顯露明顯可游離出脾動脈、結扎, 無需脾動脈離斷。托起脾臟, 電刀切開或者銳性分離脾周粘連。托出脾臟到切口外, 用三鉗法處理脾蒂, 并在靠近脾門位置將脾蒂切斷,大塊縫扎處理脾蒂殘端。脾窩部位做縫扎或電凝止血處理, 常規放置引流,常規術后補液、抗感染、護肝、止血等治療。
1.3 觀察指標及其判定方法 手術時間:指從開皮到切口關閉的時間。術中出血量[6]:選用目前在臨床上普遍運用的目測法,觀察吸引瓶、手術單、無菌巾及手術紗布的吸血量從而估算出實際出血量。由術者和麻醉師共同評估負壓瓶中的出血量結果×2;術中紗布的出血量按大紗每塊濕透50 mL,小紗每塊濕透30 mL估算、輔料的出血量按面積法估算,累計計算術中出血總量。術后引流量:觀察并記錄插管到拔管后的引流量。術后并發癥:①門靜脈系統血栓形成:術前、術后第7、14天,數字彩色超聲波診斷儀(Prosound α6),專人檢測門靜脈主干及分支、腸系膜上下靜脈、脾靜脈是否有血栓形成。②腹腔出血:主要是通過對術后引流量估測:>200 mL/h,持續3~5 h;2 h內引流管溢血大于500 mL;引流量50~100 mL/h,持續12~24 h,總量大于2 000 mL;引流管溫度接近人體溫度。住院時間:從入院治療到術后康復的全過程。
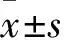
2 結果
精準組手術時間、住院時間分別為(144.5±44.9)min、(33±25)d,傳統組分別為(138.7±133.7)min、(42±25)d,兩組手術時間比較,P=0.675、>0.05,住院時間比較,P=0.000、<0.05;精準組術中出血量、術后引流量分別為(377±402)、(603±613)mL,傳統組分別為(502±592)、(809±1 541) mL,兩組比較,P=0.000、0.018,均<0.05。精準組腹腔出血、發熱、門靜脈血栓分別為22(30%)、60(57.1%)、58例(55.2%),傳統組分別為40(55.6%)、54(75.0%)、56例(77%);兩組比較,χ2分別為22.72、5.941、9.466,P分別為0.000、0.015、0.002。
3 討論
乙肝肝硬化門脈高壓癥常因肝功能衰竭、脾腫大脾功能亢進、出血傾向、食管胃底靜脈叢曲張繼發曲張靜脈破裂致上消化道大出血而危及患者生命,手術行脾臟切除是重要的外科治療方式[7]。據統計,每年因慢性乙型肝炎及其并發病死亡的患者約100萬人。臨床數據[8]表明, 肝硬化代償期患者5年病死率為16%,肝硬化失代償期患者5年病死率為86%。肝豆狀核變性是一種好發于青少年的常染色體隱性遺傳銅代謝障礙疾病,由于定位于13號染色體q14.3上的ATP7B基因突變導致銅轉運障礙,大量銅沉積于基底神經節、豆狀核、肝小葉、腎小管及眼角膜等部位,引起精神認知和錐體外系癥狀,角膜K-F環及不可逆性的肝、腦、腎損害等[9]。本病在我國的發病率遠高于其他國家,且男性多于女性[10],是目前發現的極少數可用藥物驅銅治療控制的神經遺傳病之一。另一方面,當HLD患者發生肝硬化并引發脾功能亢進時,重度的白細胞和PLT減少往往會影響驅銅治療,并嚴重威脅患者的生命。脾切除為治療HLD的有效手術方法[11]。當脾臟因原發或繼發病變需行手術切除時常合并有肝功能儲備不足或不同程度的肝功能減退、出血傾向、嚴重外傷或惡性腫瘤消耗,這導致脾切除后并發癥發生率高[12]。
近年,隨著手術技術的提高以及臨床影像技術的增強,精準的理念在臨床應用中越來越受到重視。然而精準脾切除的臨床研究尚不多見。本研究中,我們在傳統脾切除的基礎上,創新性地推出了精準脾切除的理念,其內容包括術前精心準備、術中精細操作、術后精確處理三個環節。精心的術前準備是順利完成手術的前提和保障,包括術前肝功能準備和凝血功能準備。對于肝硬化門靜脈高壓所致繼發性脾功能亢進患者,應予以術前肝功能分級評估,盡量使術前肝功能恢復到或接近A級。對于凝血功能較差的患者,我們的原則是預防和治療相結合。術中的精細操作是與傳統脾切除術式區分的關鍵所在,傳統脾切除主要行傳統脾血管集束結扎后切除脾臟,此方式重視精細游離脾周韌帶和脾門原位解剖,切除脾臟后,脾床止血難度高[13]。精準脾切除則是先進腹腔后進行脾動脈結扎和脾血自體回輸,然后行脾臟血管的分束分離和結扎,最后脾切除和創面徹底止血。經過脾動脈的結扎和自體回輸,減少了術中出血量,如本研究所示精準組的術中出血量和術后引流量明顯少于傳統組。減少術中出血,有利于減少手術應激及并發癥,加速患者術后的康復,這符合現代快速康復的理念[14]。精準組患者平均住院時間明顯少于傳統組,這也是符合現代快速康復理念的又一佐證。術后的精確處理則是對患者未來生活質量的重要保障,脾切除后并發癥的監測要精準、精細,對于門靜脈血栓形成、脾熱、術后腹腔出血等并發癥要做到及早發現,及早預防。本研究發現,精準組術后血栓形成率(57.1%)小于傳統組54例(75%),但據流行病學調查顯示,脾切除術后門靜脈系統血栓發生率約為22%[15~18],這可能與我們手術的病例數較多和專人影像檢測門靜脈系統血栓有關。精準組術后脾熱發率(57.1%)低于傳統組術后脾熱發生率(75%),同時精準組術后出血率(30%)也小于傳統組(55.6%),這可能與術中結扎了脾動脈,然后在無血狀態下逐一結扎脾臟2~3級血管和充分暴露胰腺尾部有關。相關研究表明,術中減少或避免損傷胰尾,防止胰漏,能減少脾熱的發生[19~21]。
綜上所述,在肝豆狀核變性及乙肝肝硬化合并脾功能亢進的患者中,精準脾切除術具有以下優點:術中出血量低,術后引流量少,術后并發癥率較低、患者康復快、生活質量明顯提高,是值得進一步推廣的脾切除術式。

