索拉非尼治療轉移性腎癌的臨床療效與安全性
秦 軍,武國軍,王福利,秦衛軍,袁建林
(空軍軍醫大學西京醫院泌尿外科,陜西西安 710032)
腎癌發病率占全部腫瘤的3%~5%,在泌尿系統腫瘤中排第3位[1]。其中25%~30%腎癌患者就診時已有遠處轉移[2],即使行根治性腎切除術后,30%患者也會出現轉移復發[3]。而且,腎癌對傳統細胞毒性藥物和激素治療均不敏感。近年來,由于分子靶向藥物的臨床應用,轉移性腎癌患者無進展生存期(progression free survival,PFS)顯著提高,其總體生存期(overall survival,OS)從細胞因子治療時代的12個月提高到分子靶向治療時代的26個月[4]。
索拉非尼是第一個治療轉移性腎癌的多激酶抑制劑,目前用于一線治療及免疫治療失敗患者的二線治療,其療效主要體現在良好的疾病控制率和顯著延長的無進展生存期。本文回顧性分析索拉非尼治療38例轉移性腎癌患者的臨床療效和安全性,同時分析了患者無進展生存期和腫瘤縮小之間的關系,旨在為轉移性腎癌臨床治療提供可借鑒的經驗。
1 資料與方法
1.1病例資料本研究對2012年8月至2014年9月在西京醫院泌尿外科確診的38例轉移性腎癌患者臨床資料進行回顧性分析。其中男性14例,女性24例;年齡27~78歲,中位年齡55歲。38例均經病理證實為腎透明細胞癌,腫瘤TNM分期均為IV期;腫瘤遠處轉移至肺32例,肝3例,骨8例,腹腔淋巴結5例;轉移淋巴結數目1個3例,2個10例,3個22例,4個及以上9例。美國東部腫瘤協作組(Eastern Cooperative Oncology Group,ECOG)體能狀態評分0分者10例,1分者15例,2分者8例,3分者5例。
1.2治療方案38例患者中,12例既往接受過干擾素治療;另有18例行原發腫瘤切除術。治療方案為索拉非尼口服400 mg,2次/d,間隔12 h。給藥前后2 h禁止患者食用高脂食物。根據藥物不良反應等級調整劑量,必要時劑量減少到400 mg/d,然后降至每隔400 mg/2d(隔日),直至停藥。如出現疾病進展,劑量則增至每次600 mg,2次/d。
1.3療效評價采用實體腫瘤療效評價標準(Response Evaluation Criteria in Solid Tumors,RECIST)作為療效判斷標準,并通過CT和MRI測量的腫瘤最大直徑變化來評價治療反應和療效。客觀反應率(objective response rate,ORR)用完全緩解(complete response,CR)和部分緩解(partial response,PR)二者總和占全部患者比例評價。疾病控制率(disease control rate,DCR)用CR、PR和疾病穩定(stable disease,SD)三者總和占全部患者比例評價。以首次服用索拉非尼時間為研究起點,研究終點為死亡或末次隨訪時間,記錄分析OS和PFS。治療后的不良反應事件依據不良事件通用術語標準(Common Terminology Criteria Adverse Events,CTCAE)v3.0對其進行分級。數據統計截止時間內尚存活或中途失訪的患者,以最后一次隨訪日期記錄為截尾數據。
1.4統計分析采用SPSS16.0進行統計分析。用Kaplan-Meier法描述患者生存狀況。采用t檢驗對兩組數據進行分析,以P<0.05為差異有統計學意義。
2 結 果
2.1臨床療效38例患者總體ORR為21.1%,DCR為52.7%。最佳療效為PR,有8例(21.1%);其中1例PR患者為干擾素治療失敗后應用索拉非尼治療12周,胸部CT顯示肺轉移灶明顯縮小,轉移灶數目減少。SD患者12例(31.6%),8例患者轉移灶數量減少;其轉移瘤直徑縮小的為中位數11.25%(5%~25%),與治療前比較有顯著性差異(P<0.05)。疾病進展患者18例(47.4%),其中4例原發灶腫瘤直徑增大>20%,8例出現腹膜后淋巴結轉移,6例發生肺轉移;出現淋巴結或肺轉移的14例患者最終均進展至死亡。截止數據統計結束,16例患者發生死亡(42.1%),14例死于疾病進展,2例死于心肺疾病。38例患者的中位PFS、中位OS分別為50.5周(95%CI:40.3~59.0)和52.5周(95%CI:43.1~61.4,圖1)。進一步分析發現,與20例原發灶未切除患者相比,18例原發灶切除患者口服索拉非尼治療的PFS和OS均顯著延長;而既往使用干擾素治療則對索拉非尼治療療效沒有顯著影響(圖2)。
此外,我們還分析了PFS與腫瘤直徑縮小之間的關系,發現16例PR和SD伴腫瘤縮小的患者中,其輕微腫瘤縮小(25%~50%)和顯著腫瘤縮小(>50%)間的PFS差異并不顯著[(70.58±6.21)dvs.(81.50±2.90)d,P>0.05,圖3]。
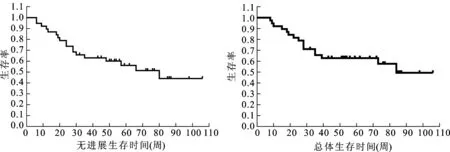
圖1患者疾病無進展生存期(PFS)與總體生存期(OS)
2.2不良反應所有患者在治療前2周均存在不同程度的不良反應,但經對癥治療和減少劑量后可得到緩解。多數不良反應為1~2級,12例(31.6%)為3~4級(表1)。
最常見不良反應包括:手足皮膚反應(hand-foot skin reaction,HFSR)、高血壓、惡心、厭食癥、吞咽困難、疲勞、腹瀉和口腔潰瘍。3~4級毒副反應以高血壓(28.9%)、HFSR(13.2%)、吞咽困難(13.2%)、口腔潰瘍(10.5%)、腹瀉(7.9%)為主。3~4級毒副反應中,高血壓和腹瀉經對癥治療后緩解,口腔潰瘍和吞咽困難癥狀在整個治療過程中持續存在,但程度有所減輕。HFSR癥狀在推薦劑量方案降至400 mg/d后降低,但當劑量調整為400 mg,2次/d時,HFSR又復發;隨著治療的繼續,HFSR癥狀逐漸減輕。實驗室異常包括血紅蛋白減少(23.7%,3~4級占5.3%)和丙氨酸氨基轉移酶水平增加(13.2%);二者變化均是短暫的,很少與臨床表現相關,經過適當的對癥治療后可恢復。
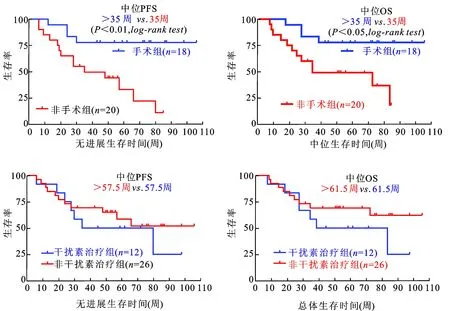
圖2患者疾病無進展生存期(PFS)與總體生存期(OS)
表1索拉非尼治療38例轉移性腎癌的不良反應
38例患者中有8例(21.1%)因發生不良事件而減少藥物劑量,但未觀察到停藥和治療相關的死亡,無住院或治療相關的持久性或嚴重殘疾。導致劑量減少的最常見不良事件是HFSR(7.9%)、吞咽困難(7.9%)和高血壓(5.3%)。
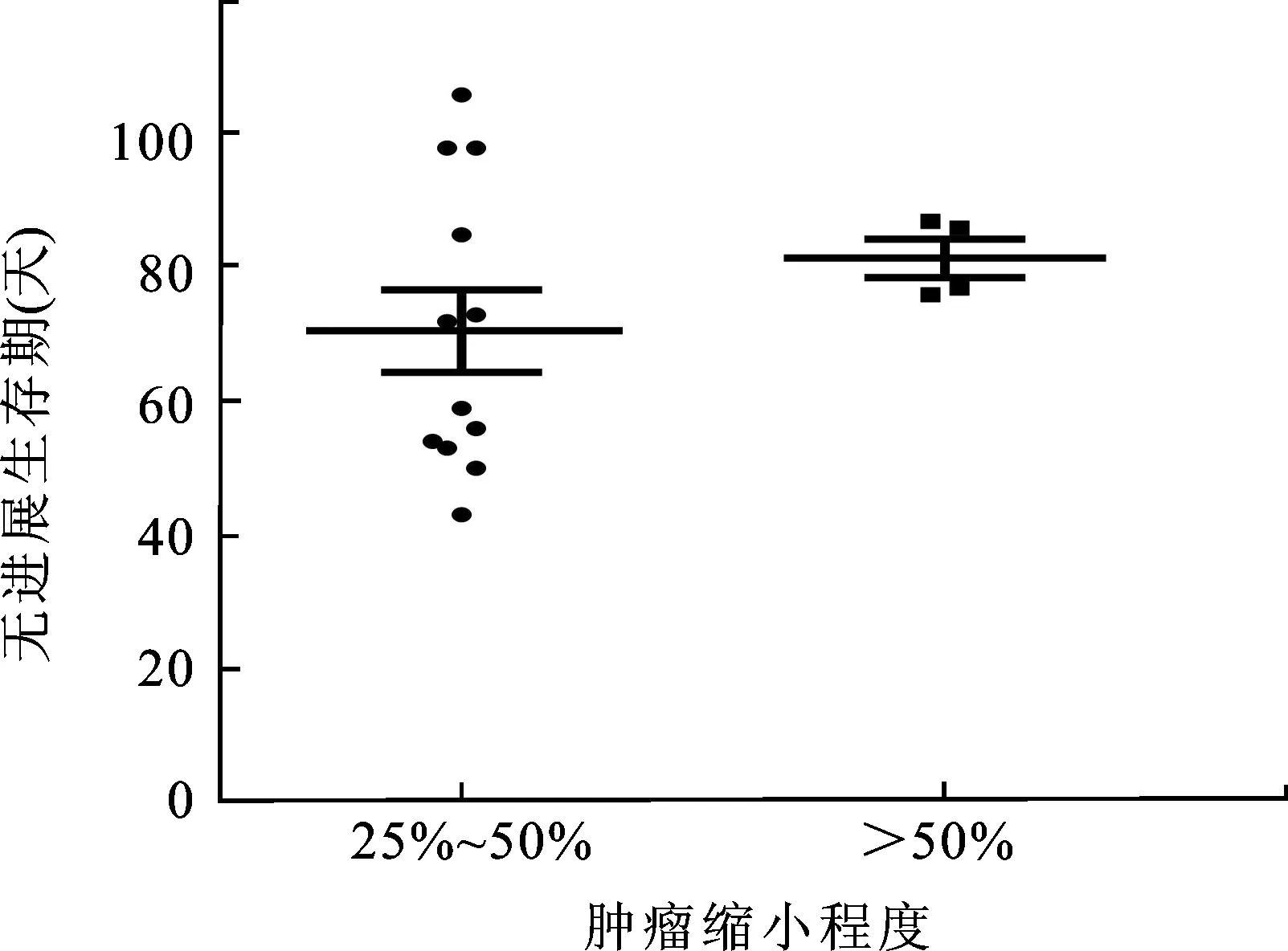
圖3 腫瘤輕微縮小(25%~50%)與顯著縮小(>50%)的患者PFS比較
3 討 論
本組研究結果表明,索拉非尼對既往細胞因子治療失敗的轉移性腎癌有一定的療效,患者中位PFS、OS分別為50.5周和52.5周,與ESCUDIER等[5]報道Ⅲ期臨床試驗和后續擴大準入試驗(EU-ARCCS,NA-ARCCS,AUS1)[6]相比,中位PFS顯著延長;另外,本研究與以往針對中國腎癌患者的數個單中心及多中心研究結果相一致[7-13],這說明索拉非尼對于中國患者PFS的療效優于歐美患者。OS方面,本研究結果與歐美及中國多中心報道均一致,中位OS為13.1~17.8月。我們研究結果顯示,患者對索拉非尼的ORR 為21.1%,DCR為52.7%,均低于歐美及國內多中心報道的結果(>80%)。這可能和本研究隨訪時間較短,患者病灶浸潤及惡性程度更高等因素有關。根據ESCUDIER等[5]研究結果,索拉非尼開始的治療標準建議是作為細胞因子治療失敗后的二線治療 。本研究發現,干擾素治療失敗后進行索拉非尼治療,并不能顯著提高患者的生存期;但是,在手術切除原發灶后使用索拉非尼治療,其療效則顯著高于未切除原發灶組。隨后,索拉非尼又被證明是一種有效的一線治療,189例患者中,一線索拉非尼與一線干擾素治療相比,索拉非尼劑量增加至超過400 mg 2次/d時,其療效顯著提高(PFS:79.4%vs.64.1%)[14]。因此,美國和歐洲醫學腫瘤學學會(European Society for Medical Oncology,ESMO)建議:索拉非尼作為轉移性腎癌的標準二線治療藥物或一線治療備選藥物[3,15]。
本研究結果表明,腫瘤縮小微弱(25%~50%)與縮小顯著(>50%)的患者相比,PFS沒有顯著差異。同樣,Ⅱ期隨機對照試驗也顯示腫瘤縮小25%~50%和縮小>50%的患者之間的PFS沒有差異[16]。從索拉非尼治療的分子機制來看,其對疾病進展的控制似乎與腫瘤大小的減少無關,而與抑制腫瘤血管生成和腫瘤細胞壞死有關。另外,本組中有5例患者(13.2%)其原發腫瘤和肺轉移瘤對索拉非尼治療的反應不同,表現為肺轉移瘤不同程度縮小和數量減少,而原發腫瘤無明顯減少。可能由于原發腫瘤和轉移瘤具有不同的基因/蛋白表達譜和細胞生物學特征,導致了治療反應不同[17]。就索拉非尼治療靶點血管內皮生長因子(vascular endothelial growth factor,VEGF)和血小板衍生生長因子(platelet derived growth factor,PDGF)而言,其在轉移性腫瘤血管中表達明顯高于原發灶,故應用索拉非尼治療時會引起肺轉移瘤縮小和數量減少。
我們研究結果中,索拉非尼的安全性與以往國內的多中心研究結果一致,體現為不良事件類型相似,但發生的級別與頻率不同[7-11]。例如,高血壓發生率高(52.6%vs.21%~36%),腹瀉發生率較低(28.9%vs.33%~63%),而HFSR(76.3%vs.58%~80%)和乏力、厭食、惡心等(39.5%~50%vs.15%~68%)的發生率則相似。患者文化差異和疾病進展程度不同可能是導致不良事件發生率差異的原因。研究表明,HFSR的出現與藥物療效呈正相關,可能是治療效果的相應信號[18]。據報道,腎癌患者中索拉非尼積累越多,HFSR發病率就越高[19]。在我們的臨床實踐中,1~2級HFSR無需治療,3級以上HFSR出現影響手部運動時可給予對癥治療,但通常沒有必要停藥或減少劑量。
高血壓是索拉非尼治療中常見的副作用,發生率在41%~49.7%;且有研究認為,高血壓是索拉非尼抗腫瘤療效的體現[3,20]。因此,索拉非尼治療過程中需定期監測血壓。研究表明,高血壓的發生主要是VEGF抑制,內皮細胞釋放一氧化氮(nitric oxide,NO)減少,內皮通透性降低,血管收縮以及腎素-血管緊張素-醛固酮系統的改變所致。常規抗高血壓治療如血管緊張素轉換酶抑制劑和血管緊張素Ⅱ受體拮抗劑能夠長期有效地控制血壓,此外降低用藥劑量也可恢復血壓。本研究的11例(28.9%)3~4級高血壓患者中,9例采取常規降壓治療,2例采取了減少劑量的治療策略。索拉非尼主要由肝臟細胞色素P-450酶家族重要成員CYP3A4代謝清除,其藥代動力學會受影響此酶功能的藥物影響;索拉非尼與CYP3A4誘導劑共同使用可致其血漿濃度降低,應避免或監測其毒性[20-21]。
本組研究中,5例患者(13.2%)谷丙轉氨酶升高,這一副作用在CHENG等[22]的研究試驗中亦有報道。經治療4周后,患者谷丙轉氨酶升高,經谷胱甘肽和多烯磷脂酰膽堿肝保護治療4周后恢復,治療過程中我們維持了索拉非尼常規劑量。
本研究表明,索拉非尼對于轉移性腎癌患者是一種有效的治療藥物。雖然本研究中沒有出現完全緩解病例,但腫瘤控制率和PFS均較好。對于低ECOG評分或預后較差患者而言,該治療方案耐受性好,安全性亦可接受。盡管新型分子靶向藥物如貝伐珠單抗、帕唑帕尼、依維莫司、阿昔替尼已逐漸應用于臨床,但至少目前索拉非尼仍是不可替代的轉移性腎癌治療藥物。腎癌分子靶向治療藥物的未來發展趨勢,將是依據預測因子(如HRSF、血壓升高)或生物標志物(如血清VEGF水平)選擇對索拉非尼有良好反應的患者進行精準醫療,或序貫使用針對VEGF主要信號通路和針對mTORC1、MET、IL-8次要信號通路的抑制劑或抗體藥物進行聯合治療。

