培養系統思維能力 提高化工流程復習效率
熊建飛 吳利敏
河南
系統思維是把認識對象作為系統,從各要素的性質以及系統和要素、要素和要素、系統和環境之間的相互作用、相互影響中綜合地考查認識對象的一種思維方式。系統思維重視整體思考,同時注意在整體的前提下具體研究解決局部問題。在分析和處理問題的過程中,始終從整體來考慮,在整體觀的指導下,使局部問題得到解決。在進行系統思維時,注意系統內部的結構性,各部分既相對獨立,又相互聯系,從結構方面入手,使思維更清晰。在具體解決局部問題時,抓住關鍵要素,使目標更明確。把所要研究的對象看作一個系統,然后深入系統內部細致分析問題,再跳出系統看系統。
一、從系統思維的角度分析教材

化工流程這類試題“起點高,落點低”,考查的知識點比較分散,都是初、高中教材中出現的比較基礎的知識,其特點比較零散、不系統。針對所考查的知識點,對人教版初高中教材進行系統分析,結果如下表1所示:
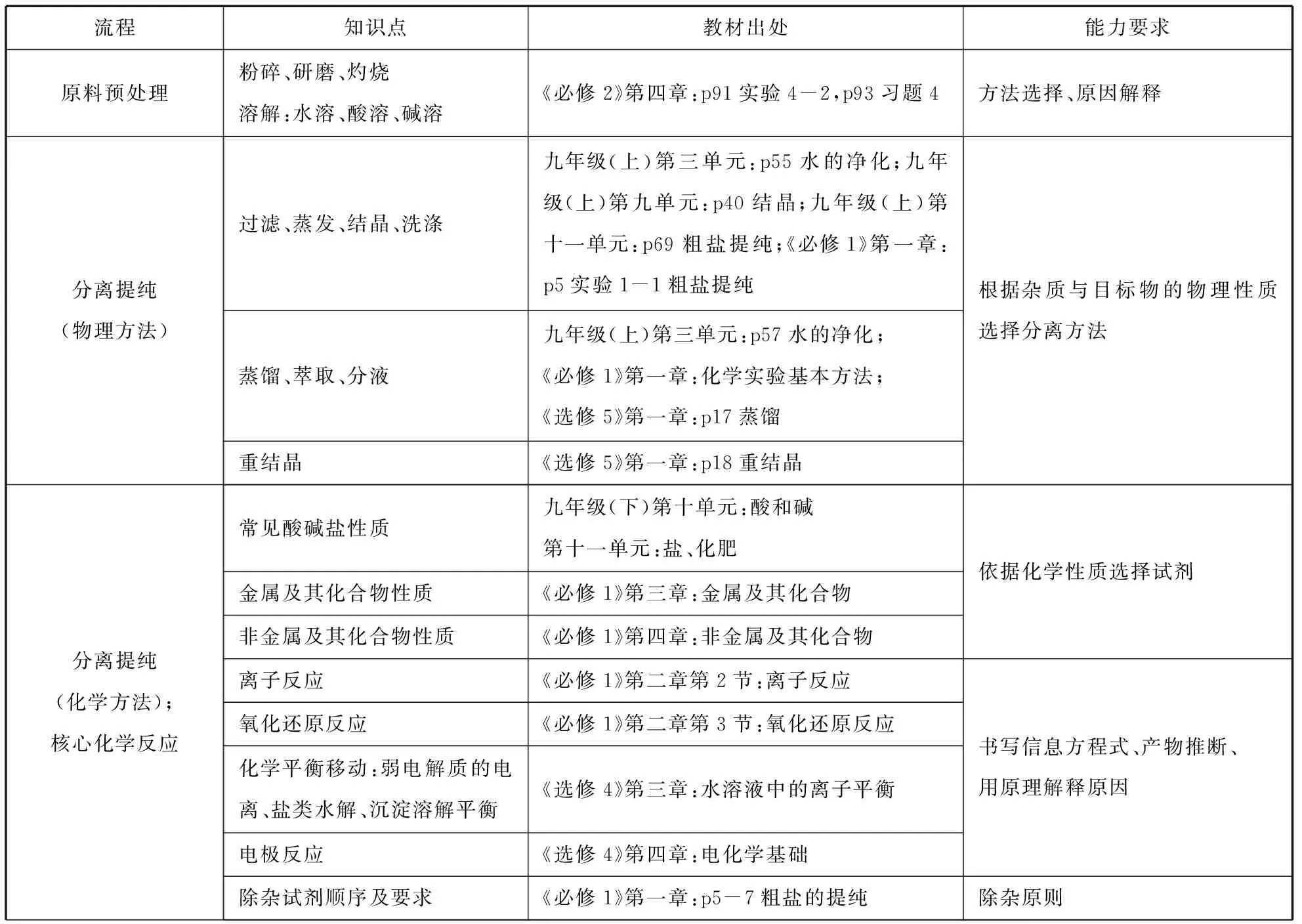
表1 從系統思維的角度分析教材
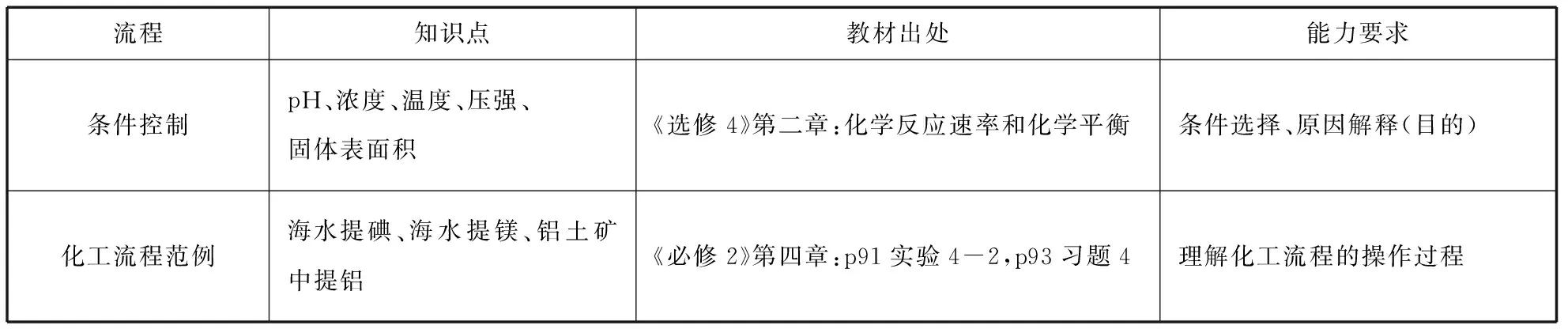
續表
由表1可以看出,化工流程題所涉及的知識點包括九年級(上、下)冊部分內容,《必修1》全冊,《必修2》第四章,《選修4》第二章、第三章、第四章,《選修5》第一章。
二、從系統思維的角度分析化工流程
化工流程的目的是通過一系列的除雜過程獲得最終的產品,我們就可以將整個流程看作是一個系統,而其中的每個步驟即是系統中的部分,核心化學反應和基本實驗操作則可看作是各部分的要素。因此,用系統思維分析化工流程試題具有可行性。
例12015新課標Ⅰ第27題:
硼及其化合物在工業上有許多用途。以鐵硼礦(主要成分為Mg2B2O5·H2O和Fe3O4,還有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)為原料制備硼酸(H3BO3)的工藝流程如圖所示:
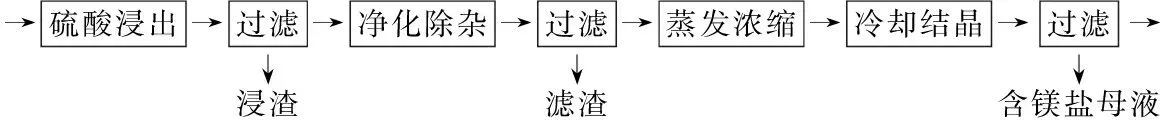
回答下列問題:
(1)寫出Mg2B2O5·H2O與硫酸反應的化學方程式__________。為提高浸出速率,除適當增加硫酸濃度外,還可采取的措施有_________(寫出兩條)。
(2)利用________的磁性,可將其從“浸渣”中分離。“浸渣”中還剩余的物質是________(化學式)。
(3)“凈化除雜”需先加H2O2溶液,作用是________。然后再調節溶液的pH約為5,目的是________。
(4)“粗硼酸”中的主要雜質是________(填名稱)。
(5)以硼酸為原料可制得硼氫化鈉(NaBH4),它是有機合成中的重要還原劑,其電子式為________。
(6)單質硼可用于生成具有優良抗沖擊性能硼鋼。以硼酸和金屬鎂為原料可制備單質硼,用化學方程式表示制備過程:__________。
1.從總體上認識和把握
把整個流程看作一個系統,此題的目的是以鐵硼礦為原料來制備硼酸,從題所給的信息來看,原料中含有較多的雜質,而這些雜質都是要在中間過程中被除去。在除雜的時候要用到多個核心化學反應和分離提純操作,在具體分析每一個步驟時,要始終明確一點:保留目標物質,雜質分步除去,這是所要解決的關鍵問題。
2.深入系統內部細致分析問題
在分析的時候,不能就題論題,要“既看到樹木,又看到森林”。整個流程可以看作一個大系統,而每個步驟可以看作一個小系統,每個小系統既是相對獨立的,又是彼此關聯的。在分析某一個小系統時,既要向前看到上一個小系統含有的雜質,又要向后看到下一個小系統所含的雜質,對比前后減少的雜質即是被此步操作除去的。明確了此步操作的目的后,即可根據已有知識或題中信息作出解答。
將本題分成三個小系統:
系統1. 硫酸浸出和過濾
本系統所涉及的問題為(1)和(2)。

系統2. 凈化除雜和過濾
本系統所涉及的問題為第(3)小問:“凈化除雜”需先加H2O2溶液,作用是__________。然后再調節溶液的pH約為5,目的是__________。
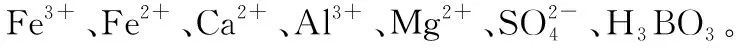
系統3. 蒸發濃縮、冷卻結晶和過濾
本系統所涉及的問題為第(4)小問:“粗硼酸”中的主要雜質是________(填名稱)。
3.跳出系統看系統
化工流程的目的是要得到人們所需要的產品,而所得的產品肯定有它的用途和價值,在用途和價值方面,可以設置一些問題,起到了與其他知識相銜接的作用,如原料利用率的計算、產品純度計算等。在情感態度與價值觀方面,培養學生對化學的正確認識,化學是一把雙刃劍,在給人們提供便利的同時,也帶來了環境問題。如第(5)、(6)小問從硼酸用途的角度來設置問題。

例22018新課標Ⅰ第27題:
焦亞硫酸鈉(Na2S2O5)在醫藥、橡膠、印染、食品等方面應用廣泛。回答下列問題:
(1)生產Na2S2O5,通常是由NaHSO3過飽和溶液結晶脫水制得。寫出該過程發生的化學反應方程式:_________________。
(2)利用煙道氣中的SO2生產Na2S2O5的工藝為
①pH=4.1時,Ⅰ中為___________ 溶液。
②工藝中加入Na2CO3固體,并再次充入SO2的目的是____________________。
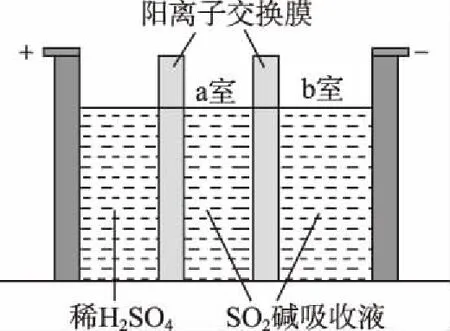
(3)制備Na2S2O5也可采用三室膜電解技術,裝置如圖所示,其中SO2堿吸收液中含有NaHSO3和Na2SO3,陽極的電極反應式為____________________。電解后, 室的NaHSO3濃度增加,將該室溶液進行結晶脫水,可得到Na2S2O5。
(4)Na2S2O5可用作食品的抗氧化劑,在測定某葡萄酒中Na2S2O5的殘留量時,取50.00 mL葡萄酒樣品,用 0.010 00 mol·L-1的碘標準液滴定至終點,消耗10.00 mL,滴定反應的離子方程式為_________________________,該樣品中Na2S2O5的殘留量為___________g·L-1(以SO2計)。
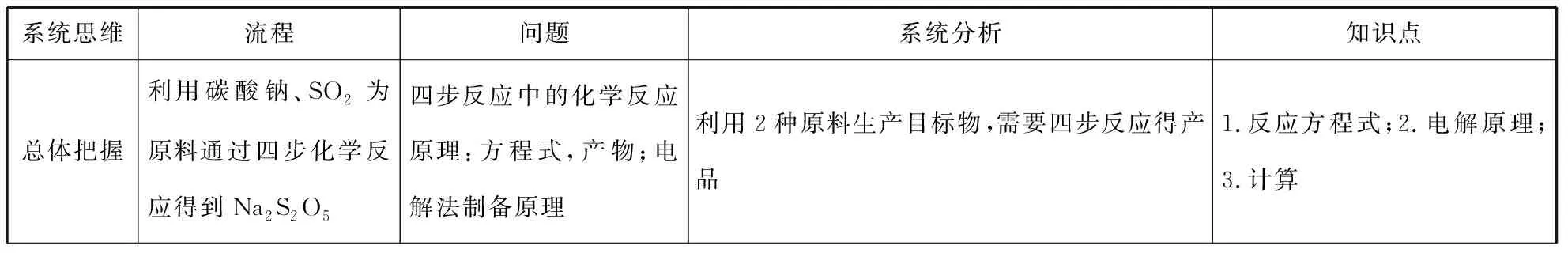
表2 從系統思維的角度分析2018新課標Ⅰ第27題
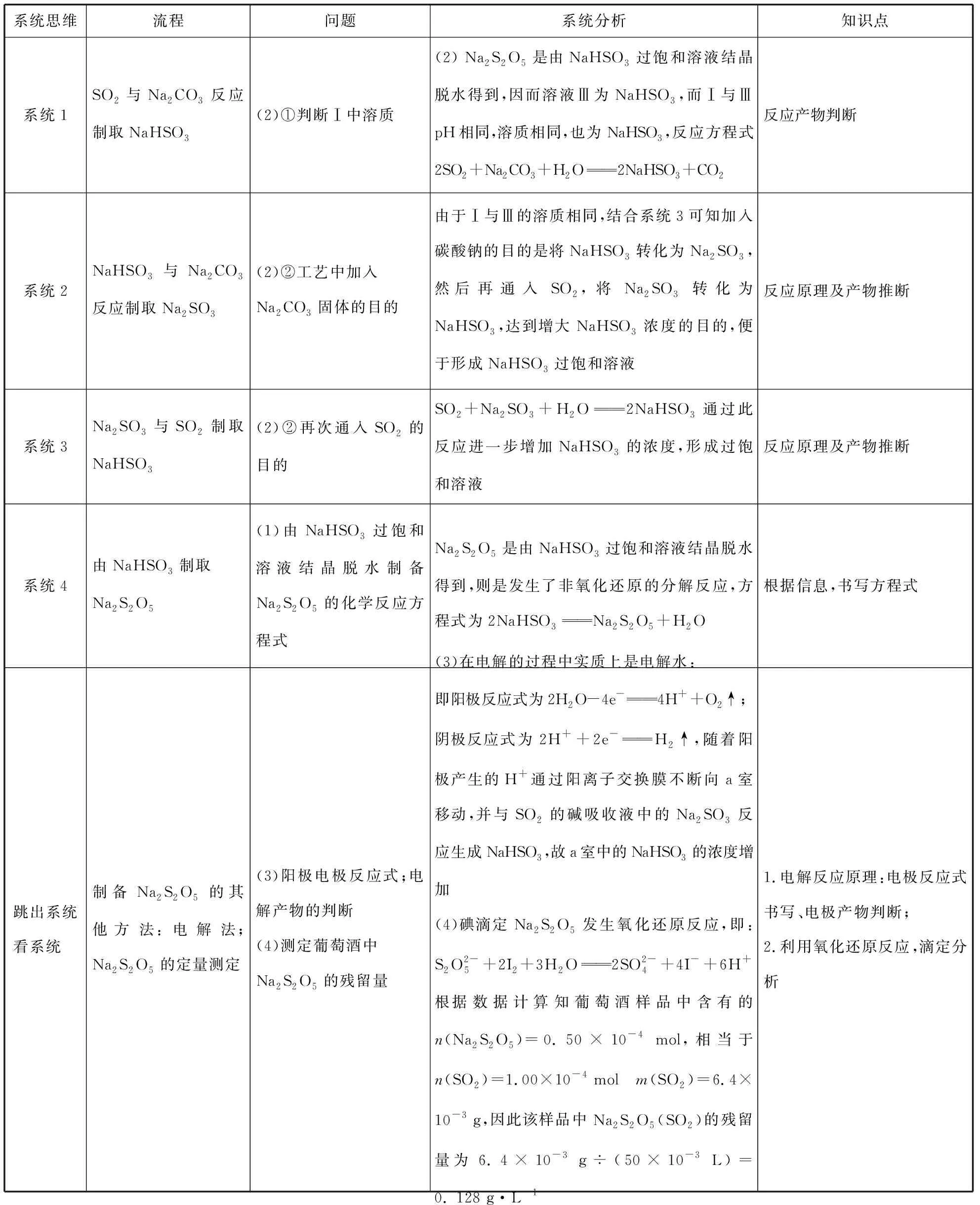
續表
三、系統思維的可行性


