綠蘿花中化合物分離與抗氧化活性研究
李克新,錢 程
(中央民族大學(xué) 生命與環(huán)境科學(xué)學(xué)院,北京 100081)
綠蘿花為瑞香科(Thymelaeaceae)結(jié)香屬滇結(jié)香(Edgeworthia gardneri)的干燥花蕾,是民族特色習(xí)用藥材。據(jù)《藏醫(yī)養(yǎng)生圖說(shuō)》[1]記載,綠蘿花對(duì)糖尿病、高血壓等具有良好的治療效果。根據(jù)文獻(xiàn)報(bào)道,綠蘿花中含有黃酮類物質(zhì)、香豆素、多糖、揮發(fā)油以及微量元素等多種化合物[2-4]。
本實(shí)驗(yàn)以綠蘿花為研究對(duì)象,對(duì)其乙酸乙酯萃取層經(jīng)反復(fù)柱色譜與循環(huán)制備液相色譜,得到5個(gè)化合物,并采用波譜學(xué)方法解析化合物的結(jié)構(gòu),采用1,1-二苯基-2-硝基苯肼自由基清除法(DPPH)對(duì)分離得到的化合物進(jìn)行抗氧化活性評(píng)價(jià),為更深入地研究和開(kāi)發(fā)綠蘿花的藥用價(jià)值及資源的充分利用提供理論依據(jù)。
1 實(shí)驗(yàn)部分
1.1 儀器
材料:薄層色譜用青島海洋化工廠分廠硅膠板,柱色譜用青島海洋化工廠分廠柱硅膠和拌樣硅膠,seph -dex LH-20,DPPH,乙醇、石油醚、乙酸乙酯、正丁醇、氯仿、甲醇、丙酮等均為分析純,儀器用甲醇為色譜純,水為超純水。
儀器:旋轉(zhuǎn)蒸發(fā)儀,制備型高效液相色譜儀(LC-20AP),分析型高效液相色譜儀(LC-20A),循環(huán)制備色譜儀,多功能酶標(biāo)儀(Enspire),超導(dǎo)核磁共振波譜儀(AVANCE 600MH)。
1.2 實(shí)驗(yàn)方法
1.2.1 化合物的分離與鑒定
取600 g干燥的綠蘿花藥材,以75%的乙醇溶液采用溶劑提取法加熱回流2 h,提取2次,合并濾液減壓濃縮得到綠蘿花總提取物100 g。用浸膏∶水=1∶40的比例溶解總浸膏,依次用石油醚和乙酸乙酯進(jìn)行萃取,減壓濃縮得到綠蘿花乙酸乙酯粗提物10 g。經(jīng)硅膠柱色譜以石油醚-乙酸乙酯-甲醇(100∶0∶0-0∶50∶50)梯度洗脫、TLC薄層色譜合并浸膏,尋找適宜洗脫劑條件。再經(jīng)硅膠柱色譜,凝膠柱色譜,減壓硅膠柱色譜,循環(huán)制備色譜等色譜學(xué)方法分離,得到5種單體化合物。采用核磁共振氫譜法進(jìn)行結(jié)構(gòu)解析。
1.2.2 化合物抗氧化活性測(cè)定
采用DPPH自由基清除法測(cè)定化合物抗氧化活性。將化合物及陽(yáng)性對(duì)照維生素E配制成1 mg/mL的母液,并梯度稀釋配制成0.5 mg/mL至0.001 mg/mL的10個(gè)質(zhì)量濃度溶液,DPPH溶液質(zhì)量濃度為400 μg/mL。將樣品及維生素E溶液依濃度梯度加入96孔板中,加樣量為100 μL。再加入等體積DPPH溶液,并設(shè)置樣品溶液和DPPH溶液空白對(duì)照。每組設(shè)置3個(gè)重復(fù)試驗(yàn)。將加液完成的96孔板置于多功能酶標(biāo)儀中,在37 ℃下選擇震蕩10 s,并在酶標(biāo)儀中靜置30 min至反應(yīng)完全,此后在517 nm波長(zhǎng)下進(jìn)行測(cè)量,讀出吸光度值,計(jì)算清除率。

A0—DPPH溶液空白對(duì)照的吸光度測(cè)量值;A1—樣品反應(yīng)液的吸光度測(cè)量值;A2—樣品及維生素E溶液的吸光度測(cè)量值。
2 實(shí)驗(yàn)結(jié)果
2.1 化合物結(jié)構(gòu)信息
以綠蘿花為研究對(duì)象,對(duì)乙酸乙酯粗提物經(jīng)反復(fù)柱色譜與循環(huán)制備液相色譜分離純化得到化合物。用TLC薄層色譜經(jīng)3個(gè)不同體系進(jìn)行顯色,均為單斑,證明為單體化合物。結(jié)構(gòu)信息如圖1~5所示。

圖1 tiliroside,R-H

圖2 isoquercetin
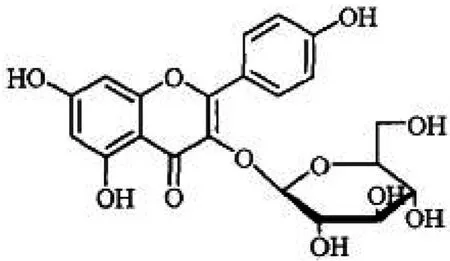
圖3 kaempferol-3-O-β-D-glucoside
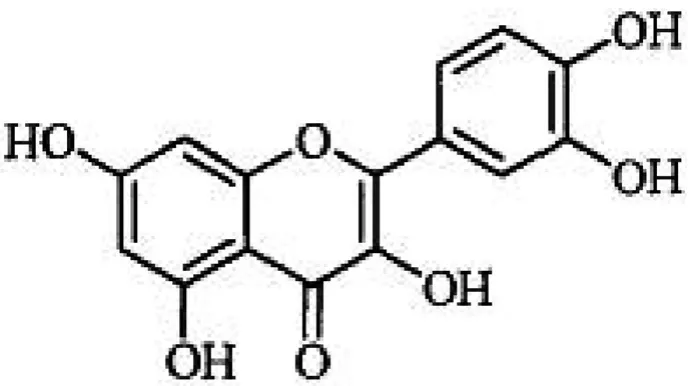
圖4 quercetin
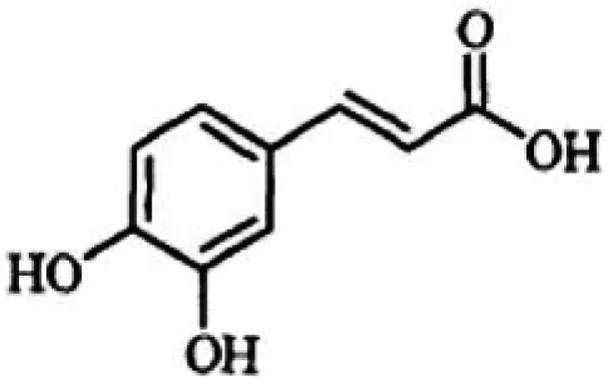
圖5 Caffeic acid
2.2 化合物結(jié)構(gòu)鑒定
化合物1:在1H-NMR譜圖中,顯示存在苯環(huán)上典型的AA′BB′系統(tǒng)的氫信號(hào),6.12(1H,d,J=1.7 Hz,H-6),6.35(1H,d,J=1.7 Hz,H-8)分別為苯環(huán)上6、8位的質(zhì)子信號(hào),可推斷化合物的苷元部分為山奈酚,與文獻(xiàn)數(shù)據(jù)對(duì)照基本一致[5],故鑒定為銀椴苷(tiliroside)。
化合物2:1H-NMR譜圖與文獻(xiàn)中槲皮素的1H-NMR譜數(shù)據(jù)非常相近,判斷譜圖中5.24(1H,d,J=7.2Hz,H-1’’)是β-D-葡萄糖端基質(zhì)子。與文獻(xiàn)數(shù)據(jù)對(duì)照基本一致[6],故鑒定為異槲皮素(isoquercetin)。
化合物3:1H-NMR譜中,顯示苯環(huán)上典型的AA′BB′系統(tǒng),J=8.8 Hz,為B環(huán)上質(zhì)子耦合,提示4′位有取代。δH6.33、6.15氫信號(hào)是AB系統(tǒng),J=2.0 Hz,為A環(huán)上間位質(zhì)子耦合,提示該化合物的苷元部分為山奈酚。δH5.19(1H,d,J=6.0 Hz)為葡萄糖端基質(zhì)子,由其偶合常數(shù)推斷糖端基構(gòu)型為β型。與文獻(xiàn)數(shù)據(jù)對(duì)照基本一致[7],故鑒定為山奈酚-3-O-β-D-葡萄糖苷(kaempferol-3-O-β-D -glucoside)。
化合物4:1H-NMR譜中,顯示B環(huán)ABX自旋耦合系統(tǒng)中的H-2’,H-6’,H-5’信號(hào);δH6.38,δH6.17的氫信號(hào)是AB系統(tǒng),J=2.0 Hz,為A環(huán)上間位質(zhì)子耦合,提示A環(huán)5,7位有取代。與文獻(xiàn)中[8]槲皮素基本一致,故鑒定為槲皮素(quercetin)。
化合物5:1H-NMR譜中,根據(jù)δH7.02(1H,d,J=2.0 Hz),6.76(1H,d,J=8.8 Hz),6.95(1H,dd,J=8.8,2.0 Hz)為苯環(huán)上的ABX耦合系統(tǒng)的氫信號(hào),分別為苯環(huán)上2,5,6位上的氫信號(hào),根據(jù)δH7.52(1H,d,J=15.6 Hz),6.21(1H,d,J=15.6 Hz)判斷苯環(huán)上接有一個(gè)反式雙鍵,與文獻(xiàn)[9]數(shù)據(jù)對(duì)照基本一致,故鑒定為咖啡酸(caffeic acid)。
3 結(jié)語(yǔ)
經(jīng)多功能酶標(biāo)儀測(cè)得,不同濃度的樣品溶液和維生素E溶液在37 ℃下與等體積的DPPH溶液反應(yīng)0.5 h后測(cè)得的吸光度計(jì)算抗氧化活性,得到以下結(jié)果。
與0.04 mg/mL的DPPH溶液反應(yīng),化合物1-5抗氧化活性IC50值分別為0.011 mg/mL,0.004 mg/mL,0.012 mg/mL,0.005 mg/mL,0.021 mg/mL,VE的抗氧化活性IC50值為0.006 mg/mL,則抗氧化活性2>4>VE>1>3>5。

