血清中CEA、NSE與CYFRA21-1聯合檢測在診斷肺癌中的臨床意義及預后評估價值
黃倩 ,丁顯平
1.四川大學生命科學學院,四川成都 610044;2.成都市第七人民醫院檢驗科,四川成都 640041
肺癌作為一種高發病、高致死惡性腫瘤,早期診斷對臨床治療、預后評估具有重要意義[1],既往有大量研究認為腫瘤標志物可用于早期診斷、療效監測及預后評估[2-3],近年隨著腫瘤分子生物學理論的成熟,越來越多的腫瘤標志物被用于肺癌早期診斷[4]。CEA、CYFRA21-1、NSE均為惡性腫瘤常用腫瘤標志物,但有關三者聯合診斷的臨床研究較少,該次研究選取2010年10月—2012年10月該院收治的肺癌、良性腫瘤、健康患者各30例為研究對象,對單一、聯合診斷方法進行對照,為肺癌早期診斷及預后評估提供指導,現報道如下。
1 資料與方法
1.1 一般資料
選取該院肺癌、良性腫瘤、健康患者各30例為研究對象,肺癌組納入標準:病理組織學檢查確診為肺癌;體溫正常;血常規檢測無異常;無嚴重肝腎功能障礙;未合并肺部良性疾病;無其他感染性疾病;無其他部位惡性腫瘤。其中男16例,女14例,年齡29~84歲,平均(61.36±5.94)歲,其中鱗癌 7 例,腺癌 6 例,小細胞癌9例,未分類癌8例;TNM分期Ⅰ期12例,Ⅱ期8例,Ⅲ期10例。良性患者納入標準:無肺炎、支氣管擴張、肺結核等其他呼吸系統疾病;未合并其他惡性腫瘤或肝、腎等嚴重內科疾病,其中男18例,女12例,年齡 30~81 歲,平均(62.44±6.34)歲。正常組男 16名,女 14 名,年齡 32~81 歲,平均(60.94±7.44)歲。 3組年齡、性別等基線資料比較差異無統計學意義(P>0.05),具有可比性,且所選病例均通過倫理委員會的批準,患者及家屬均知情同意。
1.2 檢測方法
檢測儀器為羅氏MODULAR E170電化學發光免疫分析儀,試劑盒購自上海鼓臣生物公司。CEA、NSE與CYFRA21-1采取電化學發光免疫法測定,根據試劑說明書嚴格操作,取術前1個月清晨空腹靜脈血3 mL,常規離心,分離血清并保存。CEA>4.7 ng/mL,NSE>16.3 ng/mL,CYFRA21-1>3.3 ng/mL。
1.3 敏感性、特異性計算
敏感性=真陽性例數/(真陽性例數+假陰性例數),特異性=真陰性例數/(真陰性例數+假陽性例數),3項檢測中有任何一項陽性則視為聯合檢測陽性。
1.4 統計方法
2 結果
2.1 肺癌與正常者血清CEA、NSE與CYFRA21-1比較
肺癌組CEA、NSE、CYFRA21-1表達顯著高于良性、正常組(P<0.05),良性組與正常組組間比較差異無統計學意義(P>0.05)。見表 1。肺癌組 CEA、NSE 及CYFRA21-1陽性患者分別15例、22例、17例,CEA診斷肺癌靈敏度50.00%(15/30)、特異性81.67%(49/60);NSE 診斷靈敏度 73.33%(22/30),特異性 66.67%(40/60);CYFRA21-1 靈敏度 56.67%(17/30),特異性71.67%(43/60); 聯合診斷靈敏度 93.33%(28/30),特異性 50.00%(30/60)。
表1 肺癌與正常者血清CEA、NSE與CYFRA21-1比較[(±s),ng/mL]
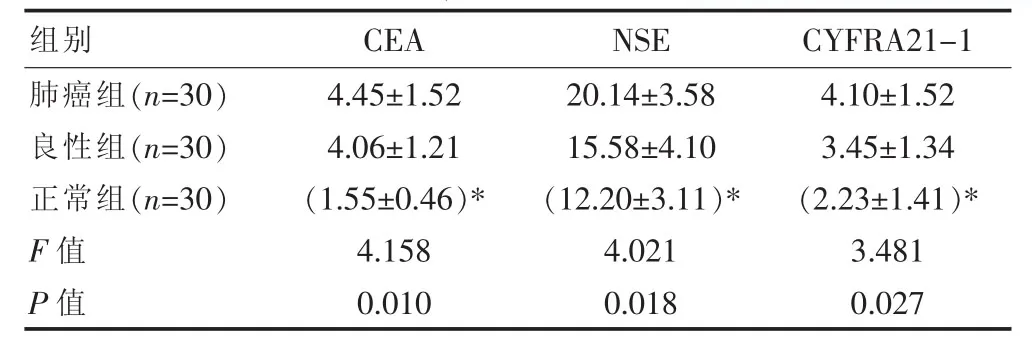
表1 肺癌與正常者血清CEA、NSE與CYFRA21-1比較[(±s),ng/mL]
注:與肺癌組比較,*P<0.017。
組別 C E A N S E C Y F R A 2 1-1肺癌組(n=3 0)良性組(n=3 0)正常組(n=3 0)F值P值4.4 5±1.5 2 4.0 6±1.2 1(1.5 5±0.4 6)*4.1 5 8 0.0 1 0 2 0.1 4±3.5 8 1 5.5 8±4.1 0(1 2.2 0±3.1 1)*4.0 2 1 0.0 1 8 4.1 0±1.5 2 3.4 5±1.3 4(2.2 3±1.4 1)*3.4 8 1 0.0 2 7
2.2 不同預后肺癌患者血清CEA、NSE與CYFRA21-1比較
存活及死亡患者CEA、NSE與CYFRA21-1水平比較差異有統計學意義(P<0.05)。見表2。存活患者中CEA陽性10例,NSE陽性10例,CYFRA21-1陽性8例,聯合診斷陽性14例。死亡患者CEA陽性5例,NSE陽性12例,CYFRA21-1陽性9例,聯合診斷陽性14例。
表2 不同預后肺癌患者血清CEA、NSE與CYFRA21-1比較[(±s),ng/mL]
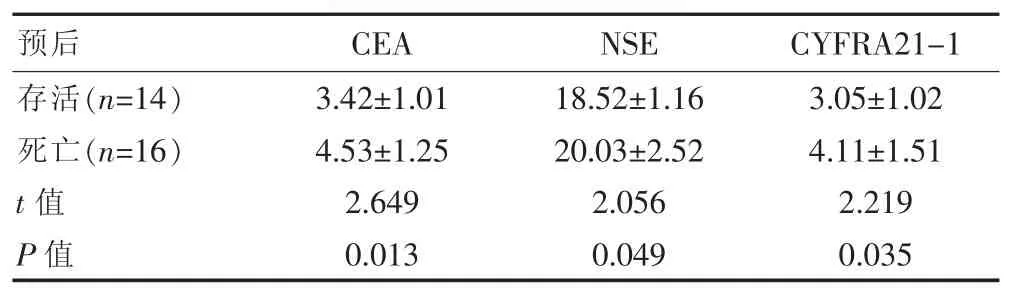
表2 不同預后肺癌患者血清CEA、NSE與CYFRA21-1比較[(±s),ng/mL]
預后 C E A N S E C Y F R A 2 1-1存活(n=1 4)死亡(n=1 6)t值 P值3.4 2±1.0 1 4.5 3±1.2 5 2.6 4 9 0.0 1 3 1 8.5 2±1.1 6 2 0.0 3±2.5 2 2.0 5 6 0.0 4 9 3.0 5±1.0 2 4.1 1±1.5 1 2.2 1 9 0.0 3 5
3 討論
肺癌發生機制與吸煙、空氣污染、營養失衡等眾多因素相關[5],此病具有明顯的異質性,目前臨床診斷方式主要包括痰細胞學、血清學或影像學檢測,本文三者單一及聯合應用的效果進行分析,旨在為肺癌早期診斷提供依據。
CEA為最早發現的腫瘤標志物,最早在結腸癌、胎兒腸組織內發現,外周血內含量較低,后被作為結腸癌首選標志物用于臨床;NSE即磷酸烯醇化酶,屬酸性蛋白酶,僅在神經元、神經內分泌細胞中表達,因此在檢測神經系統受損中具有重要價值;CYFRA21-1是具有40 KDa的酸性糖蛋白,屬于上皮細胞骨架的一部分,由人類KPT19基因編碼,主要維持上皮細胞完整性,參與細胞粘附、生長、浸潤等過程,血液中CYFRA21-1主要源于上皮腫瘤細胞分解,分解后溶于血清內,既往研究顯示CYFRA21-1是較敏感的腫瘤標準物,尤其對于鱗癌具有較高的診斷價值[6]。
該次研究顯示聯合診斷靈敏度達93.33%,這與王文濤等[7]學者在相關研究中得出聯合檢測的靈敏度可達96.12%,與該文的研究結果相近,提示三項指標聯合檢測可充分利用各指標在不同類型癌癥中的檢測優勢。有研究[8]認為人體內有循環抗動物蛋白抗體,可能影響腫瘤標志物檢測結果,容易發生假陽性、假陰性,如人體處于感染狀態時,炎性物質可能釋放具有抗原性的活性物質,此類物質與腫瘤標志物結合導致假陽性結果,另非腫瘤患者體內分泌的腫瘤相關抗原釋放到血液循環中,如伴有肝損傷則可能導致抗原代謝受阻,最終導致假陽性,另有研究認為術后腫瘤標志物對預后的評估價值更高,對此仍需后期深入研究。
綜上所述,聯合診斷CEA、CYFRA21-1、NSE可提高肺癌診斷準確性,對肺癌不同病理類型、分期有一定鑒別價值,并對預后有一定預測作用,臨床價值較高。

