血站血液檢測設備性能對比方法的探討
范文成 王 棚 馮 霞 劉旭明艷 何小艷 陳素瓊
血站實驗室對于不同血液檢測設備性能進行對比是實驗室質量管理與控制的基本要求。我國《血站技術操作規程(2015年版)》[1]及《美國實驗室改進法案修正案》[2]均明確規定:在血站實驗室使用多臺儀器對同個項目進行檢測前,需對儀器分析性能進行確認比較,以確保不同檢測設備檢測結果的可比性與溯源性。對于新購入的儀器設備應根據其分析類型,確定性能參數后與原有儀器性能進行對比分析。國外要求對血液檢測設備性能檢測每半年進行一次,國內則要求一年一次[3-5]。本研究遵循上述要求,對綿陽市紅十字中心血站實驗室的全自動酶免分析儀及全自動生化儀檢測設備進行對比,旨在為血站血液檢測設備性能對比提供參考。
1 材料與方法
1.1 FAME全自動酶免后處理系統比對試驗
1.1.1 儀器設備
Xantus150型全自動加樣儀(深圳愛康);2臺全自動酶免分析后處理系統(FAME1620簡稱FAME1、FAME2420,簡稱FAME2,瑞士HAMILTON)。
1.1.2 試劑
(1)HBsAg ELISA試劑:①試劑1,北京萬泰,批號為B20160408,質控品為0.2 IU/ml,北京康徹斯坦,批號為201610025;②試劑2,BIO,批號為6B0209,質控品為0.1 IU/ml,北京康徹斯坦,批號為201612009。
(2)抗-HCV ELISA試劑:①試劑1,北京萬泰,批號為CS20160302,質控品為0.05 NCU/ml,北京康徹斯坦,批號為201601103;②試劑2,Murex,批號為V929020,質控品為2 NCU/ml,北京康徹斯坦,批號為201612021。
(3)抗-TP ELISA試劑:①試劑1,北京萬泰,批號為N20160311,質控品為6 mIU/ml,北京康徹斯坦,批號為201612016;②試劑2,珠海麗珠,批號為2016040508,質控品為6 mIU/ml,北京康徹斯坦,批號為201611017。
(4)抗-HIV ELISA試劑:①試劑1,北京萬泰,批號為H20160101,質控品為0.5 NCU/ml,北京康徹斯坦,批號為201511025;②試劑2,BIO,批號為6B0351,質控品為4 NCU/ml,北京康徹斯坦,批號為201511013。
1.1.3 試驗標本
室內質控22份,2015年室間質評標本16份,獻血者血液標本50份。
1.1.4 試驗方法
參照試劑說明書及標準操作規程,采用同一臺全自動加樣儀(Xantus 150)加樣,分別用2臺FAME、8種ELISA試劑檢測同樣的標本88份,其中包括室內質控標本22份,2015年室間質評標本16份,獻血者標本50份。計算22份室內質控的均值、標準差及變異系數。室間質評和獻血者標本結果應用Kappa檢驗,比較2臺全自動酶免分析后處理系統檢測結果的一致性。
1.2 全自動生化分析儀比對試驗
1.2.1 儀器與試劑
(1)儀器設備。C311全自動生化分析儀(德國羅氏);B-480全自動生化分析儀(深圳邁瑞)。
(2)ALT測定試劑盒(批號621149)及其質控(低值質控品批號、高值質控品批號174794)(德國羅氏診斷有限公司)。
1.2.2 試驗標本
低值和高值室內質控品以及24份獻血者血液標本。
1.2.3 試驗方法
(1)選用ALT低值和高值質控進行常規室內質控檢測,計算6個月的質控數據,計算比對方差,確定檢測系統的不精密度,驗證兩套全自動生化分析儀的可比性[7]。
(2)常規使用羅氏C311檢測,每周使用邁瑞B-480檢測1次,檢測標本8個,分析連續3周24個標本的檢測結果,采用回歸分析2臺全自動生化分析儀的檢測結果。
1.2.4 質控方法
實驗室室溫控制在18~25 ℃,濕度30%~70%,所有試劑在使用前均經過30 min的平衡;抽取血液標本后采用EDTA-K2進行抗凝處理,以3000 r/min轉速進行離心15 min。設備均在校準期內,且運行無異常。
2 結果
2.1 全自動酶免后處理系統檢測性能比對
(1)2臺全自動酶免后處理系統檢測室內質控結果。2臺全自動酶免后處理系統使用8種ELISA試劑檢測室內質控標本22份,2臺儀器批內CV值均在15%以內,其各試劑檢測值均無顯著性差異,見表1。
(2)選取無償獻血者血液標本50份、室間質量評價標本16份,使用2臺FAME全自動酶免分析后系統檢測結果對比,2臺儀器檢測結果均一致,見表2。
2.2 全自動生化分析儀比對
2.2.1 質控品檢測結果可比性分析
(1)收集2臺儀器近6個月的質控品檢測數據,計算出m總和CV合并,分析不精密度,見表3。

表1 兩臺全自動酶免后處理系統8種ELISA試劑檢測22份室內質控結果

表2 兩臺全自動酶免后處理系統檢測獻血者血液標本以及室間質量評價標本比較
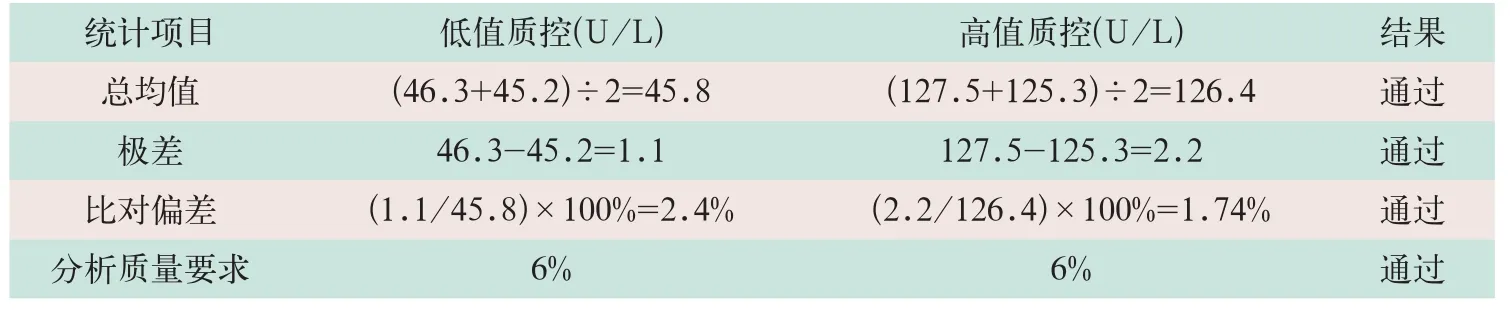
表5 兩臺全自動生化分析儀樣本檢測結果分析
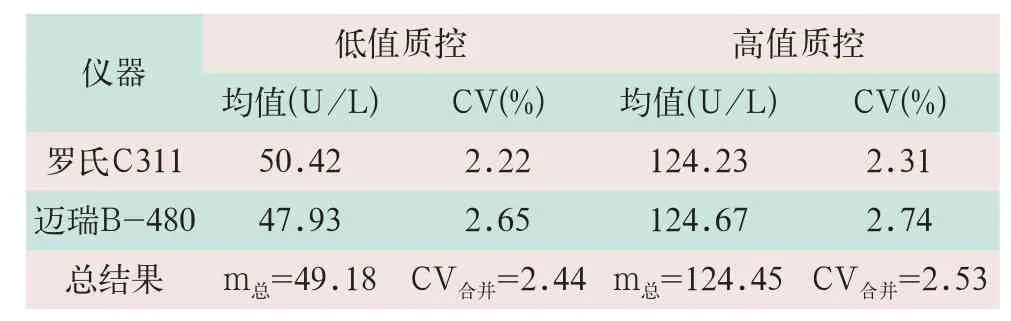
表3 兩臺全自動生化分析儀不精密度分析
(2)以每個質控品濃度水平的總均值m總×(1+20%)作為樣品濃度的選擇范圍,得到低值質控濃度范圍為39.3~59.0 U/L,高值質控濃度范圍為99.6~149.3 U/L。依照醫療機構內定量檢驗結果的可比性驗證指南[8]確定低值質控、高值質控檢測重復次數各為3次,見表4。
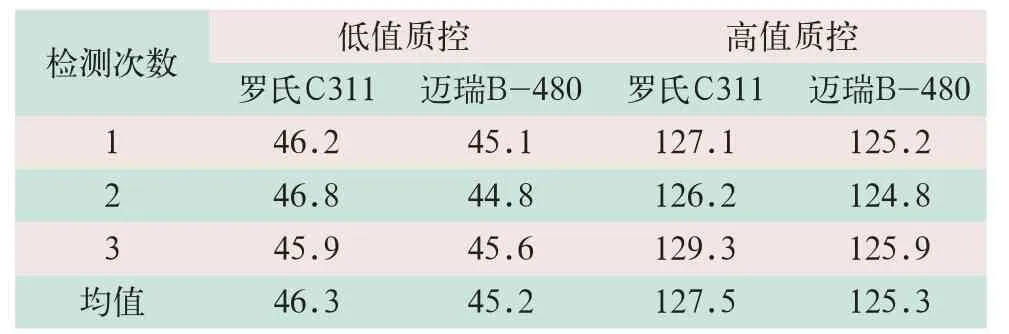
表4 兩臺全自動生化分析儀樣本檢測結果
(3)根據低值、高值質控均值得出極差和比對偏差,ALT的個體內生物學變異為18%,故實驗室將CV1的1/3,即6%作為分析質量要求,小于分析質量要求,結論為通過,見表5[9]。
通過計算,兩個濃度樣本的比對偏差分別為2.4%和1.74%,均在6%以內,故認為2臺設備檢測結果符合檢測系統要求。
2.2.2 獻血者血液標本檢測結果對比
每周同時使用2臺全自動生化分析儀檢測8個標本,連續3周共24個標本的檢測結果,分析2臺設備的一致性,見表6。
以羅氏C311檢測結果為y,邁瑞B480檢測結果為x,做線性回歸計算,得出回歸方程 ,如圖1所示。
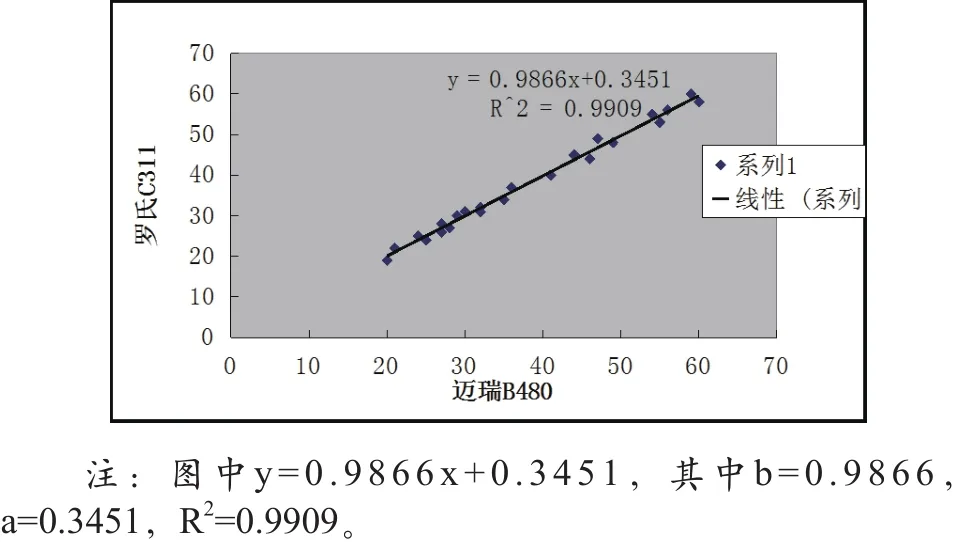
圖1 兩臺全自動生化分析儀檢測24份獻血者ALT結果的回歸線性圖
3 討論
目前,全國大部分的血站實驗室仍使用多套設備對輸血相關傳染病血清學標志物進行檢測,且不同設備間常互為備用[10]。血站實驗室工作強度大,設備長時間的運行其各部件老化程度不同,設備之間可能會出現差別,而導致不同設備之間檢測一致性不高,影響結果的準確性[11]。因此,在校準周期內對設備性能進行確認,同時進行設備間性能對比是血站血液檢測質量管理的重點。保證并保持實驗室內檢測作用相同的自動化設備性能的一致,是提高血液檢測實驗室檢測質量的重要手段。
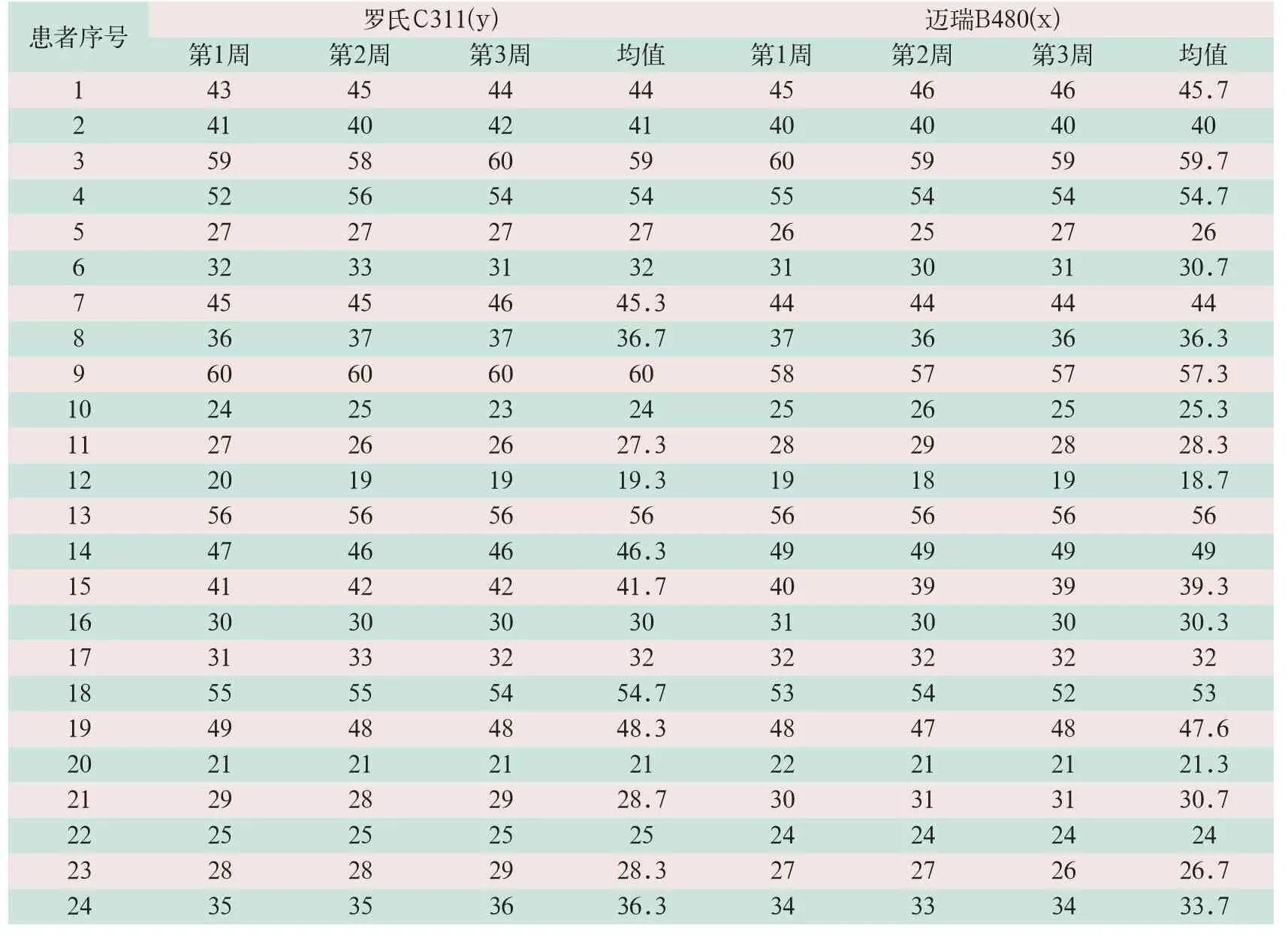
表6 兩臺全自動生化分析儀檢測24份獻血者標本的結果
根據上述質控要求結合自身情況,本研究對2臺全自動酶免分析后處理系統與2臺全自動生化分析儀設計了定性與定量對比分析。設備性能是否一致主要通過檢測結果的一致性分析結果來體現,檢測結果的一致性主要受檢測設備、試劑、質控品、試驗標本等的影響。全自動酶免分析后處理系統性能對比,選取室內質控標本22份,結果顯示:2臺設備用室內質控做重復性檢測,均值接近,批內變異系數均在15%以內,經x2檢驗,8種ELISA試劑的t值分別為:1.746、-1.903、2.113、0.816、2.273、-2.538、1.793以及1.442,P值均>0.05,2臺FAME檢測的精密度好。16份已知檢測結果的室間質評標本,正確率均100%,做常規已知獻血者血液標本的檢測時,2臺FAME的檢測結果一致,表明2臺設備用同一試劑的檢測性能一致。對于全自動生化分析儀選擇6個月以上的室內質控品檢測結果對不精密度和檢測均值進行分析,結果分別為2.4%和1.74%,均低于分析質量要求(6%),2臺全自動生化分析儀均通過,24份獻血者標本在2臺全自動生化分析儀上的檢測結果經回歸分析,兩者一致性為優,可以認為2臺全自動生化分析儀檢測ALT的結果符合檢測系統要求。
血站血液檢測設備性能對比應注意的問題:①設備應處于校準期內且可正常運行,試驗過程中需要使用的器具應保持清潔;②有適宜的質控品。本研究所涉及的設備各2臺,故采用室間質評標本,若設備較多標本量不夠時可選擇血清盤標本作為質控品[12]。
4 結語
設備間性能對比是一項嚴謹的工作,在試驗方案設計、結果判斷及結論定論方面均需要有足夠的理論依據與數據支撐。通過對全自動檢測設備性能對比,可有效保證實驗結果的準確性,維護獻血者利益,保證患者用血安全,同時也為實驗室間檢驗結果互認提供了可靠依據[13]。然而,本次開展的設備間性能比對研究還有許多需要完善的地方。

