術前紫杉醇聯合順鉑新輔助化療肺鱗癌的療效觀察
楊昌杰 楊 莉
肺鱗癌又名肺鱗狀上皮細胞癌,主要是由于支氣管黏膜柱狀上皮細胞長期受到刺激,從而導致細胞損傷,喪失纖毛,最終使基底細胞不典型增生、鱗狀化生后發育不完全,最終導致突變形成癌細胞。肺鱗癌主要表現為中央型肺癌,并隨著病情發展向胸管腔內生長遷移,其臨床表現為反復發熱、咯血、咳嗽以及胸痛[1]。在原發性肺癌中肺鱗癌發病率高達51%,是肺癌中最常見的一種類型,目前研究表明該疾病與吸煙密切相關,故老年男性的發病率居高不下[2]。臨床治療主要以化療、放療以及手術治療為主。本研究旨在探討術前紫杉醇聯合順鉑新輔助化療治療肺鱗癌的臨床療效。
1 資料與方法
1.1 臨床資料
選取2014年1月至2015年1月在我院確診并接受治療的鱗狀細胞癌患者60例作為研究對象。納入標準:①所有患者均經病理學檢查并確診為肺鱗癌;②cTNM分期主要為Ⅲa期以及Ⅲb期;③未經過化療治療且經CT或MRI檢測存在明確的可測量病灶;④所有患者及家屬對本研究知情同意,并簽署知情同意書;排除標準:①合并有嚴重的心、肝、肺、腎等重大器官性疾病;②患者對治療藥物過敏。隨機將患者分為2組,每組30例。對照組男性25例,女性5例,年齡35~58歲,平均年齡(41.5±3.5)歲,其中Ⅲa期23例、Ⅲb期7例。研究組男性24例,女性6例,年齡38~55歲,平均年齡為(42.1±4.1)歲,其中Ⅲa期20例、Ⅲb期10例。2組患者在性別、年齡、cTNM分期方面并不具有統計學差異(P>0.05),具有臨床可比性。
1.2 方法
對照組:直接進行手術治療,根據患者自身情況進行肺葉、全肺或者袖式切除術配合淋巴清掃術。研究組:在對照組的基礎上先進行新輔助化療,即新輔助化療前12 h、6 h給予患者口服地塞米松20 mg,化療前30 min肌肉注射苯海拉明50 mg,地塞米松10 mg以及西米替丁300 mg,隨后化療第1天給予含135~175 mg/m2的紫杉醇的500 ml 5%葡萄糖液進行靜脈滴注3 h,隨后第2~4天給予含50 mg/m2的順鉑的100 ml 3%鹽水進行靜脈滴注,化療期間每隔15 min對患者的心率、血壓以及脈搏進行檢測,化療期間采用格拉司瓊進行鎮吐,間隔3周再進行1個療程,第2次化療結束后2~3周再進行手術治療[3-4]。
1.3 觀察指標
1.3.1 新輔助化療的毒副作用和化療療效 按照WHO抗癌藥物的不良反應分度標準Ⅰ~Ⅳ度進行評價,并按照WHO制定的療效評定標準[5]對新輔助化療的療效進行判斷并計算有效率。
1.3.2 遠期療效觀察 對所有患者術后進行1~2年的隨訪,對患者的生存狀況以及復發率進行比較分析。
1.3.3 生存質量調查 對所有患者的睡眠、疲乏、日常生活狀況、食欲、治療副反應、心絞痛程度進行問卷調查,總分60分,生活質量與分數成正比。
1.4 統計學分析
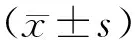
2 結果
2.1 研究組術前化療療效
研究組患者cTNM分期中Ⅲa期患者術前化療有效率達到85.0%,Ⅲb期術前有效率只有30.0%,化療總有效率為66.67%。見表1。

表1 術前化療效果(例,%)
2.2 研究組化療后的腫瘤大小
研究組患者化療前腫瘤直徑為4.2~7.5 cm,平均直徑為(5.8±0.5)cm;在經過新輔助化療后腫瘤直徑降低為2.9~3.8 cm,平均直徑為(3.3±0.4)cm。結果表明患者經過化療后腫瘤顯著減小,對研究組患者化療前后的腫瘤大小進行比較,差異具有統計學意義(t=2.671,P<0.05)。
2.3 研究組化療的毒副作用
研究組患者在經過化療后,消化系統主要表現為惡心嘔吐、厭食,共計22例(73.33%),但均在可耐受范圍內;血液系統主要表現為不同程度骨髓抑制,具體表現在白細胞、紅細胞以及血紅蛋白含量下降,其中Ⅰ度11例、Ⅱ度14例、Ⅲ度5例,但經過相關的補救措施后均有所改善;其他表現主要包括脫發、疲乏、肌肉關節疼痛、外周神經炎等癥狀,患者均可耐受。
2.4 遠期療效觀察
對照組患者術后復發以及轉移率為33.33%、而研究組患者只有16.67%,2組差異有統計學意義(P<0.05);同時對照組患者術后1年的生存率為93.33%,2年則降低為83.33%,與研究組的生存率相比,差異具有統計學意義(P<0.05)。見表2。

表2 2組患者遠期療效觀察(例,%)
2.5 生存質量調查
2組患者在治療前生存質量并沒有統計學差異(P>0.05),但2組患者治療后生存質量均得到明顯改善,與治療前相比均具有顯著性差異(P<0.05);與對照組相比,研究組患者恢復較為明顯,且2組差異具有統計學意義(P<0.05)。見表3。
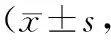
表3 2組患者治療前后生存質量評分比較分)
3 討論
肺鱗癌是臨床上較為常見的一種呼吸系統惡性腫瘤,臨床表現主要是不規則胸痛、發熱咳嗽且痰中帶血,該疾病的發病率以及死亡率都很高,嚴重危害人類的生命健康。肺鱗癌的高發人群主要是50歲左右的老年男性,調查研究表明這與患者吸煙這一習慣有著密不可分的關系。由于該疾病早期生長緩慢,所以其轉移速度有較慢這一特性,早期采取手術治療是目前臨床上的首要之選[6-7]。同時為了保證患者的預后以及生存率,臨床上通常采用新輔助化療進行輔助治療。新輔助化療 (neoadjuvant chemotherapy,NAC)在1982年由Feri首次提出,近年來在臨床上應用較多的術前輔助治療措施,它主要是在患者進行放療或手術治療前先進行藥物化療,可以在腫瘤血管沒有破環之前,有利于化療藥物進入腫瘤,使腫瘤瘤塊減小,降低腫瘤的分期以及癌細胞活力,有利于手術期間全部切除,同時對可能存在的微轉移灶進行消除或抑制,降低腫瘤在手術中以及術后的轉移,降低腫瘤復發的幾率,提高手術質量,改善患者的預后[8-9]。
目前臨床上對于肺鱗癌采用較多的化療方案是紫杉醇聯合順鉑,主要是由于紫杉醇作為具有抗癌活性的二萜生物堿類化合物,是一種新型的抗細胞內微管藥物,它可以特異性地結合于小管β位,抑制微管蛋白的解聚作用并促進聚合,通過破壞微管的解聚與聚合之間的動態平衡,使細胞在有絲分裂期間無法形成紡錘體結構,最終抑制腫瘤細胞的分裂與繁殖,誘導腫瘤細胞發生凋亡[10-11]。順鉑作為鉑金屬絡合物,具有細胞毒性,屬于細胞周期的非特異性藥物,具有較強的廣譜抗癌作用,其藥理作用與類烷化劑相同,主要通過與DNA鏈發生交叉連接,使模板的復制功能無法進行,抑制DNA的復制,同時對細胞膜上的結構造成損傷,由于與正常細胞相比,癌細胞的增殖速度更快,因此對順鉑的細胞毒性作用敏感度更高[12]。
本研究結果表明,研究組患者在經過新輔助化療后,腫瘤直徑由原來的(5.8±0.5)cm降低為(3.3±0.4)cm,這就表明患者經過化療后腫瘤顯著減小,同時研究組患者cTNM分期中Ⅲa期患者有效率達到85.0%,Ⅲb期術前有效率只有30.0%,化療總有效率為66.67%;同時患者在接受化療后消化和血液系統均出現不同程度的毒副作用,但均為Ⅰ~Ⅱ度,經過相關的補救措施后均有所改善。根據患者自身情況進行肺葉、全肺或者袖式切除術配合淋巴清掃術,對2組患者術后的療效進行統計分析,結果顯示相比于對照組,研究組患者術后局部復發以及轉移的幾率都明顯降低,同時患者的生存率顯著增加,且2組之間差異具有統計學意義(P<0.05)。對2組患者的治療前后的生存質量進行評分比較,結果表明兩組患者在經過治療前生存質量并沒有顯著性差異(P>0.05),但2組患者經過治療后生存質量均得到明顯改善,與治療前相比均具有顯著性差異(P<0.05),同時對治療后的2組比較表明,與對照組相比,治療組患者恢復較為明顯,且兩者差異具有統計學意義(P<0.05)。由此可見,術前采取新輔助化療可以顯著減小腫瘤體積,降低腫瘤分期,并且毒副作用較輕,患者基本可以耐受,同時患者術后復發以及轉移的幾率都顯著降低,生存質量顯著上升,提高患者的生存率。
綜上所述,紫杉醇聯合順鉑新輔助化療在肺鱗癌的治療中效果較好,同時毒副作用較輕,可以增加腫瘤的完整切除率,同時降低患者術后的復發及轉移率,保證患者術后的生存率和生存質量,值得臨床推廣。

