誘導助劑對石墨烯負載的TiO2顆粒分布、結構和光催化活性的影響
周鐵路,劉會娥,陳 爽,丁傳芹,齊選良
(中國石油大學(華東) 重質油國家重點實驗室,山東 青島 266580)
TiO2由于其無毒、高活性、低成本[1]等優點,一直是光催化研究領域的焦點。然而由于其只能吸收387nm以下波長的紫外光[2],其應用一直受到限制。為了解決這一難題,研究者們在金屬摻雜[3-4]、非金屬摻雜[5]、半導體復合[6-10]、有機物敏化[11-12]方面做了大量工作。然而,傳統的金屬或非金屬離子摻雜至TiO2將會導致結晶的熱穩定性下降,在催化劑的表面或骨架中引入缺陷位捕獲光生電子,從而產生大量的光生電子-空穴復合中心[13]。
將可見光響應的碳材料引入TiO2中被視為一種提高TiO2光催化效率的有效途徑。相比較于其他的碳材料(如碳納米管,富勒烯),石墨烯由于其高比表面積、優異的力學性能、杰出的電子導電性、特殊的光電化學性質和可控的禁帶寬度,在近年備受關注[14-18]。Jiang等[19-20]在十六烷基三甲基溴化銨(CTAB)輔助下制備了插層型TiO2/石墨烯復合材料,展示出優異的光催化降解苯酚活性。Gu等[21]通過葡萄糖胺誘導,大幅度提高了TiO2在石墨烯片層上的分散度。Qiu等[22]借助葡萄糖,合成了石墨烯負載TiO2的介孔氣凝膠材料。Wang等[23]以聚乙烯醇(PVA)修飾氧化石墨烯,來提高其對染料分子的吸附和TiO2的負載量。
還原氧化石墨烯表面呈疏水性,而一般的金屬氧化物呈親水性[24],為了使金屬氧化物更均勻地負載在還原氧化石墨烯上,在體系中引入誘導助劑也是非常有必要的。本工作采用葡萄糖(glucose)、十二烷基硫酸鈉(SDS)、聚乙烯吡咯烷酮(PVP)分別代表有機小分子、表面活性劑、高分子聚合物作為誘導助劑,系統研究了其對TiO2/石墨烯復合材料結構和光催化活性的影響,以期為該類金屬氧化物/石墨烯復合材料的進一步設計和制備提供指導。
1 實驗材料與方法
1.1 實驗材料
Ti(SO4)2(CP),H2SO4(AR),鹽酸(AR),NaNO3(AR),KMnO4(AR), H2O2(AR),石墨粉(99.95%),十二烷基硫酸鈉(CP),葡萄糖(AR),聚乙烯吡咯烷酮(GR),乙醇(AR),以上試劑均來自國藥集團化學試劑有限公司(滬試)。P25購自德固賽公司。
1.2 催化劑制備
1.2.1 氧化石墨的制備
本工作的氧化石墨(Graphite Oxide,GO)采用改進的Hummers法[25]制備。具體如下:首先在干燥的燒杯中加入濃硫酸23mL和硝酸鈉0.5g,冰浴條件下冷卻。當體系的溫度低于5℃時,攪拌中加入鱗片石墨1g,攪拌1h, 控制溫度低于5℃。混合均勻,慢慢加入高錳酸鉀3g,每次0.5g,間隔5min,控制反應液溫度不超過5℃,繼續反應1h。然后將燒杯置于68℃的恒溫水浴中,均勻攪拌,待混合液升溫到68℃后,繼續攪拌30min,然后慢慢加入46mL去離子水,控制反應溫度在68℃保持30min。再加入去離子水140mL,同時逐滴加入雙氧水溶液(30%,5mL),混合液從磚紅色變為鮮亮的黃色,反應終止。靜置至少12h至溶液完全分層,將上清液倒出。下層沉淀物用大量的5%HCl溶液沖洗,去除雜質。靜置,去除上清液。用去離子水沖洗,至溶液pH值達到中性。離心,冷凍干燥得GO固體備用。
1.2.2 TiO2/石墨烯的制備
取一定量的氧化石墨配制成2mg/mL的GO溶液,超聲1h。稱量2.4g Ti(SO4)2,溶解于上述GO溶液中。配制相同溶液3份,再分別稱量葡萄糖,SDS,PVP各120mg溶解于上述溶液中,超聲2h。磁力攪拌12h,分別轉移至聚四氟乙烯內襯的不銹鋼水熱反應釜中,置于烘箱中180℃保持12h。自然冷卻至室溫,洗滌,冷凍干燥,得到的樣品分別簡記為G-C,S-C,P-C(分別代表復合材料Glucose-Composites,SDS-Composites和PVP-Composites)。作為對比,在不加任何誘導助劑情況下制備復合材料,記為none,不加誘導助劑和GO情況下制備純TiO2,記為pure TiO2。所有樣品放入馬弗爐中,于400℃焙燒2h。
1.3 光催化實驗
將在1.2節中制備的100mg催化劑與250mL甲基橙溶液(20mg/L)在暗室內充分攪拌30min后轉移至反應瓶內,置于500W汞燈光照下,每隔15min取樣離心。取上清液用752型紫外可見分光光度計于464nm波長處測其吸光度,來評價甲基橙降解率。
1.4 催化劑表征
物質結構由X’Pert PRO MPD型X射線衍射儀、NEXUS FT-IR型傅里葉變換紅外光譜儀進行表征,微觀形貌采用S-4800型冷場發射掃描電子顯微鏡、JEM-2100UHR型透射電子顯微鏡觀察,采用DXR-Microscope型智能拉曼光譜儀、U-4100型紫外/可見/近紅外光譜儀進行光學特性分析。
2 結果與分析
2.1 晶體結構分析(XRD)
圖1為樣品的XRD圖譜。從圖中可看到GO在2θ為10.6°處出現了較強的(001)晶面衍射峰,對應的層間距為0.832nm,此峰是由于大量的含氧官能團插入碳原子層導致層間距增大形成的[26]。而在none,G-C,S-C,P-C 4個樣品中此峰消失,可證實GO在水熱過程中已被還原。除GO外的五個樣品均在25.3°,37.8°,48.1°,54.0°,55.1°處出現較強的峰,分別對應銳鈦礦TiO2的(101),(004),(200),(105),(211)晶面,估算其晶粒尺寸為21nm。不過可以很明顯看出,峰強差別非常小,可以推斷出誘導助劑并未影響到TiO2/石墨烯復合材料的晶體結構。
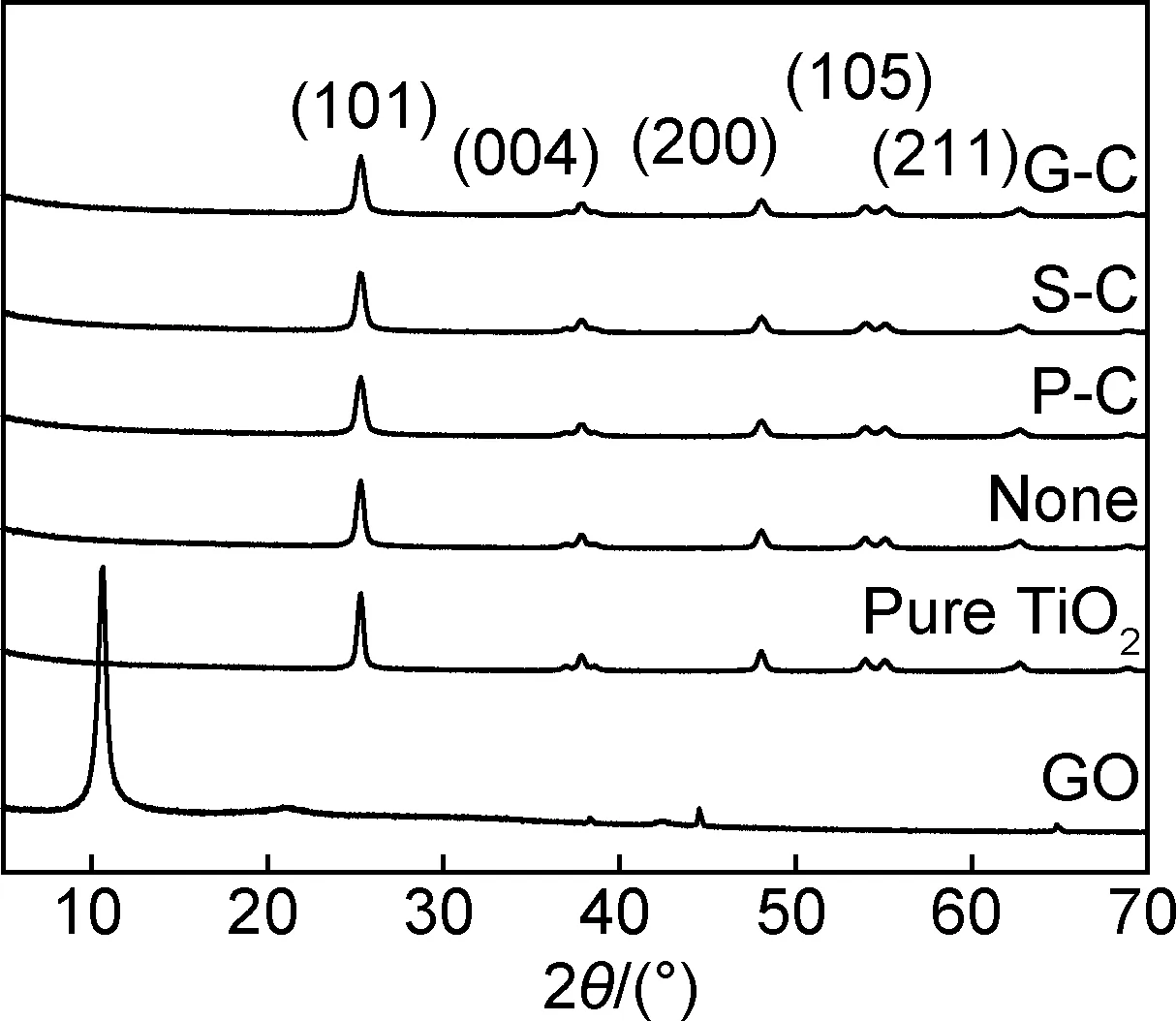
圖1 不同材料的XRD圖Fig.1 XRD patterns of different samples
2.2 微觀形貌分析
圖2為各樣品的SEM照片,圓圈內所示為顆粒團聚狀態,pure TiO2團聚最為嚴重,樣品none和P-C次之,而S-C和G-C分散效果最好,如部分方框區域內顆粒呈鱗片狀分布,直徑大小也比較均勻,有利于催化劑顆粒與染料分子充分接觸,提高降解效果。從圖2(c)中可看出,樣品P-C的片層分布參差不齊、結構散亂,而樣品G-C則比較平整有序,未有明顯凹凸不平處。
圖3為各樣品的TEM照片,在樣品G-C中(圖3(a)),還原氧化石墨烯幾乎是透明的,僅在邊緣處出現褶皺,可證明制備的還原氧化石墨烯片層薄且質量佳,有利于TiO2粒子的負載。在樣品P-C(圖3(b))、none(圖3(d))中有大量黑色陰影部分,可歸因于TiO2粒子的無序分布及團聚,而G-C(圖3(a))、S-C(圖3(c))中TiO2粒子分布較均勻。樣品P-C(圖3(b))中可觀察到扭曲交錯的黑色線狀條紋,而G-C(圖3(a))卻未出現此現象,可能與PVP為鏈狀高聚物有關。
在樣品G-C(圖3(a)),none(圖3(d))中分別觀察到 0.355nm和0.359nm的晶格間距,對應于銳鈦礦TiO2的(101)晶面[27]。值得注意的是,在樣品G-C(圖3(a))中出現了5.98nm的介孔孔道,這是由于在TiO2結晶成核過程中,葡萄糖分子較小可摻雜至其中并隨晶核長大,在后期焙燒處理過程中被除去,留下介孔孔道,其介孔性質可增強對染料分子的吸附,此項結果與Qiu[22]等的工作吻合。

圖3 不同材料的TEM照片 (a)G-C;(b)P-C;(c)S-C;(d)noneFig.3 TEM images of G-C(a),P-C(b),S-C(c) and none(d)
葡萄糖、SDS和PVP均為兩親性物質,葡萄糖分子內的羥基、SDS中的硫酸根和PVP中的內酰胺基呈親水性(見圖4圓圈),而其余部分的甲基和亞甲基均為疏水性(見圖4方框),故它們都可作為誘導助劑一端與金屬氧化物相連,另一端與石墨烯相連,在復合材料中扮演鉚釘的作用,影響TiO2粒子的分布。
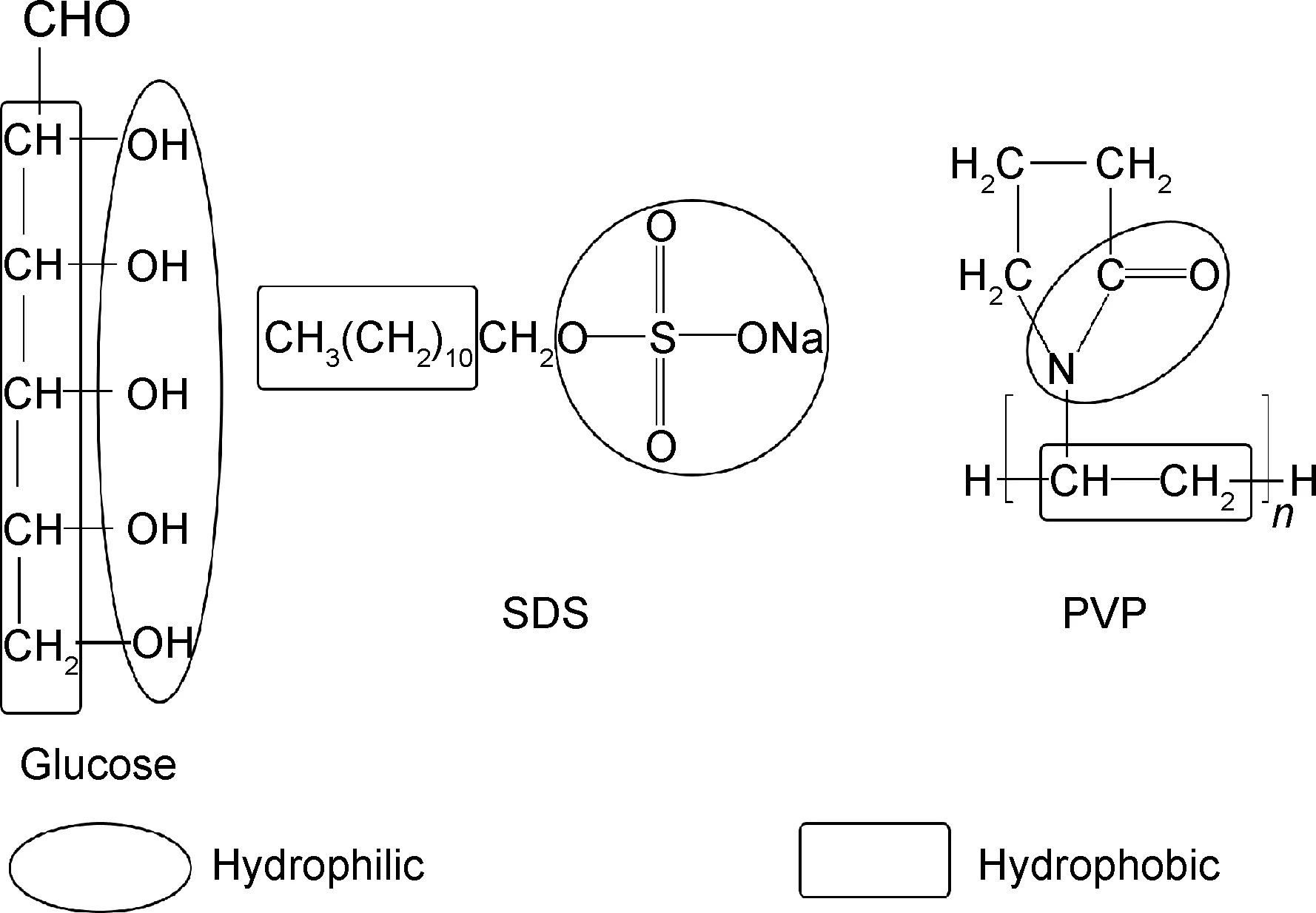
圖4 分子性質分析Fig.4 Analysis of molecular structure
具體的水熱合成機理示意見圖5。所不同的是,PVP作為一種長鏈狀高聚物,在水熱過程中難免會扭曲纏繞,互相交聯,而附著在上面的TiO2粒子就會形成另一種形式的團聚。

圖5 水熱合成機理示意Fig.5 Mechanism of the hydrothermal synthesis process
2.3 紅外光譜分析(FT-IR)

2.4 拉曼光譜分析(Raman)
從圖6(b)的拉曼光譜中可看到GO中D峰(1352cm-1處)和G峰(1585cm-1處)的出現,且D峰位置由1352cm-1處遷移至樣品none和G-C中的1330cm-1處,可證明GO在水熱過程中被成功還原[30]。而ID/IG由0.96(GO)增大至1.33和1.34可推斷水熱處理不僅還原了氧化石墨烯,還引入了缺陷位[31],增加了體系的無序混亂度。
2.5 紫外可見吸收光譜分析(UV-Vis)
圖6(c)的UV-Vis譜圖顯示相比較于pure TiO2的吸收邊(417nm),樣品none和G-C的吸收邊分別紅移至440nm和470nm,這與石墨烯網狀結構的π-π共軛有關[32]。而且none和G-C在200~800nm整個光譜范圍內的吸收強度增強,雖然none稍遜色一點,但這表明復合材料可充分利用太陽光來促進光催化反應進程。由庫貝卡-芒克(Kubelka-Munk)理論[33],可以將紫外可見吸收光譜的數據轉化為Tauc圖,即(ahv)1/2-hv,見圖6(d)。在曲線的線狀區做切線,可由切線與橫軸的交點估算帶隙值。很明顯,帶隙寬度由pure TiO2的2.98eV減小至2.37eV和2.22eV,這意味著復合材料將在可見光催化中有良好的應用前景。
2.6 X射線光電子能譜分析(XPS)
為了進一步研究表面元素組成和電子態,進行了XPS表征(圖7)。首先,在圖7(d)中可看出GO只含有C,O兩種元素,不含其他雜峰,證明GO制備過程中的錳、鉀、鈉離子已全部除去,且G-C也只多了一個Ti 元素的峰,強度較高,也可反映出復合效果好。GO

圖6 不同材料的光譜分析 (a)GO和G-C的FT-IR圖;(b)GO,none,G-C的拉曼光譜;(c)pure TiO2,none和G-C的紫外可見吸收光譜;(d)Tauc圖在C1s軌道區域284.8,286.5,288.5eV處有3個最主要的峰,分別對應sp2雜化的C(C—C),環氧/氫氧基C(C—O),羧基C原子(CO)[34]。相比較于GO,樣品G-C在C1s中286.5,288.5eV處的峰強顯著降低,證實GO已被成功還原。圖7(c)458.7eV和464.4eV電子結合能處的峰,對應于Ti4+化學價的Ti 2p3/2和Ti 2p1/2軌道激發的光電子,這與已報道的TiO2的XPS數據非常一致[35]。

圖7 不同材料的XPS譜圖 (a)GO的C1s XPS譜;(b)G-C的C1s XPS譜;(c)G-C的Ti2p XPS譜;(d)GO和G-C的全掃描XPS譜Fig.7 XPS spectra of different samples (a)C1s XPS spectrum of GO;(b)C1s XPS spectrum of G-C;(c)Ti2p XPS spectrum of G-C;(d)XPS survey spectra of GO and G-C
2.7 光催化降解甲基橙
用甲基橙模擬污染物,對不同樣品進行了光催化反應評價,并與商用P25作對比,見圖8。與石墨烯復合之后,復合材料的光催化活性均優于pure TiO2和P25,且以葡萄糖和SDS為誘導助劑的復合材料表現最優,樣品S-C稍遜于G-C,可能與G-C樣品中出現介孔結構有關。而樣品P-C和none的活性相差無幾,主要是二者都出現了TiO2粒子分布不均和團聚,詳見圖5。其中,紫外光照射30min樣品G-C降解率可達92%,而商用P25降解率達到90%需要120min,復合材料可將光催化反應時間縮短3/4。如此大幅度活性的改善主要歸因于石墨烯材料超高的電子遷移率[36],其對TiO2光生電子-空穴對的分離大有幫助。
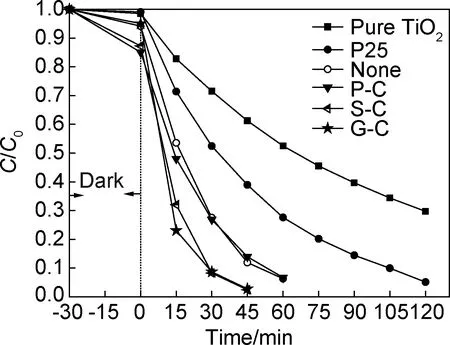
圖8 不同樣品降解甲基橙效果圖Fig.8 Degradation of methyl orange(MO) over different samples
2.8 動力學分析
為了定量分析光降解反應動力學,進行了準一級反應動力學模型的擬合,如圖9所示,擬合結果很好。從表1可得,樣品S-C和G-C的準一級反應速率常數k值最高,約為P25的4倍; none和P-C的次之,約為P25的2倍。由此可見,樣品S-C和G-C由于其顆粒良好的分散性、部分結構呈現介孔狀,可使光催化反應速率明顯提高。
2.9 反應機理分析
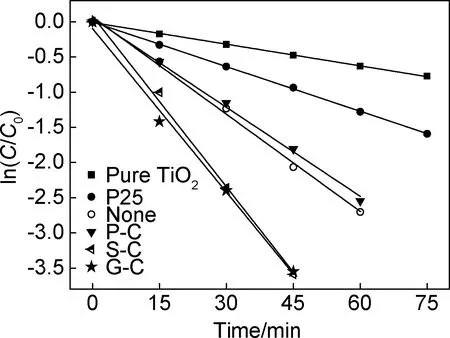
圖9 光降解反應準一級動力學擬合Fig.9 Photocatalytic reaction kinetics of MO decomposition

Samplek/min-1Pure TiO20.01027P250.02117None0.04607P-C0.04218S-C0.08087G-C0.07851
3 結論
(1)有機小分子和表面活性劑均可改善TiO2粒子在石墨烯片層的分散性,減少團聚現象。
(2)焙燒后的復合材料在石墨烯和TiO2間形成了較強且穩定的化學作用力。
(3)光催化效率最高的樣品G-C紫外可見吸收邊紅移至470nm以及其帶隙值減小至2.22eV,預示著復合材料的應用可拓展至可見光催化領域。
(4)在葡萄糖分子影響下合成的銳鈦礦型介孔材料光催化速率是商用P25的4倍,光照射30min甲基橙降解率可達92%,高電子遷移率的石墨烯與TiO2復合后,可大幅降低TiO2光生電子-空穴對的復合概率,從而提高催化活性。

