核磁共振橫向弛豫時間與金屬種類之間的關系
(南京林業大學現代分析測試中心, 南京 210037)
1 引言
水是地球上生物賴以生存的最重要物質之一。自然界中的水分子不是孤立的,而是通過氫鍵的作用使得若干個分子聚合在一起,形成水分子團。自從Dyke等人[1]于1977年驗證了二元水結構以來,水分子團[2-6]的實驗和理論研究已經成為一個重要的研究方向。多數的硫酸鹽易溶于水,溶液中的離子會使溶液中的水分子重新排列,而這樣排列的水分子結構與純水結構有較大的差異。因此鹽溶液中的氫核弛豫的研究對于水分子團的研究具有重要的理論和現實意義。
低場核磁共振技術[7]是基于自旋核在射頻磁場中的性質對材料進行分析的的一種測試方法。低場核磁共振因其成本低廉、無損、快速等優點在糧油食品[8-11]、地質勘探[12,13]、石油化工[14-18]等領域得到了廣泛的應用。本實驗利用低場核磁共振技術研究了硫酸鹽溶液中氫核,研究了鹽中的金屬離子的種類和溶液濃度對氫的弛豫時間的影響。
2 實驗部分
2.1 實驗試劑
實驗試劑為:硫酸銅(分析純);硫酸鎂(分析純);硫酸鈉(分析純);硫酸鋅(分析純);硫酸鐵(分析純);去離子水。
2.2 實驗儀器
VTMR20-010-T型低場核磁共振儀,磁場強度為0.5T,磁體溫度35℃,內徑為10mm的射頻線圈(蘇州紐邁科技有限公司);BSA224S型電子天平(北京賽多利斯科學儀器有限公司);Milli-Q超純水系統(美國密理博公司)。
2.3 實驗方法
分別以Na2SO4、MgSO4、MnSO4、Fe2(SO4)3、CuSO4、ZnSO4配制出濃度為0.01~0.10g/mL的硫酸鹽溶液作為實驗樣品。取相同體積各濃度的溶液樣品分別裝入試劑瓶內待測。
利用自由感應衰減信號調節共振中心頻率。將待測樣品充分溶解并靜置過夜后放入射頻線圈中心,利用CPMG[19,20]脈沖序列測量樣品的衰減信號。CPMG實驗采用的參數:P90=4.0μs,P180=9.0μs,回波個數=16000, 重復等待時間TW=5s,重復掃描次數NS=8。利用核磁共振弛豫時間采用Sirt算法反演,迭代次數10000次得到自旋-自旋弛豫時間。
3 結果與討論
3.1 水和硫酸溶液的自旋-自旋弛豫
采用CPMG脈沖序列掃描純水樣品的CPMG衰減曲線,利用多指數軟件對其進行反演,得到橫向弛豫時間分布。實現低場核磁共振信號的穩定性和測試結果的準確性的一個重要條件是保持樣品所在區域靜磁場的相對均勻。影響核磁共振信號的信噪比的主要因素是樣品量和測試區域的范圍。圖1是橫向弛豫時間反演峰面積與試樣量之間的線性關系圖,可以看出樣品量在1.5mL以下橫向弛豫時間反演峰面積與試樣量之間的相關性較強,相關系數R2=0.9995。為了使試樣在樣品腔中的磁場相對均勻,實驗中的樣品量控制在0.5mL。
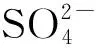
圖1 水量和橫向弛豫峰面積的關系圖
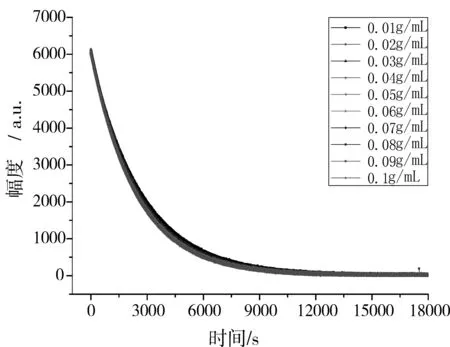
圖2 不同濃度的硫酸中氫核的CPMG衰減曲線
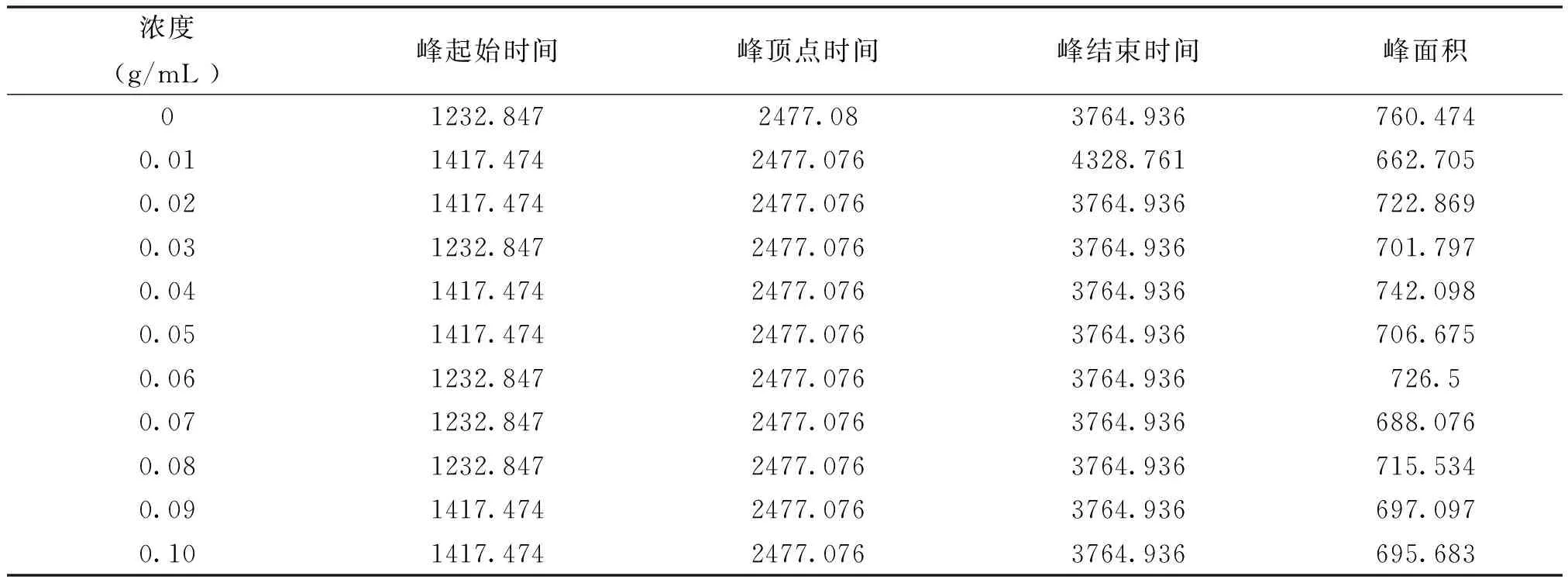
濃度(g/mL )峰起始時間峰頂點時間峰結束時間峰面積0 1232.8472477.083764.936760.4740.011417.4742477.0764328.761662.7050.02 1417.4742477.0763764.936722.8690.03 1232.8472477.0763764.936701.7970.04 1417.4742477.0763764.936742.0980.05 1417.4742477.0763764.936706.6750.06 1232.8472477.0763764.936726.50.07 1232.8472477.0763764.936688.0760.08 1232.8472477.0763764.936715.5340.09 1417.4742477.0763764.936697.0970.10 1417.4742477.0763764.936695.683
3.2 金屬離子對溶液中的自旋-自旋弛豫的影響
圖3為體積為500μm、濃度為0.01g/mL的8種硫酸鹽溶液的T2譜。相比較而言,MnSO4水溶液的質子T2變化最大,這說明Mn2+與氫質子發生自旋-自旋相互作用最強。在硫酸鹽溶液中,由于金屬陽離子的附近具有電場,周圍的電場可以使部分水分子發生定向排列,水的微觀結構發生變化,氫核被周圍環境束縛的更緊,弛豫過程變快。
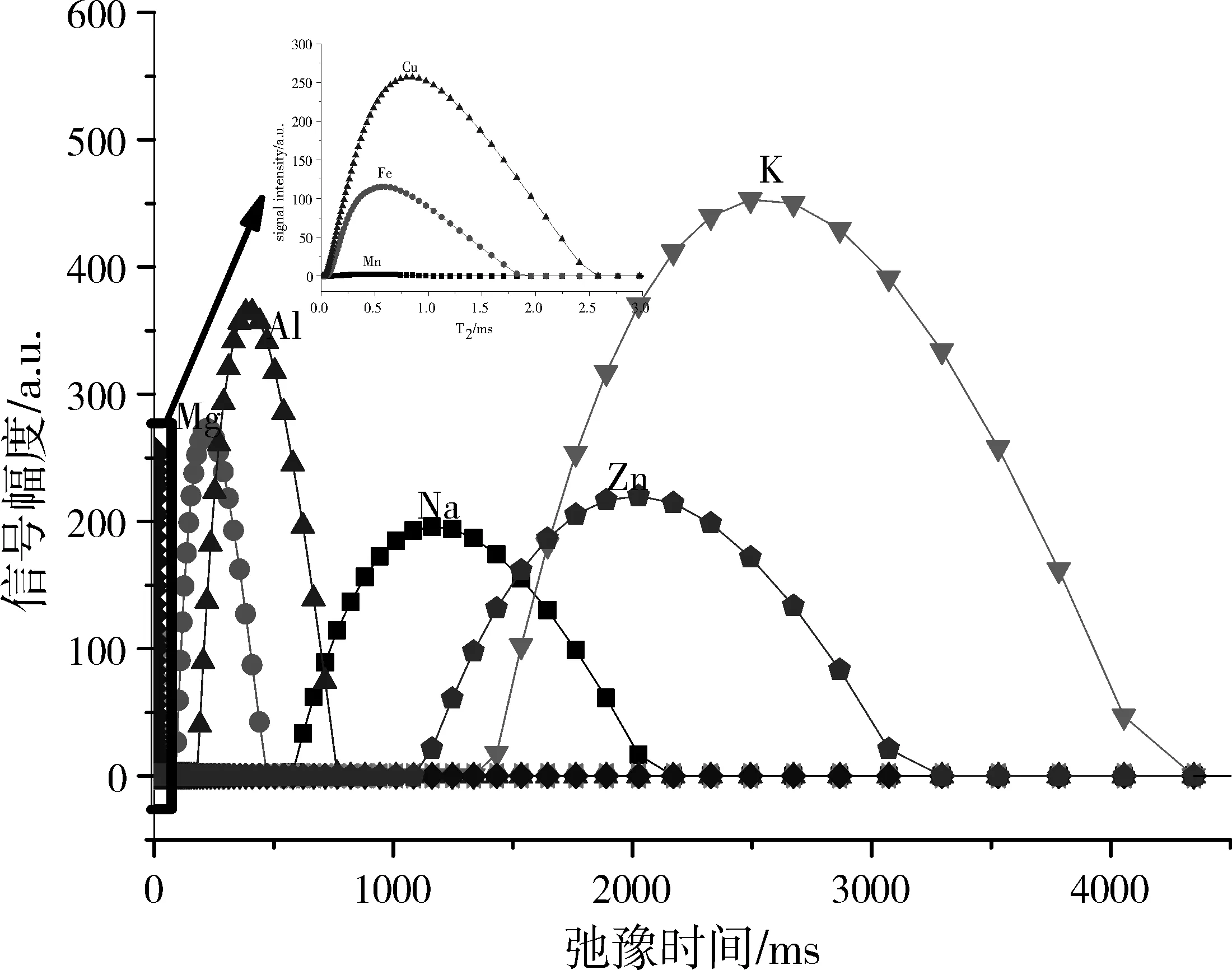
圖3 在濃度為0.01 g/mL的硫酸鹽中的氫核的橫向弛豫時間分布曲線
圖4是不同金屬離子對硫酸鹽溶液中的氫核的橫向弛豫時間的影響柱狀圖。圖中虛橫線是純水中的氫核的弛豫時間,不同金屬陽離子對液體中氫核的弛豫快慢有差異,由強到弱的順序如下:Mn2+>Fe3+>Cu2+>Mg2+>Al3+>Na+>Zn2+>K+。
3.3 金屬離子濃度與自旋-自旋弛豫時間的關系
選取0.01~0.1g/mL等間隔的10份硫酸鹽溶液進行核磁共振橫向弛豫時間的測試,得到回波信號衰減圖,采用儀器反演軟件對回波信號數據進行擬合,得到不同濃度下溶液中氫質子的橫向弛豫時間分布圖。隨著金屬鈉離子濃度的增加,質子的弛豫過程加快,橫向弛豫時間縮短。T2峰的半高寬和面積隨著濃度增加而變小。硫酸鹽在水中溶解后,溶液中存在大量的陽離子,陽離子周圍的電場束縛住靠近離子的水分子,使得氫核的弛豫變短。
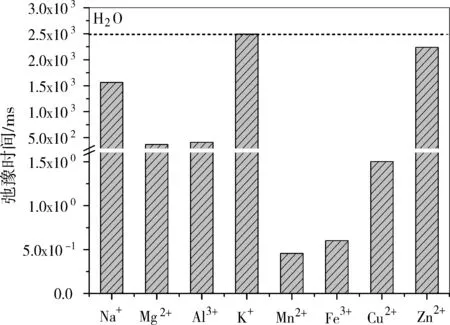
圖4 不同金屬離子對硫酸鹽溶液中的氫核的橫向弛豫時間的影響
圖5是不同溶液濃度與1/T2的關系曲線。從圖中可以看出,金屬離子Na+、Mg2+、Al3+、K+、Mn2+、Fe3+、Cu2+、Zn2+都可以使水中氫核的T2變小,但影響程度不同。為進一步研究陽離子的加入對氫核的低場核磁橫向弛豫時間的影響,實驗對弛豫時間的倒數隨溶液濃度變化關系進行擬合,數據如表2所示。結果顯示,K+離子加入對溶液中氫核的橫向弛豫時間的影響不大,抗磁性金屬離子Zn2+除外,價態相同時,半徑越大,橫向弛豫時間越小。在Na2SO4、MnSO4、Fe2(SO4)3和ZnSO4溶液中的質子的1/T2與溶液濃度之間的相關性較小,Mg2+、Al3+、Cu2+溶液中的氫核的1/T2與溶液濃度之間的相關性較大,相關系數大于0.99,可用于離子的定量測定。
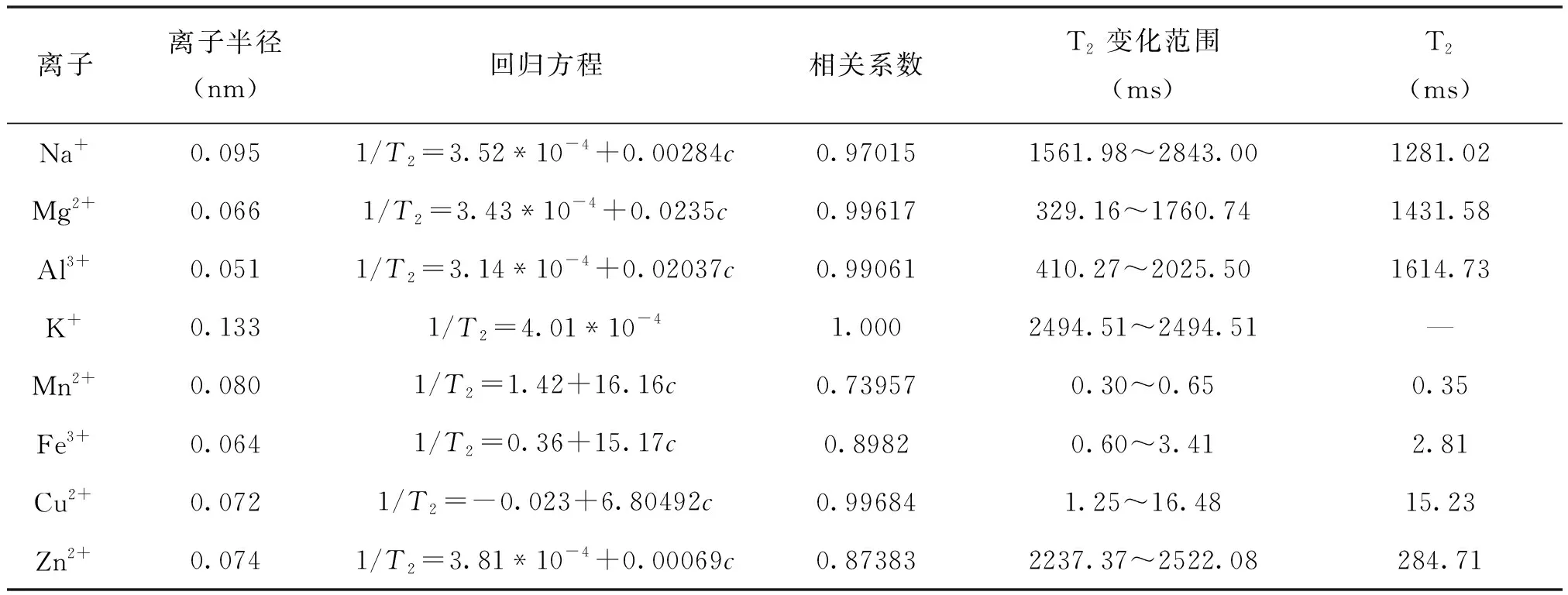
表2 弛豫參數與硫酸鹽的相關性
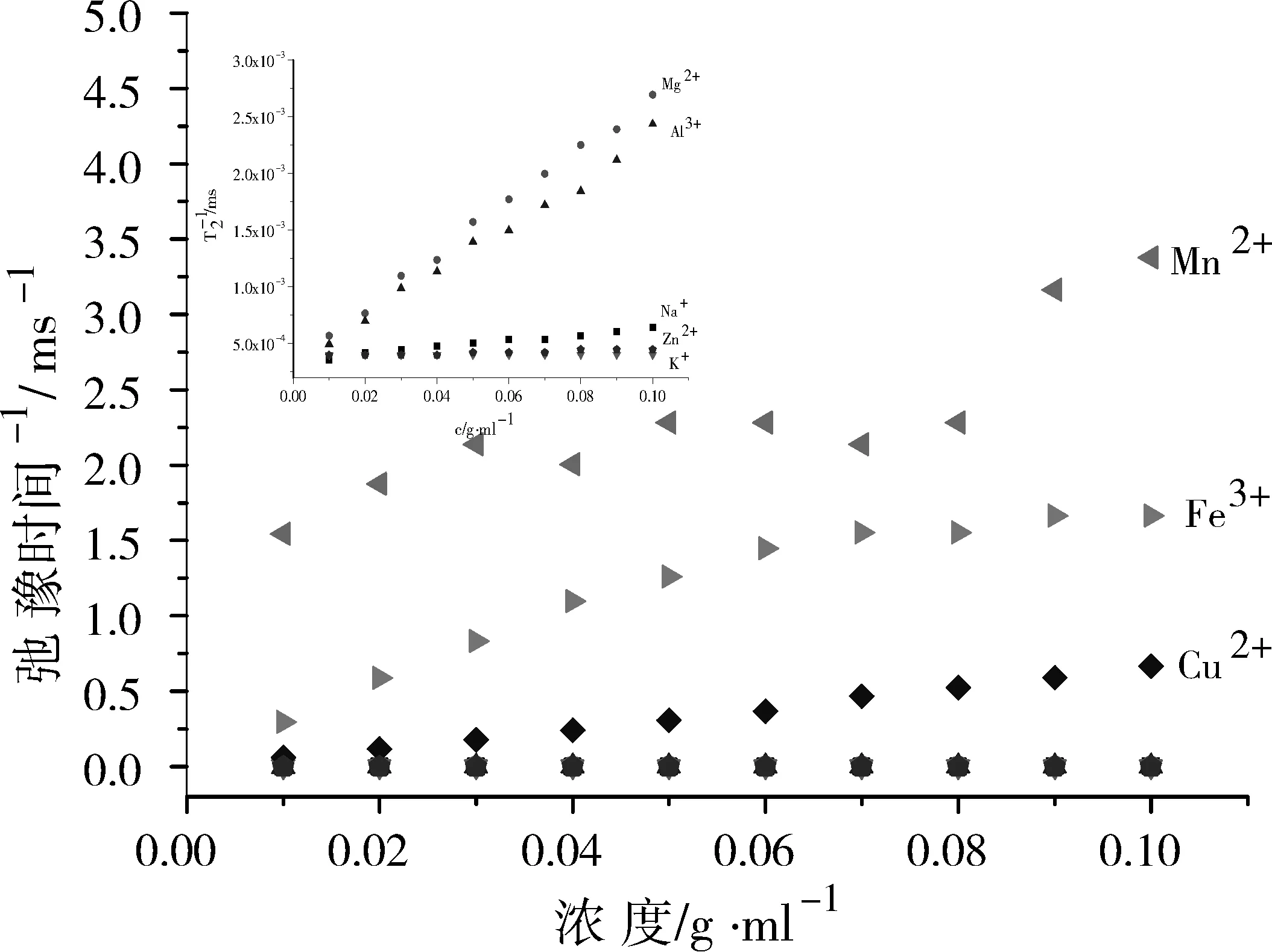
圖5 隨硫酸鹽濃度的變化
4 結 束 語
利用低場核磁共振技術測量了不同硫酸鹽溶液中的氫核的橫向弛豫時間,研究了核磁共振信號隨離子種類和濃度的變化規律,在一定濃度下,金屬離子對水中的氫質子的橫向弛豫時間的影響程度由強到弱的順序為:Mn2+>Fe3+>Cu2+>Mg2+>Al3+>Na+>Zn2+>K+。金屬陽離子的濃度越高,陽離子產生的電場,使得水分子更緊密的結合在陽離子周圍,形成體積較大的水團簇,氫核的束縛緊密,氫核的弛豫時間越短。Mg2+、Al3+和Cu2+溶液中的質子的橫向弛豫時間與離子濃度成反比例關系。利用這個關系提出一種通過測試核磁共振T2譜確定離子濃度的方法。

