靜脈造影引導及連續X線透視輔助下PICC置管術的可行性研究*
陳 潔,李雙喜,黨 磊,宋來昌,杜靜媛,薛四倩,李佩佩,甘培英
蘭州大學第一醫院,甘肅 蘭州730000
外周中心靜脈置管術(PICC)是一種經由外周靜脈插入導管,在中心靜脈(上腔靜脈)定位導管尖端的深靜脈置管技術。PICC導管具有操作便捷、穿刺痛苦小、保護外周血管、保留時間長、創傷小、經培訓后護士可獨立操作、并發癥少等優點,適用于輸注高滲性、刺激性藥物、腫瘤化療、長期靜脈輸液治療、腸外營養的患者。常規置管技術程序繁瑣,適應癥有限[1]。國內外在穿刺入路選擇、改良置管技術及B超等的引導方面,取得了一定成果。本研究在靜脈造影引導下,從入路選擇、置管過程及最后定位,全程監測,提高了PICC置管成功率,降低了置管并發癥的發生,具有廣泛的臨床應用前景[2-3]。本研究對進行PICC置管的150例患者分別進行了盲穿、超聲引導下、靜脈造影引導及連續X線透視輔助下的PICC置管術,取得了一定成果,現報道如下:
1 資料與方法
1.1臨床資料將2012年1月至2013年12月因惡性腫瘤長期化療在蘭州大學第一醫院進行PICC置管術的患者150例按隨機數字表法分為盲穿組(A組)、超聲引導下穿刺組(B組)、靜脈造影引導及連續X線透視輔助穿刺組(C組),每組50例,各組均采用巴德公司生產的3項瓣膜式4F PICC導管。A組中男34例,女16例;年齡46~75歲,平均(61.2±3.8)歲;乳腺癌8例,肺癌33例,食管癌9例。B組中男29例,女21例;年齡42~76歲,平均(62.3±4.1)歲;乳腺癌12例,肺癌27例,食管癌11例。C組中男32例,女18例;年齡48~80歲,平均(65.2±2.9)歲;乳腺癌14例,肺癌22例,食管癌14例。3組患者基線資料比較差異無統計學意義(P>0.05)。
1.2納入標準納入:1)年齡>18歲者;2)所患疾病不限:3)臨床資料完整,符合醫學倫理學要求,知情同意,且簽署知情同意書者。
1.3排除標準排除:1)血流動力學不穩定,不宜進行PICC置管術者;2)上肢靜脈疾病患者;3)凝血障礙異常患者;4)精神失常無法進行溝通交流者。
1.4方法
1.4.1 物品與器械準備 全數字化大平板DSA血管造影機1臺,萬級層流導管室1間,三向瓣膜F4 PICC導管(巴德,美國);改良賽丁格穿刺組件(泰爾茂公司,日本);PICC穿刺包(內含消毒敷料2塊、洞巾1塊、眼科剪1把、彎頭止血鉗1把);止血帶,短微導絲,無菌生理鹽水,碘海醇對比劑,一次性注射器,安爾碘皮膚消毒劑,無菌手套;Progreat微導管配套微導絲備用。
1.4.2 盲穿組PICC操作方法 囑患者平臥于病床上,在肘下兩橫指處選擇靜脈及穿刺點,測量置管長度,進行消毒。操作者需穿無菌手術衣,鋪無菌孔巾,20°~30°角進針,保持穿刺點位置推進插管鞘,松開止血帶,固定插管鞘,將導管自插管鞘內緩慢、勻速送入。置管完成后拍胸部X線片確定導管末端位置。
1.4.3 超聲組PICC操作方法 患者平臥于病床上,用彩超或B-Flow技術探查、引導穿刺肘關節區靜脈,在超聲引導下評估肘上關節2~4 cm最佳穿刺部位,在穿刺點做標記并測量置管長度,常規消毒、鋪巾、穿無菌手術衣,用保護套保護無菌探頭。穿刺前在超聲引導下再次定位血管,左手固定探頭,右手在B超引導下以30°~45°角穿刺進入皮膚,穿刺完成后固定穿刺針,將導絲經由穿刺針芯送入,撤出穿刺針,沿導絲送入插管鞘,然后撤離導絲,將導管自插管鞘內置入預期長度,剝離套管,采用超聲探頭探測貴要靜脈、正中靜脈、頭靜脈,確定無異常后固定導管,拍胸部X線片明確導管頭端位置。
1.4.4 靜脈造影引導及連續X線透視輔助下PICC操作方法 患者平臥于DSA導管床上,手背穿刺普通頭皮針1枚,在患者肩關節下兩橫指處扎止血帶,推注造影劑20 mL,全面觀察上肢靜脈走行路線。根據靜脈造影圖像,在X線透視下定位并找出穿刺靶靜脈(常用貴要靜脈),確定PICC置管路徑。用泰爾茂專用靜脈穿刺針穿刺靜脈,待回血后松開止血帶,退出套管針穿刺針,將親水涂層短導絲經由套管針外套管置入,導絲插入深度大于10 cm,否則不能為導管鞘的置入提供足夠的支撐力。將導絲留置于靜脈中,緩慢退出外套管,沿著親水涂層短導絲將導管鞘緩慢置入,需留置導管鞘管于皮膚外4~5 cm,方便PICC管的放置。將導管鞘內的擴張管拔出,剪去導管鞘閥門,在導管鞘殘端墊敷料,因為此時靜脈血會從導管鞘殘端流出。為避免患者流血過多,操作者可用手指堵住導管鞘殘端,囑助手準備PICC管,由操作者在最短時間內將PICC管插入,靜脈造影透視下沿預定途徑經腋靜脈、鎖骨下靜脈送至上腔靜脈內,置管過程中如出現靜脈段狹窄,走行迂曲,靜脈成角銳利等情況,可以拔除PICC導管內的支撐導絲后置入Progreat微導管配套微導絲,通過導管導絲配合技術置管。待置管完成后,退出導管鞘殘端,用眼科剪將PICC管外露部分剪短,保留一定長度在體外,用消毒棉球擦凈血漬后安裝連接器,用透明敷貼固定,攝片。
1.5觀察指標比較各組1次穿刺置管成功率、操作時間、穿刺過程中并發癥發生率(心律失常、靜脈血栓、靜脈炎、局部血腫、穿刺點感染、導管異位);判定各組PICC成功標準:導管是否到達上腔靜脈(輸液是否通暢)。
1.6統計學方法數據采用SPSS 15.0統計軟件分析,計數資料采用χ2檢驗,計量資料采用LSD-t檢驗,檢驗水準為α=0.05。
2 結果
2.1置管操作時間置管操作時間A、B、C組分別為(12.8±3.1)min、(8.4±1.2)min、(5.2±2.1)min,A、B 組比較差異具有統計學意義(P<0.05),B、C 組比較差異具有統計學意義(P<0.05)。
2.21次置管成功率1次置管成功率A、B、C組分別為 72%、90%、92%,A、B 組比較差異具有統計學意義(χ2=5.26,P<0.05);B、C 組比較差異無統計學意義( χ2=0.12,P>0.05),見表 1。
2.3穿刺過程中并發癥發生情況并發癥發生率 A、B、C 組分別為 22%、8%、2%,A、B 組比較差異具有統計學意義( χ2=3.84,P<0.05);B 組并發癥發生率高于C組,但2組比較差異無統計學意義(χ2=1.89,P>0.05),見表 2。
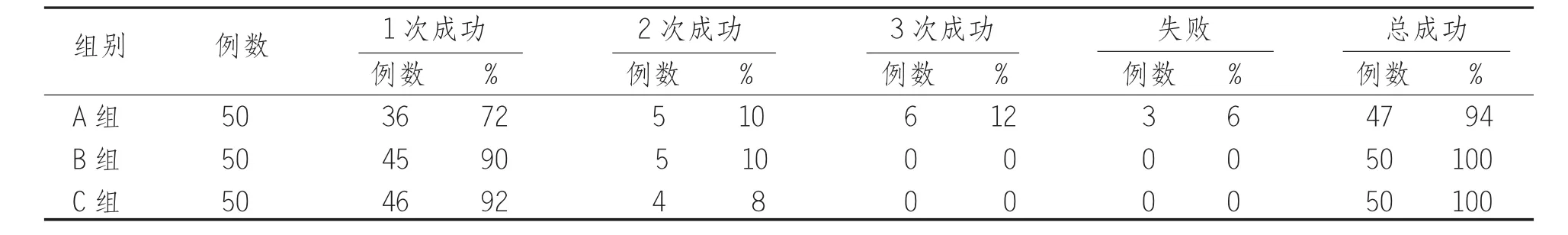
表1 3組患者1次置管成功率比較
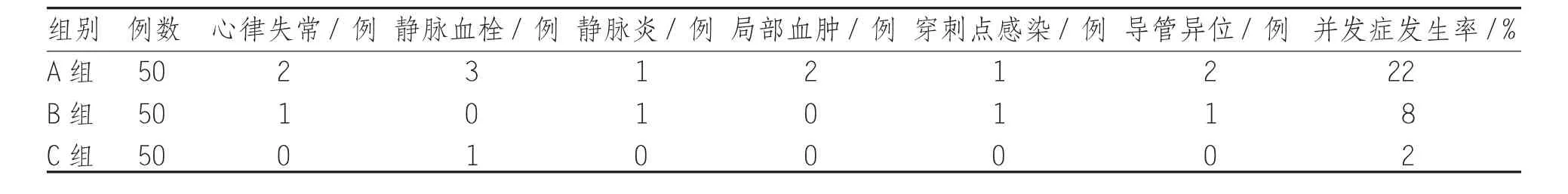
表2 3組患者穿刺過程中并發癥發生情況
3 討論
中心靜脈置管術(central venous catheters,CVC)在20世紀中期開始應用于臨床,且隨著相關技術發展的不斷成熟,CVC已經成為臨床常見的操作項目,據英國NHS 2004統計結果表明,每年進行CVC操作的患者達到200 000例,且有逐漸增加趨勢[4-5]。進行CVC操作可進行血液透析及輸注血制品、化療藥物和抗生素、特殊藥物(如血管加壓素)、血流動力學測定等。根據CVC的使用時間、目的、功能的不同可分為植入性輸液港(PORT)、永久性中心靜脈置管(隧道型CVC)、暫時性中心靜脈置管(非隧道型 CVC)、PICC[6-7]。PICC具有簡單易學,風險低,對操作者要求低等優點,在臨床上已被廣泛應用[8-9]。PICC已被證實在操控性方面優于其他CVC,臨床進行置管時一般經肘部血管穿刺將PICC管送至上腔靜脈內,但由于PICC穿刺套管針較粗,當肘部血管顯示不清時會給操作者穿刺帶來困難。且在進行反復補液后上肢靜脈內膜易破損,在進行放、化療后容易閉塞鎖骨下靜脈、腋靜脈,頭靜脈匯入深靜脈時角度過小等給PICC置管術帶來難度,甚至導致置管失敗[10-11]。
靜脈造影引導下X線透視輔助進行PICC可避免上述缺陷,可根據靜脈走行及時調整穿刺方向,且可直觀觀察導管穿刺到靜脈后的終端位置,提高穿刺成功率[12-13]。相關研究[14-15]表明,經彩超引導下的PICC置管術有10.1%的異位率,采用X線透視輔助置管可及時避免異位的發生,可對PICC置管后頭端進行X線攝片定位,連續X線透視下PICC置管可及時糾正插管過程中出現導管打折、迂回、異位而導管末端未能到達上腔靜脈情況,導管末端100%在上腔靜脈。
本研究結果表明,超聲引導組及靜脈造影引導X線透視輔助下置管組的1次置管成功率明顯高于盲穿法組(P<0.05),超聲引導組、靜脈造影引導X線透視輔助下置管組的1次置管成功率比較差異無統計學意義(P>0.05);盲穿法組的并發癥發生率高于超聲引導組(P<0.05);靜脈造影引導X線透視輔助下置管組的并發癥發生率高于超聲引導組,但2組比較差異無統計學意義,可能與樣本量較少有關(P>0.05);置管操作時間靜脈造影引導X線透視輔助下置管組高于超聲引導組(P<0.05),超聲引導組高于盲穿法組(P<0.05)。表明靜脈造影引導下的PICC靜脈穿刺成功率不低于彩超引導下的PICC置管,連續X線透視下動靜脈置管和在靜脈造影引導下PICC置管可明顯減少置管時間,減少并發癥的發生率。
綜上所述,采用靜脈造影引導X線透視輔助下PICC置管術1次置管成功率與超聲引導下無差別,且能夠降低并發癥的發生率,減少操作時間,值得臨床推廣使用。

