血清VEGF、ES、adropin聯合檢測在多囊卵巢綜合征中的診斷效能
孫琳,裴史灼,覃英梅
(三亞市婦幼保健院,海南三亞 57200)
多囊卵巢綜合征(PCOS)在育齡期女性中發病率高達5%~10%,且呈逐年上升趨勢,其中因PCOS導致患者不孕的幾率高達74%[1],僅低于輸卵管阻塞,且患者遠期易患子宮內膜增生、阻塞性睡眠呼吸暫停、焦慮、抑郁等,嚴重影響患者的身體健康和生活質量[2~3]。PCOS具體發病機制尚未明確。卵巢血管生成異常是導致PCOS發生發展的原因之一[4]。VEGF可對血管生成進行調節,同時改善血管通透性,ES是VEGF的拮抗因子,adropin蛋白是一種新型的分泌性蛋白,可調節能量平衡。VEGF、ES、adropin蛋白均與PCOS的發生具有密切關聯[5],但血清VEGF、ES、adropin蛋白聯合檢測在PCOS中的診斷效能尚不明確。本研究觀察了血清VEGF、ES、adropin蛋白聯合檢測在PCOS中的診斷效能。現報告如下。
1 資料與方法
1.1 臨床資料 選擇2015年6月~2016年6月收治的47例PCOS患者作為觀察組。納入標準[6]:①符合2003年鹿特丹國際會議所制定的關于PCOS的診斷標準,同時符合以下2項者可確診:a排卵率低;b經超聲可見多個囊性卵泡,直徑為2~10 mm,但無優勢卵泡;c具有高雄激素的臨床表現或患有高雄激素血癥。②不孕病史高于1年;③配偶生殖功能正常。排除標準:①患有全身炎性疾病、腎上腺疾病、高泌乳素血癥等;②近期有激素類藥物服用史。觀察組患者年齡23~37(28.03±3.61)歲。選擇同期因男方因素不孕而接受體檢的健康女性47例作為對照組。納入標準:①因男方患有不孕病癥而就診的生育期女性;②月經規律;③超聲下子宮及附近無異常;④無其他盆腔病變。排除標準同觀察組。對照組患者年齡23~37(28.03±3.61)歲。兩組患者年齡相比,P>0.05。本研究已獲醫院醫學倫理委員會批準。入組者均簽署知情同意書。
1.2 血清VEGF、ES、adropin蛋白檢測及胰島素抵抗指數(HOMA-IR)測算 收集兩組受試者卵泡早期,即月經周期第2~4天時晨起空腹靜脈血靜脈血5 mL,3 000 r/min離心10 min,提取上層血清后置入EP管,并置于冷凍箱內儲存以備檢測。血清VEGF、ES及adropin蛋白均采用酶聯免疫吸附法進行檢測,試劑盒購于赫澎(上海)生物科技有公司,儀器均使用Formacs TOC/TN分析儀。所有操作均嚴格按照試劑盒說明進行。采用全自動生化分析儀檢測兩組受試者血清胰島素和血糖,HOMA-IR=血清胰島素×血糖/22.5。
2 結果
2.1 兩組血清VEGF、ES、adropin蛋白及HOMA-IR比較 兩組血清VEGF、ES、adropin蛋白及HOMA-IR見表1。觀察組患者血清VEGF、ES及HOMA-IR水平顯著高于對照組(P均<0.05);觀察組患者血清adropin蛋白水平明顯低于對照組,(P<0.05)。
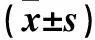
表1 兩組血清VEGF、ES、adropin蛋白水平及HOMA-IR比較
注:與對照組相比,*P<0.05。
2.2 血清VEGF、ES、adropin蛋白聯合檢測在PCOS中的診斷效能 血清VEGF、ES水平與HOMA-IR呈正相關(r=0.717、0.554,P均<0.05),血清adropin蛋白水平與HOMA-IR呈負相關(r=-0.275,P<0.05)。血清VEGF、ES、adropin蛋白水平及三者聯合檢測診斷PCOS的AUC分別為0.670(95%CI為0.560~0.780)、0.747(95%CI為0.646~0.849)、0.830(95%CI為0.749~0.911)、0.916(95%CI為0.862~0.970)。血清VEGF、ES、adropin蛋白水平單獨診斷PCOS檢測的AUC和聯合檢測診斷PCOS的AUC相比,P均<0.05),聯合檢測診斷PCOS的AUC較高。
3 討論
卵巢是血管生成最為活躍的器官之一[7,8]。當卵巢處于生殖周期時,血管生成發生障礙或異常則會導致卵巢間質、卵泡囊血管增生,造成卵巢增大,故血管生成在PCOS的進展中具有重要作用[9,10]。VEGF是一種可高效促進血管生成的因子,通過酪氨酸激酶受體而對血管內皮細胞的分裂起促進作用,從而促進組織血管生成[11]。涂銨素等[12,13]研究發現,VEGF存在于卵巢和子宮中,且生殖器是機體循環中VEGF最為主要的來源,可維持卵泡周圍的血流,同時提高機體毛細血管的通透性,引起血漿蛋白外滲、卵巢增大,最終對卵泡、黃體血管生長起促進作用。VEGF在PCOS患者體內呈過量表達。本研究結果也顯示,PCOS患者血清VEGF水平顯著高于健康人群,且與HOMA-IR呈正相關,與上述觀點一致,提示PCOS患者機體卵泡囊及卵巢間質微血管均存在增生,同時VEGF水平呈高表達則是卵巢間質發生血管化的基礎,可能是PCOS的發病機制之一。
ES是特異性血管生成抑制因子,該因子通過提高內皮細胞的凋亡率,降低血管內皮增殖,阻礙血管內皮細胞遷移等對新生血管的形成進行有效抑制[14,15]。相關研究發現,ES可誘導內皮細胞一氧化氮合酶失活,從而降低VEGF所誘導的一氧化氮的生成,從而抑制由VEGF所介導的血管生成及血管通透性上升[16]。有學者提出,因胰島素對血管內皮細胞的活動具有刺激作用,尤其是機體血清中內皮素、VEGF等,使腎素-血管緊張素-醛固酮系統呈現過度活躍,最終導致機體脂肪組織合成激素、分泌細胞因子出現異常,這也可能是PCOS患者ES增高的原因之一[17,18]。本研究結果顯示,PCOS患者血清ES水平顯著高于健康人群,且與HOMA-IR呈正相關,筆者分析其原因是在PCOS發展過程中,卵巢組織合成分泌出VEGF以促進血管生成,而機體為維持自身穩定,則會產生大量抑制劑對卵巢血管生成的高水平進行抑制,但這種自身的代償作用無法將卵巢環境恢復至正常,最終會因調節失衡而導致卵巢增生。
adropin蛋白是一種分泌型蛋白,可參與到能量的平衡調節及糖、脂肪酸的代謝控制當中。相關研究指出,adropin蛋白表達與代謝性疾病、內皮功能等均具有密切的關聯[19]。血清adropin可通過激活葡萄糖氧化的限速酶(丙酮酸脫氫酶),提高細胞膜的葡萄糖轉運蛋白4的水平,最終有效提高機體對胰島素的敏感性。本研究結果顯示,PCOS患者血清adropin水平低于健康人群,且與HOMA-IR呈負相關,提示adropin可作為診斷PCOS的輔助參考指標。
本研究結果顯示,血清VEGF、ES、adropin蛋白水平聯合診斷PCOS的AUC為0.916,高于上述各指標單獨診斷PCOS的AUC,提示血清VEGF、ES、adropin蛋白水平聯合檢測在診斷PCOS上具有更高的效能,應引起臨床重視。
參考文獻:
[1] 史曉明,祁秀娟,呂映頻,等. 多囊卵巢綜合征患者血清VEGF及PEDF與卵巢過度刺激綜合征的關系[J]. 現代婦產科進展,2015,24(05):360-362+365.
[2] 陳曉紅,徐彩生,劉璇芝. 胰島素抵抗對多囊卵巢綜合征患者血清性激素水平的影響[J]. 山東醫藥,2015,55(14):50-51.
[3] Naji M, Aleyasin A, Nekoonam S, et al. Differential Expression of miR-93 and miR-21 in Granulosa Cells and Follicular Fluid of Polycystic Ovary Syndrome Associating with Different Phenotypes[J]. Sci Rep, 2017 ,7(1):14671.
[4] 宋夢玲,王飛苗,李彩艷,等. 血清及卵泡液中肝素結合性表皮生長因子水平與多囊卵巢綜合征關系的研究[J]. 實用婦產科雜志,2015,31(7):508-511.
[5] 艾風連,徐玉萍,趙林海,等. 多囊卵巢綜合征患者促甲狀腺素濃度與性激素、胰島素抵抗及血脂關系的分析[J]. 生殖與避孕,2015,35(7):463-467.
[6] Zheng Q, Li Y, Zhang D, et al.ANP promotes proliferation and inhibits apoptosis of ovarian granulosa cells by NPRA/PGRMC1/EGFR complex and improves ovary functions of PCOS rats[J]. Cell Death Dis, 2017,8(10):3145.
[7] 李揚璐,阮祥燕,崔亞美,等. 四種血清脂蛋白比值對多囊卵巢綜合征患者發生代謝綜合征的診斷預測價值[J]. 首都醫科大學學報,2015,36(4):559-566.
[8] 孔雯,肖西悅,曾天舒,等. 二甲雙胍對多囊卵巢綜合征患者血清同型半胱氨酸水平影響的系統評價[J]. 華中科技大學學報(醫學版),2015,44(5):540-544.
[9] Zhao H, Zhou D, Chen Y,et al.Beneficial effects of Heqi san on rat model of polycystic ovary syndrome through the PI3K/AKT pathway[J]. Daru, 2017 ,25(1):21.
[10] 李修陽,張寧,任健,等. 多囊卵巢綜合征痰濕證患者血清代謝組學分析及其生物標志物篩選[J]. 山東醫藥,2015,55(37):15-18.
[11] 李艷秋,侯麗輝,高金金,等. 多囊卵巢綜合征中醫證型分布規律及血清性激素、糖代謝特點的研究[J]. 中華中醫藥學刊,2016,34(3):579-582.
[12] 趙曉蘭,馮琳. 二甲雙胍聯合維格列汀對多囊卵巢綜合征合并糖代謝異常的臨床療效研究[J]. 中國臨床藥理學雜志,2016,32(6):517-519,528.
[13] 涂銨素,鐘影,毛熙光. 多囊卵巢綜合征合并不孕癥患者血清TOS,TAS水平變化及其與血漿載脂蛋白(a)的關系[J]. 南方醫科大學學報,2016,36(03):405-409.
[14] 王利娟,阮祥燕,崔亞美,等. 多囊卵巢綜合征不同表型的血清抗苗勒管激素水平特征的分析[J]. 首都醫科大學學報,2016,37(4):444-448.
[15] Vital-Reyes VS, Lopez-Alarcón MG, Inda-Icaza P, et al.Subtle metabolic alterations in adolescents with obesity and polycystic ovarian syndrome[J].Gac Med Mex,2017,153(Supl 2):34-41.
[16] 任春瓊,肖涌,李毅,等. 二甲雙胍對多囊卵巢綜合征患者性激素水平、胰島素抵抗及相關指標的影響[J]. 中國藥房,2016,27(27):3791-3794.
[17] Tessaro I, Modina S, Lodde V, et al.Ultra-low Doses of Follicle Stimulating Hormone and Progesterone Attenuate the Severity of Polycystic Ovary Syndrome Features in a Hyperandrogenized Mouse Model[J].J Reprod Infertil,2017 ,18(3):288-297.
[18] 劉梅梅,丁慧,尹曉靜,等. 多囊卵巢綜合征患者血清血管內皮生長因子、內皮抑素水平及對卵巢間質血流的影響研究[J]. 中國全科醫學,2017,20(04):448-453.
[19] 何興鳳,汪慶如,姚慧,等. 多囊卵巢綜合征患者血清adropin的表達及意義[J]. 廣東醫學,2017,38(10):1505-1508.

