鎂及鎂合金植入性醫療器械的應用研究進展
吳戍戌,王守仁,劉文濤
(濟南大學機械工程學院,山東 濟南 250022)
隨著鎂及鎂合金材料的不斷發展,其作為生物醫用材料制造植入性醫療器械的研究受到材料學和醫學領域研究者的廣泛關注。早在19世紀初,植入性醫療器械的材料主要是不銹鋼,20世紀初又出現了鈷-鉻基合金、鈦合金等金屬材料的植入性醫療器械[1]。這些金屬材料稱為惰性金屬,因為具有優異的耐腐蝕性能、力學性能和機械加工性能,在臨床上得到廣泛應用,但仍存在許多缺點,例如其密度及彈性模量與自然骨相差較大,容易造成應力遮擋現象,影響骨組織的生長和延長愈合時間等等。這些金屬材料制備的植入性醫療器械植入人體內后基本上不會發生降解,還需要進行二次手術將其取出來,這增加了患者的痛苦和經濟負擔。另外,這些金屬材料在人體內會發生磨損和磨蝕,釋放有毒的離子(鋁離子、鎳離子等),從而引發炎癥,造成組織損傷[2-4]。從20世紀50年代開始,生物陶瓷和高分子材料開始受到研究者的關注,這些材料雖然具有優異的生物相容性和骨誘導性,但是其力學性能較差[5]。
基于以上原因,尋找一種既滿足力學性能又滿足生物相容性的植入性醫療器械材料成為關鍵。而鎂及鎂合金材料就符合以上要求:(1)鎂合金與人體自然骨的力學性能指標(表1)最為接近,這樣就能夠有效地避免應力遮擋效應,展現出良好的力學相容性;(2)鎂具有較低的標準電極電位(-2.37 V),化學性質活潑,在人體體液中特別容易與Cl-等發生化學反應,可自主完全降解;(3)鎂不但是人體中必不可少的基本元素,而且是體內含量第四的陽離子,具有良好的骨誘導效應,會縮短骨折修復時間,對組織無刺激性,多余的Mg2+將隨尿液排出體外。(4)鎂在自然界中分布非常廣泛,是地殼中含量第八的元素,價格低廉,易于加工成型[6-9]。為此,在20世紀初期,研究者開始基于鎂及鎂合金在體內的可自主完全降解性和生物相容性,研制出新一代的植入性醫療器械,并將其用于骨科及心血管等領域[10]。本文對鎂及鎂合金植入性醫療器械在骨科和心血管領域的應用研究進展進行綜述,以期為醫療器械領域材料研究提供參考依據。
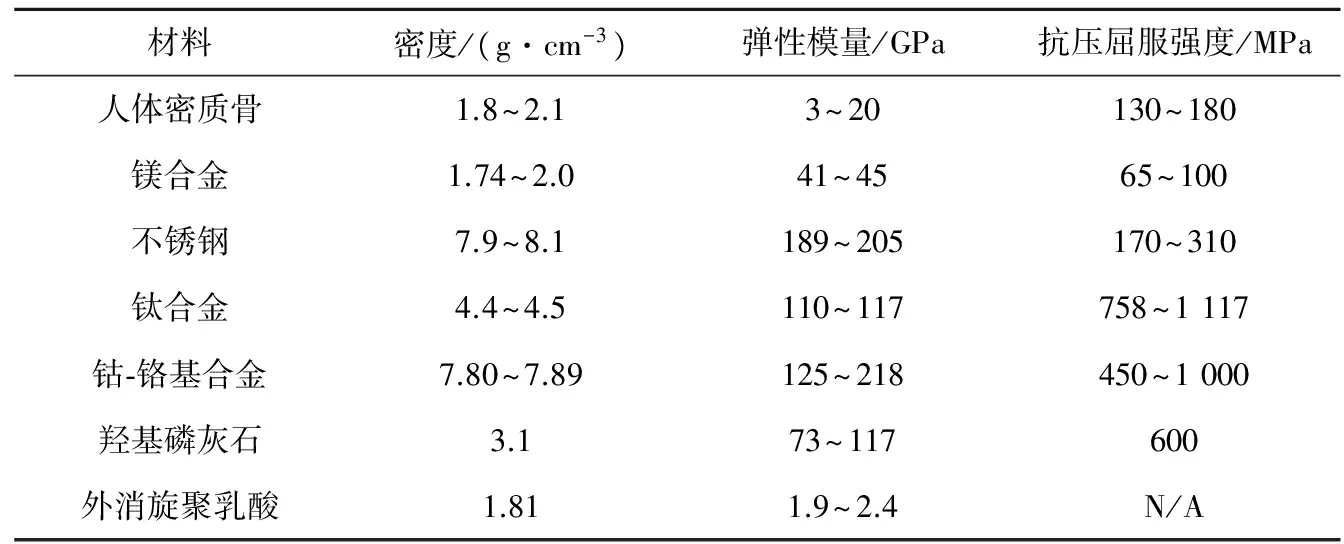
表1 自然骨和現有骨植入材料的力學性能對比[11]Table 1 Comparison of mechanical properties of various currently available implant materials and naturalbone [11]
1 骨科領域
1.1 骨板和螺釘
鎂及鎂合金骨板和螺釘通過植入,對骨折處進行良好的復位和堅強固定,通過骨組織的再生能力實現骨折處的自我修復,從而達到治愈的目的[12]。1907年,Lambotte[13]將純鎂制備的骨板和螺釘進行植入,發現除了在骨板周圍產生少量的氣體外,并沒有出現其他癥狀,骨折處愈合。隨后在1938年,Mcbride[14]將鎂錳合金制備的骨板和螺釘進行骨折內固定,發現鎂合金全部降解,而且該材料有可能會促進硬質骨的形成。1944年,Troitskii等[15]將鎂鈣合金制備的骨板和螺釘植入34例骨折患者中,其中有9例患者由于感染或皮下氣腫等原因而失敗,但是所有患者的血清中均未出現Mg2+濃度升高的現象。以上早期對鎂及鎂合金骨板和螺釘的研究表明,其具有優異的生物相容性并且有可能會刺激新骨的形成,但是由于其在體內耐腐蝕性較差、降解速度太快,短時間內產生大量的氣體,無法長期提供有效的固定支撐,再加上隨著不銹鋼等惰性金屬的應用,限制了其在臨床上的應用。直到二十世紀90年代[16],隨著冶金、金屬表面防護處理、熱處理及塑性加工工藝等技術的快速發展,鎂及鎂合金的耐腐蝕性得到顯著提高,其作為骨板和螺釘等植入性醫療器械材料的研究取得了較大的發展。
1.1.1 改進鎂及鎂合金的冶金技術
1.1.1.1 提高鎂的純度
當具有雜質(Fe、Cu、Ni等元素)的鎂及鎂合金與腐蝕介質接觸時,電極電位較低的鎂與電極電位較高的雜質將會形成原電池,加速鎂及鎂合金的腐蝕[17-18]。其中,Fe、Cu、Ni 3種元素在純鎂中容許極限(質量分數)是1.70×10-4、1.0×10-3、5×10-6,當雜質含量超過其容許極限時,純鎂的耐腐蝕性能會急劇下降[19]。為此,通過凈化熔煉技術、選用高純度原料等方法可以有效地提高鎂及鎂合金的耐腐蝕性能,減緩其降解速率。Han等[20]利用凈化熔煉技術制備高純度鎂(HP Mg)螺釘,發現HP鎂螺釘在兔股骨髁間骨折固定顯示形態均勻且具有足夠彎曲力。Chaya等[21]選用高純度鎂(99.9%)制備骨板,并將其在兔尺骨骨折模型中進行評估,發現其降解速度減緩,而且骨板周圍形成新的骨組織。Wang等[22]利用凈化熔煉技術制備高純度鎂骨板,并在Hank動態液和靜態液中進行分析,發現在穩定環境下,鎂的表面會形成一層磷酸鹽類保護膜,提高了其耐腐蝕性。雖然提高鎂的純度可以改善其耐腐蝕性,但是工藝復雜、效率低,在臨床上應用的較少。
1.1.1.2 制備新型鎂合金
通過添加不同含量的鈣、鋁、稀土、鍶及鋅等元素進行冶煉而得到新型鎂合金,可以改善鎂合金的耐腐蝕性能、力學性能及生物相容性[23]。Naujokat等[24]用鎂合金(WE43)制備骨板和螺釘,發現其降解速度緩慢,平均腐蝕率為0.122±0.042 mm/a,而且骨板的外形和體積基本上不變,仍起到固定作用。Zhang等[25]發現在鎂鋅合金中加入0.2%的鈣元素后,鎂合金的腐蝕速率下降約1/3,其表面膜層電阻增加了5倍,但是隨著鈣含量的增加,其腐蝕速率加快。Feyerabend等[26]在鎂合金Mg-Nd-Zn-Zr(JDBM)中加入少量的稀土元素,發現不但能保證鎂合金具有良好的力學性能,并且還可以提高鎂合金的電極電位,從而提高鎂合金的耐腐蝕性能。張廣道[27]將AZ31B鎂合金制備的骨板植入新西蘭大白兔下頜骨,觀察到在骨板周圍包裹有一層纖維結締組織,將該纖維結締組織與骨板分離,可見骨板邊緣處有新生骨生成。目前應用比較成熟的新型鎂合金大多都是商用鎂合金,雖然這些鎂合金可以有效地改善其耐腐蝕性能,但是并沒有考慮生物相容性,大多含有對人體有害的元素。
1.1.2 提高鎂及鎂合金的表面防護處理技術
金屬表面防護處理技術是改善鎂及鎂合金腐蝕過快問題最有效的方法之一。通過化學轉化涂層、有機高分子涂層、微弧氧化涂層、激光表面處理等方法,不僅能夠有效地改善鎂及鎂合金耐腐蝕性能,而且還能提高生物相容性。Wu等[28]利用微弧氧化技術,在鎂合金(AZ31)骨板上制備了具有生物相容性MAO涂層,并設置未處理的鎂合金骨板為對照組,發現有MAO涂層和未涂層的鎂合金骨板均能促進骨折愈合,但是有涂層的降解速度緩慢。Schaller等[29]對鎂合金(WE43)骨板表面進行等離子體電解,將未處理的鎂合金骨板設置為對照組,實驗結果表明具有涂層的骨板改善了其耐腐蝕性能,而且具有很好的穩定性。Wang等[30]通過脈沖電沉積法在鎂合金(Mg-Zn-Ca)骨板表面制備羥基磷灰石(HA)涂層,發現該涂層不僅顯著提高了鎂合金的耐腐蝕性能,而且具有優異的生物相容性。曲立杰[31]采用超聲微弧氧化技術對鎂合金螺釘進行表面處理,發現其起到固定作用的時間長達半年,而且血液中鎂離子的濃度均在參考范圍內。雖然鎂及鎂合金表面防護處理技術繁多,但是其成本較高、部分處理技術污染較為嚴重,而且缺乏在不同的環境下都具有突出性能的表面防護處理技術。
1.1.3 改進鎂及鎂合金的熱處理及塑性加工工藝
熱處理及塑性加工工藝不但可以調整鎂及鎂合金內部的組織,獲得更好的強韌化效果,而且能轉變組織中的第二相的結構、形態和分布,從而改善其綜合性能[32-33]。常見的熱處理方法有固溶處理、固溶時效處理、人工時效處理等,塑性加工工藝有擠壓、軋制、鍛造等。Zhang等[34]研究了固溶處理和時效處理對Mg-4.5Zn-4.5Sn-2Al合金的顯微組織和力學性能的影響,并在模擬體液中檢測其腐蝕速度,結果表明,經熱處理后合金的強度和塑性都得到了提高,而且其腐蝕速度下降。Gu等[35]研究ZK60合金在模擬體液中的耐蝕性能,發現擠壓態ZK60合金的晶粒得到了優化,因此減小了其腐蝕速率。Kuwahara等[36]將熱處理后的純鎂置于HBSS溶液中浸泡,發現試樣的重量不但沒有減小,反而有所增加,表明熱處理工藝處理的純鎂在其表面形成的氧化層,有效地提高了其耐蝕性。雖然鎂合金熱處理和塑性加工工藝的方法較多,但是加工過程復雜、成本高,而且不同系列的鎂合金在加工過程中出現的微觀組織形態、分布和數量各有不同,還需要對其進行深入研究。
1.2 骨組織多孔支架
骨組織多孔支架是植入體內一個具有生物活性的多孔三維支架,通過誘導骨細胞的繁殖、分化,在支架表面及孔隙中生長出新的礦化骨組織,同時生物三維支架逐漸降解、吸收,達到修復骨缺損、實現骨再生的目的[37-38]。Witte等[39]發現孔隙率為72%~76%的多孔鎂合金(AZ91D)支架的降解對周圍骨組織無任何有害影響,且有良好的生物相容性,能促進新骨的形成和再吸收。Zhang等[40]制備的相互連接的多孔鎂合金支架,孔隙率為33%~54%,實驗測得其彈性模量和抗壓屈服強度范圍分別為0.10 GPa~0.37 GPa和11.1 GPa~30.3 MPa,這與自然骨的力學性能類似。

鎂及鎂合金骨組織多孔支架由于增加了其與體液的接觸面積,所以其腐蝕更加嚴重,降解速率加快。為了改善這種情況,通過表面防護處理技術、冶金技術、熱處理等方法能提高其耐腐蝕性能,但是效果最明顯的方法還是表面防護處理技術[45]。Yu等[46]在多孔可降解的AZ31鎂合金支架表面用氟化物處理來獲得MgF2涂層,結果表明增強了多孔支架的耐腐蝕性,減緩了降解速度,而且在體內誘導形成更多的新骨。Yazdimamaghani等[47]在低真空條件下,采用浸涂技術,在多孔鎂合金支架表面制備聚己內酯(PCL)和生物活性玻璃(BG)的生物活性陶瓷涂層,實驗結果表明復合支架的生物活性、機械完整性、耐蝕性和降解速度均明顯改善。沈劍等[48]采用粉末冶金方法制備的多孔生物鎂,孔隙率為35%,并通過堿熱處理法對其進行表面改性,實驗結果表明制得的多孔生物鎂的力學性能可以滿足作為植入材料的要求,而且耐腐性顯著增強。
1.3 國內外臨床應用現狀
在骨科臨床應用方面,目前應用最多的是鈦合金材料,用來制作骨板、螺釘和骨組織多孔支架等[49]。由于鎂及鎂合金的降解速率未得到有效的控制,耐腐蝕性較差以及可降解金屬體內風險評估標準未健全等問題,在臨床上應用的較少,主要處于實驗室研究階段,目前只有鎂合金螺釘在臨床上得到應用[50-51]。國外最具代表的是德國的漢諾威公司生產的鎂合金螺釘,在2013年獲得歐盟的CE認證,應用于治療手部、腳部骨折的手術中[52]。2015年,韓國U&I公司生產的鎂鈣合金螺釘也獲得了韓國藥監局的認證,應用在手部骨折內固定手術中[53]。在國內,中國科學院、上海交通大學、重慶大學等高校對鎂合金植入性醫療器械進行了大量的相關研究,并取得了可喜的成果[54-55]。其中,東莞宜安科技和大連大學附屬中山醫院合作制備的鎂合金金屬螺釘,已經在中國食品藥品安全檢定研究院進行注冊形式檢驗[56]。2017年,滬創醫療科技(上海)有限公司與上海交通大學合作已將JDBM鎂合金制備成骨板和螺釘,正在申請臨床實驗[57]。
雖然我國研究者對鎂及鎂合金的理論研究走在了世界的前列,但是在臨床應用與轉化方面已經落后于德國和韓國等發達國家,目前需要加快國內鎂及鎂合金植入性醫療器械的臨床應用轉化進程。
2 心血管領域
2.1 血管支架
血管支架置入重建血運是臨床上治療心絞痛、急性心肌梗死以及各種心腦血管疾病的重要手段[58]。鎂及鎂合金血管支架具有克服傳統惰性金屬支架因長期植入引起的慢性炎癥、晚期支架血栓以及需長期服用抗血小板藥物等問題的潛在優勢[59]。Erbel等[60]將鎂合金(WE43)血管支架植入患者的冠狀動脈中,發現器官狹窄率由61.5%±13.1%降低到12.6%±5.6%,支架完全降解后總體靶病變血運重建率為45%。Waksman[61]將鎂合金支架(AMS)植入患者的冠狀動脈內,發現鎂合金支架緩慢消失,血管通暢率72.4%,保肢率為94.7%,與永久性血管支架相比,避免了慢性炎癥和內膜增生。孫建紅[62]通過有限元分析鎂合金WE43材料和316L不銹鋼材料的心臟血管支架,發現鎂合金支架的變形抗力和膨脹內壓力均小于不銹鋼支架,而回彈率和順柔性較高,從而在治療心血管狹窄疾病方面具有很大的潛力。
改善鎂及鎂合金血管支架的耐腐蝕性和制備藥物洗脫支架,已成為近幾年的研究熱點[63]。
(1)通過冶金、表面防護處理等技術能有效地改善鎂及鎂合金血管支架的耐腐蝕性,減緩其降解速率。Lu等[64]通過在鎂合金AZ81血管支架表面上制備微弧氧化/聚乳酸(MAO/ PLL A)復合涂層,在Hank's溶液中進行體外分析,其結果顯示耐腐蝕性提高,減緩了其降解速率,而且相比于316L不銹鋼具有更好的血液相容性。Liu等[65]在新型鎂合金Mg-Zn-Y-Nd血管支架上制備了復合涂層,上層為聚多巴胺(PDA)層,下層為MgF2層,將其進行體外實驗測試,實驗結果顯示其耐腐蝕性增強、具有良好的細胞粘附和增殖性能。毛琳等[66]在鎂合金Mg-Nd-Zn-Zr支架(JDBM)表面制備了一層均勻的納米級MgF2涂層,并進行體外腐蝕性能測試,發現鎂合金支架的腐蝕速度從之前的0.337±0.021 mm/a下降到了0.269±0.043 mm/a,耐腐蝕性能提高了約20%,而且MgF2膜層的表面鱗片有利于細胞的增殖、粘附,從而增強了支架的生物相容性。
(2)藥物洗脫支架不但可以對血管進行擴張,而且可以避免出現血管局部炎癥。Shi等[67]在鎂合金Mg-Nd-Zn-Zr血管支架上制備了雷帕霉素載藥涂層,在磷酸鹽緩沖系統中進行分析研究,發現鎂合金支架上的載藥系統對體外平滑肌細胞增殖具有有效的長期抑制作用,而且支架腐蝕緩慢。Gu等[68]在鎂合金血管支架表面制備聚乳酸-乙醇酸共聚物(PLGA)涂層,將其植入大鼠血管中,并采用裸支架作為對照組,實驗結果顯示該涂層有效地改進了支架的耐腐蝕性和減少血管中血栓的沉積。Zhang等[69]通過在聚合物(3-羥基丁酸酯-3-羥基己酸酯)中,添加阿魏酸(FA)的方法制備可生物降解的藥物洗脫鎂合金血管支架的涂層,實驗結果顯示該涂層能夠抑制血液凝固,具有更好的血液相容性。在鎂及鎂合金血管支架上載藥進行局部治療不僅是未來發展的趨勢,而且是整個植入性醫療器械的發展趨勢。
2.2 血管縫合線
血管縫合線是用來結扎血管傷口、縫合止血的一種特殊用線。目前在臨床上使用的主要為人工合成高分子血管縫合線,而鎂及鎂合金血管縫合線應用的較少[70]。在二十世紀初,國外研究學者曾嘗試使用鎂絲進行血管縫合手術。然而,因為技術問題導致鎂絲的延展性達不到要求,妨礙了其用作可降解的縫合線的研究進程[71]。Seitz等[72]將鎂鈣合金通過拉拔成形工藝,制造直徑為0.1 mm~0.5 mm的縫合線,這些縫合線符合手術縫合線所需的各個參數,相對于傳統縫合線,鎂及鎂合金血管縫合線具有良好的力學性能和可降解性。付婧怡[73]利用室溫冷拉拔和中高溫退火的工藝將高純度鎂直徑從5.0 mm拉拔至0.9 mm,獲得符合各種手術參數的血管縫合線,發現晶粒細化可提高縫合線的強度和硬度,并可以提高耐腐蝕性。
2.3 國內外臨床應用現狀
在心血管臨床應用方面,應用最多的是高分子聚合物可降解支架,其次是鎂合金降解支架[74]。在鎂及鎂合金降解支架領域,國外最具代表性的是德國的Biotronik公司采用鎂合金WE43研制的全降解血管支架,其開展工作最早,臨床應用也最成熟[75]。至今,其生產的鎂合金血管支架經歷了裸支架(AMS-1)到紫杉醇藥物洗脫支架(DREAMS 1G)再到雷帕霉素藥物洗脫支架(DREAMS 2G)不同階段的發展,支架植入部位也從風險較小的下肢動脈發展到風險較高的冠狀血管,其中雷帕霉素藥物洗脫支架(DREAMS 2G)已于2016年獲CE認證[76-77]。在國內,我國自主研究的鎂合金血管支架主要有上海交通大學袁廣銀教授組[78]采用自主研發的鎂合金(Mg-2.5Nd-0.2Zn-0.4Zr)制備的血管支架和北京大學奚廷斐研究員[79]采用鎂合金(Mg-2.0Zn-0.5Y-0.5Nd)制備的血管支架。其中袁廣銀教授制備的鎂合金血管支架在臨床上已經證明具有良好的生物相容性、優異的力學性能和耐腐蝕性能。
3 存在問題與未來發展趨勢
3.1 存在問題
從21世紀初開始,應用鎂及鎂合金作為植入性醫療器械的材料是國內外的研究熱點,但是由于相關技術難度大、人體內環境復雜等原因,現階段鎂及鎂合金植入性醫療器械仍存在許多不足。
(1)耐腐蝕較差。在體內復雜的環境中,由于體液富含Cl-,并且在腐蝕過程中伴隨著pH的不斷變化,鎂及鎂合金的腐蝕情況復雜的多。其在模擬體液中的腐蝕主要以電偶腐蝕、點蝕、疲勞腐蝕和磨損腐蝕等局部腐蝕為主,其中以電偶腐蝕和點蝕對鎂及鎂合金的損壞最為巨大。
(2)降解速度未得到有效的控制。由于降解過快,無法提供長期有效的固定支撐功能,再加上其降解過程中短時間內產生大量的氣體,造成皮下氣腫;其腐蝕產物為Mg(OH)2,會導致局部體液堿化,從而造成組織損傷。
(3)植入性醫療器械容易造成局部感染。一方面,植入性醫療器械植入后對機體來說是異物,機體會產生免疫排斥反應;另一方面,在手術過程中,通過其本身帶入感染源,常常誘發感染的發生,導致手術失敗。
(4)雖然有大量的實驗證明鎂及鎂合金植入醫療器械具有良好的生物相容性和新骨誘導性,但是大部分實驗都是小規模、簡單的隨機實驗,得到的數據不足以說明鎂及鎂合金植入性醫療器械具有良好的遠期臨床效果,而且可能存在著尚未發現的不良反應。
(5)目前研究的醫用鎂合金大部分都是商用鎂合金,設計之初并沒有考慮生物的相容性。例如鋁元素是鎂合金常用的合金元素,由于鎂合金AZ31降解,產生的Al離子可能會對神經造成傷害,從而引發老年癡呆等癥狀。
3.2 未來發展趨勢
為了解決目前鎂及鎂合金植入性醫療器械存在的問題,未來主要從以下個方面進行入手:
(1)利用冶金技術研制新型醫用鎂合金。通過添加Ca、Zn、Re、Sr、Mn等元素或者調整合金元素的含量,來提高鎂合金的抗腐蝕性能及生物相容性。例如Mg-Re系合金,其中稀土元素具有固溶強化和沉淀強化的作用,可以改善鎂合金的高溫拉伸和蠕變性能,同時有利于提高耐蝕性。
(2)開發低成本、環保、適應性廣的表面處理技術,提高鎂及鎂合金的耐腐蝕性能并控制降解速度。其方法包括超聲微弧氧化、激光表面改性、冷噴涂等,這些方法可以使鎂及鎂合金表面具有的單層防護性能的膜層結構轉變為復雜多層的膜層結構。
(3)利用新型的熱處理及塑性加工工藝增強鎂及鎂合金的塑性變形能力,調整微觀結構組織,從而提高其強度和改善其耐腐蝕性。例如激光熔覆、氫化處理、化學熱處理等。其中經過化學熱處理后可以得到表面均勻平整、無污染、耐腐蝕性能優于傳統工藝的防護膜。
(4)研制具有抗感染作用的新型鎂及鎂合金植入性醫療器械,以減少植入感染的發生,改善臨床療效。例如原位多孔納米涂層儲運聚維酮碘內固定器械、藥物洗脫鎂合金支架。其中原位多孔納米涂層儲運聚維酮碘內固定器械不但能夠滿足內固定的需求,而且又能減少感染的發生。
(5)建立標準的實驗體系,使鎂及鎂合金的腐蝕和降解速度獲得更加可靠的科學依據,從而了解其在體內的力學性能和降解速度,避免出現尚未發現的不良反應,建立可降解金屬的體內風險評估標準。
4 結論
綜上所述,鎂及鎂合金植入性醫療器械由于具有優異的力學相容性、良好的生物相容性、可自主完全降解并且資源豐富、易于加工成型等優勢,在骨科和心血管領域得到了廣泛的應用。隨著科學技術的發展和研究的不斷深入,鎂及鎂合金植入性醫療器械將表現出巨大的應用前景。而且,我國已將鎂及鎂合金植入性醫療器械的研發及制備列入了國家“十三五”計劃[80]中,相信在不久的將來,我國自主研發的鎂及鎂合金植入性醫療器械能夠在臨床上得到廣泛應用。
參考文獻:
[1]鄭凱,于秀淳,郭征,等.生物金屬材料在骨科的應用及發展[J].生物骨科材料與臨床研究,2013,10(2): 31-33.
[2]王昌,王嵐,宇森,等.可降解鎂及鎂合金作為骨植入材料的研究進展[J].廣東化工,2016,43(15): 124-126.
[3]《中國組織工程研究與臨床康復》雜志社學術部.醫用金屬材料相關產品的應用現狀和發展趨勢[J].中國組織工程研究,2010,14(51): 9621-9622.
[4]PERSAUD-SHARMA D,McGORON A.Biodegradable magnesium alloys:a review of material development and applications [J].Journal of Biomimetics Biomaterials & Tissue Engineering,2011,12: 25-39.
[5]ZHANG X,PENG X,ZHANG S W.7-Synthetic biodegradable medical polymers:polymer blends [EB/OL].[2017-11-23].https://www.sciencedirect.com/science/article/pii/B9780081003725000076.
[6]張濤,武肖娜,尹慶水,等.鎂合金AZ31B材料表性與成骨細胞的黏附[J].中國組織工程研究,2013,17(12): 2123-2130.
[7]殷正正,曾榮昌,崔藍月,等.醫用可降解鎂合金表面磷酸鹽涂層研究進展[J].山東科技大學學報(自然科學版),2017,36(2): 57-69.
[8]李濤,張海龍,何勇,等.生物醫用鎂合金研究進展[J].功能材料,2013,44(20): 2913-2918.
[9]WANG J,TANG J,ZHANG P,et al.Surface modification of magnesium alloys developed for bioabsorbable orthopedic implants: a general review [J].Journal of Biomedical Materials Research Part B: Applied Biomaterials,2012,100(6): 1691-1701.
[10]ZHENG Y F,GU X N,WITTE F.Biodegradable metals [J].Mater Sci Eng,2014,77: 1-34.
[11]LI R W,KIRKLAND N T,TRUONG J,et al.The influence of biodegradable magnesium alloys on the osteogenic differentiation of human mesenchymal stem cells [J].Journal of Biomedical Materials Research Part A,2014,102(12): 4346-4357.
[12]成翔宇,紀斌,龐金輝.骨折的生物學內固定及內固定材料性能分析[J].中國組織工程研究,2012,16(22): 4121-4124.
[13]LAMBOTTE A L.L'utilization du magnesium comme matériel perdu dans l'ostéosynthèse [J].Bull Mém Soc Nat Cir,1932,28: 1325-1334.
[14]McBRIDE E D.Absorbable metal in bone surgery [J].Journal of the American Medical Association,1938,111(27): 2464-2467.
[15]TROITSKII V V,TSITRIN D N.The resorbing metallic alloy 'Osteosinthezit' as material for fastening broken bone [J].Khirurgiia,1944,8: 41-44.
[16]劉宣勇,彭峰.醫用可降解鎂合金表面改性研究進展[J].硅酸鹽學報,2017,45(10): 1421-1431.
[17]王新印.純鎂腐蝕行為研究[D].杭州:浙江大學,2015.
[18]QIAO Z,SHI Z,HORT N,et al.Corrosion behaviour of a nominally high purity Mg ingot produced by permanent mould direct chill casting [J].Corrosion Science,2012,61: 185-207.
[19]李智,周世杰,趙炯.生物醫用純鎂的腐蝕性能研究[J].熱加工工藝,2012,41(16): 53-56.
[20]HAN P,CHENG P F,ZHANG S X,et al.In vitro andinvivostudies on the degradation of high-purity Mg (99.99wt.%) screw with femoral intracondylar fractured rabbit model [J].Biomaterials,2015,64: 57-69.
[21]CHAYA A,YOSHIZAWA S,VERDELIS K,et al.Invivostudy of magnesium plate and screw degradation and bone fracture healing [J].Acta Biomaterialia,2015,18: 262-269.
[22]WANG H,SHI Z.Invitrobiodegradation behavior of magnesium and magnesium alloy [J].Journal of Biomedical Materials Research Part B Applied Biomaterials,2011,98 (2):203-209.
[23]ATRENS A,LIU M,ABIDIN N I Z,et al.3-Corrosion of magnesium (Mg) alloys and metallurgical influence [EB/OL].[2017-11-09].http://linkinghub.elsevier.com/retrieve/pii/B9781845697082500032.
[24]NAUJOKAT H,SEITZ J M,A?IL Y,et al.Osteosynthesis of a cranio-osteoplasty with a biodegradable magnesium plate system in miniature pigs [J].Acta Biomaterialia,2017,62: 434-445.
[25]ZHANG B P,HOU Y L,WANG X D,et al.Mechanical properties,degradation performance and cytotoxicity of Mg-Zn-Ca biomedical alloys with different compositions [J].Mater Sci Eng C,2011,31(8): 1667-1673.
[26]FEYERABEND F,FISCHER J,HOLTZ J,et al.Evaluation of short-term effects of rare earth and other elements used in magnesium alloys on primary cells and cell lines [J].Acta Biomaterialia,2010,6(5): 1834-1842.
[27]張廣道.AZ31B生物可降解鎂合金植入兔下頜骨生物學行為的實驗研究[D].沈陽:中國醫科大學,2009.
[28]WU Y F,WANG Y M,JING Y B,et al.Invivostudy of microarc oxidation coated biodegradable magnesium plate to heal bone fracture defect of 3mm width [J].Colloids & Surfaces B Biointerfaces,2017,158: 147-156.
[29]SCHALLER B,SAULACIC N,IMWINKELRIED T,et al.Invivodegradation of magnesium plate/screw osteosynthesis implant systems: Soft and hard tissue response in a calvarial model in miniature pigs [J].Journal of Cranio -Maxillo -Facial Surgery,2016,44 (3): 309-317.
[30]WANG H X,GUAN S K,WANG X,et al.Invitrodegradation and mechanical integrity of Mg-Zn-Ca alloy coated with Ca-deficient hydroxyapatite by the pulse electrodeposition process [J].Acta Biomater,2010,6(5): 1743-1748.
[31]曲立杰.鎂合金表面超聲微弧氧化生物涂層的組織結構與性能[D].哈爾濱:哈爾濱工業大學,2015.
[32]張玉,黃曉鋒,馬振鐸,等.熱處理工藝對Mg-6Zn-2Sm-0.4Zr鎂合金顯微組織和力學性能的影響[J].中國有色金屬學報,2017,27(10): 1961-1969.
[33]王爾德.鎂合金塑性加工產業技術研究進展[J].精密成形工程,2014,6(6): 22-30.
[34]ZHANGG H,CHEN J H,YAN H G,et al.Effects of artificial aging on microstructure and mechanical properties of the Mg-4.5Zn-4.5Sn-2Al alloy [J].Journal of Alloys and Compounds.2014,592: 250-257.
[35]GU X N,LI N,ZHENG Y F,et al.Invitrodegradation performance and biological response of a Mg-Zn-Zr alloy [J].Materials Science and Engineering: B,2011,176(20): 1778-1784.
[36]KUWAHARA H,ALABDULLAT Y,MAZAKI N,et al.Precipitation of magnesium apatite on pure magnesium surface during immersing in Hank’s solution[J].Materials Transactions,2001,42(7):1317-1321.
[37]CANCEDDA R,GIANNONI P,MASTROGIACOMO M.A tissue engineering approach to bone repair in large animal models and in clinical practice [J].Biomaterials,2007,28(29): 4240-4250.
[38]SOMMAR P,PETTERSSON S,NESS C,et al.Engineering three-dimensional cartilage- and bone-like tissues using human dermal fibroblasts and macroporous gelatine microcarriers [J].Journal of Plastic Reconstructive & Aesthetic Surgery,2010,63(6): 1036-1046.
[39]WITTE F,ULRICH H,RUDERT M,et al.Biodegradable magnesium scaffolds Part 1: appropriate inflammatory response [J].Journal of Biomedical Materials Research Part A,2007,81 (3): 748-756.
[40]ZHANG X,LI X W,LI J G,et al.Preparation and mechanical property of a novel 3D porous magnesium scaffold for bone tissue engineering [J].Materials Science & Engineering: C,2014,42: 362-367.
[41]牛麗媛.醫用多孔鎂基合金材料制備技術的研究進展[J].熱加工工藝,2010,39(4): 1-3.
[42]KANG M,JUNG H,KIM S,et al.Production and bio-corrosion resistance of porous magnesium with hydroxyapatite coating for biomedical applications [J].Materials Letters,2013,108: 122-124.
[43]LI Y,ZHOU J,PAVANRAM P,et al.Additively manufactured biodegradable porous magnesium [J].Acta Biomaterialia,2017,67:378-392.

[45]張贊,陳曉偉,夏興川,等.多孔鎂合金的研究現狀[J].特種鑄造及有色合金,2015,35(6): 580-585.
[46]YU W,ZHAO H,DING Z,et al.Invitroandinvivoevaluation of MgF2 coated AZ31 magnesium alloy porous scaffolds for bone regeneration [J].Colloids & Surfaces B Biointerfaces,2017,149: 330-340.
[47]YAZDIMAMAGHANI M,RAZAVI M,VASHAEE D,et al.Surface modification of biodegradable porous Mg bone scaffold using polycaprolactone/bioactive glass composite [J].Materials Science & Engineering C,2015,49(4): 436-444.
[48]沈劍,鳳儀,王松林,等.多孔生物鎂的制備及其表面改性[J].中國機械工程,2007,18 (10): 1230-1235.
[49]譙波,蔣電明.接骨板材料的研究現狀[J].重慶醫科大學學報,2017,42(2):180-184.
[50]阿迪亞提·阿不拉提,艾合買提江·玉素甫.生物可吸收內固定材料及其在掌骨干骨折治療中的應用[J].國際骨科學雜志,2017,38(6):357-359.
[51]李曉,劉京,吳強,等.接骨板用材料的研究現狀及發展前景[J].生物醫學工程學雜志,2016,33(6):1214-1219.
[52]SEITZ J M,LUCAS A,KIRSCHNER M.Magnesium-based compression screws: A novelty in the clinical use of implants [J].JOM,2016,68(4): 1177-1182.
[53]LEE J W,HAN H S,HAN K J,et al.Long-term clinical study and multiscale analysis of in vivo biodegradation mechanism of Mg alloy [J].Proceedings of the National Academy of Sciences of the United States of America,2016,113(3): 716-721.
[54]譚麗麗,陳軍修,于曉明,等.生物可降解MgYREZr合金的研究進展[J].金屬學報,2017,53(10): 1207-1214.
[55]佚名.中科院金屬研究所研發出新型可降解鎂銅合金[J].中國有色冶金,2016,37(5): 36.
[56]王祝堂.宜安科技鎂合金骨釘可于2014年年底臨床試驗[J].輕金屬,2016(1): 62.
[57]袁廣銀,牛佳林.可降解醫用鎂合金在骨修復應用中的研究進展[J].金屬學報,2017,53(10): 1168-1180
[58]譚志剛,周倩,蔣宇鋼.生物可降解鎂合金血管支架:缺點及未來研究趨勢[J].中國組織工程研究,2015,19(8): 1284-1288.
[59]LI J L,ZHENG F,QIU X,et al.Finite element analyses for optimization design of biodegradable magnesium alloy stent [J].Mater Sci Eng:C,2014,42: 705-714.
[60]ERBEL R,Di MARIO C,BARTUNEK J,et al.Temporary scaffolding of coronary arteries with bioabsorbable magnesium stents: a prospective,non-randomised multicentre trial [J].Lancet,2007,369(9576): 1869-1875.
[61]WAKSMAN R.Metallic bioabsorbable stents: Concepts,experimental findings,early clinical results,and the future [J].Acc Current Journal Review,2005,14(10): 36-43.
[62]孫建紅.鎂合金心臟血管支架結構設計及性能[D].沈陽:沈陽工業大學,2015.
[63]張小農,左敏超,張紹翔,等.醫用可降解血管支架臨床研究進展[J].金屬學報,2017,53(10): 1215-1226.
[64]LU P,FAN H N,LIU Y,et al.Controllable biodegradability,drug release behavior and hemocompatibility of PTX-eluting magnesium stents [J].Colloids & Surfaces B Biointerfaces,2011,83(1): 23-28.
[65]LIU X L,ZHEN Z,LIU J,et al.Multifunctional MgF2/polydopamine coating on Mg alloy for vascular stent application [J].Journal of Materials Science & Technology,2015,31(7): 733-743.
[66]毛琳,MINSUK K,陳佳慧,等.氟化鉀化學轉化涂層提高鎂合金血管支架耐蝕性和生物相容性[J].中國醫藥導刊,2015,17(增刊): 1-8.
[67]SHI Y J,PEI J,ZHANG L,et al.Understanding the effect of magnesium degradation on drug release and anti-proliferation on smooth muscle cells for magnesium-based drug eluting stents [J].Corrosion Science,2017,123: 297-309.
[68]GU X Z,MAO Z W,YE S H,et al.Biodegradable,elastomeric coatings with controlled anti-proliferative agent release for magnesium-based cardiovascular stents [J].Colloids Surf B Biointerfaces,2016,144: 170-179.
[69]ZHANG E L,FENG S.Blood compatibility of a ferulic acid (FA)-eluting PHBHHx system for biodegradable magnesium stent application [J].Materials Science & Engineering: C,2015,52: 37-45.
[70]KUMAR R S,SUNDARESAN S,宮慶雙.手術縫合線[J].國際紡織導報,2014,42(11):46-48.
[71]汪園園,馬愛斌,李玉華,等.可吸收醫用鎂合金縫合線的研究進展[J].功能材料,2015,46(s2): 32-37.
[72]SEITZ J M,DURISIN M,GOLDMAN J,et al.Recent advances in biodegradable metals for medical sutures: a critical review [J].Advanced Healthcare Materials,2015,4(13): 1915-1936.
[73]付婧怡.純鎂絲材拉拔工藝及在模擬體液中的腐蝕行為研究[D].哈爾濱:哈爾濱工業大學,2009.
[74]鄭玉峰,楊宏韜.血管支架用可降解金屬研究進展[J].金屬學報,2017,53(10):1227-1237.
[75]SERRUYS P W,CHEVALIER B,SOTOMI Y,et al.Comparison of an everolimus- eluting bioresorbable scaffold with an everolimuseluting metallic stent for the treatment of coronary artery stenosis (ABSORB II): A 3 year,randomised,controlled,single-blind,multicentre clinical trial [J].Lancet,2016,388(10059): 2479-2491.
[76]HAUDE M,ERHEL R,ERNE P,et al.Three-year clinical data of the Biosolve-I study with the paclitaxel-eluting bioabsorbable magnesium scaffold (Dreams) and multi-modality imaging analysis [J].Journal of the American College of Cardiology,2013,62(18): B13.
[77]HAUDE M,INCE H,ABIZAID A,et al.Safety and performance of the second- generation drug- eluting absorbable metal scaffold in patients with de- novo coronary artery lesions (BIOSOLVE- II): 6 month results of a prospective,multicentre,non-randomised,firstin-man trial [J].Lancet,2016,387(10013): 31-39.
[78]袁廣銀,章曉波,牛佳林,等.新型可降解生物醫用鎂合金JDBM的研究進展[J].中國有色金屬學報,2011,21(10): 2476-2488.
[79]奚廷斐,魏利娜,劉婧,等.鎂合金全降解血管支架研究進展[J].金屬學報,2017,53(10): 1153-1167.
[80]國務院.“十三五”國家科技創新規劃[EB/OL].[2017-10-23].http://www.gov.cn/zhengce/content/2016-08/08/content_5098072.htm.

