次全結腸切除術與Ⅱ期手術治療左半結腸癌伴急性腸梗阻的療效比較分析
馮海洋 劉卓 翟瑾潔 陳寅波 范永田 鞠海星?
結腸癌引起的腸梗阻是常見的外科急腹癥之一,8.0%~33.9%的結腸癌患者首發癥狀表現為急性完全或不完全性機械性腸梗阻[1-3]。約70%的結腸癌引起的腸梗阻位于左半結腸。對于左半結腸癌引起的腸梗阻,由于屬于閉襻性腸梗阻,腸管水腫較明顯,腫瘤遠近端腸管口徑相差較大,Ⅰ期吻合后容易引起吻合口漏;結直腸癌患者中老年患者較多,合并多種基礎疾病,病程較長,多存在貧血、低蛋白血癥,水電解質紊亂等危險因素,使得手術方式爭議較大。本文通過回顧性分析2001~2013年本院收治的60例左半結腸癌致急性完全性腸梗阻患者,比較行次全結腸切除、Ⅰ期吻合(次全切除組)與左半結腸切除、回腸造口(Ⅱ期手術組),對這兩種手術方式的術中、術后資料進行對比分析。
1 臨床資料
1.1 一般資料 2001年1月至2013年12月浙江省腫瘤醫院結直腸外科收治60例左半結腸癌伴急性完全性腸梗阻患者,其中男32例,女28例;平均年齡56歲。左半結腸癌Ⅰ~Ⅲ期伴有急性腸梗阻,無感染性休克表現。次全結腸切除術組患者(n=30)切除部位位于乙狀結腸、降結腸、脾曲及橫結腸分別有5例、8例、6例和11例,Ⅱ期手術組患者(n=30)切除部位位于乙狀結腸、降結腸、脾曲及橫結腸分別有7例、9例、5例和9例。兩組患者一般資料比較差異均無統計學意義(P>0.05),具有可比性。
1.2 治療方法 60例經積極非手術保守治療,癥狀及體征無緩解或進行性加重者,進行短時間積極術前準備后接受手術治療,術前準備包括:診斷明確后立即行持續有效的胃腸減壓;梗阻患者均有不同程度的水電解質及酸堿平衡紊亂,術前給予積極糾正,貧血患者予以糾正。
1.3 術前準備 患者進行手術治療前,首先給予胃腸減壓,對于有貧血癥狀的患者要適當糾正,通過CT等影像檢查確定病灶具體位置。
1.4 手術方法 所有患者的手術均為剖腹手術,次全結腸切除具體切除范圍包括末端回腸、右半結腸、橫結腸、游離結腸脾曲,同時切除部分降結腸,保證遠端切除距離腫瘤≥10cm,結扎切斷回結腸動脈,右結腸動脈和結腸中動脈,行回腸與乙狀結腸吻合。術中為了手術操作方便,可以將小腸移出腹腔外并用溫鹽水巾保護。游離結腸脾曲要特別注意勿損傷脾臟,在游離完畢后可以進行小腸減壓。對結腸斷端進行消毒處理后,回腸端放入吻合器抵釘座,將回腸與乙狀結腸行端側吻合,結腸殘端切割閉合器閉合[4]。Ⅱ期手術組行標準左半結腸切除加回腸造口,2~3個月后行回腸造口回納。
1.5 術后處理 所有患者術后均行8~12周期Folfox或Capoex方案輔助化療。
1.6 統計學方法 采用SPSS 12.0統計軟件。計數資料采用χ2檢驗,計量資料采用t檢驗或確切概率法,采用Kaplan-Meier法繪制生存曲線,P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者術中、術后情況比較 見表1。
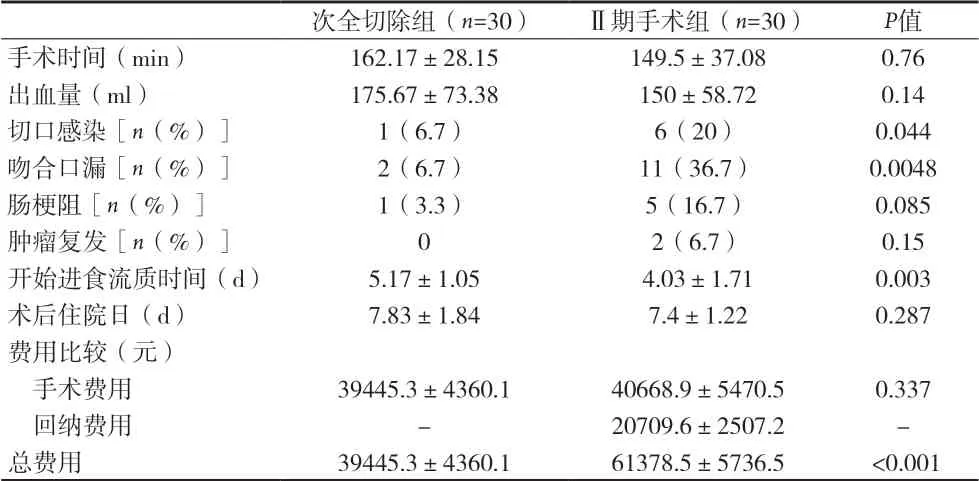
表1 兩組患者術中、術后情況比較(x±s)
2.2 兩組患者術后腸功能及營養狀況比較 見表2。

表2 兩組患者術后腸功能及營養狀況比較(x±s)
2.3 兩組患者生存分析 兩組患者的5年生存率無顯著差異(次全切除組65.2% vs.Ⅱ期手術組59.2%,P>0.05),見圖1。
3 討論
結直腸癌并急性腸梗阻是常見的外科急腹癥之一,其中以左側結腸癌梗阻最為常見,約占全部梗阻性大腸癌病例的2/3[5]。由于左半結腸癌并腸梗阻多數為閉袢性腸梗阻,腸內糞便淤積厭氧菌增多,血運不如右半結腸,結腸壁薄容易發生缺血壞死穿孔,引起糞性腹膜炎,中毒性休克等并發癥而死亡。
急診施行切除后行Ⅰ期吻合較危險,因此,傳統手術主張行兩種分期手術方式,但是均不理想:第一種是分期手術(Ⅰ期近端腸造口,Ⅱ期腫瘤切除術,Ⅲ期造口閉合術),雖然手術安全,但是不能降低術后并發癥發生率,腫瘤切除延遲也會降低患者生存期,延長住院時間,目前已經較少使用。第二種是標準左半結腸切除加回腸造口,可以一次性切除腫瘤,避免發生吻合口漏,以往被普遍接受。對于年齡較大、梗阻明顯、全身情況較差的患者,造口會使患者術后生活質量明顯下降,且需要進行Ⅱ期造口回納術。分期手術有反復手術的痛苦,腸造瘺對患者心理、生活均造成不良影響。
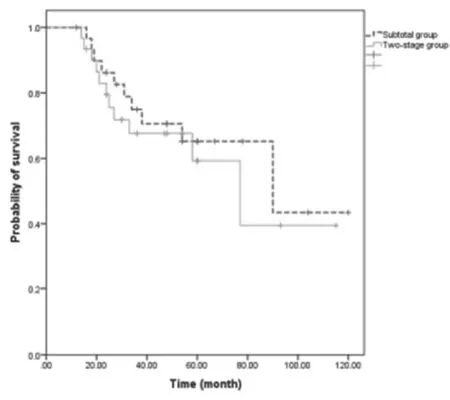
圖1 兩組患者生存分析
結腸次全切除對于治療左半結腸癌伴急性腸梗阻具有一定優勢。結腸次全切除相對于左半結腸切除術,可以切除可能同時存在的原發癌和腺瘤,能清掃更廣范圍的淋巴結,更符合腫瘤學清掃的范圍。相對于標準左半結腸切除術和術中灌洗術式,結腸次全切除術可降低感染性休克發生率,能縮短住院時間,減少住院費用。Kaser等[6]報道結腸次全切除術后吻合口瘺發生率低于腸部分切除。Torralba等[7]報道在術后并發癥發生率和手術時間方面,結腸次全切除術優于結腸灌洗。本組病例采用術前留置腸梗阻導管,術中利用腸梗阻導管進行小腸減壓,留置的腸梗阻導管還能起到腸排列作用,防止術后粘連型腸梗阻的發生。本組病例術后無1例發生粘連型腸梗阻。采用次全結腸切除手術,梗阻近端的結腸大量糞便留在切除的結腸內,不需要術中切開結腸進行減壓灌洗,而且預切除腸管采用直線切割閉合器切除,完全杜絕了術中腹腔污染,顯著縮短了手術時間,明顯減少了手術風險。本組病例術中和術后均未出現感染性休克和腹腔感染。由于切除了完全性腸梗阻導致的血供不好的近端結腸,而回腸末端經減壓后血供良好,術中無需判斷梗阻近端的腸管血供問題。將血供良好的末端回腸和正常粗細的殘結腸行端側吻合術,吻合口漏的風險和正常擇期手術的Ⅰ期回腸結直腸吻合是一樣的。而在正常情況下,回結腸吻合與結結直腸吻合相比,吻合口漏的發生率明顯降低。與Ⅱ期手術組比較,次全切除組均Ⅰ期吻合,無吻合口漏發生,提示對急性腸梗阻病例,行次全結腸切除安全可靠。
左半結腸癌并急性完全性腸梗阻的患者,行Ⅰ期次全結腸切除吻合術,要做到以下幾點:(1)嚴格掌握適應證及禁忌證。患者全身情況尚可,能耐受手術。梗阻結腸腸管水腫嚴重,張力較高。或者腸壁明顯肥厚,血供較差,行結結腸吻合風險較大的可行此手術。對于腸穿孔等腹腔污染嚴重的放棄Ⅰ期切除吻合,行腫瘤切除后腸造口或單純腸造口以確保患者安全。而對于梗阻腸管擴張不嚴重,張力不大,血供良好的,應切除腫瘤將近端結腸放置腹腔外,套入腹腔鏡袋子減壓后,行結結直腸Ⅰ期吻合。(2)手術操作輕柔熟練,避免過度牽拉損傷腸管和周圍組織。腫瘤切除及淋巴結清掃快速完成。未減壓狀態下游離結腸脾曲是手術難點,脾結腸韌帶較薄,應注意分辨。可采用內外側上方三路匯合游離脾曲。(3)保證吻合口無張力,良好的血運是吻合口順利愈合關鍵因素。(4)術后放置肛管或擴肛,可有效降低腸腔內壓力,保證吻合口的順利愈合。(5)合理的引流管放置。術后吻合口漏多發生在第5~7天,引流管的放置對于吻合口漏的早期發現和治療至關重要。引流管以雙套管引流為宜,要保證低位,勿壓迫吻合口,放置時間以超過發生吻合口漏的危險期為宜。(6)術后患者的精心管理:包括合理抗感染、胃腸減壓、維持水電解質酸堿平衡及營養支持等。
綜上所述,左半結腸癌伴急性完全性腸梗阻的外科治療的目的是切除腫瘤和解除梗阻,改善患者生活質量,Ⅰ期吻合是理想的手術方式。如嚴格掌握適應證及禁忌證,進行合適的術前準備及次全結腸切除術,行Ⅰ期切除吻合手術是安全可行的。

