一線抗結(jié)核藥物血藥濃度與早期痰菌陰轉(zhuǎn)的相關(guān)性研究
劉其會(huì) 孫峰 孫濤 賈小芳 蘇菲菲 施伎蟬 張麗軍 蔣賢高 張文宏
我國(guó)是結(jié)核病高發(fā)國(guó)家,結(jié)核病患者例數(shù)約占全球8.3%。隨著肝腎功能異常、并發(fā)糖尿病、并發(fā)艾滋病的結(jié)核病患者數(shù)量的增多,抗結(jié)核藥物治療方案的制定亟需個(gè)體化[1]。近年來(lái),國(guó)外研究人員在抗結(jié)核藥物的藥代動(dòng)力學(xué)研究方面進(jìn)行了較多的工作,包括體外實(shí)驗(yàn)、動(dòng)物實(shí)驗(yàn)及臨床研究,并且在結(jié)核病治療過(guò)程中進(jìn)行治療藥物濃度監(jiān)測(cè),為臨床個(gè)體化用藥提供依據(jù)[2-5]。然而,在國(guó)內(nèi)鮮有在結(jié)核病患者群體中進(jìn)行抗結(jié)核藥物藥代動(dòng)力學(xué)研究及其與療效相關(guān)性的研究。因此,筆者定點(diǎn)收集服用利福平(R)、異煙肼(H)、乙胺丁醇(E)這3種藥物進(jìn)行抗結(jié)核藥物治療患者的血漿,測(cè)定這些一線抗結(jié)核藥物血藥濃度,了解其在我國(guó)結(jié)核病患者中的藥代動(dòng)力學(xué)特點(diǎn),并探討其藥代動(dòng)力學(xué)參數(shù)與患者早期痰菌陰轉(zhuǎn)率的相關(guān)性。
材料和方法
1.研究對(duì)象:采用前瞻性研究方法,招募溫州市中心醫(yī)院感染科2015年10月1日至2016年1月31日住院部的肺結(jié)核患者作為研究對(duì)象,共72例。納入標(biāo)準(zhǔn):(1)初治或復(fù)治次數(shù)不超過(guò)1次的肺結(jié)核患者;(2)抗結(jié)核藥物治療方案為口服R、H、E、吡嗪酰胺(Z)超過(guò)7 d,不包括其他二線抗結(jié)核藥物;(3)診斷為菌陽(yáng)肺結(jié)核患者或菌陰肺結(jié)核患者[5];(4)菌陽(yáng)肺結(jié)核患者采用BACTEC MGIT 960系統(tǒng)藥物敏感性試驗(yàn)(簡(jiǎn)稱“藥敏試驗(yàn)”)對(duì)R、H、E均敏感。
2.病史資料收集:收集研究對(duì)象基本信息,包括性別、年齡、體質(zhì)量、并發(fā)疾病、合并用藥、影像學(xué)檢查結(jié)果、初治或復(fù)治狀態(tài)、用藥方案等,完成病例記錄表。
3.病原學(xué)檢查:所有研究對(duì)象均行痰抗酸染色涂片、痰標(biāo)本液體培養(yǎng)及藥敏試驗(yàn),有條件者可行GeneXpert MTB/RIF檢測(cè)。
4.治療方案的制定及記錄:參照文獻(xiàn)[1,5]的要求根據(jù)患者體質(zhì)量確定具體用藥劑量。R、H、E均為每天早餐前頓服,Z為3次/d、每次2片口服。記錄入組的每例研究對(duì)象藥物劑量及給藥時(shí)間。
5.收集血漿標(biāo)本:研究對(duì)象住院期間抗結(jié)核藥物治療超過(guò)1周后,服藥前0.5 h、服藥后2 h、4 h、6 h、8 h采用紫帽管采血1 ml,采血后30 min之內(nèi)離心,取上清,干冰轉(zhuǎn)移至-80 ℃冰箱保存。
6.血藥濃度監(jiān)測(cè):將所采集的樣本送至上海市公共衛(wèi)生臨床中心Ⅰ期臨床試驗(yàn)中心處理,采用液相色譜-串聯(lián)質(zhì)譜聯(lián)用(LC-MS-MS)方法測(cè)定所收集樣本的血漿藥物濃度。
7.隨訪:每例研究對(duì)象每月至少來(lái)院隨訪1次痰涂片檢查;痰培養(yǎng)可于治療2個(gè)月末復(fù)查。
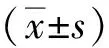
結(jié) 果
1.基本情況:本研究共招募72例口服H-R-Z-E四聯(lián)抗結(jié)核藥物治療方案的肺結(jié)核患者,其中1例患者痰培養(yǎng)結(jié)果為耐多藥肺結(jié)核,1例失訪,最終納入70例進(jìn)行分析。70例研究對(duì)象中,男51例(72.9%),女19例(27.1%);平均年齡(37.01±17.07)歲,體質(zhì)量指數(shù)(BMI)平均值為20.61±3.74。初治肺結(jié)核患者65例(92.9%),復(fù)治肺結(jié)核患者5例(7.1%)。10例并發(fā)糖尿病,1例并發(fā)矽肺,11例乙型肝炎病毒表面抗原陽(yáng)性。既往有吸煙史者20例,有飲酒史者7例。18例患者胸部CT掃描提示有空洞病灶,5例并發(fā)結(jié)核性胸膜炎、胸腔積液。菌陽(yáng)肺結(jié)核患者54例,其中47例痰或肺泡灌洗液抗酸染色涂片陽(yáng)性;菌陰肺結(jié)核患者16例。所有患者HIV抗體均陰性。
2.藥代動(dòng)力學(xué)參數(shù)范圍:所有研究對(duì)象均采用H-R-Z-E四聯(lián)口服抗結(jié)核藥物治療方案。R、H、E為每天早餐前頓服。R給藥劑量為(9.79±1.42) mg/kg,H為(5.29±0.96) mg/kg,E為(13.24±2.40) mg/kg。研究對(duì)象服藥1周達(dá)到穩(wěn)態(tài)藥物濃度后進(jìn)行采血,每例均采集5個(gè)時(shí)間點(diǎn),即服藥前0.5 h,服藥后2 h、4 h、6 h、8 h,然后采用LC-MS-MS檢測(cè)每份樣品的藥物濃度。70例研究對(duì)象共采集342份血漿標(biāo)本,藥代動(dòng)力學(xué)參數(shù)分布情況見(jiàn)表1。國(guó)際上推薦的峰值濃度參考范圍:R為8~24 μg/ml、H為3~6 μg/ml、E為2~6 μg/ml[6]。本次研究中,25.7%(18/70)的研究對(duì)象R峰值濃度低于推薦范圍(<8 μg/ml),38.6%(27/70)H峰值濃度低于推薦范圍(<3 μg/ml),65.7%(46/70)E的峰值濃度低于推薦范圍(<2 μg/ml)。
3.早期痰菌陰轉(zhuǎn)率與血藥濃度的相關(guān)性:研究對(duì)象中54例為菌陽(yáng)肺結(jié)核患者,抗結(jié)核藥物治療2個(gè)月末,進(jìn)行痰涂片、痰培養(yǎng)檢查,48例患者痰菌陰轉(zhuǎn),6例未陰轉(zhuǎn),治療2個(gè)月末痰菌陰轉(zhuǎn)率為88.9%。按照痰菌陰轉(zhuǎn)和未陰轉(zhuǎn)分為兩組,兩組患者R、H、E給藥劑量接近,差異無(wú)統(tǒng)計(jì)學(xué)意義。對(duì)兩組患者R、H、E的C2 h、Cmax、AUC0~8值進(jìn)行比較,治療2個(gè)月末痰菌陰轉(zhuǎn)組患者E的C2 h、Cmax、AUC0~8值均明顯高于未陰轉(zhuǎn)組;H的C2 h、Cmax值均明顯高于未陰轉(zhuǎn)組,見(jiàn)表2。
討 論
筆者收集并檢測(cè)了70例肺結(jié)核患者采用抗結(jié)核藥物化療方案H-R-Z-E治療后的血漿藥物濃度,并探討峰值濃度與治療2個(gè)月末痰菌陰轉(zhuǎn)率的相關(guān)性。目前,此類研究數(shù)量有限,國(guó)內(nèi)鮮有報(bào)道。本次研究中,25.7%的患者R峰值濃度低于推薦范圍,38.6%的患者H峰值濃度低于推薦范圍,65.7%的患者E峰值濃度低于推薦范圍。因此推測(cè),我國(guó)部分肺結(jié)核患者血藥濃度不能滿足國(guó)際上推薦的參考范圍,尤其是E的給藥劑量為每例患者750 mg/d,平均給藥劑量為(13.24±2.40) mg/kg,低于推薦的15~25 mg·kg-1·d-1[7],可能存在劑量上的不足。
70例患者中,54例為菌陽(yáng)肺結(jié)核患者,一線抗結(jié)核藥物治療2個(gè)月末,48例痰菌陰轉(zhuǎn),6例未陰轉(zhuǎn),治療2個(gè)月末痰菌陰轉(zhuǎn)率為88.9%。筆者發(fā)現(xiàn),治療2個(gè)月末痰菌能否陰轉(zhuǎn)可能與H、E的血藥濃度相關(guān),這個(gè)結(jié)果與H和E峰值濃度分布情況一致;38.6%的患者H峰值濃度未達(dá)到推薦范圍,65.7%的患者E峰值濃度未達(dá)到推薦范圍,H和E的峰值濃度符合有效濃度的患者比例偏低,故治療2個(gè)月末痰菌未能陰轉(zhuǎn)可能與H、E的血藥濃度偏低有關(guān)。因此,國(guó)內(nèi)H和E的給藥劑量可能還需調(diào)整。本研究中,治療2個(gè)月末痰菌陰轉(zhuǎn)者R的峰值濃度與未陰轉(zhuǎn)者比較未見(jiàn)差異,原因可能如下:一方面,此結(jié)果與上述R峰值濃度分布情況一致,大于70%的患者R的峰值濃度達(dá)到推薦范圍,符合有效濃度的比例較高;另一方面,樣本例數(shù)有限,2個(gè)月末痰菌未陰轉(zhuǎn)者例數(shù)太少,只有6例,個(gè)體差異較大,需擴(kuò)大樣本量開(kāi)展進(jìn)一步研究。
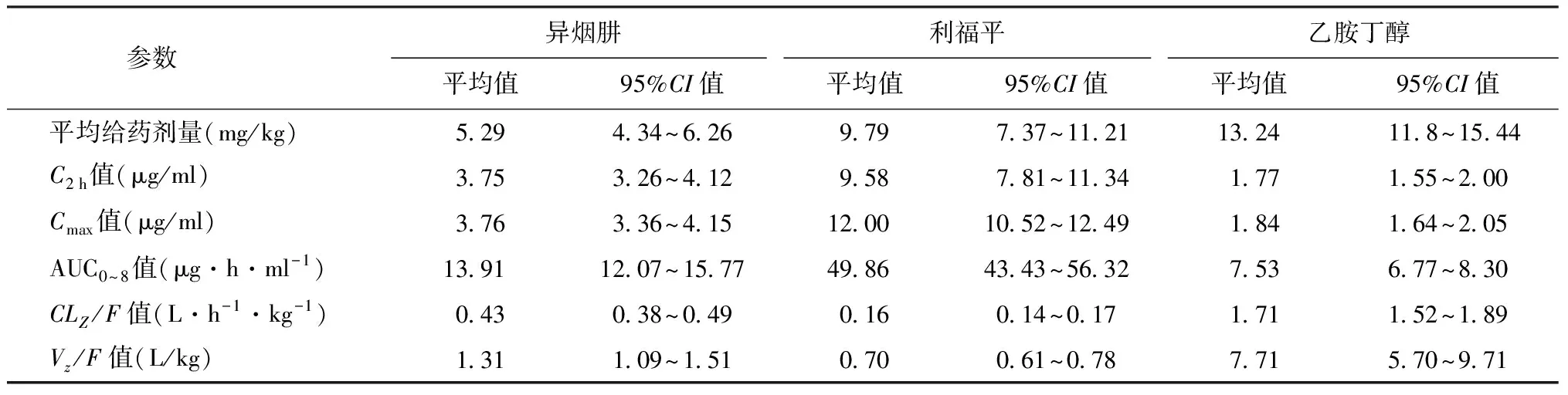
表1 研究對(duì)象異煙肼、利福平、乙胺丁醇的藥代動(dòng)力學(xué)參數(shù)
注C2 h:服藥后2 h濃度;Cmax:峰值濃度;AUC0~8:服藥后8 h曲線下面積;CLZ/F:經(jīng)過(guò)生物利用度校正的清除率;Vz/F:經(jīng)過(guò)生物利用度校正的表觀分布容積
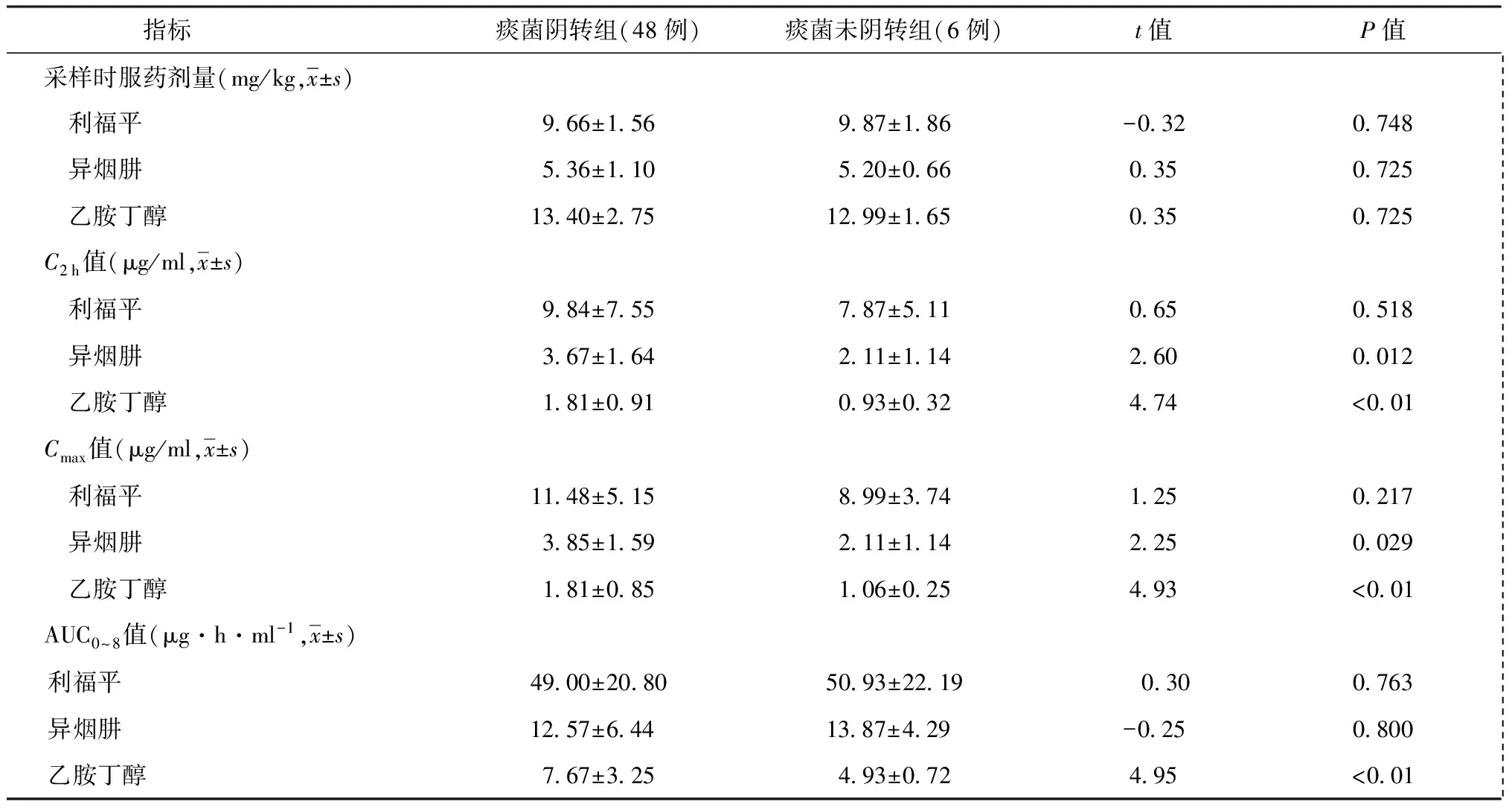
表2 治療2個(gè)月末各類一線抗結(jié)核藥物藥代動(dòng)力學(xué)參數(shù)在痰菌陰轉(zhuǎn)組與未陰轉(zhuǎn)組中的比較
注C2 h:服藥后2 h濃度;Cmax:峰值濃度;AUC0~8:服藥后8 h曲線下面積
本研究存在著一些不足之處:(1)樣本量較小,樣本量的不足可能會(huì)造成一些潛在的相關(guān)性未能發(fā)現(xiàn);(2)因?yàn)閆的藥物性肝損傷及胃腸道反應(yīng)較大,本次研究對(duì)象的服用方案為3次/d,每次2片,口服。Z的藥代動(dòng)力學(xué)參數(shù)考察需要設(shè)置另一種采血方案,因此,本次研究未考察其峰值濃度及其與早期痰菌陰轉(zhuǎn)率的相關(guān)性。此外,考慮到HIV感染的患者更容易出現(xiàn)藥物吸收不良的情況,且常服用多種藥物,藥物與藥物之間存在相互作用[8-9],HIV與MTB雙重感染的患者可能相比于MTB單純感染者更具有治療藥物濃度檢測(cè)的必要性。但本次研究只檢測(cè)了HIV陰性的肺結(jié)核患者,研究對(duì)象疾病類型較單一,檢測(cè)的血藥濃度分布范圍結(jié)果可能不能向同時(shí)并發(fā)HIV感染的患者人群推廣。
綜上所述,肺結(jié)核患者采用標(biāo)準(zhǔn)四聯(lián)抗結(jié)核藥物化療方案治療后,部分患者血漿藥物峰值濃度低于推薦參考水平,尤其是H和E,藥物劑量可能需要調(diào)整。此外,本次研究發(fā)現(xiàn)治療2個(gè)月末痰菌陰轉(zhuǎn)率與H、E的血漿藥物峰值濃度具有相關(guān)性,治療2個(gè)月末痰菌陰轉(zhuǎn)者H、E的峰值濃度明顯高于未陰轉(zhuǎn)者。治療藥物濃度監(jiān)測(cè)廣泛應(yīng)用于腫瘤患者、器官移植患者及部分抗生素應(yīng)用領(lǐng)域,但在肺結(jié)核治療領(lǐng)域應(yīng)用較少。因此,對(duì)活動(dòng)性肺結(jié)核患者進(jìn)行治療藥物濃度監(jiān)測(cè),具有臨床意義和價(jià)值,值得臨床醫(yī)生和研究者關(guān)注和重視。
[1] World Health Organization. Global tuberculosis report 2016. Geneva: World Health Organization, 2016.
[2] Nielsen EI, Friberg LE. Pharmacokinetic-pharmacodynamic modeling of antibacterial drugs. Pharmacol Rev, 2013, 65(3): 1053-1090.
[3] Reynolds J, Heysell SK. Understanding pharmacokinetics to improve tuberculosis treatment outcome. Expert Opin Drug Metab Toxicol, 2014, 10(6): 813-823.
[4] van Heeswijk RP, Dannemann B, Hoetelmans RM. Bedaquiline: a review of human pharmacokinetics and drug-drug intera-ctions. J Antimicrob Chemother, 2014, 69(9): 2310-2318.
[5] 中華醫(yī)學(xué)會(huì)結(jié)核病學(xué)分會(huì). 肺結(jié)核診斷和治療指南. 中國(guó)實(shí)用鄉(xiāng)村醫(yī)生雜志, 2013, 20(2): 7-11.
[6] Alsultan A, Peloquin CA. Therapeutic drug monitoring in the treatment of tuberculosis: an update. Drugs, 2014, 74(8): 839-854.
[7] 中國(guó)防癆協(xié)會(huì). 耐藥結(jié)核病化學(xué)治療指南(2015). 中國(guó)防癆雜志, 2015, 37(5): 421-469.
[8] Tostmann A, Mtabho CM, Semvua HH, et al. Pharmacokinetics of first-line tuberculosis drugs in Tanzanian patients. Antimicrob Agents Chemother, 2013, 57(7): 3208-3213.
[9] Holland DP, Hamilton CD, Weintrob AC, et al. Therapeutic drug monitoring of antimycobacterial drugs in patients with both tuberculosis and advanced human immunodeficiency virus infection. Pharmacotherapy, 2009, 29(5): 503-510.
- 中國(guó)防癆雜志的其它文章
- 武漢市涂陽(yáng)肺結(jié)核患者藥物治療依從性的影響因素分析
- 結(jié)核科護(hù)理人員對(duì)肺結(jié)核并發(fā)2型糖尿病知識(shí)的問(wèn)卷調(diào)查結(jié)果分析
- 上海市閘北區(qū)肺結(jié)核患者治療費(fèi)用分析及減免政策滿意度調(diào)查
- 2011—2016年合肥市非結(jié)核病防治機(jī)構(gòu)網(wǎng)絡(luò)報(bào)告肺結(jié)核患者追蹤未到位的影響因素分析
- 《中國(guó)防癆雜志》與《結(jié)核病與肺部健康雜志》征訂啟事
- 內(nèi)蒙古自治區(qū)二級(jí)以上醫(yī)療機(jī)構(gòu)實(shí)驗(yàn)室開(kāi)展結(jié)核病相關(guān)檢測(cè)項(xiàng)目的調(diào)查分析

