分子模擬評價離子液體作為萃取精餾中萃取劑
張學崗,劉伯潭,胡威
(1.科林泰克科技有限公司,天津 300384; 2.天津市海洋資源與化學重點實驗室,天津 300457; 3.天津大學 化工學院,天津 300072)
分子模擬評價離子液體作為萃取精餾中萃取劑
張學崗1,劉伯潭2*,胡威3
(1.科林泰克科技有限公司,天津 300384; 2.天津市海洋資源與化學重點實驗室,天津 300457; 3.天津大學 化工學院,天津 300072)
探索性地使用分子模擬軟件Material Studio計算二元物系中溶劑分子(離子液體)與溶質分子間的混合能,并以兩者的混合能差值評價萃取劑的優劣。計算了離子液體與溶質的二元物系的混合能差,并用文獻中的無限稀釋活度系數,得到選擇性Ss以驗證模擬計算結果。結果表明選擇性與混合能差值之間有一定規律可循,為進一步深入研究打下基礎。
分子模擬;萃取精餾;萃取劑;溶劑;離子液體
萃取精餾是化工分離的有效手段[1]。在萃取精餾的開發過程中,萃取劑的選擇關系到分離效果和成本,是至關重要的問題[2],當前,對萃取精餾溶劑的選擇基本上還依賴于經驗篩選和實驗方法,其效果往往很難令人滿意[3]。基于計算的萃取劑篩選方法目前有分子設計方法(CAMD)[4,5],可以做到在更廣闊的范圍內進行萃取劑選擇,但是分子設計方法依賴基團貢獻法,其本身的局限決定了結果并不一定精確,甚至只有方向性的意義。隨著計算機技術的不斷提高以及分子模擬理論的完善,研究者越來越傾向于認為每一項新理論的誕生都已經離不開分子模擬工作[6]。目前,在高分子材料學科中,已經出現了以計算混合能判斷兩種物質相容性的文獻報導[7-11]。萃取劑的作用原理是通過不同物質的分子間作用而體現出性質的差異,而兩種物質的相容性與萃取精餾的效果往往是相關聯的。因此基于分子模擬的選擇萃取精餾溶劑的方法在理論上應該也是成立的,但是目前在文獻中并沒有看到使用分子模擬的方法進行萃取劑篩選方面的研究報道。
離子液體作為萃取劑目前是萃取精餾發展的新熱點。文獻中利用離子液體作為萃取劑的報到屢見不鮮[12]。離子液體是一種由陰陽離子組成的熔點低于常溫的鹽類物質,飽和蒸汽壓低,溶解性強,近年以來離子液體已成功用于廢水中苯衍生物、金屬離子的萃取和機動車燃油中有機硫脫除等方面。離子液體幾乎沒有揮發性的特點使其與傳統的萃取劑相比具有先天的優勢,因此,作為一種新型的萃取劑,離子液體在萃取精餾中的應用前景廣闊。
本文使用分子模擬軟件Material Studio評價萃取劑篩選,使用二元物系中溶劑分子與溶質分子間的混合能差值作為評價指標評價萃取劑性能,用溶質的無限稀釋活度系數作為驗證,離子液體與溶質的無限稀釋活度系數使用文獻中的實驗數據。以比較經典的醇-水體系、醇-苯體系、苯-環己烷體系的萃取精餾溶劑篩選問題為例,探索了混合能差值與溶劑選擇性的變化關系。
1 Material Studio Blends模塊計算方法
在Material Studio軟件中的Blends模塊可以評估二元混合物的混溶性,預測混合的熱力學信息。可以篩選聚合物-聚合物、聚合物-溶劑、溶劑-溶劑相互作用。可用于研究:相圖、相互作用參數χ、混合能、混合自由能、能量分布等。
最簡單和最著名的理論混合熱力學和相分離的二元系統是Flory-Huggins模型[13],一般的二元體系的混合自由能的表達形式為:
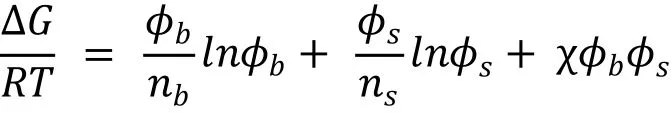
前兩項代表組合熵,最后一項是相互作用自由能。相互作用參數χ定義為:
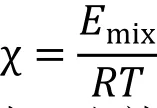
其中Emix是混合能,也就是純態和混合態之間由于混合而產生的自由能之差。在Flory-Huggins模型中,每個分子占據一個晶格單元,對于一個晶格單元有一個配位數 Z。混合能可以表示為:
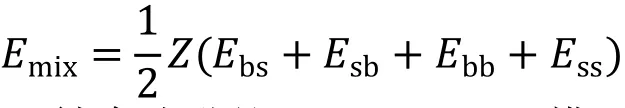
Blends結合改進的Flory-Huggins模型和Monte Carlo抽樣技術[14]計算二元混合物的相容性,Flory-Huggins模型重要的改進在于:Blends集成了一個顯式的溫度依賴相互作用參數,這是通過產生大量陣列的交互作用來計算結合能,其次是溫度平均使用玻耳茲曼因子和計算結果隨溫度而變的相互作用參數[15]。Blends是一個off-lattice計算,這意味著分子不像原安排在常規的晶格Flory-Huggins理論。配位數是顯式計算為每個可能的分子對使用分子模擬[16]。
2 選擇性的計算
在選擇萃取精餾溶劑時首先需考慮的是溶劑的選擇性SS[17],即加入溶劑S使原系統關鍵組分(A和B)之間的相對揮發度按照分離要求的方向改變的程度,一般可以利用關鍵組分在溶劑中的無限稀釋活度因子之比表示:
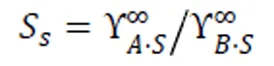
使用FORTRAN語言編寫程序用NRTL方程計算無限稀釋活度因子,首先對各種物質由氣液相平衡手冊中找到各個物質之間的相互作用參數建立數據庫,對于不存在相互作用參數的物質對編寫程序使用UNIFAC方法擬合未知的NRTL參數。
3 計算過程與結果
3.1 醇-水體系的計算
二取代咪唑類離子液體從稀水溶液中萃取醇類呈現出很好的潛力。關于離子液體選擇性的文獻報導較多。如以1-乙基-3-甲基咪唑二氨腈鹽為溶劑,在含水物系中選擇性的測定[18]。Krummen等[19,20]測定了多種溶劑在[mmim][Tf2N]、[emim][Tf2N]、[bmim][Tf2N]、[emim][C2H5OSO3]等離子液體中的無限稀釋活度系數,計算了這些離子液體對環己烷-苯、環己烯-苯、等體系的選擇性系數,推斷離子液體分離此物系的可能性[21]。
本文選擇了計算不同溫度下醇、水在1-乙基-3-甲基二氨腈鹽([EMIM][N(CN)2])離子液體中的混合能,以上節所述的混合能差值評價萃取精餾分離效果,以文獻[18]中報導的選擇性做對比,計算該離子液體在含水物系中的混合能差值。選擇力場Universal,設置計算精度為Ultra-fine,分別計算了水、乙醇、異丙醇、正丁醇在1-乙基-3-甲基二氨腈鹽([EMIM][N(CN)2])離子液體中的混合能,與文獻值對比計算了353.15、343.15、333.15、323.15 K下的混合能,并計算了混合能的差值,不同溫度下的計算結果分別列入表1-4。
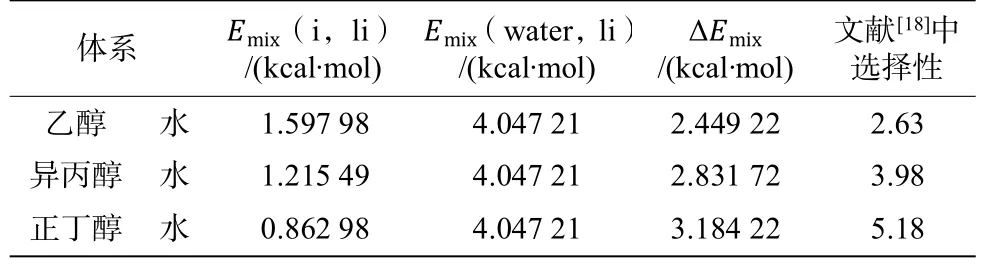
表1 353.15K下醇-水體系的混合能差值和選擇性Table1Differenceofmixingenergyandselectivityof alcohol water system under 353.15 K

表2 343.15 K下醇-水體系的混合能差值和選擇性Table 2 Difference of mixing energy and selectivity of alcohol watersystemunder343.15K
以各個溫度下混合能差值與選擇性做圖,由圖1可以看出,1-乙基-3-甲基二氨腈鹽([EMIM][N(CN)2])離子液體萃取精餾分離醇-水體系的選擇性以正丁醇-水體系為最高,異丙醇-水體系次之,乙醇-水體系選擇性最差,選擇性隨溫度的增加成下降趨勢。各個溫度下選擇性與混合能差值呈現良好的線性關系,即選擇性隨著混合能差值的增大而增大。
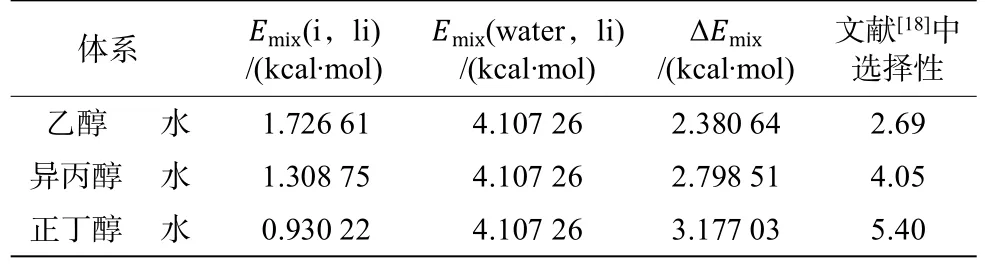
表3 333.15 K下醇-水體系的混合能差值和選擇性Table3Differenceofmixingenergyandselectivityof alcohol water system under 333.15 K
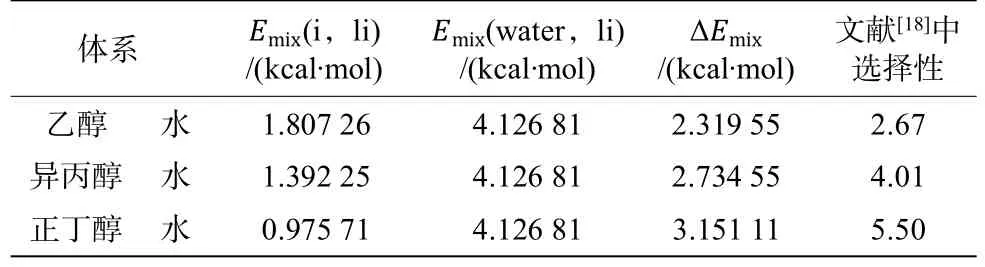
表4 323.15K下醇-水體系的混合能差值和選擇性Table4Differenceofmixingenergyandselectivityof alcohol watersystemunder323.15K
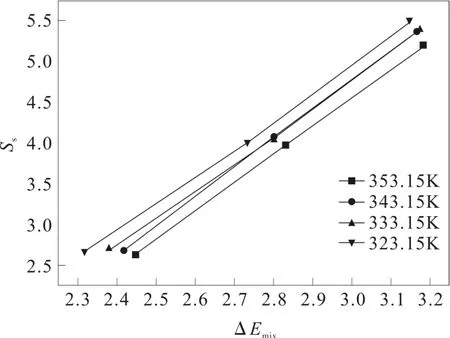
圖1 不同溫度下醇-水體系混合能差值與選擇性的關系圖Fig.1Therelationshipbetweenthedifferenceofthemixed energyandtheselectivityofthesystematdifferent temperatures
3.2 醇-苯體系的計算
苯、甲醇、乙醇和異丙醇都是常用的溶劑,其中乙醇-苯混合物是一種最低共沸液體混合物,在101.3 kPa時其共沸點溫度為68℃,共沸摩爾組成中含有44.8%的乙醇[22]。本文選擇了計算不同溫度下的醇和苯在1-乙基-3-甲基二氨腈鹽([EMIM][N(CN)2])離子液體中的混合能,并計算混合能的差值,以混合能差值評價萃取精餾分離效果。以文獻[18]中報導的選擇性做對比,計算了三種醇和苯在該離子液體在的混合能,并計算差值。選擇力場Universal,設置計算精度為Ultra-fine,分別計算了不同溫度下苯、甲醇、乙醇、異丙醇在1-乙基-3-甲基二氨腈鹽([EMIM][N(CN)2])離子液體中的混合能,與文獻值對比計算了353.15、343.15、333.15、323.15 K下的混合能,并計算了混合能的差值,不同溫度下的計算結果分別列入表5-8。
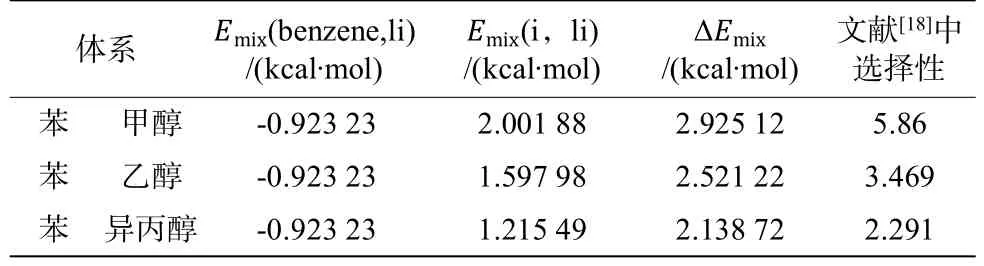
表5 353.15 K下苯-醇體系的混合能差值和選擇性Table 5 Difference of mixing energy and selectivity of benzene-alcohol system under 353.15 K
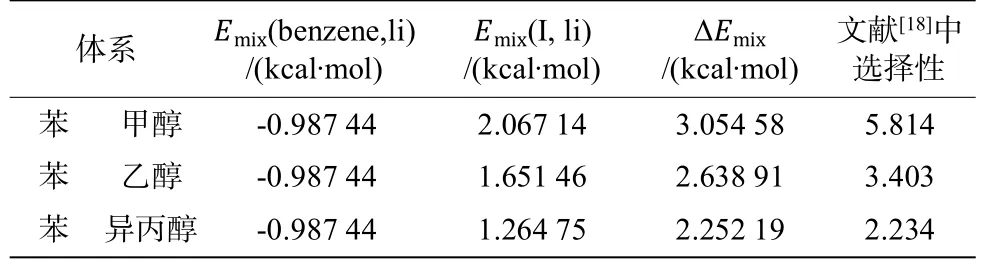
表6 343.15K下苯-醇體系的混合能差值和選擇性Table 6 Difference of mixing energy and selectivity of benzene-alcohol system under 343.15 K
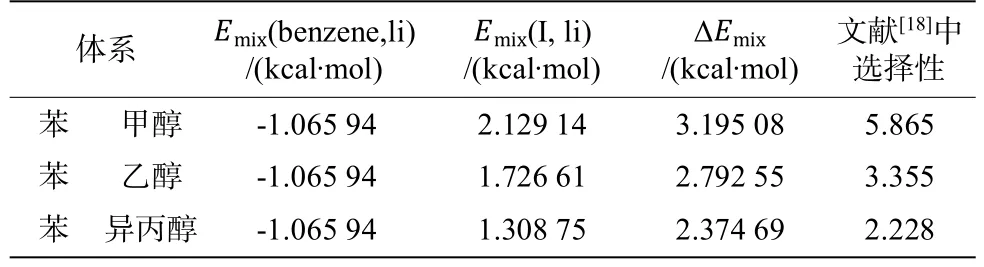
表7 333.15K下苯-醇體系的混合能差值和選擇性Table 7 Difference of mixing energy and selectivity of benzene-alcoholsystemunder333.15K
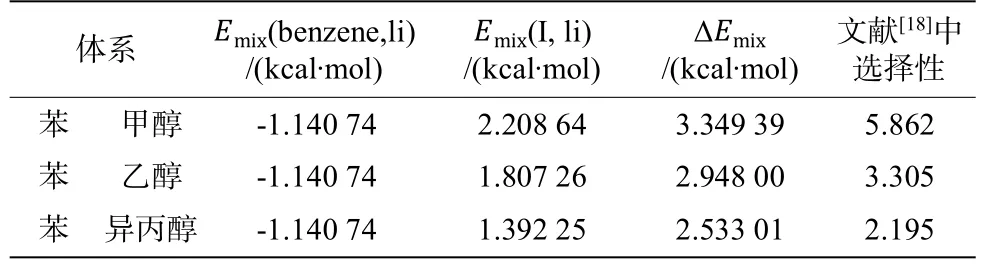
表8 323.15K下苯-醇體系的混合能差值和選擇性Table 8 Difference of mixing energy and selectivity of benzene-alcoholsystemunder323.15K
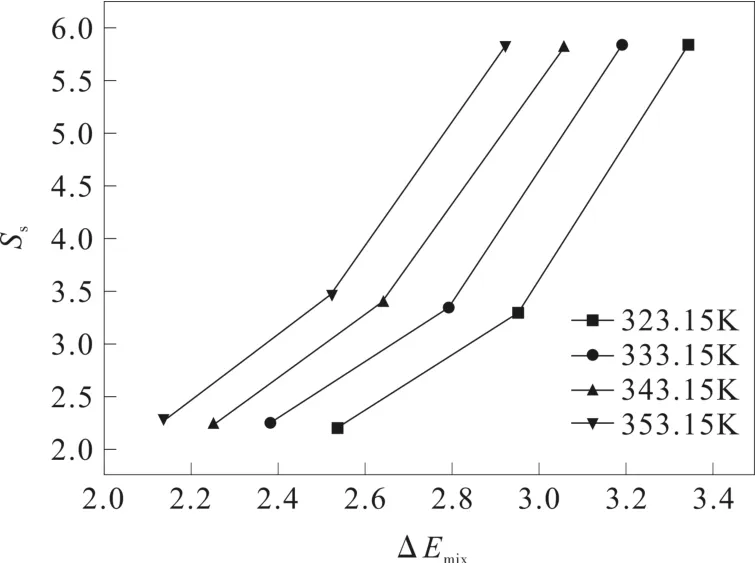
圖2 不同溫度下苯-醇體系混合能差值與選擇性的關系圖Fig.2 The relationship between the difference of mixing energyandtheselectivityofthesystematdifferent temperatures
以各個溫度下混合能差值與文獻中的選擇性作圖,由圖2可以看出,1-乙基-3-甲基二氨腈鹽([EMIM][N(CN)2])離子液體萃取精餾分離苯-醇體系的選擇性以甲醇-苯體系為最高,乙醇-苯體系次之,異丙醇-苯體系選擇性最差。各個溫度下選擇性均隨著混合能差值的增大而增大。
3.3 苯-環己烷體系離子液體的計算
苯和環己烷都是重要的化工原料,常壓下苯和環己烷沸點相差僅0.6℃,因此苯和環己烷混合物系的分離是化工分離領域一個典型范例,常用萃取精餾的方法分離。文獻[19]報導了 [mmim][(CF3SO2)2N],[emim][(CF3SO2)2N], [bmim][(CF3SO2)2N],三種離子液體分離苯-環己烷物系的選擇性。本文選擇了計算不同溫度下的苯、環己烷分子在不同離子液體中的混合能,并計算兩個混合能的差值,與文獻報導的選擇性對比。計算過程的力場選擇Universal力場,精度設置為 Ultra-fine,分別計算了313.15、323.15 K溫度下的混合能和混合能的差值,結果列入表9-10。
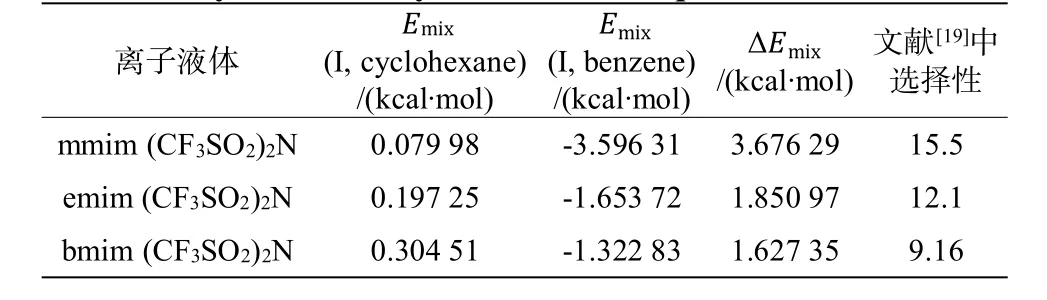
表9 313.15K下離子液體分離苯-環己烷體系的混合能差值與選擇性Table9Differenceofmixingenergyandselectivityof benzene-cyclohexane system in ionic liquid under 313.15 K
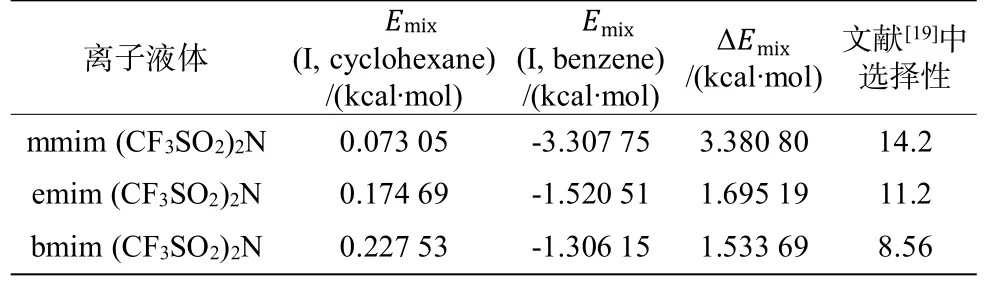
表10 323.15 K下離子液體分離苯-環己烷體系的混合能差值與選擇性Table 10 Difference of mixing energy and selectivity of benzene-cyclohexanesysteminionicliquidunder323.15K
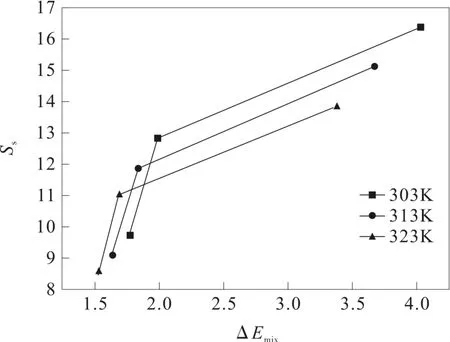
圖3 不同溫度下苯-環己烷體系混合能差值與選擇性的關系圖Fig.3Therelationshipbetweenthedifferenceofmixing energyandtheselectivityofbenzene-cyclohexanesystemat different temperatures
以各個溫度下混合能差值與文獻中的選擇性作圖,由圖3可以看出,[mmim][(CF3SO2)2N]離子液體分離苯-環己烷體系的選擇性最高,[emim][(CF3SO2)2N]次之,[bmim][(CF3SO2)2N]選擇性最差。各個溫度下選擇性隨著混合能差值的增大而增大的趨勢是成立的。
4 結論
本文介紹了分子模擬軟件Material Studio的blends模塊計算分子間混合能的方法。計算了離子液體1-乙基-3-甲基咪唑二氨腈鹽為溶劑萃取分離乙醇-水體系、異丙醇-水體系、正丁醇-水體系、甲醇-苯體系、乙醇-苯體系、異丙醇-苯體系時離子液體與待分離的兩種分子間的混合能,并計算混合能的差值,以文獻報導的選擇性做對比,對比結果表明隨著混合能差值的增大選擇性也是增大的,這說明使用混合能差值為評價指標衡量萃取劑分離效果的合理性。
本文的計算表明,總的來說隨著混合能差值的增大,選擇性基本是增加的趨勢,這對于離子液體作為萃取劑的初步篩選有一定的指導意義,為萃取精餾的萃取劑篩選尋找到另一條可行道路。如果能與其他方法相結合,有可能發展出一套便捷、可靠的溶劑篩選方法。
當然,選擇萃取溶劑指標很多,選擇性僅僅是其中之一。本文模型考慮的因素還比較少,盡管如此,本文的計算結果仍然是令人鼓舞的。
符號說明:
Emix—混合能
Δ Emix—混合能差
Eij—i與j單元之間的結合能
ΔG—混合自由能
n1—組分i的聚合度
R—氣體常數
T—熱力學溫度,K
Ss—溶劑s的選擇性
Z—配位數
γ∞A·S—溶質A在溶劑S中的無限稀釋活度系數
γ∞B·S—溶質B在溶劑S中的無限稀釋活度系數
Φ1—組分的體積分數
χ—交互參數
[1] Liu Guobiao,Liu Botan,Yuan Xigang,et al.Computational mass transfer simulation of extractive distillation and its experimental confirmation[J].CIESC Journal,2010,61(7):1809-1814.
[2] Li Rui,Cui Xianbao,Wu Tian,et al.Selection of ionic liquid solvent for liquid-liquid extraction based on COSMO-SAC model[J].CIESC Journal,2013,64(2):452-469.
[3] Song Haihua,Zhang Xuegang,Song Gaopeng.Selection of solvents for extractive distillation(Ⅰ)Artificial neural network model for QSPR of solvents[J].CIESC Journal,2007(08):2010-2015.
[4] Zhang Xuegang.Computer Aided Molecular Design of Solvents for Separation Processes[D].Tianjin:Tianjin University,2008.
[5] Song Jing.Computer—Aided Molecular design of Environmental friendly solvents for Separation Process[D].Tianjin:Tianjin University,2008.
[6] Frenkel D,Smit B.Understanding molecular simulation:from algorithms to applications[M].San Diego:Academic Press,2002.
[7] Mei Linyu,Han Rui,Fu Yizheng,et al.Solvent selection for polyacrylonitrile using molecular dynamic simulation and the effect of process parameters of magnetic-field-assisted electrospinning on fiberalignment[J].High Performance Polymers,2015,27(4):439-448.
[8] Ahmadi A,Freire J J.Molecular dynamics simulation study of compatibility for the polyvinylmethylether/polystyrene mixture[J].Molecular Simulation,2008,34(10-15):1253-1258.
[9] Abou-Rachid H,Lussier L S,Ringuette S,et al.On the correlation between miscibility and solubility properties of energetic plasticizers/polymer blends:Modeling and simulation studies[J].Propellants Explosives Pyrotechnics,2008,33(4):301-310.
[10]Zhuang Q X,Xue Z J,Liu X Y,et al.Molecular Simulation of Miscibility of Poly(2,6-dimethyl-1,4-phenylene ether)/Poly(styreneco-acrylonitrile)Blend With the Compatibilizer Triblock Terpolymer SBM[J].Polymer Composites,2011,32(10):1671-1680.
[11]Ramirez-Gutierrez D,Nieto-Draghi C,Pannacci N,et al.Surface Photografting of Acrylic Acid on Poly(dimethylsiloxane).Experimental and Dissipative Particle Dynamics Studies[J].Langmuir,2015,31(4):1400-1409.
[12]張親親,潘奮進,張愛笛,等.萃取精餾分離甲醇-丁酮萃取劑的選擇.[J].化學工業與工程,2015(05):92-97
[13]Flory P J.Principles of Polymer Chemistry[M].Cornell University Press,1953.
[14]Akkermans R L C,Spenley N A,Robertson S H.Monte Carlo methods in Materials Studio[J].MolecularSimulation.2013,39(14-15):1153-1164.
[15]Blanco M J.Molecular silverware 1.General solutions to excluded volume constrained problems[J].Comput.Chem,1991,12:237–247.
[16]Fan C F,Olafson B D,Blanco M,et al.Application of molecular simulation to derive phase diagrams of binary mixtures[J].Macromolecules,1992,25(14):3667-3676.
[17]Zhang Zhigang,Xu Shimin,Li Xingang,et al.Influence of temperature on solvent selectivity for extractive distillation[J].Journal of Chemical Industry and Engineering(China),2004,55(10):1740-1742.
[18]Ma Lina,Ji Weirong,Ji Jianbing.Measurement of Infinite diluted activity coefficient of solutes in1-Ethyl-3-methylimidazolium dicyanamide[J].Journal of Chemical Engineering of Chinese Universities,2008(04):547-552.
[19]Krummen M.,Wasserscheid P.,Gmehling J.Measurement of activity coefficients at infinite dilution in Ionic liquids using the dilutor technique[J].Journal of Chemicalamp;Engineering Data,2002,47(6):1411-1417.
[20]Kato R.,Gmehling J.Activity Coefficients at Infinite Dilution of Various Solutes in the Ionic Liquids [Mmim]+[CH3SO4]?,[Mmim]+[CH3OC2H4SO4]?,[Mmim]+[(CH3)2PO4]?,[C5H5nC2H5]+[(Cf3SO2)2n]? and[C5H5nH]+[C2H5OC2H4OSO3]?[J].Fluid Phase Equilibria,2004,226:37-44.
[21]焦真;陳志明萃取精餾中離子液體萃取劑的研究進展 [J].化工進展2010(11):2010-2018.
[22]張宗飛,馬正飛,姚虎卿,變壓精餾乙醇苯混合物分離工藝模擬計算[J].南京工業大學學報,2006(04):48-51.
MolecularSimulationEvaluationofIonicLiquidas ExtractionAgentinExtractiveDistillation
ZHANG Xue-gang1,LIU Bo-tan2*,HU Wei3
(1.Tianjin Cleantech Co.,Ltd.,Tianjin 300384,China;2.TianjinKeyLaboratoryofMarineResourcesandChemistry,Tianjin300457,China;3.SchoolofChemicalEngineeringandTechnology,TianjinUniversity,Tianjin300072,China)
The molecular simulation software Material Studio was used to evaluate the mixing energy between solvent(ionic liquid)and solute molecules in binary mixture,and extraction agents were evaluated based on the difference values of mixing energy.The infinite dilution activity coefficients from the literatures were used in order to obtain the selectivity Ss,and the simulation results were verified.The results show that there is certain law between the selectivity and the difference of mixing energy,which can lay the foundation for further research.
Molecular simulation;Extractive distillation;Extraction agent;Solvent;Ionic liquid
TQ 028.3
A
1671-0460(2017)11-2192-05
教育部資助項目(No.2015BAC04B01)。
2017-03-17
張學崗(1975-),男,天津科林泰克總工程師,研究方向:分離節能。E-mail:zhangxuegang@163.com。
劉伯潭,男,副教授,碩士生導師,研究方向:傳質分離。E-mail:liubotan@tju.edu.cn。

