保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術臨床研究
何 威,王衛東,劉清波,陳堅平,林 杰,馬 靖,葉 劍,左海波
佛山市順德區第一人民醫院,廣東 佛山 528300
保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術臨床研究
何 威,王衛東,劉清波,陳堅平,林 杰,馬 靖,葉 劍,左海波
佛山市順德區第一人民醫院,廣東 佛山 528300
目的探討保留脾臟的全腹腔鏡下選擇性賁門周圍血管離斷術治療門靜脈高壓癥上消化道出血的療效。方法2011年2月~2014年12月期間接受保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術患者11例。觀察其保脾斷流手術前后血常規、肝功能、凝血功能、并發癥以及手術時間、手術中出血量等指標,術后對患者進行長期隨訪,觀察再出血率和生存情況。結果11例患者均在全腹腔鏡下完成保留脾臟的選擇性賁門周圍血管離斷術。手術時間110~225 min,平均157±31 min;手術中出血30~150 mL,平均83±37 mL。術后住院時間5~14 d(平均9.4 d)。患者手術后1周外周血白細胞、血小板、血紅蛋白、總膽紅素、白蛋白和凝血功能等與手術前比較均無明顯統計學差異(P>0.05)。結論保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術為食管胃底靜脈曲張破裂出血的患者提供了一種更為安全、有效的治療手段。
門靜脈高壓癥;選擇性賁門周圍血管離斷術;脾臟;腹腔鏡手術
雖然門靜脈高壓癥的內科及外科治療手段多樣,但各有其優缺點,且沒有一種治療手段能達到滿意的治療效果。理想的門靜脈高壓癥斷流手術應該在根除食管胃底曲張靜脈和有效降低再次靜脈曲張破裂出血風險的同時,減少對門靜脈系統血液循環的影響,保證向肝血流的灌注,并最大限度地減少門靜脈系統血栓形成及肝功能惡化的風險。賁門周圍血管離斷術仍是外科治療門靜脈高壓癥上消化道出血的主要術式之一[1-4]。傳統標準的賁門周圍血管離斷術,以及近年來所開展的腹腔鏡下賁門周圍血管離斷術,手術風險大,圍手術期并發癥發生率高,術后常見的并發癥多與脾臟切除有關,特別是門靜脈系統血栓形成及術中出血等[5]。然而,賁門周圍血管離斷術是否一定要包括脾切除臨床上尚存在爭議[6]。目前,開腹手術中保留脾臟的賁門周圍血管離斷術有零星報道,而腹腔鏡下賁門周圍血管離斷術中保留脾臟的手術方式罕見報道。因此,我們在選擇性賁門周圍血管離斷術基礎上,逐步探討保留脾臟的全腹腔鏡下選擇性賁門周圍血管離斷術。本研究通過回顧性分析我院2011年2月~2014年12月間11例接受保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術患者的資料,評估其療效及可行性。
1 資料與方法
1.1 一般資料
2011年2月~2014年12月期間接受保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術患者11例。其中男性9例,女性2例,年齡41~69歲,平均52.4歲。均為肝硬化門脈高壓癥并食道胃底靜脈曲張及破裂出血,其中病毒性肝炎后肝硬化8例,酒精性肝硬化4例(其中1例肝炎后肝硬化合并酒精性肝硬化)。均有上消化道出血史,有1次出血史者5例,有多次出血史者6例,曾接受內鏡下注射止血或套扎止血患者7例,術前檢查提示8例患者有輕-中度腹水。肝功能Child分級:A級3例,B級5例,C級3例。急診手術4例,經胃鏡檢查提示活動性出血,止血效果不佳后選擇急診手術治療;擇期手術7例,有上消化道出血病史,胃鏡檢查提示食管-胃底靜脈中到重度曲張,紅色征陽性;無預防性手術病人。所有患者術前均有不同程度的脾大和脾功能亢進癥狀,術前外周血白細胞計數為(6.19±3.82)×109/L,血紅蛋白計數為88±23 g/L,血小板計數為(89±36)×109/L。
1.2 治療方法
本組患者均行完全腹腔鏡下保留脾臟的選擇性賁門周圍血管離斷術。常規氣管插管麻醉后,建立操作通道。首先處理胃網膜及其動靜脈,LigaSure自弓內離斷胃大彎側網膜上的血管,包括胃網膜左動、靜脈和所有胃短血管,保留胃網膜右動、靜脈,離斷胃結腸韌帶左半側和脾胃韌帶中下段,既起到結扎胃底曲張靜脈預防出血的效果,又可以保留大網膜的血供。沿胃大彎朝賁門方向,將胃短血管、胃后靜脈和左膈下靜脈離斷。于胃小彎側緊貼胃壁,在胃冠狀靜脈發出食管旁靜脈分支的遠端離斷胃冠狀靜脈分支及伴行的胃左動脈分支,保留其冠狀靜脈主干;用超聲刀或LigaSure繼續分離胃后組織離斷胃后靜脈,繼續沿胃小彎朝賁門方向逐一切斷食管旁靜脈進入食管壁的分支和高位食管支進入食管肌層和胃底賁門區的分支。完成離斷術后的食管下段和胃底賁門區的四周壁應完全懸空。特別注意要離斷靠近食管裂孔處的高位穿支靜脈,這是引起食管靜脈曲張破裂出血的主要血管。離斷過程中大部分病人可見到明顯的食管旁靜脈,保留完整的冠狀靜脈主干及食管旁靜脈即為選擇性賁門周圍血管離斷術。
1.3 觀察指標
記錄手術前后血白細胞、血紅蛋白、血小板、白蛋白、總膽紅素、谷丙轉氨酶、谷草轉氨酶以及凝血功能指標,記錄手術時間、手術中出血量,記錄手術后并發癥、拔管時間、進食時間、活動時間、住院時間等。出院后對患者進行隨訪,定期行胃鏡、上腹部CT、彩超等相關檢查,定期復查血常規、肝功能、凝血功能等,記錄患者再出血發生情況及術后生存情況。
1.4 統計學處理
2 結果
本組11例患者均在全腹腔鏡下完成保留脾臟的選擇性賁門周圍血管離斷術,無中轉開腹病例,圍手術期無死亡病例。手術時間110~225 min,平均157±31 min;手術中出血30~150 mL,平均83±37 mL。7例常規手術患者術中無輸血,4例急診患者術中輸紅細胞400~800 mL。患者術后24~36 h開始下床活動并逐步飲水及進食流質。術后2~4 d拔除腹腔引流管。患者手術后1周外周血白細胞、血小板、血紅蛋白、總膽紅素、白蛋白和凝血功能等與手術前比較均無明顯統計學差異(P>0.05,表1)。
表1 手術前后血象和肝功能等變化情況()
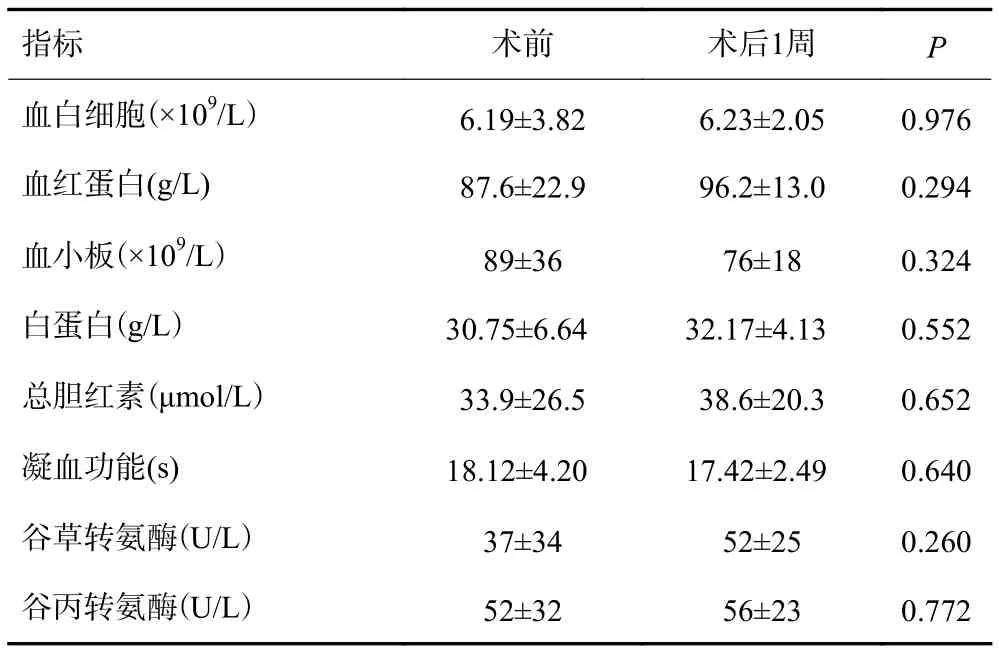
表1 手術前后血象和肝功能等變化情況()
指標 術前 術后1周P血白細胞(×109/L)6.19±3.826.23±2.050.976血紅蛋白(g/L)87.6±22.996.2±13.00.294血小板(×109/L)89±3676±180.324白蛋白(g/L)30.75±6.6432.17±4.130.552總膽紅素(μmol/L)33.9±26.538.6±20.30.652凝血功能(s)18.12±4.2017.42±2.490.640谷草轉氨酶(U/L)37±3452±250.260谷丙轉氨酶(U/L)52±3256±230.772
術后短期無腹腔出血、脾窩感染、腸瘺、胰瘺、膈下積液、肺部感染等并發癥。1例患者術后有中量淺黃色腹水,通過加強利尿、護肝、營養支持治療后腹水消退。1例患者術后出現應激性潰瘍,經胃鏡檢查證實,予以加強制酸等對癥處理后好轉。術后住院時間5~14 d(平均9.4 d)。10例患者術后進行了4~36個月隨訪,1例外地病人失訪。隨訪期間無再發消化道出血癥狀,無肝性腦病發生。
3 討論
門靜脈高壓癥作為一種病理生理變化復雜的外科疾病,治療方式多種多樣,但除肝移植外,至今尚無一種確切的手術方法能完全治愈,手術治療的重點仍然是治療其消化道出血及脾功能亢進癥狀,而非病因方面的治療。2014年,衛生和計劃生育委員會公益性行業科研專項專家組編寫了《門靜脈高壓癥食管胃靜脈曲張靜脈破裂出血治療技術規范專家共識》[7],共識中明確提出賁門周圍血管離斷術在門靜脈高壓癥治療中的突出作用,相對于肝臟移植高昂的費用以及肝源獲得的困難,賁門周圍血管離斷術不失為一種控制急性出血并降低再出血風險的有效選擇[1]。傳統的斷流手術經過幾十年的發展,已經總結了大量的經驗,除了表明他的各種優勢之外,所體現出來的越來越多的缺點也不容忽視。如術后門靜脈壓力降低不明顯,甚至部分病人還不降反升[8];而脾切除加劇了門靜脈血流淤滯以及術后門靜脈高壓,容易形成門靜脈系統血栓[9-10]。另外,與脾切除相關的其他并發癥如術后腹腔出血、發熱、感染及鄰近臟器副損傷也很常見。
本研究所采取的選擇性賁門周圍血管離斷術,術中僅離斷胃底小彎側以及食管賁門區漿膜外的穿支血管,維持其主干血管的完整,從而達到斷流徹底和保持機體自發性分流的目的[11-13]。選擇性賁門周圍血管離斷術既能阻斷胃底和食管下段出血區的反常血流,又能疏導門靜脈系統的高壓血流狀態,適當降低門靜脈血流量的同時,又可保證合理的門靜脈向肝血流灌注,緩解胃壁的充血狀態和預防門奇靜脈間的側支循環的重建,從而降低復發出血率。但根據我們既往的觀察,并非所有病例均適合行選擇性賁門周圍血管離斷術。如果食管旁靜脈的主干直接進入食管壁,或者食管賁門區的曲張血管形成靜脈叢或靜脈團,難以辨認食管旁靜脈時,或者既往有硬化治療病史,賁門周圍解剖結構不清時,亦應采用非選擇性賁門周圍血管離斷術,以確保能確切阻斷食管胃底曲張靜脈的反常血流,從而控制有致命危險的大出血。本組11例病例均順利行選擇性賁門周圍血管離斷,術中將食管向下方及外側牽引,使之與食管旁靜脈之間形成一定張力,能更好的暴露及分離食管旁靜脈。
本研究在選擇性賁門周圍血管離斷術基礎上,逐步探討保留脾臟的腹腔鏡下選擇性賁門周圍血管離斷術。手術中需要注意以下幾個方面:(1)手術在完全腹腔鏡下完成,無需另外行輔助手術切口,真正實現微創;(2)在胃大彎血管弓與胃之間游離大網膜,能夠保留完整的大網膜血供及交通支,保護大網膜血循環,能有效減少術后腹水等并發癥發生;(3)術中保留脾臟或保留大部分脾臟血供,同時盡量保留脾臟周圍自然形成的血管分支;(4)保留冠狀靜脈主干及食管旁靜脈;(5)完全離斷食管支及高位食管支;(6)必要時可行脾門動脈的部分結扎而非脾動脈主干的結扎,防止術后出現急性脾壞死;(7)若急診手術則以控制出血、搶救生命為前提,不能單純為手術而手術。
國內冷希圣[14-15]首先提出了保留脾臟的選擇性賁門周圍血管離斷術。本研究認為,門靜脈高壓癥脾亢患者因三系減低引起的易發感染機會、自發性出血幾率本身并不高,而重度脾亢患者在臨床上也并非常見,多數患者為輕-中度脾亢。而食管胃底靜脈曲張程度與脾亢程度并無明顯相關性。并且賁門周圍血管離斷術圍手術期并發癥多與脾切除有關。因此,并非所有行賁門周圍血管離斷術的患者都需要行脾切除,應根據患者具體情況而定,既往認為可以通過切除脾臟來對門靜脈系統實施減壓也許是一種錯誤的觀點。也就是說,在大多數情況下,脾切除不僅是不必要的,而且常常是有害的[16]。而且,不根據患者實際病情需要,盲目地切除脾臟會破壞其周圍業已自發形成的門體靜脈系統交通支,不僅造成術中出血量大,手術風險增高,而且會造成術后門靜脈壓力不降反升,進一步加劇門靜脈血流淤滯,手術后再出血及血栓形成風險極高。既往的研究也表明,保脾斷流術在保證肝臟門靜脈血流供應的基礎上,術中輸血量及術后門靜脈血栓發生率較低[17]。
在斷流術中保留脾臟,不僅保留了其對門靜脈血容量的調節和緩沖作用,避免因形成脾靜脈盲端而在該處發生湍流、血流停滯,同時避免術中鉗夾及擠壓脾靜脈所致內膜損傷及膠原纖維暴露等PVT高危狀態,保證了脾靜脈的正常血流,降低了PVT風險[18]。保留脾臟的賁門周圍血管離斷術,手術目的不僅僅是保脾,關鍵還在于對冠狀靜脈主干及其屬支的正確處理,以及對脾周分支血管及形成的側枝循環的保護,這比單純保脾要更為重要[19-20]。脾周自然形成的側枝循環能有效分流門靜脈血流,降低門靜脈壓力,同時自然形成的分流也極少導致肝性腦病的發生。本研究在保留脾臟的賁門周圍血管離斷術中,對于中度或中-重度的脾亢患者,在完成賁門周圍血管離斷術后,選擇性的進行脾門血管離斷,保留部分脾血供,以期減輕患者脾亢癥狀。根據術后觀察,患者脾亢癥狀均有不同程度的減輕,但因實施例數較少,尚無臨床大規模系統研究結果,尚不知道是否在所有患者中均有療效。有文獻報道,在保脾斷流術中部分結扎脾動脈,減少入脾血流,可在一定程度上改善脾功能亢進,同時可降低PVT發生率,而發生PVT的患者經規律抗凝治療后血栓再通率可達100%[21]。
在本組患者中,有4例為急診手術患者。經保留脾臟的全腹腔鏡賁門周圍血管離斷術后,除1例術后出現中量腹水外,其他3例患者均順利康復出院,術后未出現嚴重并發癥。我們認為,門靜脈高壓癥消化道大出血患者急診行腹腔鏡下保脾斷流術,因術中無需對脾門及脾臟周圍進行分離,明顯縮短了手術時間,減少了手術中出血等并發癥發生,降低了圍手術期患者死亡的風險,對于胃底食管靜脈曲張破裂并大出血內科治療不能控制的門靜脈高壓患者,不僅止血效果確切,且明顯降低圍手術期風險,降低圍手術期死亡率,不失為一種可取的治療方案。王東等[21]研究也表明,急診手術及肝功能Child C級的病人并非手術的絕對禁忌癥。在選擇切脾或保脾的手術方式時,應根據病人的年齡、肝功能分級、門靜脈壓力、脾臟大小、脾功亢進程度、出血情況、既往手術史和全身情況出發,在“個體化”原則指導下施行。是否行選擇性賁門周圍血管離斷術,可根據術前影像學檢查觀察有無明顯的食管旁靜脈,或手術中胃底賁門部有無形成難以解剖分離的粘連瘢痕等決定;對于僅輕度或輕-中度的脾亢患者,術中可行保脾手術,對于中度或中-重度的脾亢患者,術中行胃底賁門周圍血管離斷后,可根據情況行脾血管部分結扎,對于重度脾亢患者,急診時也可行脾門血管部分結扎的保脾手術,若患者一般情況好,切脾手術也是可行的,不能盲目的為了追求“保脾”而保脾。
保留脾臟的全腹腔鏡選擇性賁門周圍血管離斷術既簡化了手術步驟、縮短了手術時間和減少切脾帶來的嚴重合并癥,同時對肝臟功能和內臟血液循環的干擾較小,不增加術后門靜脈壓力,降低了術后門靜脈系統血栓形成的風險。對肝硬化失代償期并食管胃底靜脈曲張破裂出血的患者提供了一種更為安全、有效的治療手段。
[1]周光文. 肝移植時代門靜脈高壓癥外科手術方式的選擇[J]. 中國普外基礎與臨床雜志, 2013, 20(1): 10-2.
[2]冷希圣. 門靜脈高壓癥治療的現狀與展望[J]. 中國普外基礎與臨床雜志, 2013, 20(1): 1-3.
[3]Goyal N, Singhal D, Gupta S, et al. Transabdominal gastroesophageal devascularization without transaction for bleeding varices:results and indicators of prognosis[J]. J Gastroenterol Hepatol, 2007, 22(1): 47-50.
[4]Sharma A, Vijayaraghavan P, Lal R, et al. Salvage surgery in variceal bleeding due to portal hypertension[J]. Indian J Gastroenterol, 2007, 26(1): 14-7.
[5]鄧美海, 鄧 鵬, 林 楠, 等. 門靜脈高壓癥斷流手術后門靜脈血栓形成的調查[J]. 中華普通外科雜志, 2007, 22(8): 616-8.
[6]汪 謙. 門靜脈高壓癥脾臟保留與切除之爭[J]. 外科理論與實踐,2007, 12(2): 114-5.
[7]衛生和計劃生育委員會公益性行業科研專項專家組. 門靜脈高壓癥食管胃曲張靜脈破裂出血治療技術規范專家共識(2013版)[J]. 中華消化外科雜志, 2014, 13(6): 401-4.
[8]Yoshida H, Mamada Y, Taniai N, et al. New methods for the management of gastric varices[J]. World J Gastroenterol, 2006,12(37): 5926-31.
[9]孫勇偉, 羅 蒙, 陳 煒, 等. 門靜脈高壓癥外科手術后門靜脈系統血栓形成[J]. 外科理論與實踐, 2006, 11(3): 198-200.
[10]Zhang Y, Wen TF, Yan LN, et al. Preoperative predictors of portal vein thrombosis after splenectomy with periesophagogastric devascularization[J]. World J Gastroenterol, 2012, 18(15): 1834-9.
[11]王衛東, 林 杰, 陳小伍, 等. 全腹腔鏡選擇性賁門周圍血管離斷術的可行性[J]. 中華腔鏡外科雜志:電子版, 2013, 6(4): 284-7.
[12]王衛東. 腹腔鏡選擇性賁門周圍血管離斷術的方法和技巧[J]. 嶺南現代臨床外科, 2013, 13(2): 84-6.
[13]王衛東, 陳小伍, 吳志強, 等. 腹腔鏡經胃前、后雙入路選擇性賁門周圍血管離斷術[J]. 中華普通外科雜志, 2013, 28(11): 889-90.
[14]冷希圣. 肝移植時代如何看待門靜脈高壓癥的斷流手術[J]. 中國現代普通外科進展, 2007, 10(1): 1-4.
[15]冷希圣. 肝移植時代門靜脈高壓癥治療策略[J]. 中國實用外科雜志, 2009, 29(5): 373-6.
[16]Orozco H, Mercado MA, Martinez R, et al. Is splenectomy necessary in devascularization procedures for treatment of bleeding portal hypertension?[J]. Arch Surg, 1998, 133(1): 36-8.
[17]Voros D, Polydorou A, Polymeneas G, et al. Long-term results with the modified Sugiura procedure for the management of variceal bleeding: standing the test of time in the treatment of bleeding esophageal varices[J]. World J Surg, 2012, 36(3): 659-66.
[18]楊 威, 胡虞乾, 莫瑞祥. 門靜脈高壓癥脾切除賁門周圍血管離斷術后早期門靜脈血栓形成的預測[J]. 中華普通外科雜志, 2010, 25(9): 710-2.
[19]楊 鎮. 選擇性賁門周圍血管離斷術的發展與手術技巧[J]. 中國實用外科雜志, 2009, 29(5): 450-1.
[20]楊 鎮. 選擇性賁門周圍血管離斷術的解剖基礎和操作要點[J].外科理論與實踐, 2006, 11(3): 188-9.
[21]王 東, 栗光明, 朱繼業, 等. 保脾斷流術治療門靜脈高壓癥上消化道出血的療效分析[J]. 中國普外基礎與臨床雜志, 2013, 20(1):29-32.
Clinical study of total laparoscopic selective pericardial devascularization without splenectomy
HE Wei, WANG Weidong, LIU Qingbo, CHEN Jianping, LIN Jie, MA Jing, YE Jian, ZUO Haibo
the First People's Hospital of Shunde, Foshan 528300, China
ObjectiveTo evaluate the therapeutic effect of total laparoscopic selective pericardial devascularization without splenectomy.MethodsThe clinical data of 11 patients who
total laparoscopic selective pericardial devascularization without splenectomy from Feb 2011 to Dec 2014 were retrospectively analyzed. The blood routine, hepatic function, blood coagulation function, perioperative compliations, operation time and amount of bleeding were observed. The patients were followed-up and the re-bleeding rate and survival rate were observed.ResultsAll of the 11 operations were completed successfully under laparoscope. The mean operation time was 157 min (ranged from 110 to 225 min). The mean intraoperative blood loss was 83 ml (ranged from 30 to 150 ml). The mean postoperative hospital stay was 9.4 days(ranged from 5 to 14 days).There was no significant difference in the levels of the leukocyte, platelet, hemoglobin, total billrubin, albumin and blood coagulation function between pre- and a week after postoperative (P>0.05).ConclusionTotal laparoscopic selective pericardial devascularization without splenectomy is a safe and effective method for treatment of portal hypertension with upper gastrointestinal hemorrhage.
selective pericardial devascularization; portal hypertension; spleen; laparoscopic surgery
2017-03-06
佛山市醫學類科技公關項目(2014AB002413)
何 威,E-mail: weiweih@126.com
王衛東,E-mail: wangweidong1968@126.com

