核酸檢測與酶免檢測在寧夏地區無償獻血者血液篩查中的應用
閆玉剛楊立輝丁 靜陜 姍王 琦
1寧夏醫科大學 寧夏回族自治區銀川市 750001 2寧夏血液中心 寧夏回族自治區銀川市 750001
核酸檢測與酶免檢測在寧夏地區無償獻血者血液篩查中的應用
閆玉剛1,2楊立輝2丁 靜2陜 姍2王 琦1
1寧夏醫科大學 寧夏回族自治區銀川市 750001 2寧夏血液中心 寧夏回族自治區銀川市 750001
目的:對ELISA和NAT檢測結果進行分析,找出兩種檢測方法在血液篩查中的優勢、劣勢。方法:收集寧夏地區2016年1月到2016年12月無償獻血者標本,進行ELISA和NAT檢測,并對檢測數據進行比對分析。結果:兩種檢測方法比對中共檢測標本60958份,酶免檢測總陽性數為477份,陽性率為0.78%,NAT檢測陽性數154份,陽性率為0.25%。ELISA雙試劑陽性標本與核酸檢測結果的符合率為65.14%,單試劑陽性標本與核酸檢測結果的符合率為2.17%,灰區陽性標本與核酸檢測結果符合率為0。ELISA檢測陰性標本NAT檢測陽性數為57例,全為HBV DNA陽性,經電化學發光檢測乙肝兩對半結果為50例是隱匿性乙肝感染,7例檢測結果為陰性。結論:NAT檢測假陽性率較ELISA低,ELISA方法漏檢主要為隱匿性乙肝感染的漏檢。NAT檢測方法在獻血者血液篩查中優于ELISA檢測方法。
核酸檢測;酶免檢測;無償獻血者;血液篩查
獻血者標本檢測質量優劣很大程度取決于檢測方法、檢測試劑、檢測設備的先進程度,酶聯免疫檢測方法主要檢測的是血漿中的傳染性標志物抗原、抗體,當抗原進入體內到產生抗體,再到抗體達到一定濃度被檢測出來之前的這段時間稱作“窗口期”。酶聯免疫檢測方法最主要的風險就是血清轉換窗口期的漏檢[1],病毒變異致使檢測試劑不識別以及低病毒載量的慢性攜帶狀態是漏檢的另一原因[2]。核酸檢測的是病毒的DNA和RNA,可有效縮短病毒感染的窗口期,是目前國際上最先進的血液安全檢測方法,通過檢測可將乙肝、丙肝和艾滋病病毒的檢測“窗口期”由原來的50天、72天和22天,分別縮短到25天、59天和11天,血液安全將得到更好保障。因此,核酸檢測已經被視為降低酶免檢測窗口期漏檢風險,以及低病毒載量檢出的最佳檢測方法[3]。基于以上的研究結果,現在越來越多的國家和地區將核酸檢測納入到無償獻血者血液的篩查中,以期降低輸血殘余風險。本文通過對2016年1月到2016年12月酶免和核酸檢測結果的比較、分析中得出兩種檢測方法在血液篩查中的優勢、劣勢。
1 材料與方法
1.1 數據來源
數據來源于寧夏地區2016年1月到2016年12月無償獻血者標本60958份,經核酸和酶免檢測后的試驗數據。
1.2 儀器與試劑
1.2.1 試劑
血液篩查用酶聯免疫試劑:乙型肝炎病毒表面抗原診斷試劑盒(法國伯樂,北京萬泰);丙型肝炎抗體診斷試劑盒(上海科華,北京萬泰);人類免疫缺陷病毒抗原/抗體診斷試劑盒(法國伯樂,北京萬泰);HbsAg,抗-HCV,HIV 抗原/抗體,抗-TP質控物均為康徹斯坦。所有試劑均經批批檢定合格,并在有效期內使用。血液篩查用核酸檢測試劑:乙型肝炎病毒、丙型肝炎病毒、人類免疫缺陷病毒(1+2型)核酸檢測試劑盒(PCR-熒光法)(美國羅氏診斷產品有限公司),所有試劑均經批批檢定合格,并在有效期內使用。
1.2.2 儀器
血液篩查用酶聯免疫儀器:全自動酶免加樣儀(瑞士漢密爾頓STAR8CH);全自動酶免分析儀(瑞士漢密爾頓FAME24/20)。血液篩查用核酸儀器:全自動核酸提取儀(COBAS AmpliPrep)全自動核酸擴增儀(COBAS TaqMan)(瑞士羅氏公司)。
1.2 研究方法
(1)60958份標本先進行酶免檢測,檢測陰性的進行核酸檢測,核酸檢測結果中HBV DNA陽性的再進行乙肝五項化學發光檢測。(2)酶免檢測灰區陽性、單試劑陽性、雙試劑陽性的標本分別進行核酸檢測,比較兩種方法的檢測結果。
2 結果
(1)60958份獻血者標本ELISA檢測情況:HbsAg、抗-HCV、 HIV 抗原/抗體總陽性數為477份,陽性率為0.78%,HbsAg陽性率最高為0.43%,HIV 抗原/抗體陽性率最低為0.11%。單試劑陽性數368份,陽性率為0.60%,雙試劑陽性數為109份,陽性率為0.18%。單試劑陽性數是雙試劑的3.33倍。結果見表1。

表1:60958份獻血者標本ELISA檢測情況
(2)酶免檢測陰性標本核酸檢測情況:NAT檢測的總陽性數為57例,全為HBV DNA陽性,陽性率為0.09%。結果見表2。

表2:酶免檢測陰性標本核酸檢測情況
(3)57例HBV DNA陽性結果乙肝五項檢測結果(化學發光法):57例HBV DNA陽性中有34例抗-HBs 和抗-HBc 陽性,16例抗-HBs、抗-Hbe和抗-HBc陽性,共 50例屬于隱匿性感染。5例檢測結果為抗-HBs陽性其他陰性,2例檢測結果為五項全陰性。結果見表3。

表3:57例HBV DNA陽性結果乙肝五項檢測結果
(4)ELISA檢測陽性標本與核酸檢測結果符合率比較:
將ELISA檢測陽性標本分為雙試劑陽性組、單試劑陽性組、灰區陽性組,分別與核酸檢測結果進行比對,各項目灰區陽性標本與核酸檢測結果的符合率均為0。HbsAg雙試劑陽性標本(S/CO≥1)與核酸的符合率為80.36%,;單試劑陽性標本(S/CO≥1)與核酸的符合率為12.31%。抗-HCV雙試劑陽性標本(S/CO≥1)與核酸的符合率為62.07%,單試劑陽性標本(S/CO≥1)與核酸的符合率為0。HIV 抗原/抗體雙試劑陽性標本(S/CO≥1)與核酸的符合率為80.00%,單試劑陽性標本(S/ CO≥1)與核酸的符合率為0。雙試劑陽性標本(S/CO≥1)與核酸檢測結果的符合率較高,單試劑陽性標本(S/CO≥1)與核酸檢測結果的符合率較低。NAT總陽性標本為154份,陽性率為0.25%,酶免陽性率是核酸的3.12倍。結果見表4。
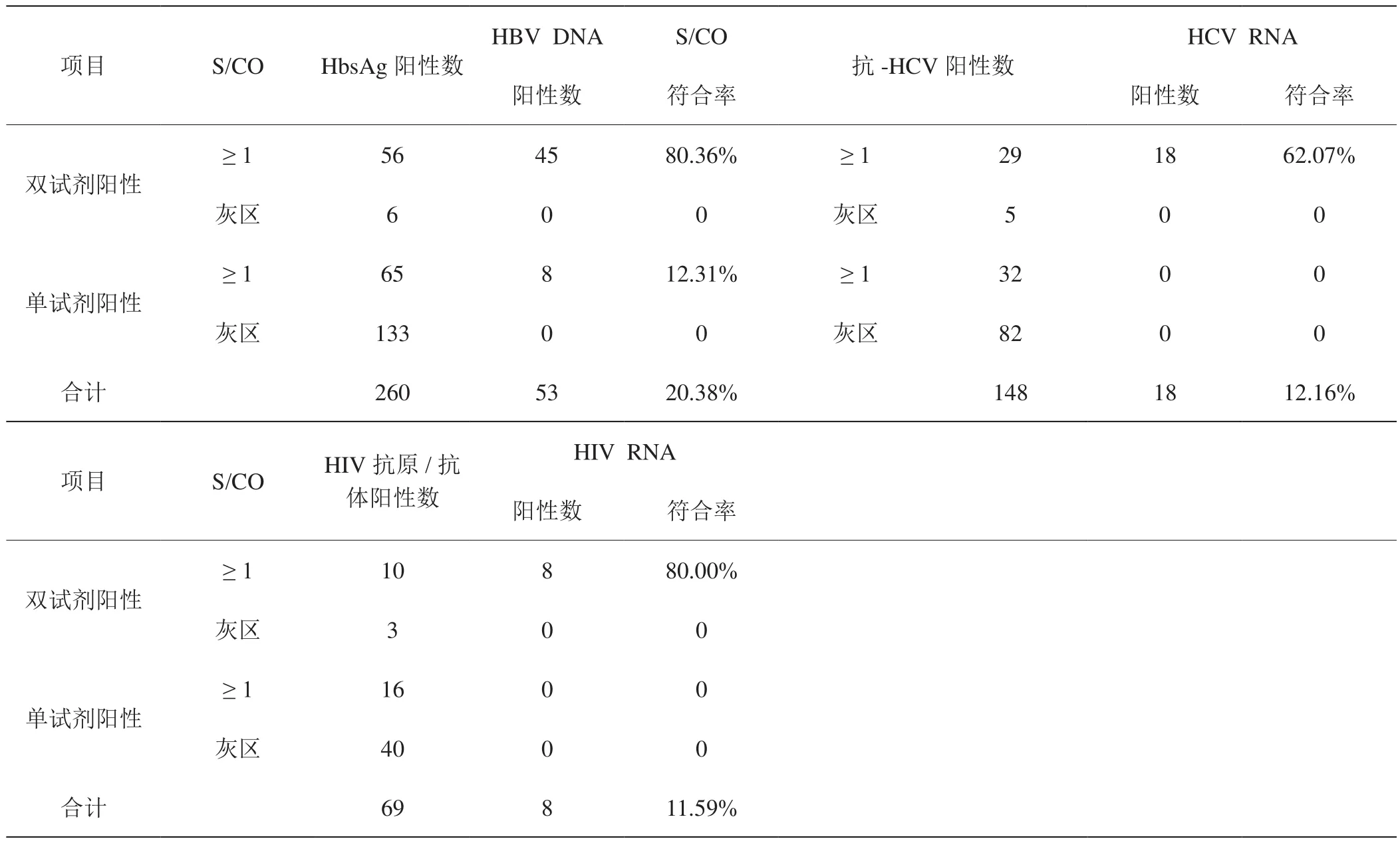
表4:ELISA檢測陽性標本與核酸檢測結果符合率比較
3 討論
從表1的數據可以看出酶免檢測主要不合格為單試劑檢測不合格,單試劑陽性數是雙試劑的3.33倍,高于溫州地區[4]。此現象主要是由于:
(1)實驗室灰區的設置:血液檢測結果至關重要,關系到受血者的健康狀況,為了預防酶免疫檢測的漏檢,很多實驗室都設置了“灰區”(既正常檢測陽性臨界值乘以灰區系數,如灰區系數為0.75正常S/CO≥1為陽性,設置灰區后0.75以上的結果為陽性),本實驗室灰區陽性比例為52.20%,占陽性數的一大半。
(2)試劑敏感性太高:據試劑廠家介紹,用于血液篩查的試劑要比醫院的敏感性高,目的也是為了防止漏檢。主要不合格項目為HbsAg,這與我國乙肝的高流行情況相吻合。
表2顯示,在酶免檢測陰性的標本中核酸檢測出57例陽性標本,陽性率為0.09%,低于廣州地區的0.22%[5],高于鄭州地區的0.06%[6],且陽性結果全部為HBV DNA,與大連地區一致[7]。在對57例HBV DNA陽性標本進行乙肝五項的檢測,檢測結果見表3。57例HBV DNA陽性中有34例抗-HBs 和抗-HBc 陽性,16例抗-HBs、抗-Hbe和抗-HBc陽性,共 50例屬于隱匿性感染。5例檢測結果為抗-HBs陽性其他陰性,2例檢測結果為五項全陰性,檢測結果與鄭州地區基本相符[6]。由此可見,隱匿性乙肝感染是酶免檢測主要的漏檢原因之一,7例乙肝五項陰性標本未做進一步確認,有可能是酶免窗口期漏檢[8],也有可能是核酸檢測假陽性,50例抗-HBc陽性與HBV DNA結果一致,增加抗-HBc檢測可以降低乙肝病毒漏檢的風險[9]。
表4得出酶免檢測灰區陽性數是249份,占酶免陽性的52.20%,與NAT的符合率為0;單試劑陽性數為368份,占酶免陽性的77.15%,與NAT的符合率為2.17%。雙試劑陽性數為109份,占酶免陽性的22.85%,與NAT的符合率為65.14%。ELISA(+)NAT(+)79份, 其 中HbsAg(+) NAT(+)53份,符合率為20.38%,低于溫州、深圳地區[4,10];抗-HCV(+)NAT(+)18份,符合率為12.16%,高于溫州地區的11.2%[4];HIV-Ab/Ag(+)NAT(+)8份,符合率為11.59%,符合率低于深圳地區[10]。ELISA檢測陽性率是NAT的3.12倍,酶免檢測陽性數明顯高于核酸檢測陽性數,灰區與單試劑陽性標本與核酸檢測符合率較低,說明這些標本的假陽性率較高[11]。這主要是由于酶免檢測抗原、抗體蛋白結構易變,檢測結果受自身抗體、交叉反應、標本內物質干擾、溶血、脂血、試劑盒抗原不純、溫度、洗液比例、洗版效果、試劑質量等的影響,易產生假陽性。核酸檢測的是DNA或RNA,能夠縮短病毒窗口期,對免疫靜默、病毒變異有很好的檢出[12],所以核酸檢測方法優于酶免檢測方法。
綜上所述,酶免檢測假陽性率較高主要為灰區(56.4%)和單試劑陽性(23.7%)所占比重較大,且各項目灰區陽性標本與核酸檢測結果的符合率均為0,單試劑陽性標本與核酸檢測結果符合率較低,故建議:
(1)取消酶免檢測灰區值的設定。
(2)對單試劑檢測陽性標本因再進行確認試驗。
核酸檢測57例陽性標本中50例為隱匿性乙肝感染,建議增加抗-HBc檢測以降低乙肝病毒漏檢的風險。
(通訊作者:王琦)
[1]Bush MP.Transfusion-transmitled viral infections:building bridges to transfusion medicine to reduce risks and understand epidemiology and parhogenesis.Transfusi on,2006,46(09):1624-1640.
[2]DelwartE,Kuhns MC,Busch MP.Surveillance of the genetic variation in incident HIV,HCV,and HBV infections in blood and plasma donors;implications for blood safety,diagnostics,treatment,an d molecular epidemiology.J Med Virol,2006,78(Suppl1):S30-35.
[3]LapercheS.Blood safety and nucleic acid testing in Europe.Euro Surveill,2005,10(02):3-4.
[4]張鋒,張瓊,林碧,等.血清學聯合核酸檢測在獻血者血液篩查中的互補性[J].中國艾滋病性病,2016,22(03):197-199.
[5]梁浩堅,汪傳喜,許結儀,等.2011-2014年廣州地區無償獻血者核酸檢測結果分析[J].中國醫藥科學,2016,6(10):138-141.
[6]趙紅娜,王藝芳,李俊英,等.核酸檢測與酶免檢測在鄭州地區血液篩查中的聯合應用[J].中國輸血雜志,2015,28(10):1269-1271.
[7]鄧雪蓮,安萬新,梁小華.大連市血液中心血清學檢測與核酸檢測并行的效果觀察[J].中國輸血雜志,2012,25(01):38-40.
[8]Yoshikawa A,GotandaY,ItabashiM,etal. Hepatitis B NAT viruspositivebolld donors in the early and tate stages of HBV infection:analyses of the window period and kinetics of HBV DNA.Vox Sang,2005,88(02):77-86.
[9]KleinmanSH,KuhnsMC,ToddDS,etal. Frequency of HBV DNA detection in US blood donors testing positive for the presence of anti-HBc:implications for transtusion transmission and donor screening. Transfusion,2003,43(06):696-704.
[10]曾 勁 峰,鄭 欣,許曉 絢.ELISA檢測與NAT在血液篩查應用中的互補性研究[J].中國輸血雜志,2012,25(10):1012-1014.
[11]陳顯,胡文佳,黃成埂,等.獻血者ELISA檢測為灰區標本的確證試驗與核酸檢測情況分析[J].中國輸血雜志,2015,28(02):198-199.
[12]顏秀娟,陸祝選,邱昌文,等.核酸檢測技術應用于血清學篩查合格的獻血者標本檢測[J].中國輸血雜志,2012,25(12):1322-1324.
[13]LluisirirotchanakulS. OotaS,KhuponsardK,etal,Occult hepatitis B virus infection in Thai blood donors[J].Transfusi on,2011,51(07):1532-1540.
[14]RenFR,WangJX,HuangY,etal. Hepatitis B virus nucleic acid testing in Chinese blood donors with normal and elevated alanine aminotransferase[J].Transfusi on,2011,51(12):2588-2595.
Analyze NAT and ELlSA detect donors blood in ningxia
Yan Yugang1,2, Yang Lihui2, Ding Jing2, Shan Shan2, Wang Qi1
1.Ningxia yinchuan, ningxia medical university 750001; 2.Blood center in ningxia Ningxia yinchuan 750001
Objective: ompared the results of ELISA with NAT detection methods, identifies the advantage and disadvantage of each other and find the complementary in reducing the infectious disease about blood transfusion. Methods: We compared the detection data of ELISA with the detection data of NAT collected at Ningxia region inJanuary to December 2016. ResultsA: total of 60,958 samples were tested for the comparison of the two test methods.The total number of samples with positive results in HbsAg, anti-HCV and HIV antigen/ antibody tests was 477, and the positive rate was 0.78%.154 results of the NAT test were positive, and the positive rate was 0.25%.The results of 57 samples were ELISA-NAT+, and they were all HBV DNA positive.The results of the electrogeneratedchemiluminescence (ECL) examination of HBsAg / anti-HBs / HBeAg / anti-HBe / anti-HBc were:50 cases of occult hepatitis B infection (OBI), and 7 negative cases. Conclusion: NAT detection of false positive rate was lower than that of ELISA, ELISA is the main method of detection of occult hepatitis B infection.
NAT(nucleic acid testing); ELISA(Enzyme-Linked ImmunosorbentAssays); Voluntary donation; Results of blood detection

