hERG鉀通道通過降低氧化應激改善肝細胞糖代謝
盧 晶 沈 涵 程 呈 宋麗妮 張怡塵 謝榮榮 袁明霞 楊金奎*
(1.首都醫科大學附屬北京同仁醫院內分泌科,北京 100730; 2.糖尿病防治研究北京市重點實驗室,北京 100730)
·內分泌與代謝病專題 ·
hERG鉀通道通過降低氧化應激改善肝細胞糖代謝
盧 晶1,2沈 涵1,2程 呈1,2宋麗妮1,2張怡塵1,2謝榮榮1,2袁明霞1,2楊金奎1,2*
(1.首都醫科大學附屬北京同仁醫院內分泌科,北京 100730; 2.糖尿病防治研究北京市重點實驗室,北京 100730)
目的 研究hERG鉀通道(human ether-α-go-go related gene channels) 在肝細胞中與糖代謝的關系。方法 用hERG鉀通道過表達載體轉染人類肝癌細胞系(liver hepatocellular carcinoma, HepG2)細胞,通過熒光定量PCR (real-time PCR, RT-PCR) 和蛋白印跡 (Western blotting) 法檢測糖代謝、糖異生、氧化應激及還原型煙酰胺腺嘌呤二核苷酸磷酸 (nicotinamide adenine dinucleotide 2′-phosphate, NADPH ) 相關亞基的表達。結果hERG鉀通道蛋白可在肝臟細胞中表達,將hERG鉀通道過表達于HepG2細胞后,糖異生相關基因葡萄糖-6-磷酸激酶 (glucose-6-phosphatase, G6Pase) 表達顯著降低,而磷酸烯醇式丙酮酸羧激酶 (phosphoenolpyruvate carboxykinase, PEPCK) 表達有降低。胰島素表達相關基因葡萄糖轉運蛋白2(glucose transporter type 2, GLUT2)、胰島素受體底物2 (insulin receptor substrate, IRS-2) 和腺苷酸活化蛋白激酶α亞基2 [(adenosine 5’-monophosphate(AMP)-activated protein kinase), AMPKα2] 的表達水平均顯著增高。NADPH4種亞基p22、p47、p67和p91表達均顯著降低。結論hERG鉀通道可以通過降低氧化應激改善肝細胞內糖代謝。
人ether-α-go-go相關基因;胰島素抵抗;氧化應激;糖代謝
流行病學研究表明,糖尿病在我國發病人數接近1億,嚴重影響我國人民健康狀況。2型糖尿病主要表現為胰島素分泌缺陷或胰島素分泌障礙[1-2]。肝臟是機體能量代謝的主要器官之一,也是胰島素作用的主要靶器官,參與維持體內空腹血糖濃度。肝臟胰島素抵抗主要是指胰島素抑制肝臟葡萄糖輸出能力,造成糖異生增加,糖原分解減少,從而導致2型糖尿病。
人ether-a-go-go相關基因 (human ether-a-go-go related gene,hERG) 編碼的離子通道稱為hERG鉀通道,屬于電壓依賴性鉀通道(voltage-dependent potassium channel, Kv) 家族成員[3]。hERG鉀通道主要參與心肌動作電位的復極化,hERG鉀通道突變后可導致外向復極鉀電流降低,QT間隙延長,引起多型性室性心動過速,嚴重者可導致猝死,即長QT綜合征 (long-QT syndrome, LQTs)[4]。 本課題組[5]前期已成功構建hERG鉀通道基因敲除小鼠,并發現hERG鉀通道基因在維持胰島β細胞的形態及功能方面具有重要作用,敲除小鼠表現為血糖水平增高和胰島素分泌降低。氧化應激是造成胰島素抵抗的重要原因之一,hERG鉀通道可能通過抑制氧化應激來改善機體內糖代謝。
本研究擬在細胞水平研究hERG鉀通道在人肝臟細胞HepG2中的表達情況,并深入研究其與氧化應激和糖代謝的關系。
1 材料與方法
1.1 細胞培養
人肝癌細胞系HepG2購自中國協和醫科大學細胞資源中心 (Cell Resource Center, IBMS, CAMS/PUMC),用DMEM (Dulbecco’s Modified Eagle’s Medium) (Gibco公司,美國)進行培養,加入10%(體積分數)胎牛血清(Gibco公司,美國)、100 U/mL青霉素和0.1 g/L鏈霉素(Gibco公司,美國),放于37 ℃,5%(體積分數) CO2孵箱內培養,每2 d用0.25%(質量分數)胰酶(Gibco公司,美國)消化后傳代,待細胞生長至90%時進行質粒轉染。
1.2 質粒構建和轉染
將hERG鉀通道基因構建到pcDNA3.1-GFP-His(-)B (PCDB) (Sino-Geno Max, 中國) 載體上。質粒DNA采用TransIntro EL Transfection Reagent(TransGen Biotech 公司,中國)脂質體轉染法,根據轉染試劑盒操作說明轉染HepG2 細胞。以pcDNA3.1-增強型綠色熒光蛋白(green fluorescence protein,GFP) 載體轉染的HepG2 細胞作為實驗對照組(control)。細胞轉染48 h后觀察GFP熒光強度并收集細胞用于后續實驗。
1.3 RNA的提取和熒光實時定量PCR
采用天根細胞組織總RNA提取試劑盒(批號:DP419)提取RNA,采用天根FastQuant cDNA第一鏈合成預混試劑(批號:KR108)合成cDNA。Beta-actin基因作為內參。采用Light Cycler 96儀器 (Roche公司,美國),SYBR Green master mix檢測RNA的表達情況。PCR反應體系為20μL,2×Enzyme mix (Transgen Biotech, 批號:AS111) 10 μL;正向引物 0.4 μL;反向引物 0.4 μL; cDNA 1.5μL, DEPC H2O 7.7 μL。擴增條件為94 ℃ 5 min,94 ℃ 30 s,60 ℃ 30 s,72 ℃ 20 s,35個循環;72 ℃ 5 min,自然冷卻至室溫,所用引物見表1。

表1 引物序列
1.4 Western blotting分析
采用BCA蛋白分析試劑盒 (碧云天生物技術有限公司,中國)測定蛋白濃度。hERG抗體購自Sigma公司(美國),批號SAB14082;PEPCK購自Santa-Cruz公司(美國),批號SC-28477;G6Pase購自Santa-Cruz公司(美國),批號SC-25486;Beta-actin作為內參,抗體購自CST(Cell Signal Technology)公司,批號8457。取80 μg總蛋白進行10%(質量分數)的SDS-PAGE電泳,濕轉(200 mA,120 min)至硝酸纖維膜上。用TBST[TBS+0.1%(體積分數) Tween-20]配制的5%(質量分數)脫脂奶粉室溫封閉1.5 h,用封閉液將一抗稀釋后與膜在4 ℃搖床孵育過夜,次日用TBST洗膜3次,每次5 min,再與辣根過氧化物酶(horseradish peroxidase, HRP)標記的二抗(1∶2 000)室溫孵育1 h。TBST洗滌,滴加增強化學發光(enhanced chemiluminescence, ECL)發光液后用Chemi-Doc Touch凝膠成像系統顯影成像,并用Image J軟件對圖像進行灰度分析。
1.5 統計學方法
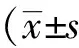
2 結果
2.1hERG載體轉染HepG2細胞
將hERG過表達質粒和pcDNA3.1-GFP質粒分別轉染HepG2細胞,48 h后觀察GFP表達情況。結果顯示,兩種質粒的GFP熒光均有明顯表達,兩種質粒均成功轉染HepG2細胞(圖1)。
2.2hERG鉀通道在肝臟細胞中表達
采用Western blotting法檢測hERG蛋白在人肝臟細胞HepG2中的表達。結果顯示,hERG蛋白在HepG2中有表達,而將hERG鉀通道蛋白過表達HepG2后,hERG蛋白表達增加明顯 (P<0.01,圖2)。
2.3hERG鉀通道對糖異生相關基因的影響
將hERG鉀通道過表達于HepG2細胞后,檢測糖異生相關基因PEPCK和G6Pase蛋白的表達。Western blotting結果顯示,hERG鉀通道過表達HepG2細胞后,G6Pase蛋白水平顯著降低 (P<0.05)。PEPCK表達水平降低(圖3)。
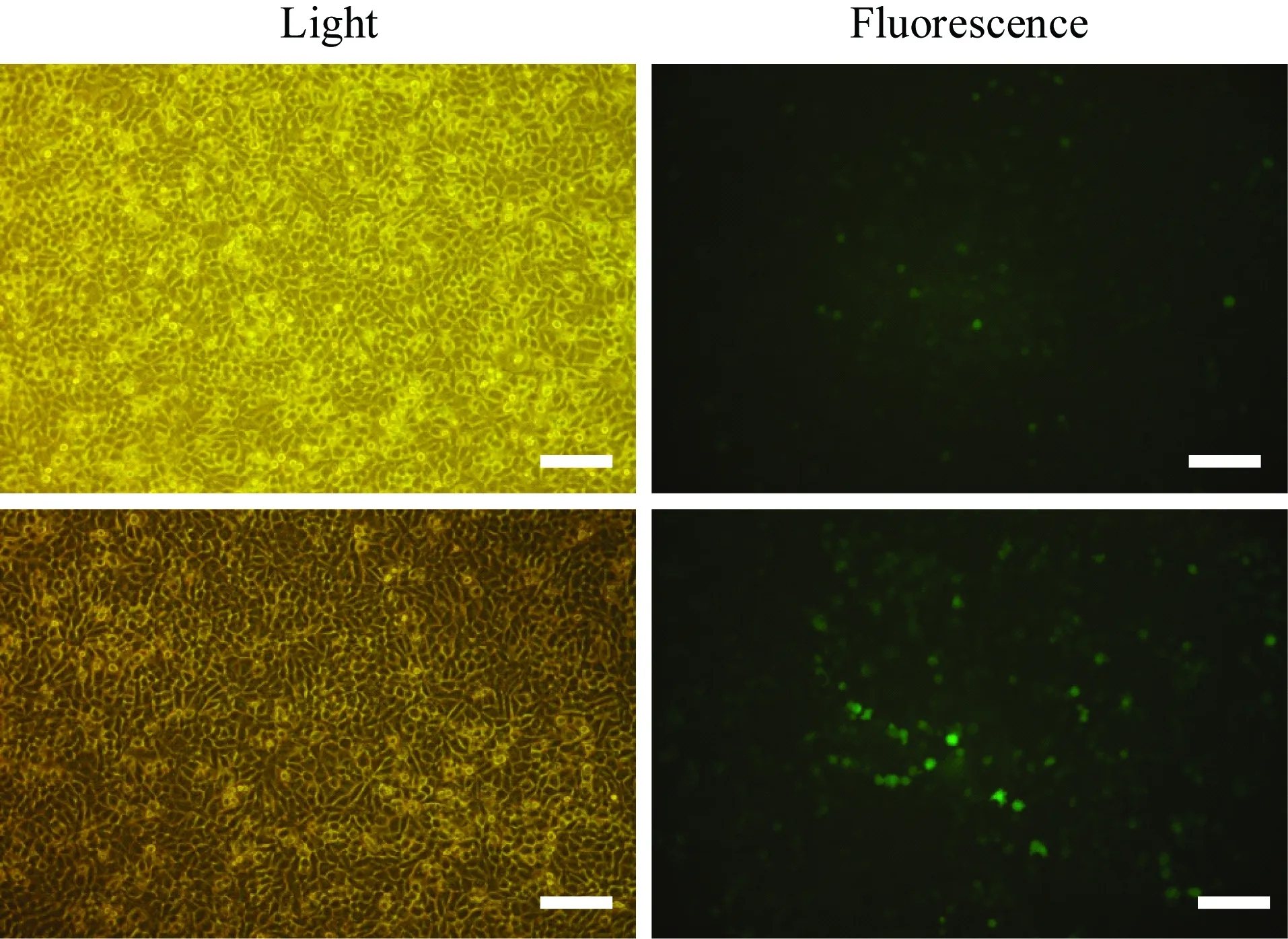
圖1 質粒轉染HepG2
A:hERGover-expression plasmid; B: pcDNA3. 1-GFP vector;hERG: human ether-a-go-go related gene; Bar: 100 μm.
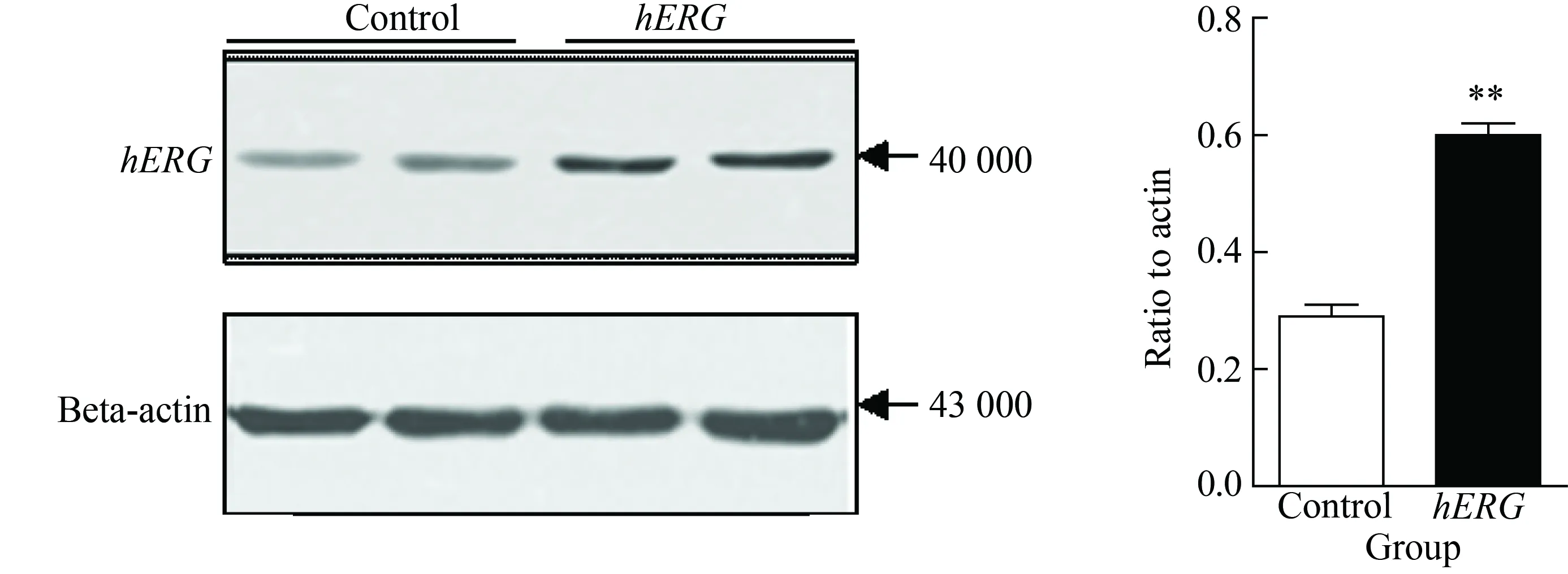
圖2 hERG鉀通道蛋白在HepG2細胞中的表達

圖3 hERG鉀通道對HepG2細胞糖異生相關基因表達的影響
*P<0.05vscontrol group,n=3;hERG: human ether-a-go-go related gene;G6Pase: glucose-6-phosphatase;PEPCK: phosphoenolpyruvate carboxykinase.
2.4hERG鉀通道對糖代謝相關基因表達的影響
將hERG鉀通道過表達于HepG2細胞后,采用RT-PCR方法檢測糖代謝相關基因GLUT2、IRS-2和AMPKα2的表達水平,結果顯示,hERG鉀通道過表達HepG2細胞后,與對照組相比,3種基因的mRNA水平顯著升高 (P<0.05)(圖4)。
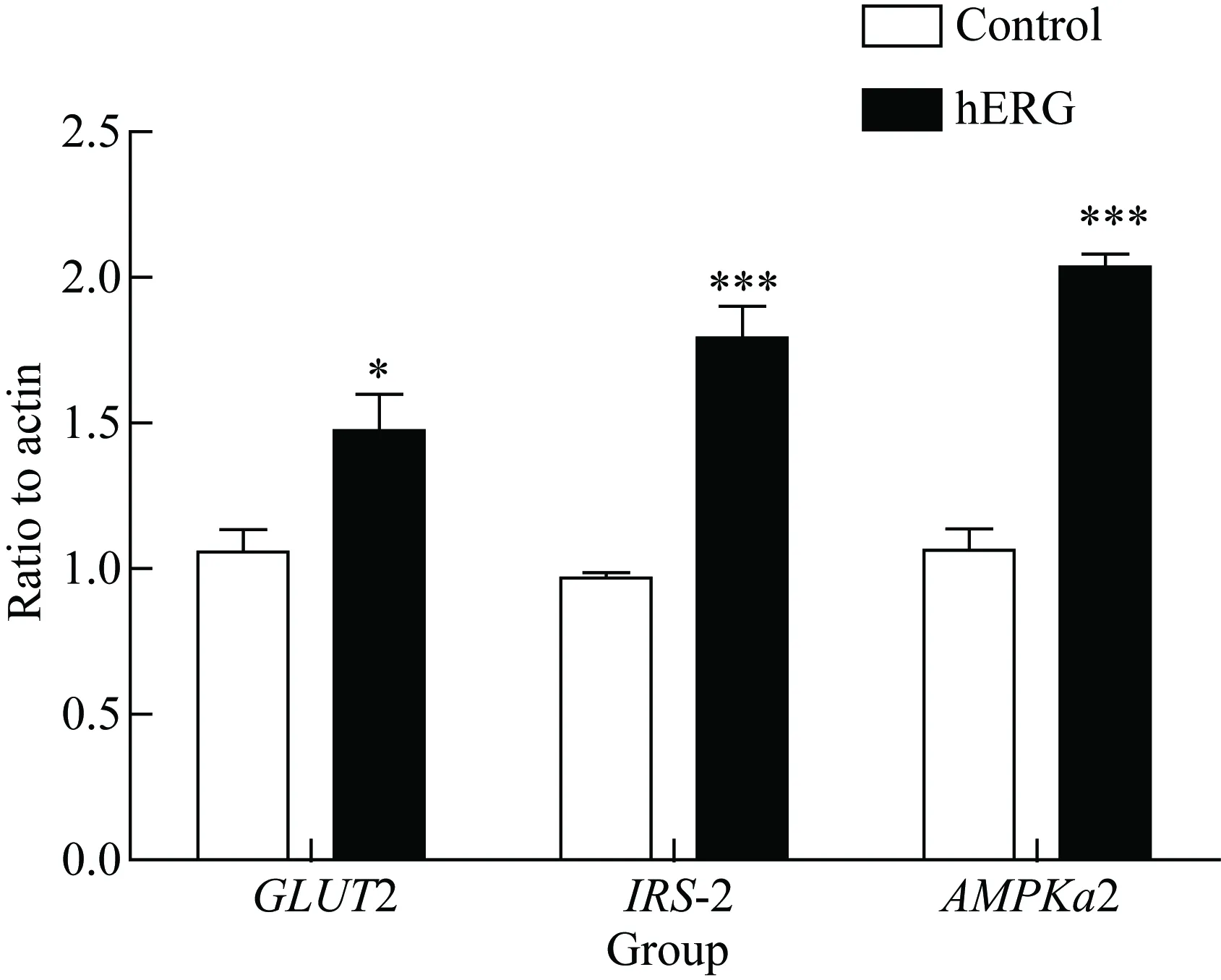
圖4 hERG鉀通道對HepG2細胞糖代謝相關基因表達的影響
*P<0.05,***P=0.000vscontrol group,n=3;hERG: human ether-a-go-go related gene;GLUT2:glucose transporter type 2;IRS-2: insulin receptor substrate-2;AMPKα2: adenosine 5’-monophosphate(AMP)-activated protein kinase α2.
2.4hERG過表達降低NADPH相關亞基的表達水平
為檢測hERG過表達后對NADPH亞基的影響,采用RT-PCR檢測NADPH亞基p22、p47、p67和p91的mRNA表達,結果顯示,hERG過表達后p22、p47、p67和p91的mRNA表達均明顯降低(P<0.05,圖5)。
3 討論
hERG鉀通道屬于電壓依賴性鉀通道家族,但是其電流特點與其他傳統的鉀通道不同,較為復雜[6]。hERG鉀通道在多種組織,如心、腦、垂體、胰腺等均有表達,并發揮不同作用[7]。本課題組[8]前期研究顯示,在C57BL/6小鼠上將hERG基因敲除后,小鼠會出現血糖增高、胰島素抵抗等糖代謝紊亂癥狀現象。肝臟是體內糖代謝的重要器官之一。胰島素抵抗是2型糖尿病發病的機制之一。氧化應激是造成胰島素抵抗的重要原因。目前尚未有研究hERG鉀通道與氧化應激及糖代謝的關系的報道。本研究在細胞水平證實,hERG鉀通道在肝臟細胞中表達,并通過降低氧化應激,減少糖異生,改善糖代謝。
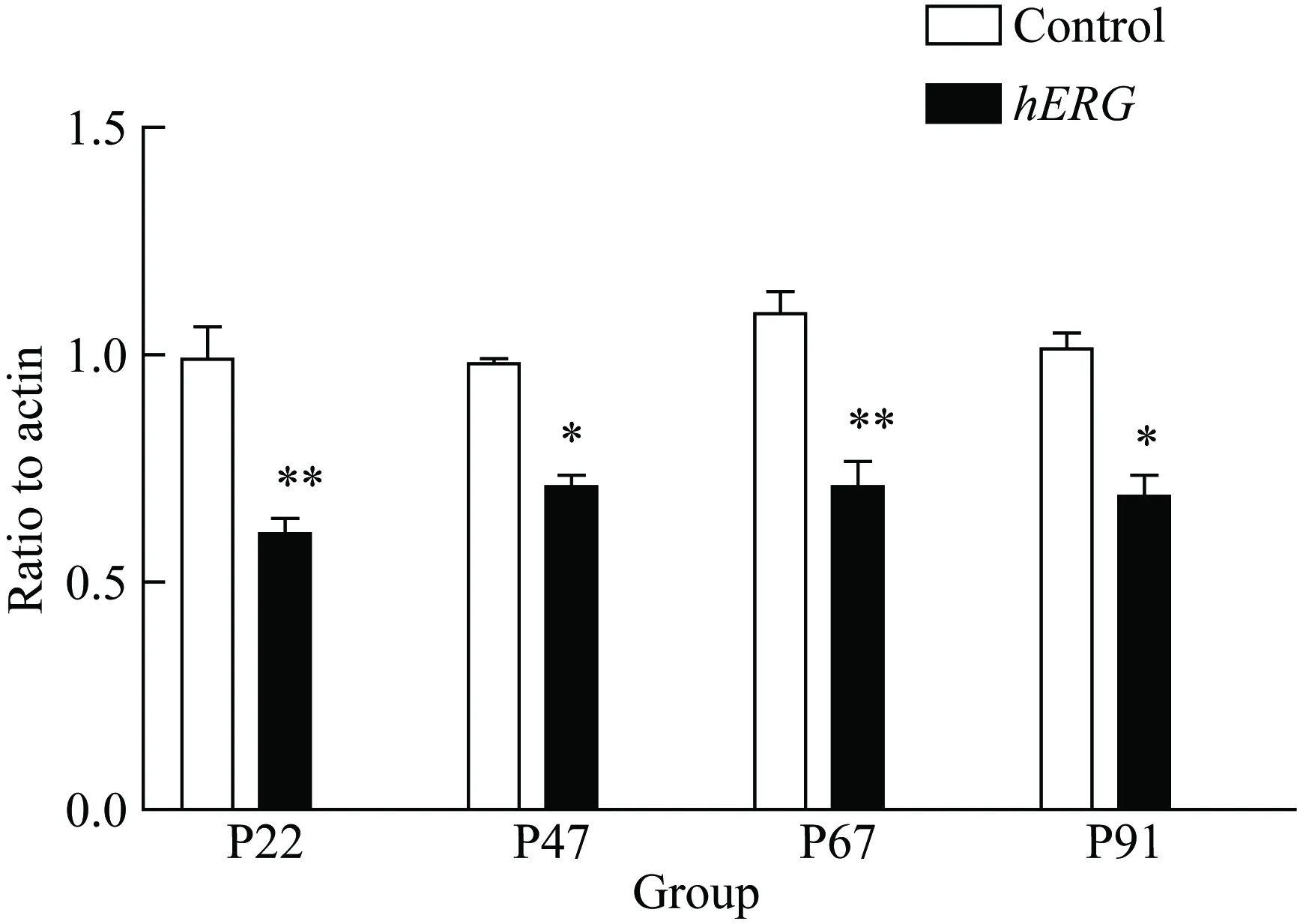
圖5 hERG降低HepG2細胞中NADPH亞基的表達
*P<0.05,**P<0.01vscontrol group,n=3;hERG: human ether-a-go-go related gene; NADPH: nicotinamide adenine dinucleotide 2′-phosphate.
AMPK是一個能量傳感器,參與調節包括胰島B細胞、肝臟、骨骼肌和脂肪在內的多種外周組織的糖脂代謝過程[9]。AMPK是一個異源三聚體蛋白,由α、β和γ 3個亞單位組成,其中α亞基起催化作用。AMPK的亞基α2的活性與胰島素抵抗相關[10-11]。本研究結果顯示,hERG可誘導AMPKα2的表達。糖代謝相關基因GLUT2和IRS-2表達也增高,PEPCK和G6Pase是糖異生的主要限速酶,hERG過表達后,糖異生基因PEPCK和G6Pase表達下降,提示hERG鉀通道在細胞水平可以降低糖異生,促進糖分解。
NADPH氧化酶屬于NOX家族成員,主要由催化亞基p91,跨膜亞基p22,胞質亞基p47、p67等組成的酶復合體。NADPH氧化酶主要的生理學功能是產生ROS,參與機體氧化應激,已有研究[12-13]表明其與胰島素抵抗密切相關。因此本研究推測,hERG鉀通道可能通過抑制氧化應激作用,減少胰島素抵抗從而改善糖代謝。本研究結果證實了這一推測,hERG過表達后,NADPH 4種亞基均有明顯降低,顯示hERG鉀通道通過降低氧化應激水平,調節糖代謝。
本研究下一步擬在兩方面進行深入研究。一方面,在動物水平,利用課題組前期構建的hERG敲除小鼠,研究hERG鉀通道敲除后,主要是肝臟內,氧化應激是否增加從而導致糖耐量異常;另一方面,目前已知的多種hERG鉀通道抑制劑,如E4031[14]、多菲利特[15]、西沙比利[3,16]、維拉帕米[17]等,這幾種藥物均在不同程度上影響hERG鉀通道的門控特性,使其改變,造成電流幅度下降甚至完全消失。本課題組將在細胞水平和動物水平分別運用這幾種藥物,研究藥物抑制后hERG鉀通道對氧化應激及糖代謝的影響。
[1] Ye J M, Dzamko N, Cleasby M E, et al. Direct demonstration of lipid sequestration as a mechanism by which rosiglitazone prevents fatty-acid-induced insulin resistance in the rat: comparison with metformin [J]. Diabetologia, 2004, 47(7):1306-1313.
[2] Fryer L G, Carling D. AMP-activated protein kinase and the metabolic syndrome [J]. Biochem Soc Trans, 2005, 33(2):362-366.
[3] Bentzen B H, Olsen S P, Roon L C B, et al. Bk channel activators and their therapeutic perspectives[J]. Front Physil, 2014, 5:389.
[4] Curran M E, Splawski I, Timothy K W, et al. A molecular basis for cardiac arrhythmia: HERG mutations cause long QT syndrome [J]. Cell, 1995, 80 (5): 795-803.
[5] Qiu H Y, Yuan S S, Yang F Y, et al. HERG protein plays a role in Moxifloxacin-induced hypoglycemia [J]. J Diabetes Res, 2016,16 (6): 298-304.
[6] 元沙沙,黃海霞,楊金奎. 胃腸動力藥西沙比利對表達于HEK293細胞的人ether-a-go-go相關基因2通道的影響[J].首都醫科大學學報,2014,35 (6): 760-764.
[7] Warmke W, Ganetzky B. A family of potassium channel genes related to eag in Drosophila and mammals [J]. Proc Natl Acad Sci USA, 1994, 91(8): 3438-3442.
[8] Taniguchi C M, Ueki K, Kahn R. Complementary roles of IRS-1 and IRS-2 in the hepatic regulation of metabolism [J]. J Clin Invest, 2005, 115 (3): 718-727.
[9] Hardie D G, Hawley S A, Scott J W. AMP-activated protein kinase-development of the energy sensor concept.[J] J Physiol, 2006, 574 (1): 7-15.
[10]Long Y C, Zierath J R. AMP-activated protein kinase signaling in metabolic regulation [J]. J Clin Invest, 2006, 116 (7): 1776-1783.
[11]王蕓姣,韓文祺,李若菲,等.AMPK參與調節大鼠脂肪肝相關性肝癌前病變的形成[J]. 首都醫科大學學報, 2016,37(2) :208-213.
[12]劉頤軒,宋桉,王蕓,等.氧化應激在肥胖及胰島素抵抗中的作用研究進展[J]. 段力園,宋光耀.解放軍醫藥雜志, 2014,26(1) :99-101.
[13]Wei Y, Sowers J R, Nistala R, et al. Angiotensin II-induced NADPH oxidase activation impaired insulin signaling in skeletal muscle cells [J]. J Biol Chem, 2006, 281(46): 35137-35146.
[14]Zhou Z, Gong Q, Ye B, et al. Properties of channels stably expressed in HEK 293 cells studies at physiological temperature [J]. Biophys J, 1998, 74(1): 230-241.
[15]Snyders D J, Chaudhary A. High affinity open channel block by dofetilide of HERG expressed in a human cell line [J]. Mol Pharrnacol, 1996, 49(6): 949-955.
[16]Mohammad S, Zhou Z, Gong Q, et al. Blockage of HERG human cardiac K+channel by the gastrointestinal prokinetic agent cisapride [J]. Am J Physiol, 1997, 273 (5 Pt 2): H2534-H2538.
[17]Calloe K, Elmedyb P, Olesen S P, et al. Hypoosmotic cell swelling as a novel mechanism for modulation of cloned HCN2 channels[J]. Biophys J, 2005,89(3): 2159-2169.
編輯 慕 萌
Human ether-α-go-go related gene channels improves glucose metabolism via anti-oxidative stress in HepG2 cells
Lu Jing1,2, Sheng Han1,2, Cheng Cheng1,2, Song Lini1,2, Zhang Yichen1,2, Xie Rongrong1,2, Yuan Mingxia1,2, Yang Jinkui1,2*
(1.DepartmentofEndocrinology,BeijingTongrenHospital,CapitalMedicalUniversity,Beijing100730,China; 2.BeijingKeyLaboratoryofDiabetesResearchandCare,Beijing100730,China)
Objective To evaluate the effect of the new pathway of human ether-α-go-go related gene (hERG) channels on glucose metabolism in hepatic cells. Methods Liver hepatocellular carcinoma (HepG2) cells were transfected withhERGchannels over-expression plasmid DNA. pcDNA3. 1-GFP plasmid was used as a negative control. The expression ofhERG, phosphoenolpyruvate carboxykinase(PEPCK) and glucose-6-phosphatase (G6Pase) were detected by Western blotting. The mRNA level of glucose transporter type 2 (GLUT2), insulin receptor substrate (IRS-2), adenosine 5′-monophosphate(AMP)-activated protein kinase (AMPKα2), p22, p47, p67 and p91 were observed by real-time PCR(RT-PCR). Results The experiments showed that hERG gene can be expressed in HepG2 cells. Over-expression ofhERGgene in HepG2 cells could down-regulate the expression of PEPCK, G6Pase. while GLUT2, IRS-2, AMPKα2 genes were up-regulated. Over-expression of hERG gene also inhibited the relative mRNA level of p22, p47, p67and p91. ConclusionhERGchannels could be involved in improving glucose metabolism via anti-oxidative effects.
human ether-α-go-go related gene channels; insulin resistance; oxidative stress; glucose metabolism
國家自然科學基金(81370946, 81400824, 81300726),北京市自然科學基金(7131005),首都醫科大學附屬北京同仁醫院科研基金 (TRYY-KYJJ-2016-013)。This study was supported by National Natural Science Foundation of China (81370946, 81400824, 81300726), Natural Science Foundation of Beijing (7131005) , Foundation of Beijing Tongren Hospital, Capital Medical University (TRYY-KYJJ-2016-013).
時間:2017-04-13 20∶07
http://kns.cnki.net/kcms/detail/11.3662.R.20170413.2007.058.html
10.3969/j.issn.1006-7795.2017.02.003]
R587.1
2017-01-20)
*Corresponding author, E-mail:jinkui.yang@gmail.com

