一種基于CP204L基因的非洲豬瘟病毒Taq Man-MGB實時熒光PCR檢測方法的建立
王建華 , 趙 丹 , 張俊哲 , 董志珍 , 趙祥平 , 王玉玲 , 肖 妍 , 王乃福 , 陳小金 , 陳本龍
(天津出入境檢驗檢疫局動植物與食品檢測中心 , 天津保稅300456)
?
一種基于CP204L基因的非洲豬瘟病毒TaqMan-MGB實時熒光PCR檢測方法的建立
王建華 , 趙 丹 , 張俊哲 , 董志珍 , 趙祥平 , 王玉玲 , 肖 妍 , 王乃福 , 陳小金 , 陳本龍
(天津出入境檢驗檢疫局動植物與食品檢測中心 , 天津保稅300456)
基于非洲豬瘟病毒(ASFV)CP204L基因序列設計1對特異性引物和TaqMan-MGB探針,通過優化反應條件建立了一種檢測ASFV的TaqMan-MGB實時熒光PCR方法。結果顯示,該方法僅對ASFVDNA呈現特異性擴增,不與豬的其他常見病毒發生交叉反應,具有良好的特異性。該方法對標準對照質粒(PCR2.1-CP204L)的線性檢測范圍為4.2×101~4.2×109copies/μL,標準曲線方程為Y=-3.452 3X+39.014,相關系數(R2)為0.998 8,檢測下線為4.2個拷貝。對5個不同濃度(4.2×103~4.2×107copies/μL)的質粒標準品進行4次雙份樣品的重復檢測,Ct值變異系數均小于1.5%,表明該方法具有良好的重現性。用該方法對總計164份的進口豬臨床樣品和生豬肌肉樣品進行ASFV檢測,結果均為陰性。該方法的建立為活豬臨床樣品和生豬肌肉樣品中ASFV檢測提供了一種快速、敏感和特異的技術手段。
非洲豬瘟病毒 ; CP204L序列 ;TaqMan-MGB探針 ; 實時熒光PCR
非洲豬瘟(African swine fever,ASF)是由非洲豬瘟病毒(Africanswinefevervirus,ASFV)引起豬的一種急性、熱性和高度接觸性傳染病,臨床癥狀以高熱、病程短、高死亡率、內臟器官廣泛性出血以及呼吸系統和神經系統功能改變為主要特征。自2009 年以來,本病經格魯吉亞等國傳播到與我國接壤的俄羅斯部分地區并多次暴發[1],目前已對我國養豬業的持續發展構成巨大威脅。對疑似發病豬群中ASFV 快速而準確的檢測,以及對可能攜帶ASFV 的野豬、軟蜱和來自疫區的生豬產品及其制品中ASFV 的監測,是我國防控ASFV傳入的重要措施。為此,本試驗基于ASF VCP204L基因的保守序列設計合成特異性引物與探針,建立了一種檢測ASFV的實時熒光PCR方法,現報告如下。
1 材料與方法
1.1 病毒核酸樣品和陽性對照質粒 非洲豬瘟病毒DNA,由意大利撒丁島動物疫病參考實驗室饋贈,偽狂犬病病毒(PRV)、豬細小病毒(PPV)和豬圓環病毒2型(PCV-2)的DNA,豬瘟病毒(CSFV)、豬繁殖與呼吸綜合征病毒(PRRSV)和豬流行性腹瀉病毒(PEDV)的cDNA,以及用作陽性對照的標準對照質粒(PCR2.1-CP204L),均由天津出入境檢驗檢疫局動植物與食品檢測中心反芻動物檢疫國家重點實驗室保存。
1.2 主要試劑和儀器 組織基因組DNA提取試劑盒,購自天根生化科技有限公司;TaKaRaTaq聚合酶、Premix ExTaqTM(Probe qPCR),購自寶生物工程(大連)有限公司;Light Cycler?480熒光PCR儀(Rochi公司)。
1.3 引物與探針的設計與合成 選取GenBank數據庫(http://www.ncbi.nlm.nih.gov/)下載的ASFV CP204L基因序列保守區域,用BeaconDesigner7.0軟件設計1對特異引物和TaqMan-MGB探針,CP204L-F:5′-GCAGGGCAAGGGTATACTGA-3′,CP204L,-P:5′-CTGTCTCCTCTTCAAACAGCAC-3′,CP204L-P:FAM-5′-CCATTCTTCTTGAGCCTG-3′-MGB,由上海英駿生物技術有限公司合成,5′端用FAM標記,3′端用MGB標記,引物和探針序列見表1,預期擴增片段長度為79 bp。
1.4 熒光PCR反應的優化 以PCR2.1-ASFV-CP204L(4.2×108copies/μL)為擴增模板,采用Premix ExTaqTM(Probe qPCR)試劑及推薦的反應體系及擴增條件,對不同濃度組合的引物(2~10 pmol/μL)和標記探針(1.5~3.5 pmol/μL)以及對56 ℃~61 ℃范圍內的退火延伸溫度,在熒光PCR儀上進行方陣篩選試驗,以確定引物和探針的最適使用濃度和最適擴增條件。
1.5 標準曲線建立、敏感性試驗、重復性試驗和特異性試驗 將已知濃度的PCR2.1-ASFV-CP204L做10倍系列稀釋,按優化的反應條件進行實時熒光定量PCR試驗,以Ct值為橫坐標,以標準對照質粒起始拷貝數濃度的對數為縱坐標建立標準曲線,并確定該方法檢測標準對照質粒最低拷貝數;選取5個濃度(4.2×103~4.2×107copies/μL)的質粒標準品DNA為模板,進行2個平行樣品的4次重復試驗,以確定該方法的可重復性;對ASFV、PRV、PPV和PCV-2的DNA以及CSFV、PRRSV、PEDV和SIV的cDNA進行熒光定量PCR檢測,以確定該方法的特異性。
1.6 實際樣本的檢測 對2012-2014年保存的164頭份進口豬的血清樣品和32份進口豬肉樣品,用組織基因組DNA提取試劑盒按操作說明書提取DNA,采用本試驗建立的熒光定量PCR方法進行ASFV核酸檢測,以評價該方法的適用性。
2 結果
2.1 熒光定量PCR反應的優化結果 通過試驗篩選確定的最適熒光定量PCR擴增條件為:在25μL反應體系中,2×Premix ExTaqTM(Probe qPCR)12.5 μL,CP204L-F(7.5 pmmol/μL)、CP204L-R(7.5 pmmol/μL)和CP204L-P(2.5 pmmol/μL)各μL,樣品DNA適量,補足純水至25 μL。反應參數為95 ℃ 2 min,然后95 ℃ 10 s,56 ℃ 10 s,60 ℃ 20 s,45個循環,在每一次循環的60℃延伸擴增結束前采集FAM通道熒光信號。
2.2 標準品曲線建立和敏感性試驗結果 對10倍系列稀釋的標準對照質粒進行的熒光PCR擴增曲線及建立的標準曲線方程分別見圖1A和圖1B,由圖1A可知該方法最低可檢出4.2拷貝數的標準對照質粒DNA分子。該方法檢測標準對照質粒的線性檢測范圍為4.2×101~4.2×109 copies/μL,標準曲線方程為Y=-3.452 3X+39.014,相關系數(R2)為0.998 8。
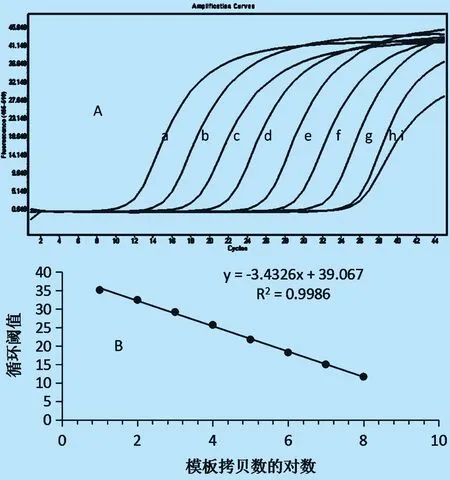
圖1 對照質粒標準品(4.2×100~4.2×109 copies /μL)熒光PCR動力學曲線(A)和標準曲線曲線(B)
a,b,c,d,e,f,g,h,i分別為4.2×109copies、4.2×108copies、4.2×107copies、4.2×106copies、4.2×105copies、4.2×104copies、4.2×103copies、4.2×102copies、4.2×101copies、4.2×100copies對照質粒標準品的擴增曲線
2.3 特異性、重復性和實際樣本檢測結果 用該方法檢測ASFV及相關病毒基因組核酸,僅ASFV的DNA出現典型的擴增曲線,而PRV、PPV和PCV-2的DNA以及CSFV、PRRSV、PEDV和SIV的cDNA>均無擴增曲線出現,表明該方法檢測ASFV核酸有良好的特異性。對5個不同濃度(4.2×103~4.2×107copies/μL)的質粒標準品進行4次雙份樣品的重復檢測,結果見表1,由表1可知Ct值變異系數均小于1.5%,表明該方法具有良好的重現性。對2012-2014年保存的162頭份進口豬血清樣品和32份進口豬肉樣品進行ASFV核酸檢測,結果均為陰性。
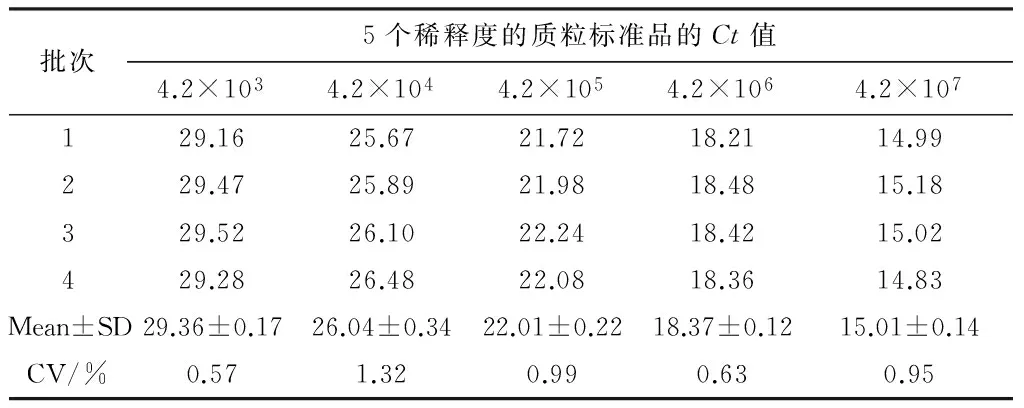
表1 非洲豬瘟病毒P30基因熒光PCR重復性試驗結果
3 討論
熒光PCR方法不僅適用于急性感染早期家豬組織樣本中ASFV檢測,而且更適用于持續性感染的野豬和軟蜱的組織樣本中ASFV檢測。已知ASFV基因組由單分子線狀雙股DNA組成,長度為170~190 kb,含有大量的毒力相關基因和宿主范圍相關基因[2]。國外King等(2003)最早基于VP72基因建立了檢測ASFV核酸的熒光PCR方法[3]國內董志珍(2009)等和郭少平(2010)等分別基于,p54基因和K205R基因建立了檢測ASFV核酸的TaqMan探針熒光PCR方法[4-5]均顯示出很高的敏感性。由于CP204L是ASFV在,感染細胞早期高豐度表達的一種編碼P30蛋白的基因,該蛋白是目前已知的激發感染動物產生抗體和用于ASFV特異抗體檢測的主要蛋白抗原之一[6]。為此,本試驗基于CP204L基因建立了一種TaqMan-MGB探針熒光PCR方法,試驗表明,該方法檢測ASFV核酸不僅特異性強,而且最低可檢測4.2個拷貝的標準陽性對照質粒,為我國預防ASFV的傳入和傳播提供了一種快速而準確的監測手段。
[1] Gogin A,Gerasimov V,Malogolovkin A,etal.African swine fever in the North Caucasus region and the Russian Federation in years 2007-2012[J].Virus Res,2013,173(1):198-203.
[2] Dixon L K,Chapman D A,Netherton C L,etal.African swine fever virus replication and genomics[J].Virus Res,2013,173(1):3-14.
[3] King D P,Reid S M,Hutchings G H,etal.Development of a TaqMan PCR assay with internal amplification control for the detection of African swine fever virus[J].J.Virol.Methods,2003,107:53-61.
[4] 董志珍,侯艷梅,趙祥平,等.非洲豬瘟病毒實時熒光定量PCR檢測方法的建立[J].中國獸醫雜志,2009年,45(9):3-6.
[5] 郭少平,劉建,吳紹強,等.非洲豬瘟病毒實時熒光定量PCR檢測技術的研究與評價[J].中國畜牧獸醫,2010,37(4):76-80.
[6] Prados F J,Vinuela E,Alcami A.Sequence and characterization of the major early phosphoprotein p32 of African swine fever virus[J].J.Virol,1993,67:2475-2485.
Development of aTaqMan-MGB probe real-time PCR assay for detection of african swine fever virus based on CP204L gene
WANG Jian-hua , ZHAO Dan , ZHANG Jun-zhe , DONG Zhi-zhen , ZHAO Xiang-ping ,ANG Yu-ling , XIAO Yan , WANG Nai-fu , CHEN Xiao-jin , CHEN Ben-long
(The Animals and Plants and Food Inspection Center of Tianjin Entry-Exit Inspection and Quarantine,Tianjin 300456,China)
By optimization of reacting conditions,aTaqMan-MGB probe real-time PCR was developed with a pair of specific primers and probe designed according to the conserved regions of the CP204L gene sequences of African swine fever virus(ASFV).The method had high specificity for the ASFV DNA and no cross-reactivity was observed among DNAs and cDNAs of other common swine viruses.The assay showed good linearity between Ct values and copies of the standarde plasmid from 4.2×101to 4.2×109copies/reaction(standard equation Y=-3.4523X+39.014,correlation coefficient R2=0.9988),and the detection limit of the assay was as low as 42 copies of the standarde plasmid.Coefficiency of variation(CV)of Ct values of the standard plasmid tested in duplicate four times ranging from 4.2×103to 4.2×107copies/μL by the assay were less than 1.5%.The164 samples from the imported pigs and porks were detected to be negative by the assay.In conclusion,the method provides a useful tool for the detection of ASFV in the samples from the pigs and porks.
African swine fever virus;CP204L gene ;TaqMan-MGB probe ; real-time quantitative PCR
2015-07-31
天津市科技支撐項目(13ZCZDNCO1300);天津市濱海新區惠民項目(2013-BK15H013)
王建華(1965-),男,高級獸醫師,博士,從事動物疫病檢測與診斷試劑研制工作,E-mail:wjhwqy1965@163.com
S852.65+1
A
0529-6005(2016)10-0023-03

