一起綿羊偽狂犬病的發生及病毒gE基因的序列變異分析
張振東,王廣文,胡東方,牛玉娟,張民霞,呂傳位,呂 林,張清林,肖一紅,劉思當
(1.山東農業大學動物科技學院,山東 泰安 271000;2.泰山職業技術學院生物系,山東 泰安 271000)
一起綿羊偽狂犬病的發生及病毒gE基因的序列變異分析
張振東1,王廣文1,胡東方1,牛玉娟1,張民霞1,呂傳位1,呂林1,張清林2,肖一紅1,劉思當1
(1.山東農業大學動物科技學院,山東 泰安 271000;2.泰山職業技術學院生物系,山東 泰安 271000)
為了確診一起綿羊偽狂犬病的發生,采集送檢病羊的皮膚、脾臟、淋巴結、腦等組織器官進行實驗室病毒分離和PCR檢測。結果顯示,病料中擴增出了偽狂犬病病毒的特異性gE基因片段。結合流行病學調查、病理剖檢和實驗室診斷,確定引起此次疫情的病原為偽狂犬病病毒。為了進一步了解此次疫情中PRV gE基因的分子特征,特對PCR擴增產物進行了連接、轉化和測序分析。遺傳進化分析表明,該分離株與亞洲各分離株處于同一分支,基因同源性高達98.4%-99.4%,與歐洲、美洲分離株同源性相對較遠,分別為97.0%-97.2%、97.2%-97.3%;gE蛋白氨基酸序列分析顯示,該分離株在gE蛋白的第48位和第492位各存在1個天冬氨酸的插入,與我國當前流行的偽狂犬變異株相同,同時在當前豬偽狂犬病病毒變異株基礎上又出現了新氨基酸位點的變異,如L49P、P160T、V406G、G445R,其分子生物學特性有待進一步的研究。本文通過綜合診斷確定該病由偽狂犬病病毒引起,為我國綿羊偽狂犬病的流行病學分析及防控提供了重要的理論依據。
綿羊偽狂犬病;濟寧;gE;分離鑒定;遺傳變異
偽狂犬病(Pseudorabies,PR)是由偽狂犬病病毒(PRV)引起的一種急性熱性傳染病,病毒主要侵害家畜以及各種野生哺乳動物的神經系統,患病動物主要表現為發熱、奇癢(豬除外)和腦脊髓炎等癥狀。該病于1813年于美國牛群首次被發現,我國在1948年首次報道該病[1]。近年來,伴隨著豬偽狂犬病的流行及肉羊養殖規模的擴大,PR在羊群中的發病情況日益嚴重,特別是發病豬場周圍的羊群時有發病死亡的情況,起初多為零星散發,往往得不到足夠地重視,以致后來造成羊群大面積發病,造成較大的經濟損失。2014年2月18日,山東濟寧地區某綿羊場發生偽狂犬病疑似病例,前來就診,經流行病學調查、癥狀觀察、病理剖檢及實驗室綜合診斷,最終確診為羊偽狂犬病。隨后及時采取了綜合防控措施,使疫情得到了及時有效的控制,避免了更大的經濟損失。
1 背景調查
該養殖場存養綿羊220只,近兩年來羊場無較大疫情發生。但于2014年2月15日下午突然出現2只病羊,表現為精神沉郁,離群站立,體溫升高至41℃以上,呼吸加快,食欲減退,不食,未引起畜主的注意,但未采取任何防控措施。2月16日早上,2只病羊均已死亡,發現鼻端、唇部發生水腫,口腔有泡沫樣唾液,皮膚存在擦傷,體側部被毛脫落。畜主將病死羊掩埋處理后,用20%石灰水對羊舍進行噴灑消毒。2月18日上午,羊群又突然出現死羊1只,病羊2只,病羊表現不安、站立不穩、偏向一側、倒地橫臥,經常啃咬發癢部位,皮膚破潰出血。畜主將病羊隔離治療,注射安痛定、頭孢噻呋鈉等藥物,但病羊在當天先后死亡。并且羊群中陸續出現病羊,故帶病羊前來就診。
畜主介紹:羊場已經營3年,從未出現過類似病情,現今羊群發病率已超過30%,死亡率幾乎100%。該羊場周邊豬場較多且養豬密度大,附近豬場近段時間內母豬群繁殖障礙的比例較高,母豬流產及產死胎現象嚴重。
2 病理剖檢
在做好人員防護措施的情況下對畜主送檢的兩只病羊進行了剖檢。剖檢發現,兩只病羊的各內臟器官僅見輕微眼觀病變,臉部皮下水腫有膠胨樣物質沉積,腹部皮膚有擦傷、充血、出血,氣管內有泡沫性黏液,肺臟水腫、充血,腦膜充血、水腫。
3 實驗室診斷
3.1病毒分離采集皮膚、肝、脾及淋巴結等組織器官,按常規方法勻漿,反復凍融3次,12 000 r/min離心30 min,將上清液經0.22 μm濾器過濾后接種于鋪滿單層的Vero細胞,置于37℃、5% CO2的培養箱中培養。每天觀察有無細胞病變,將培養96 h的細胞瓶取出,經-20℃冰箱反復凍融3次后,收獲Vero細胞及上清,于-80℃凍存備用。
3.2PCR檢測根據GenBank上公布的參考序列設計綿羊PRV gE基因的特異性擴增引物,擴增片段為2 060 bp,引物由上海生工生物工程技術服務有限公司合成。用北京全式金生物技術有限公司DNA/RNA Kit試劑盒提取細胞上清液偽狂犬病病毒DNA,取3 μL作為模板,反應體系為TaKaRa Taq 0.2 μL,2×GC Buffer 10 μL,2.5 mmol/mL dNTPs 2 μL,上游引物1 μL,下游引物1 μL,加Nucleasefree water至25 μL,混勻;擴增程序為95℃預變性5 min,95℃變性1 min,68℃退火1 min,72℃延伸2 min,35個循環,72℃延伸7 min,4℃保溫。
4 結果
根據發病情況、臨床癥狀、剖檢變化以及實驗室診斷,最終確定導致該場綿羊發病的病原為偽狂犬病病毒,可能由周邊豬場豬源偽狂犬病病毒傳播而來。通過及時采取撲殺消毒、緊急免疫、防止繼發感染等綜合措施[2-3],疫情得到了有效控制,避免了更大的經濟損失。
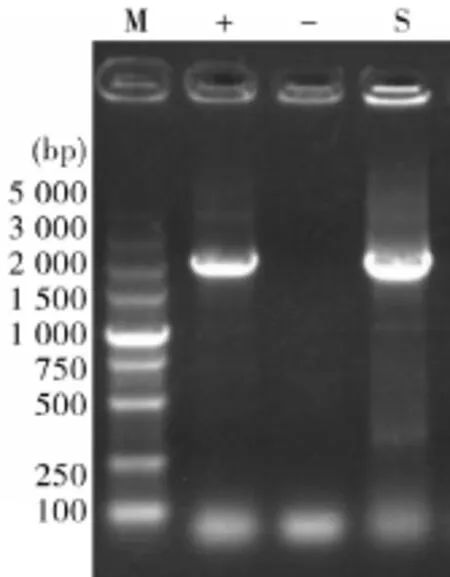
圖1 細胞上清液PRV gE擴增產物瓊脂糖凝膠電泳結果
5 序列分析
為了更深入地了解引起此次疫情的PRV的分子特征,特對PCR擴增出的gE基因目的片段進行了連接、轉化和測序。
5.1PRV gE基因遺傳進化分析對該綿羊偽狂犬病分離株序列分析表明,gE基因全長為1 740 bp(去除PCR擴增產物兩端的多余序列),編碼580個氨基酸。其與亞洲各分離株處于同一分支,基因同源性高達98.4%~99.4%,而與歐洲、美洲分離株同源性相對較遠,分別為97.0~97.2%、97.2~97.3%(圖2)。
5.2gE基因氨基酸位點差異分析氨基酸差異位點分析,該綿羊偽狂犬病病毒分離株與亞洲豬源偽狂犬病病毒分離株基本上完全一致,在氨基酸位點的48位和496~497位上分別出現了一個天冬氨酸(D)的插入(表1,2),另外,還出現了新的氨基酸變異點,如L49P,P160T,V406G,G445R。
6 討論
有關羊偽狂犬病的病例以前鮮有報道,但最近12年內該病的發病率明顯提高[3],張克山、張文花等專家學者對此病例也進行了報道分析[4-5]。近年來,豬偽狂犬病暴發流行,童光志等已發現偽狂犬病病毒全基因組和編碼蛋白的氨基酸序列發生了明顯變異[6],趙鴻遠等[7]的研究也表明,2012后我國流行的偽狂犬病病毒以變異株為主,變異株之間具有相同的分子特征,即在gE蛋白的第48位和第492位各有1個天冬氨酸的插入。該綿羊偽狂犬病病毒分離株在gE蛋白相應位點也存在同樣的插入,說明此次在綿羊偽狂犬病疫情是由偽狂犬病變異株引起的,基因同源性高達98.4%~99.4%。該羊場周邊豬場較多,豬場較為密集,且豬場近段時間內母豬產死胎及弱胎的現象嚴重,這些都進一步地證明該偽狂犬病病毒分離株極有可能是由豬傳染給了綿羊。
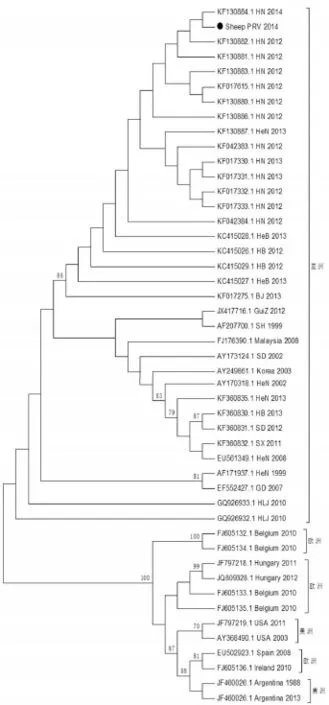
圖2 gE基因氨基酸序列遺傳進化分析

表1 該綿羊分離株與世界各國豬源偽狂犬病病毒gE氨基酸位點差異分析
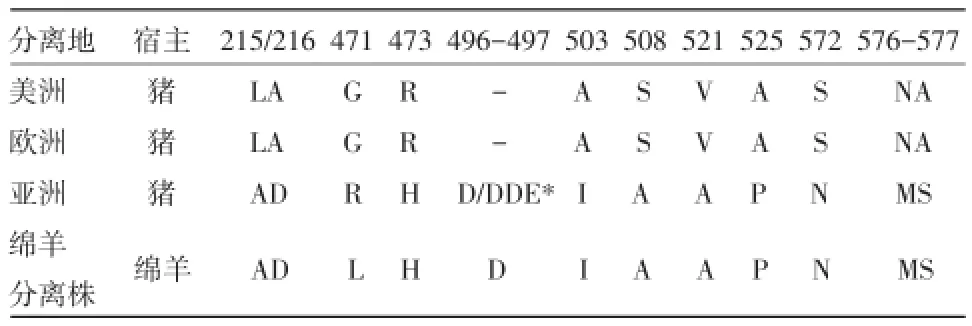
表2 該綿羊分離株與世界各國豬源偽狂犬病病毒gE氨基酸位點差異分析
我國規模化養豬場均使用Bratha-k61疫苗來免疫偽狂犬病,長期以來起到了良好的預防效果[8-9]。對于該病多發區疫苗免疫仍是防控羊偽狂犬病最為有效的方法,同時也建議羊場采取以下防控措施:第一:興建羊場時,盡量遠離豬場、牛場;第二:控制傳染源,嚴禁從患偽狂犬病的地區引進羔羊及種羊,加強對精液的管理;第三:加強飼養管理,提倡自繁自養,引種時嚴格檢疫,提高羊群對該病的抵抗力;第四:加大羊場的衛生消毒力度、做好滅鼠工作,切斷該病在易感動物間的傳播。
另外,對gE蛋白氨基酸差異位點分析,該綿羊分離株與亞洲豬源偽狂犬病病毒變異株幾乎完全一致,但又出現了新的氨基酸變異點:L49P,P160T,V406G,G445R。由于GenBank上沒有羊源偽狂犬病的gE基因序列,這些氨基酸位點的變異是否與病毒的宿主特性、毒力等相關,有待進一步的研究。
[1]衛廣森.獸醫全攻略-羊病學[M].北京:中國農業出版社,2002:116-119.
[2]趙云俠,付艷紅,郭百超.綿羊偽狂犬病的診治[J].當代畜牧,2013,03:27.
[3]李峰,張文通,王玉茂,等.波爾山羊羔羊偽狂犬病的診治[J].黑龍江畜牧獸醫,2013,08:96-97.
[4]張克山,劉永杰,孔漢金,等.綿羊偽狂犬病病毒的鑒定及序列分析[J].中國獸醫科學,2013,03:221-224.
[5]張文花,和國忠,和仕良,等.高海拔地區綿羊及牧羊犬偽狂犬病的防制[J].云南畜牧獸醫,2011,02:19.
[6]金寧一,錢軍,陳溥言.中國畜牧獸醫學會動物傳染病學分會[C].徐州:2013:427-428.
[7]趙鴻遠,彭金美,安同慶,等.豬偽狂犬病病毒變異株的分離鑒定及其gE基因的分子特征[J].中國預防獸醫學報,2014,36(7):506-509.
[8]袁慶志,吳裕祥,李亞香,等.偽狂犬病免疫的研究-偽狂犬病弱毒疫苗的研究[J].家畜傳染病,1983,5(1):1-6.
[9]楊慶芳,寧官保.豬偽狂犬病的研究進展[J].畜牧獸醫科技信息,2010,7:15-18.
TheOccurrenceof Sheep Pseudorabies and Variation Analysis of theGlycoprotein E Geneof theVirus
ZHANG Zhen-dong1,WANG Guang-wen1,HU Dong-fang1,NIU Yu-juan1,ZHANG Min-xia1,LV Chuan-wei1,LV Lin1,ZHANG Qing-lin2,XIAO Yi-hong1,LIU Si-dang1
(1.Animal Science and Technology of Shandong Agricultural University,Tai’an 271000,China;2.Biology Department of Taishan Polytechnic,Tai’an 271000,China)
To diagnose a suspected sheep pseudorabies case,pathologic autopsy was performed and tissues of the sheep were collected for virus isolation and identification using PCR.PRV was amplified from the tissues and its infection was confirmed.In order to further understand the molecule characteristic of the gE gene,the 1740-bp DNA fragment of gE gene was amplified,cloned and sequenced.Phylogenetic analysis showed that the sheep PRV isolate shared 98.4%to 99.4%sequence identity with all kinds of isolates from Asia,and shared 97.0%to 97.2%and 97.2%to 97.3%sequence identity with Europe and American isolates,respectively.The alignment results revealed that the isolate had the same sequence features with two insertions of Asp at sites of 48 and 492 comparing with the PRVs isolated from the modern prevalent mutations.Besides,four new amino acid sites emerged,and they were L49P,P160T,V406G and G445R compared with the prevalent mutated strains of swine PR.This study provides an useful information for the molecular epidemiology,prevention and control of sheep PRV in China.
sheep pseudorabies virus;Jining;gE;isolation and identification;sequence variation
LIU Si-dang
S852.65+5
A
0529-6005(2016)04-0046-03
2014-12-19
山東省牛產業技術體系資助(SDAIT-12-011-04)
張振東(1990-),男,執業獸醫師,碩士,主要從事動物臨床病理學研究,E-mail:zhangzhend90@126.com
王廣文(1989-),男,執業獸醫師,碩士,主要從事動物臨床病理學研究,E-mail:1126255119@qq.com
注:王廣文與李振東對本文具有同等貢獻
劉思當,E-mail:liusid@sdau.edu.cn

