例談分離和提純有機物的常用方法
◇ 江蘇 丁海嶸
?
例談分離和提純有機物的常用方法
◇江蘇丁海嶸
從高考的內容和形式上看,物質的分離和提純主要有3個特點:1)選取適當試劑及分離方法,除去混合物中的指定雜質; 2)確定除去混合物中指定的雜質所需加入試劑的先后順序; 3)將分離提純與物質制備、混合物成分的確定等內容融為一體,形成綜合實驗題.對有機物的分離和提純由于物質性質的特殊性,故有不同于無機物的特點,現例析歸納如下.

A通人足量的溴水;
B與高錳酸鉀溶液反應;
C點燃;
D在催化劑存在的條件下與氫氣反應


洗氣是用洗液除去氣體中的雜質,在實驗室,通常是使氣體通過盛有特定洗液的洗氣瓶,雜質氣體被洗液吸收,從而得到純凈的氣體.用洗氣瓶洗氣時要注意“長進短出”.
沸點相差較大的液態混合物常用蒸餾的方法分離.如從原油中分離出各種石油產品,若沸點相差不大,可加特定試劑使之轉化成沸點較大的物質,然后蒸餾.如分離乙醇和醋酸的混合物可先加氫氧化鈉溶液蒸餾,分離出乙醇,再在蒸餾燒瓶中加濃硫酸蒸餾出乙酸.需要注意的是,對于受熱易氧化的物質的分離,不要用蒸餾法,如苯酚的提純.

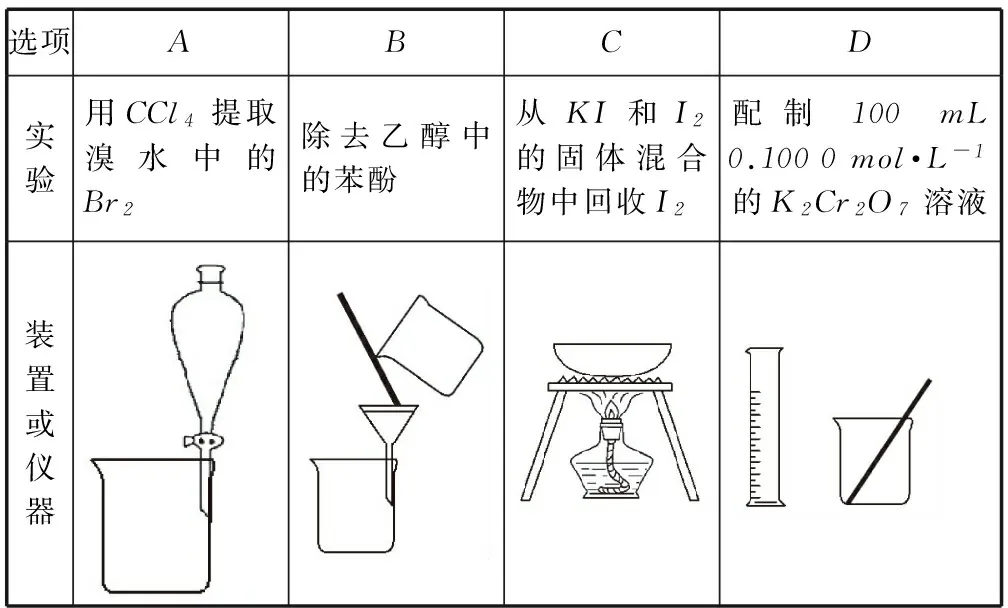
選項ABCD實驗用CCl4提取溴水中的Br2除去乙醇中的苯酚從KI和I2的固體混合物中回收I2配制100mL0.1000mol·L-1的K2Cr2O7溶液裝置或儀器


選項具體分析結論ACCl4提取了Br2后和水分層,利用分液漏斗分液可以分開二者正確B乙醇和苯酚都為有機物,互溶且二者都是液體,不能用過濾的方法分離錯誤C加熱時碘升華從碘化鉀中分離,應回收升華的碘錯誤D儀器還需要100mL的容量瓶錯誤

萃取是指用一種溶劑把溶質從另一種溶劑中提取出來的過程.用來提取溶劑的物質叫萃取劑.能做萃取劑的物質必須與原溶劑互不相溶,與原溶液不反應,且溶質在萃取劑中溶解度遠大于在原溶劑中的溶解度.如用直餾汽油可從溴水中萃取溴,不能用工業汽油或酒精從溴水中萃取溴,因為工業汽油中含烯烴,能與溴發生加成反應.用水做萃取劑,可以除去某些有機物中易溶于水的雜質.如烷烴與氯氣發生光照反應后的產物,用水洗可以得到副產品鹽酸.萃取和分液實驗常常結合在一起做,萃取過程在分液漏斗中實現.

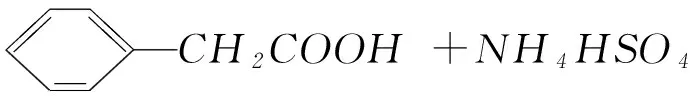
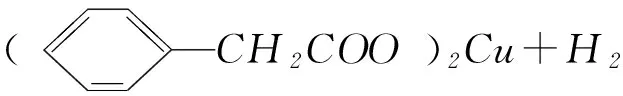
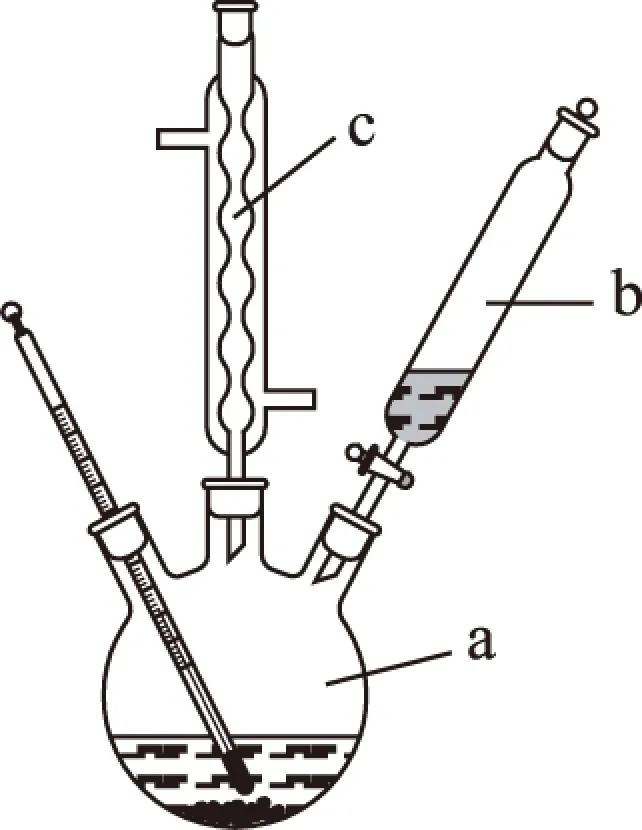
圖1
制備苯乙酸的裝置示意圖如圖1(加熱和夾持裝置等略). 已知:苯乙酸的熔點為76.5℃,微溶于冷水,溶于乙醇.
回答下列問題:
(1) 在250mL三口瓶a中加入70mL質量分數為70%的硫酸.將a中的溶液加熱至100 ℃,緩緩滴加40g苯乙腈到硫酸溶液中,然后升溫至130 ℃繼續反應.在裝置中,儀器b的作用是______;儀器c的名稱是______,其作用是________.反應結束后加適量冷水再分離出苯乙酸粗品.加入冷水的目的是________.下列儀器中可用于分離苯乙酸粗品的是________(填標號).
A分液漏斗;B漏斗;C燒杯;
D直形冷凝管;E玻璃棒
(2) 提純粗苯乙酸的方法是________,最終得到44g純品,則苯乙酸的產率是________.
(3) 將苯乙酸加入到乙醇與水的混合溶劑中,充分溶解后加入Cu(OH)2攪拌30min,過濾,濾液靜置一段時間析出苯乙酸銅晶體,混合溶劑中乙醇的作用是________.

(2) 根據苯乙酸的性質知提純的方法是重結晶.

(3) 苯乙酸在水中的溶解度小,在乙醇中大,而乙醇與水互溶,因此乙醇的作用是增大苯乙酸的溶解度,便于充分反應.

分離提純物質的方法還有很多,如結晶、重結晶、蒸發(餾)、滲析、鹽析、加熱、沉淀、氧化還原法等,只是有些不一定適合有機物的分離.
江蘇省無錫市第六高級中學)

