化學主觀題特點、分類及理答策略研究
趙銘 趙宇宣
摘要:化學主觀題在高考中比例呈現升高的態勢,隨著智能閱卷手段的日趨完善,為主觀題評閱的效度、信度和區分度提升提供有力支撐。化學主觀題從應答方式看主要有三種,從表征形式看主要有五種。主觀題的理答一般分為四個步驟:清晰目標指向、掌握轉化策略、學會調用技巧、熟練規范表述。這四個步驟并不是相互獨立的,在處理問題的過程中可以整合使用。
關鍵詞:化學主觀題;呈現方式;分類;理答策略;智能答卷
文章編號:1005–6629(2016)9–0081–05 中圖分類號:G633.8 文獻標識碼:B
隨著課程改革的深入,化學試題呈現方式正在悄然發生變革。主觀性試題的分值比例較大,以高考為例,理科綜合卷中的主觀題比例為62%,江蘇卷等單科卷主觀題比例為67%,今后有進一步增大主觀題在總分中比例的可能。因此,研究化學試題解題邏輯,尤其是怎樣將“試題語言轉化為問題語言”顯得尤為重要,因為,解決主觀題更需要一種科學嚴謹的邏輯體系來支撐。
1 主觀題的特點
主觀題(Constructed Response Item,簡稱為CR)指的是考生需要組織文字、數字、圖形等材料回答某個問題,而不是從命題者提供的若干備選答案中選擇一個或多個選項的一類開放式題型[1]。常見類型包括填空、簡答、論述、計算與推演、實驗等。從教育測量學角度看,主觀題的優點主要有三點:一是方便考查考生綜合應用能力;二是方便考查考生一些深層次的思維品質,如發散思維、創造性思維等;三是能彌補紙筆測試不足,適當滿足實踐類試題通過紙筆達成一定測量目標。眾多專家學者比較青睞主觀題對學生深度認知和思維品質考查的優勢。主觀題的缺點也比較明顯,一是隨機誤差大,評分者信度低;二是系統誤差大,內容效度低;三是趨中現象明顯,區分度低;四是命題組卷、閱卷組織等困難。因而,當前仍然保留一定比例的客觀題(選擇題等)是一種調和的做法。
隨著主觀題自動閱卷技術的實現,在不遠的將來,計算機自動評判系統日益完善,效度、信度和區分度的日益增強,主觀題比例增加甚至全覆蓋將成為趨勢。主觀題自動閱卷技術主要是模擬教師閱卷的思維,先找到考生答案中的關鍵詞(得分點),再根據語序等進行相似度匹配,最終由計算機給出考生得分[2]。自動閱卷的主要難點表現在主觀題的自動閱卷上,只有不斷完善現有的手寫識別技術、分詞技術、語義技術、智能技術等相關支持技術,才有可能在未來實現大規模的智能閱卷。
2 化學主觀題的呈現方式
化學主觀題的呈現方式按照應答方式,主要分為填空、簡答和計算等;按照學科理答所調用的知識和技能的表征形式,主要分為五種:化學用語表述、化學原理表述、實驗現象和實驗步驟表述、計算推理表述和融合式表述(兼有以上三種方式中的1~2種)。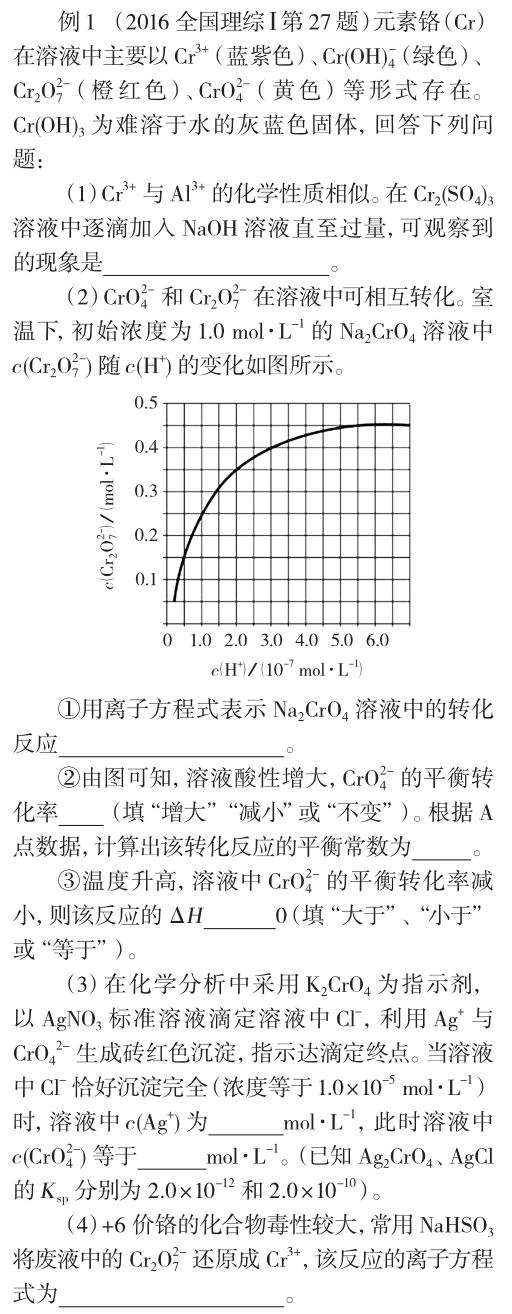
第(1)問屬于實驗現象表述,第(2)①和第(4)屬于化學用語表述,第(2)②③屬于化學原理表述,第(3)屬于計算推理表述。問題(1)要簡單調用試題信息,問題(2)①和第(4)書寫離子方程式要調用圖像信息和氧化還原反應知識,第(2)②需要調用化學平衡移動基本原理,問題(3)則要應用Ksp的計算規則,并具備代數中簡單的指數運算能力。
3 化學主觀題的理答
主觀題的理答一般分為四個步驟:清晰目標指向、掌握轉化策略、學會調用技巧、熟練規范表述。這四個步驟并不是相互獨立的,在處理問題的過程中可以整合使用。
3.1 目標指向:明析命題者考查的學科本質
專業性很強的主觀題命題者常常會站在被測試方的立場思考問題,因此,拿到主觀性試題,要有命題者的邏輯,清晰命題者的學科考查指向就顯得非常重要。以例1為例,命題者的考查邏輯應該非常明顯:提供陌生信息→簡單應用信息(復述現象)→深度結合信息(寫方程式)→調用舊知解決問題→定性走向定量(高級思維)→生產生活應用(廢液處理)。借用“鉻”這種陌生元素與化合物情境,達成考查實驗現象表述、化學原理應用和解決實際問題的目標。從本質上看,被測試者具備較為扎實的化學平衡移動原理、氧化還原反應原理和沉淀溶解平衡溶度積計算方法就能夠解決問題。
3.2 轉化策略:試題語言轉化為問題語言
將命題者的試題語言轉化為問題語言,是解決主觀題的最核心的環節。一般處理方法有以下兩種。一是轉化為具體的學科問題。
命題者要求考生回答相關措施的目的,首先我們要進行第一次轉化:過量的Ca(OH)2的目的,再進行第二次轉化:過量的Ca(OH)2作為反應物,將影響什么物質?接著,進行第三次轉化:另一種反應物是H2O2,Ca(OH)2作為反應物對它的影響是什么?最后調用化學平衡相關原理:增加一種反應物濃度(量)可以提高另一種反應物的轉化率。最后,轉化為規范表達:提高H2O2的利用率。當然,還可以進一步追問:為什么要提高H2O2的利用率?H2O2不穩定易分解,價格相對Ca(OH)2要高,這也是要提高其利用率的原因。
轉化為學科問題,就是要在大腦的知識結構中迅速搜尋相關匹配的知識和原理,要建立起一種有價值的聯系,要學會進行有效轉化,并適當去除非學科關聯。
例3 (2016年江蘇卷第20題)鐵炭混合物(鐵屑和活性炭的混合物)、納米鐵粉均可用于處理水中污染物。(2)在相同條件下,測量總質量相同、鐵的質量分數不同的鐵炭混合物對水中Cu2+和Pb2+的去除率,結果如圖所示。①當鐵炭混合物中鐵的質量分數為0時,也能去除水中少量的Cu2+和Pb2+,其原因是 。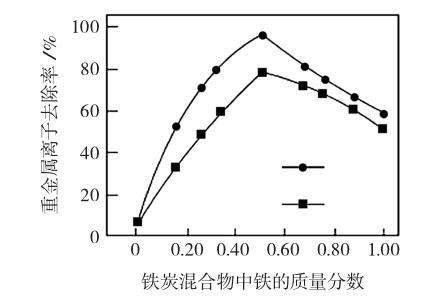
本題可進行如下轉化:鐵的質量分數為0時,Cu2+和Pb2+也能除去的原因→只有活性炭,Cu2+和Pb2+也能除去的原因→活性炭能夠吸收Cu2+和Pb2+的原因→活性炭的性質中哪一點能夠吸收有色離子→活性炭的吸附性。
二是轉化為具體的達成措施。將試題語言轉化為可以實施的具體目標、具體操作和具體步驟,也是常見主觀題的轉化策略,尤其在實驗類試題中經常使用。
例4 (2016年上海化學卷第39題)堿液吸收法是脫除二氧化碳的方法之一。已知: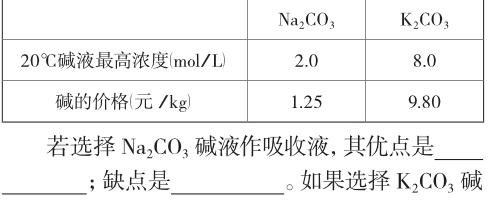

分析表格中數據,并結合命題者的問題進行轉化:Na2CO3堿液作吸收液優點顯然是成本,缺點是濃度,轉化為化學語言,就是吸收效率低。對于后一個問題,轉化為具體的達成目標:選擇K2CO3堿液作吸收液,用什么方法可以降低成本→降低成本的方法是節約用量和提高利用率;循環利用→節約用量顯然不可行,在吸收CO2的能力上,兩者一致;在提高利用率上,K2CO3濃度大,本身“抓”CO2的能力強→循環利用K2CO3→K2CO3被轉化成什么物質(KHCO3)?循環利用的原理是什么(熱分解)?耗用的資源是否有價值?
例5 (2015年江蘇化學卷第19題)實驗室用圖示裝置制備KClO溶液,并通過KClO溶液與Fe(NO3)3溶液的反應制備高效水處理劑K2FeO4。已知K2FeO4具有下列性質:①可溶于水、微溶于濃KOH溶液 ②在0~5℃、強堿性溶液中比較穩定 ③在Fe3+和Fe(OH)3催化作用下發生分解 ④在酸性至弱堿性條件下,能與水反應生成Fe(OH)3和O2。
轉化為化學措施必須要有合理的原理支撐。本題中進行了有效的“控制手段”(俗稱“堵漏”)。首先,命題者的考查意圖非常明確:實驗措施,一定是具體的操作策略。因此,如何轉化為化學問題,再轉化為可以實施的實驗操作顯得非常重要。筆者設計如下轉化流程(如圖1)。
本題的兩個措施:一是緩慢滴加濃鹽酸,二是裝置C冰水浴。對于“緩慢通入氯氣”這個答案,命題者以為不能算標準答案,可能與這個答案是“最終效果”而不是“具體操作措施”有關。也就是說,命題者需要的是考生回答具體的實驗操作。
在具體的轉化過程中,有時需要用到多角度分析和逆向分析法方法。如:某步操作要控制在60~70℃的原因,就可以轉化為:高于70℃的不利因素,低于60℃的不利因素。一般說來,溫度偏高,某些不穩定的物質可能分解、個別物質溶解度反常可能有晶體析出或發生某些副反應等。
3.3 調用技巧:運用合理的篩選方法
在對已有化學知識調用的過程中,常常涉及到合理篩選、排查推測的策略應用問題,如果片面地理解,就有可能“答非所問”,甚至“南轅北轍”。


試題中,增加O3的物質的量,O3氧化SO2的反應幾乎不受影響,在圖中表現出SO2的物質的量始終維持在150mol這個水平。因此,必然能調用SO2與O3反應的相關熱力學參數,也就是熱力學角度(看是否有發生的可能);同時,還需要分析此時反應的速率(動力學角度)。本題中并未提供相關的反應速率圖表,因此,考生必須進行理性分析。題目中所給的ΔH<0,ΔS數值沒有提供,但是反應中可以看出,前后變化不大,這個因素可以忽略,因而,反應的自發傾向還是明顯的(ΔG<0)。很多考生在分析到此處時,覺得“不可思議”,因而就“胡亂”地寫下“O3與SO2很難反應”這個結論,而沒有經過縝密的篩選、合理的推導。此題的解決邏輯可以繪制成以下流程(如圖2)。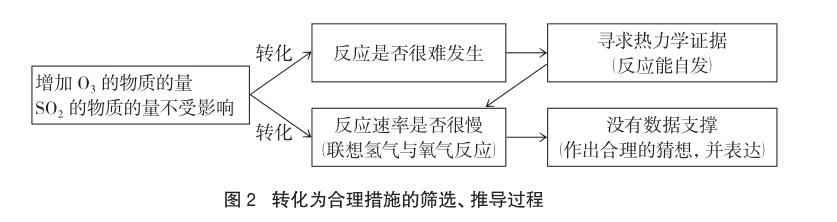
3.4 規范表述:專業精準的學科語言
在實驗試題中,有一類是步驟表述題,這種試題的得分率較低,主要原因有2個方面:一是實驗思維混亂,導致不能實現有關制備或者提純;二是缺乏專業精準的學科語言表達。在進行此類試題的解答中,一般可以分三個步驟:首先是將實驗問題轉化為實驗操作的程序,接著進行基礎表述,最后再進行精當的加工、修飾。
例7 (2015年江蘇卷第19題)題干見案例5。
(4)提純K2FeO4粗產品[含有Fe(OH)3、KCl等雜質]的實驗方案為:將一定量的K2FeO4粗產品溶于冷的3 mol·L-1 KOH溶液中, (實驗中須使用的試劑有:飽和KOH溶液、乙醇;除常用儀器外須使用的儀器有:砂芯漏斗、真空干燥箱)。
這道實驗步驟類試題從分類上看屬于除雜、提純問題,且含有兩種不同性質的雜質(溶解度差異),因此,首先是要轉化為實驗思維程序(如圖3)。
在此基礎上再進行插入操作、完善細節的步驟(如圖4)。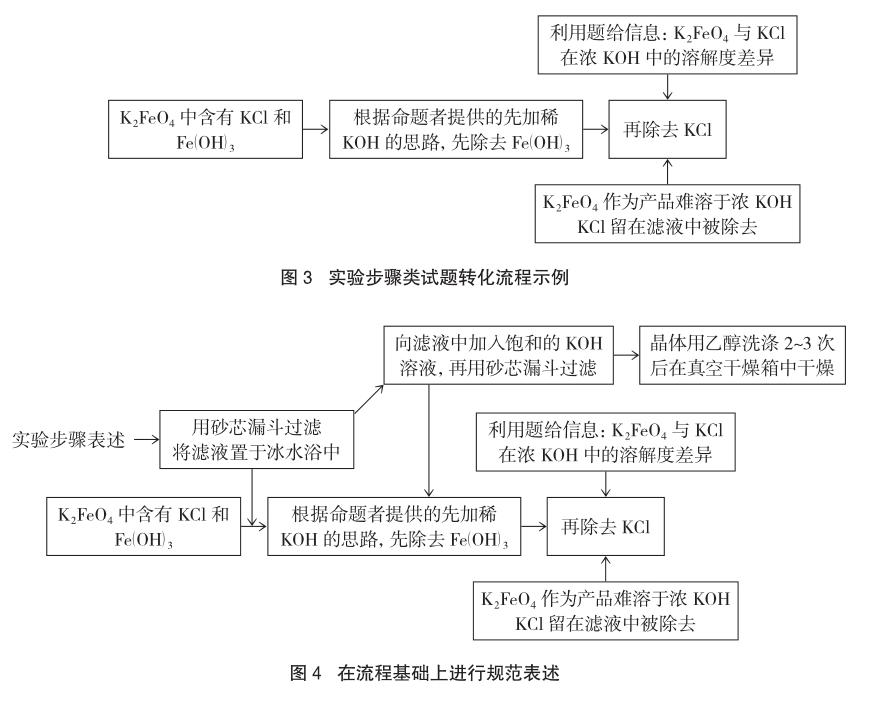
在進行實驗步驟專業表述時,一般有三類,一是物質轉化類操作,要注意試劑取用方法、取用量、混合方法(邊加邊攪拌等)、添加順序,如:量取還是稱取;足量、少量、適量、1~2滴等;混合過程中是迅速傾倒還是緩慢滴加,是否需要振蕩、攪拌、搖動等;轉化的條件也要注意,加酸或者加堿控制pH范圍、加熱或水浴加熱或在HCl氛圍中加熱等。二是物質分離提純類操作,蒸發濃縮后降溫結晶或者蒸發濃縮后趁熱過濾、過濾后的濾液檢驗、洗滌的方式、干燥的環境、萃取的萃取劑選擇、分液后的上下方溶液種類等。三是含量測定類實驗,要注意指示劑的選擇和終點的判斷,連續碘量法的測定還要注意pH的控制,雙指示劑的滴定要注意指示劑的選擇和變色情況等。
化學主觀題作為一種考查學生學科思維品質非常有益的試題,能夠培養學生對綜合問題的解決策略,而訓練學生解決這種試題的策略,這本身也是一種思維訓練。在這個過程中,學生思維的深刻性、批判性、邏輯性和創造性都得到了提升。
參考文獻:
[1]楊志明.考試中大量使用主觀題的利與弊[J].教育測量與評價,2016,(4):4.
[2]肖明,王興蘭.主觀題自動閱卷研究進展[J].中國考試,2010,(7):30.

