陽極溶出伏安法同時測定高鹽調味品中鉛鎘
彭 靜,賀與平
(1.昆明理工大學材料科學與工程學院,云南昆明 650093;2.昆明理工大學分析測試研究中心,云南昆明 650093)
?
陽極溶出伏安法同時測定高鹽調味品中鉛鎘
彭靜1,賀與平2,*
(1.昆明理工大學材料科學與工程學院,云南昆明 650093;2.昆明理工大學分析測試研究中心,云南昆明 650093)
采用濕法消解結合陽極溶出伏安法對沾水辣、醬油和魚露等高鹽調味品中鉛鎘的測定進行了方法研究。探索了儀器條件、電解質及其用量、高鹽對鉛鎘的影響,并對酸類型及酸度的干擾、共存離子干擾進行了實驗。鉛、鎘工作曲線的線性范圍分別為2~50、1~20 μg·L-1,相關系數分別為0.9999和1.0000,儀器檢出限為鉛0.043 μg·L-1、鎘 0.029 μg·L-1,方法檢出限為鉛2.17 μg·kg-1、鎘1.43 μg·kg-1。該方法測定實際樣品中鉛、鎘含量的精密度分別為1.11%~4.66%、0.69%~5.34%,加標回收率分別為93.9%~109.9%、94.7%~107.5%。結果表明方法簡便、靈敏,具有較好的選擇性和可靠性。
濕法消解,溶出伏安法,調味品,鉛,鎘
鉛和鎘為具有蓄積性、對人體有毒有害的重金屬元素,通過食物鏈進入人體,可在人體中蓄積,造成危害[1-2]。目前,各國對食品中的鉛鎘做了嚴格限量規定,我國食品衛生標準規定:調味品(食用鹽和香辛料類除外)中鉛含量≤1.0 mg/kg,鎘含量≤0.1 mg/kg;食用鹽中鉛含量≤2.0 mg/kg,鎘含量≤0.5 mg/kg;香辛料類中鉛含量≤3.0 mg/kg。
目前在含高鹽食品的鉛鎘測定中,因基體干擾較復雜,測定難度較大。國家標準規定食品中鎘含量測定方法主要有石墨爐原子吸收光譜法(GF-AAS)[3];鉛含量測定方法除了GF-AAS,還有萃取火焰原子吸收光譜法(F-AAS)、氫化物原子熒光光譜法(HG-AFS)和二硫腙比色法等[4]。GF-AAS測定含高鹽樣品中的鉛鎘,背景吸收干擾嚴重,需加合適的基體改進劑并仔細優化升溫程序,比較耗時;F-AAS要經過復雜的萃取過程,易產生實驗誤差且靈敏度低[5];二硫腙比色法使用試劑多,操作繁瑣,靈敏度低;HG-AFS靈敏度雖高,但對酸度控制有嚴格要求。測定食品中鉛和鎘還有采用電感耦合等離子體質譜法(ICP-MS)和電感耦合等離子體發射光譜法(ICP-AES)[6-9]。ICP-AES靈敏度低于陽極溶出伏安法,ICP-MS雖然具有極高的靈敏度與較寬的線性范圍,但它在測定高鹽食品時易出現積鹽現象,從而使靈敏度降低。
陽極溶出伏安法是常用的痕量元素檢測方法之一[10-12],它常用于電解液[13-14]和中藥[15-17]中的痕量重金屬元素測定。已有陽極溶出伏安法用于蔬菜中鉛鎘測定[18-19]和食鹽中鉛元素兩種方法對比測定的報道[20],但尚未見用于同時測定高鹽調味品中鉛鎘的報道。陽極溶出伏安法需要依靠鹽分環境作為電解質從而產生電流,避免了其他儀器分析方法在高鹽環境下基體干擾嚴重的問題,鉛鎘的峰電位接近,但能很好分開,互不干擾,適合在陽極溶出伏安法中同時測定。本文研究了采用濕法消解結合陽極溶出伏安法對沾水辣、醬油和魚露等高鹽固液態調味品中鉛鎘測定的方法,所建立的方法簡便、靈敏度高,具有較好的選擇性和可靠性,滿足高鹽調味品中鉛鎘的同時測定。
1 材料與方法
1.1材料與儀器
鉛、鎘標準溶液(1 mg/mL)國家標準物質中心;硝酸、鹽酸、高氯酸均為優級純;氯化鉀(3 mol/L)瑞士萬通中國有限公司;水18.3 MΩ去離子水;沾水辣1號、沾水辣2號和醬油1號、醬油2號以及魚露某超市。
瑞士萬通797VA Computrace極譜儀(AE:Pt,WE:MME多功能電極,RE:Ag/AgCl/3 mol/L KCl)瑞士萬通中國有限公司。
1.2實驗方法
1.2.1儀器測定條件采用懸汞電極,確定鉛、鎘同時測定的最佳儀器條件為:先向底液瓶中通5 min高純氮氣以除去溶液中的氧氣,富集電位-0.9 V,考慮出峰的穩定性和時間長短的合適性,確定富集時間 180 s,平衡時間 20 s,脫氧時間 300 s,進樣體積 20 mL,反應體積 20 mL,起始電位-0.70 V,終止電位-0.1 V。
1.2.2標準溶液的配制與曲線繪制用1% HNO3將鉛鎘標液稀釋至合適濃度的儲備液,再將儲備液配制成相應濃度,滿足在電解池中使鉛標準溶液系列為0.00,2.00,5.00,10.00,20.00,50.00 μg·L-1;鎘為0.00,1.00,2.00,5.00,10.00,20.00 μg·L-1。建立電流強度與鉛鎘濃度的線性方程。
1.2.3樣品處理準確稱取1 g試樣于100 mL錐形瓶中,加入10 mL硝酸、2 mL高氯酸,放置4 h后置于電爐上加熱消化,若溶液變棕黑色,補加硝酸2 mL,直至冒白煙,消化成無色透明或略帶黃色,剩約1 mL,用水沖洗杯壁,加入0.5 mL鹽酸和幾滴硝酸,加熱至微沸,冷卻后,將溶液轉移并定容至50 mL待測。同時做空白實驗。
1.2.4鉛鎘電流強度測定移取20 mL水于電解池中,加入0.1 mL 3 mol/L KCl,加入鉛鎘標準溶液使池內的濃度分別為鉛10 μg·L-1,鎘2.5 μg·L-1,按1.2.1儀器條件測定鉛鎘電流強度。
2 結果與分析
2.1電解質的選擇
2.1.1電解質種類的選擇若不往底液中加入電解質,基線很高且鉛鎘不能正常出峰,影響測定。將電解質KCl和KI進行對比實驗,結果表明:KI對鎘峰無影響但會使鉛峰右邊基線偏高,影響測定;而加入KCl基線下降且平穩,鉛鎘能正常出峰且峰形較好,所以選擇KCl做底液的電解質。
2.1.2電解質用量的選擇按1.2.4改變KCl用量,依次加入0.01~2 mL 3 mol/L KCl,隨著KCl加入量的增多,鎘峰高不增加,鉛峰高一直增加,對KCl濃度與鉛電流強度進行線性回歸,R2=0.9213,鉛峰增高與KCl中含鉛有關,見圖1、圖2。加入KCl量太少不好控制,太多造成浪費,選擇KCl電解質的量為0.1 mL 3 mol/L。
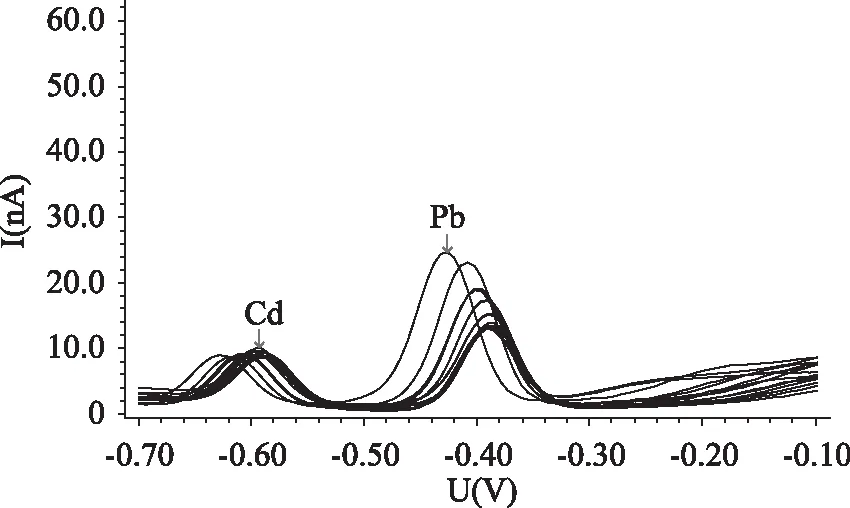
圖1 鉛鎘的溶出伏安圖Fig.1 Stripping voltammograms of Pb and Cd
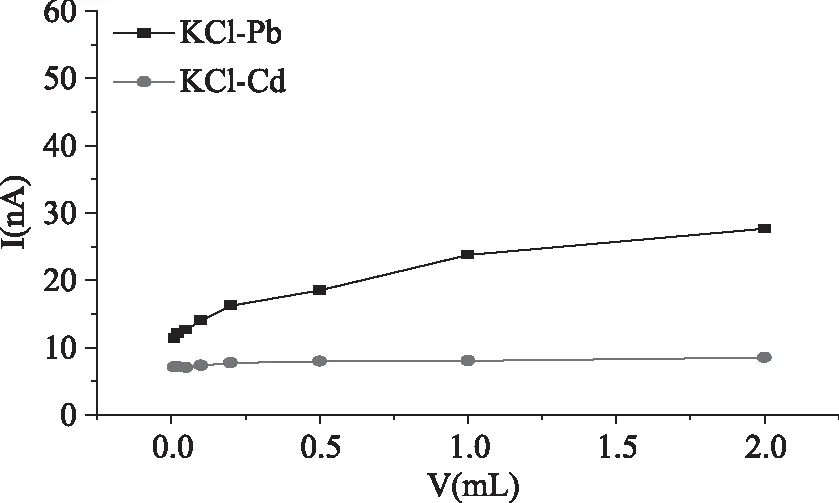
圖2 KCl對Pb,Cd的影響Fig.2 The influence of KCl on Pb and Cd
2.2NaCl濃度對鉛鎘的影響
按1.2.4向底液中依次加入NaCl溶液,使電解池中NaCl的質量分數為0.25%~1.25%,測定鉛鎘。由圖3、圖4可知,隨著NaCl濃度的增加,鎘峰高不增加,鉛峰高一直增加,對NaCl質量分數與鉛電流強度進行線性回歸,R2=0.9744,鉛峰增高與NaCl中含鉛有關,樣品按1.2.3處理后所含鹽分不會影響鉛鎘的測定。
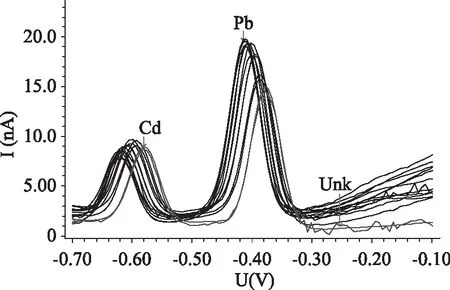
圖3 鉛鎘的溶出伏安圖Fig.3 Stripping voltammograms of Pb and Cd
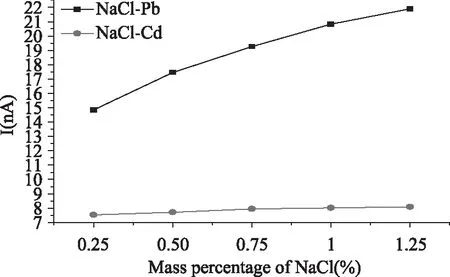
圖4 NaCl對Pb,Cd的影響Fig.4 The influence of NaCl on Pb and Cd
2.3酸類型及酸度的影響
按1.2.4向底液中分別加入HCl、HNO3、HClO4、HAc-NaAc(pH5.0),研究對鉛鎘峰的影響。結果表明這三種酸對鉛的影響是HCl>HNO3>HClO4,對鎘的影響是HNO3>HCl>HClO4;加0.1~0.5 mL HCl、HNO3、HClO4不會對鉛鎘峰產生影響。HAc-NaAc(pH5.0)分別在HCl、HNO3、HClO4不同酸度的體系中加入不同體積都不影響體系中鉛鎘的測定,為了盡量使樣品體系簡單化,不添加HAc-NaAc。
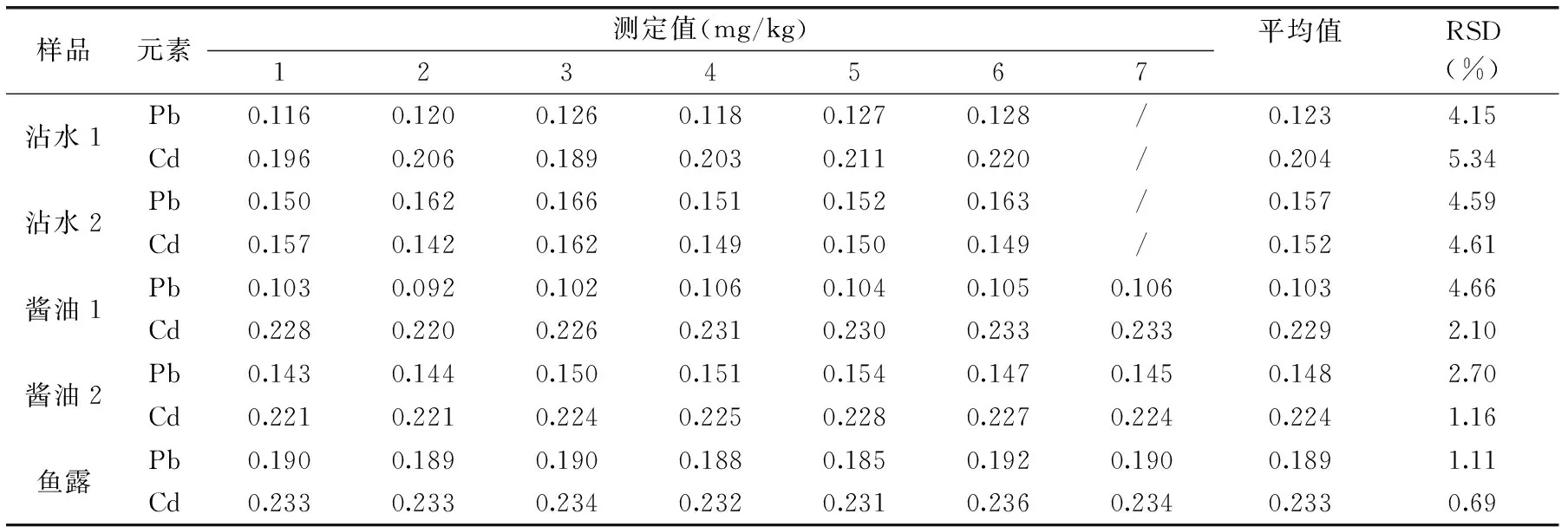
表1 精密度實驗
2.4干擾實驗
按1.2.4向底液中分別加入不同雜質元素,研究其對鉛鎘的影響,實驗表明5000倍(倍數都是指相對于底液中鉛的濃度的倍數)的Fe3+,2000倍的Zn2+,1000倍的Ca2+、Cu2+,500倍的Mg2+、Sr2+,200倍的Mn2+,100倍的Al3+,60倍的Co2+、Ni2+,10倍的Cr6+、Bi3+,5倍的As3+、Sb5+、Ge4+、Mo6+、Ba2+對鉛鎘的測定不產生干擾(對鉛鎘峰產生干擾均指影響鉛鎘正常出峰或使峰高改變達到±5%以上)。
2.5標準曲線
按1.2.2配制的標準系列溶液,測定電流強度建立與鉛鎘濃度的線性方程,結果表明:鉛、鎘的質量濃度分別在2~50 μg·L-1和1~20 μg·L-1范圍內與其峰電流強度呈線性關系。鉛的線性方程為y(nA)=4.2301x(μg·L-1)+0.4968,R2=0.9999。鎘的線性方程為y(nA)=7.1503x(μg·L-1)-0.4774,R2=1.0000。
2.6檢出限
用空白溶液(20 mL高純水+0.1 mL 3 mol/L KCl)連續測定待測元素11次,計算標準偏差,以標準偏差的3倍除以工作曲線斜率為待測元素的儀器檢出限(D.L)。鉛的SD=0.061,K=4.2301,D.LPb=0.043 μg·L-1;鎘的SD=0.068,K=7.1503,D.LCd=0.029 μg·L-1。稱取1 g樣品,前處理后定容至50 mL,方法檢出限為:鉛2.17 μg·kg-1、鎘1.43 μg·kg-1。
2.7方法學考察
2.7.1精密度實驗準確稱取兩種沾水辣樣品1 g,按1.2.3處理,同時測定6個平行樣,計算鉛、鎘的相對標準偏差(RSD),RSD在4.15%~5.34%;醬油和魚露中鉛鎘未檢出,準確稱取兩種醬油和魚露樣品1 g,在消解前加入一定量的鉛鎘標準溶液,同一份溶液連續測定7次,鉛和鎘的RSD在0.69%~4.66%之間,表明該方法具有良好的精密度,結果詳見表1。
2.7.2回收率實驗分別對沾水辣、醬油、魚露進行加標回收實驗,鉛、鎘回收率在93.9%~109.9%之間,鉛、鎘均具有良好的回收率,結果詳見表2。
3 結論
本文研究了采用濕法消解結合陽極溶出伏安法對沾水辣、醬油和魚露等高鹽調味品中的鉛鎘同時測定的方法,方法檢出限鉛為2.17 μg·kg-1、鎘1.43 μg·kg-1,鉛、鎘工作曲線的線性范圍分別為2~50、1~20 μg·L-1,該方法簡便、靈敏度高,能有效避免高鹽分基體干擾等特點。該方法測定實際樣品中鉛鎘含量的精密度在0.69%~5.34%,加標回收率在93.9%~109.9%,精密度和回收率的結果表明,完全滿足高鹽調味品中鉛鎘元素的同時測定。

表2 回收率實驗
注:表中“-”表示未檢出。
[1]Wei BG,Yang LS.A review of heavy metal contaminations in urban soils,road dusts and agricultural soils from China[J].Microchemical Journal,2010,94:99-107.
[2]Cheng Z,Man YB,Nie XP,et al.Trophic relationships and health risk assessments of trace metals in the aquaculture pond ecosystem of Pearl.River Delta,China[J].Chemosphere,2012,90(7):2142-2148.
[3]GB 5009.15-2014,食品中鎘的測定[S].
[4]GB 5009.12-2010,食品中鉛的測定[S].
[5]張志,莫曉玲.氫化物發生-原子吸收光譜法測定醬油中的鉛含量[J].中國調味品,2008,9:84-87.
[6]李敏,連曉文,姚敬,等.電感耦合等離子體-質譜法測定醬油中 12 種金屬[J].中國食品衛生雜志,2012,26(4):344-347.
[7]汪曉冬.微波消解-電感耦合等離子質譜法對 8 種市售醬油無機元素的分析[J].食品研究與開發,2010,31(11):159-161.
[8]佘曉麟,吳皓苗.電感耦合等離子提發射光譜法同時測定魚露中多種微量元素[J].公共衛生與預防醫學,2012,23(3):99-100.
[9]李玉紅,魏永生.電感耦合等離子體原子發射光譜法測定雞精中微量元素和重金屬[J].中國調味品,2014,39(8):96-98.
[10]Ouyang RZ,Zhu ZQ,Tatum CE,et al.Simultaneous stripping detection of Zn(II),Cd(II)and Pb(II)using a bimetallic Hg-Bi/singlewalled carbon nanotubes composite electrode[J].Journal of Electroanalytical Chemistry.2011,656(1/2):78-84.
[11]Torma F,Kadar M,Toth K,et al.Nafion(R)/2,2′-bipyridyl-modified bismuth film electrode for anodic stripping voltammetry[J].AnalyticaChimica Acta.2008,619(2):173-182.
[12]Achterberg EP,Braungardt C.Stripping voltammetry for the determination of trace metal speciation and in-situ measurements of trace metal distributions in marine waters[J].Analytica Chemica Acta,1999,400(S1):381-397.
[13]王燕鳳,張旭,梁龍偉,等.陽極溶出伏安法同時測定鋅電解液中微量鎘和鉛[J].礦冶,2012,21(2):111-114.
[14]李源,任鳳蓮,周恩榮,等.陽極溶出伏安法同時測定鋅電解液中鎘銅鈷[J].冶金分析,2011,31(10):14—17.
[15]馬政,郭子英.鉍膜電極溶出伏安法測定蒼耳子中鋅的含量[J].Chinese Journal of Spectroscopy Laboratory,2009,26:5-8.
[16]劉雄,林肖湘,李紅.差分脈沖陽極溶出伏安法測定中藥材樣品中的銅鉛鎘[J].廣州化工,2014,42(6):108-113.
[17]梁賀升,陳少瑾,陳宜菲.溶出伏安法測定烏藥中的銅鉛鎘[J].廣東微量元素科學,2011,18(4):41-45.
[18]于鐵力,倪蕾,王艷如,等.微分陽極溶出伏安法連續測定蔬菜中銅鉛鎘鋅[J].微量元素與健康研究,1996,13(4):48-49.
[19]賴瑢,丘福保,徐鎮耿,等.微波消解-溶出伏安法對食品中銅、鉛、鎘的同時測定[J].分析測試學報,2010,29(2):203-206.
[20]徐愛平,殷秋妙,趙沛華等.食鹽中鉛含量的測定方法研究[J].廣東農業科學,2010,(10):36-37.
Determination of lead and cadmium in high salt condiment via anodic stripping voltammetry
PENG Jing1,HE Yu-ping2,*
(1.School of Materials Science and Engineering,Kunming University of Science and Technology Kunming 650093,China; 2.Research Center for Analysis and Measurement,Kunming University of Science and Technology Kunming 650093,China)
A method was studied for determination of lead and cadmium in high salt condiment,such as dampened spicy,soy sauce and fish sauce,by the combination of wet digestion and stripping voltammetry.The impact of the instrument conditions,the type and amount of electrolyte and high salt on lead and cadmium was investigated,and the experiment was made on the disturbance of acid type and acidity as well as other coexisting ions.The linear range of the working curves of Pb and Cd are 2~50 μg·L-1and 1~20 μg·L-1respectively,the correlation coefficient were 0.9999 and 1.0000,and their instrument detection limits were 0.043 μg·L-1and 0.029 μg·L-1,their method detection limits were Pb 2.17 μg·kg-1,Cd 1.43 μg·kg-1.The content of lead and cadmium about actual sample was determined by this method,the precisions are respectively 1.11%~4.66%,0.69%~5.34%.The recovery rate were respectively 93.9%~109.9%,94.7%~107.5%.The result reveals that this was a simple,fast and higher sensitivity method which had a good selection and excellent reliability.
wet digestion;stripping voltammetry;condiment;lead;cadmium
2015-10-14
彭靜(1990-),女,在讀碩士研究生,研究方向:食品分析,E-mail:603580773@qq.com。
賀與平(1965-),男,學士,高級工程師,研究方向:光譜分析與方法研究,E-mail:1500472254@qq.com。
國家自然科學基金青年基金(51304094);科技計劃項目(14051592);云南省教育廳基金面上項目(2103Y326)。
TS207.3
A
1002-0306(2016)07-0274-04
10.13386/j.issn1002-0306.2016.07.044

