4,6-二正丁氧基-1,3-二苯磺酸喹啉-8-酯的合成及其對Sn2 + 和Bi3 + 的識別作用
張德春,王文革,胡漢祥,傅紅艷,朱莉云
(湖南工學院 材料與化學工程系,湖南 衡陽 421002)
8-羥基喹啉及其衍生物是氮雜環中非常重要的一類化合物,不僅具有良好的生理活性[1],而且在化學分析領域有著多種用途,可用作金屬離子萃取劑[2]、沉淀劑[3]及光度分析試劑[4]。近年來,有機電致發光材料作為一種新材料,具有亮度高、光效高以及易于調節發光顏色等優點,其制備與應用受到人們高度關注。8-羥基喹啉與金屬離子生成的金屬配合物具有電子傳輸性能,其可用作有機電致發光材料[5-7]。
8-羥基喹啉磺酸酯類化合物的制備與應用文獻報道較少,其結構中磺酸酯基和喹啉環上的氮原子都可與金屬離子配位,因此結構對稱的8-羥基喹啉磺酸酯類化合物的合成及其與金屬離子配位的研究,有助于人們發現新的分析試劑和開發新型高效的光電功能材料。
本文以4,6-二正丁氧基-1,3-苯二磺酰氯和8-羥基喹啉為原料,三乙胺作縛酸劑,丙酮為溶劑,合成了4,6-二正丁氧基-1,3-二苯磺酸喹啉-8-酯(化合物2),得到了IR、1H NMR 等對其結構的確認。并利用紫外光譜詳細研究了它與20 種金屬離子的配位作用。結果發現,4,6-二正丁氧基-1,3-二苯磺酸喹啉-8-酯對Sn2+顯示出一定的選擇性,由于Sn2+和Bi3+協同作用的影響,在化合物2-Sn2+的體系中加入Bi3+,紫外吸收光譜在324 nm 左右形成強烈吸收峰,這說明化合物(2)對Bi3+顯示出優于Sn2+的較好選擇性。
1 實驗部分
1.1 試劑與儀器
8-羥基喹啉、三乙胺、丙酮、石油醚、乙酸乙酯、ZnCl2、CaCl2、Pb(NO3)2、CuCl2、FeCl3、CdCl2、MnCl2、CoCl2、NiCl2、CrCl3均為分析純(溶劑經干燥處理后使用);實驗用水為超純水;4,6-二正丁氧基-1,3-苯二磺酰氯,自制[8]。
INOVA-400 MHz 型核磁共振儀;Nicolet iS10 FTIR 紅外光譜儀;UV-2700 型紫外吸收光譜儀;SLRD-I 型數字熔點測定儀。
1.2 實驗方法
100 mL 的兩口瓶中依次加入0.838 g(2 mmol)4,6-二 正 丁 氧 基-1,3-苯 二 磺 酰 氯(1)的 丙 酮(10 mL)溶液,0.580 g (4 mmol)8-羥基喹啉的丙酮(10 mL)溶液,0.54 mL 的三乙胺,室溫攪拌2 ~3 h,TLC 跟蹤原料點消失,結束反應。蒸出溶劑,經水和乙醇洗后得粗產品,在丙酮中重結晶,得到白色晶體(2)(Rf=0.51,V(石油醚)∶V(乙酸乙酯)=1.5∶1)1. 20 g,產 率93. 98%,m. p. 168 ~169 ℃;IR(KBr),ν/cm-1:792,1 047,1 075,1 186,1 215,1 229,1 373,1 500,1 558,1 597,1 620,2 874,2 935,2 961;1H NMR(400 MHz,CDCl3)δ:0. 94(t,J =7.4 Hz,6H),1. 49 ~1. 59 (m,4H),1. 77 ~1. 84(m,4H),4.17(t,J =6.4 Hz,4H),6. 56(s,1H),7.39(dd,J=8.4 Hz,2H),7.47(t,J=7.6 Hz,2H),7.53(dd,J =7. 6 Hz,2H),7. 74(dd,J =8. 4 Hz,2H),8.15(dd,J =8.4 Hz,2H),8.42(s,1H),8.77(dd,J=4.4 Hz,2H)。合成路線如下:
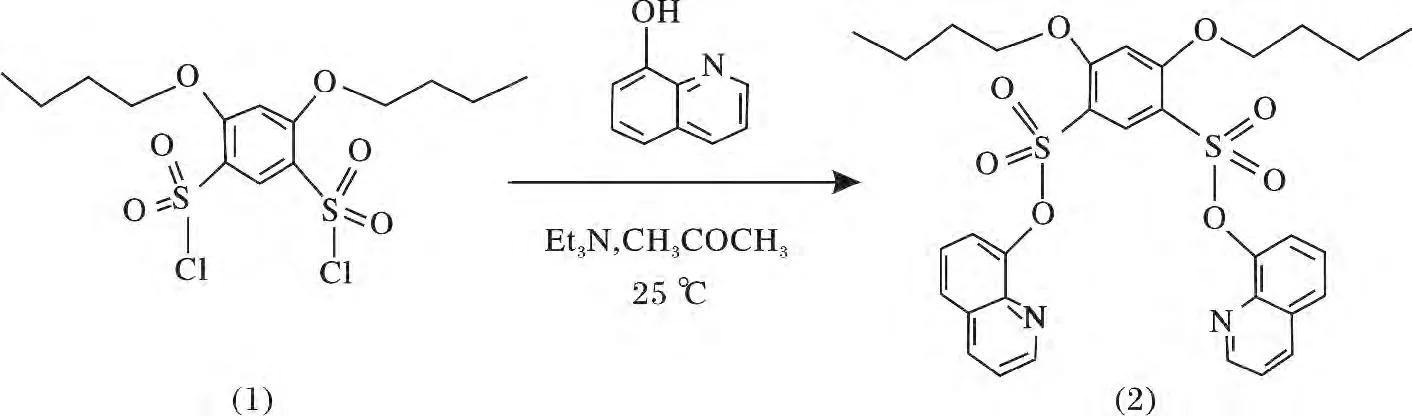
2 結果與討論
2.1 溶劑
4,6-二正丁氧基-1,3-二苯磺酸喹啉-8-酯的合成反應受反應溶劑和溫度的影響。二氯甲烷作溶劑時,合適的反應溫度是40 ~50 ℃,反應時間是5 ~6 h,化合物(2)的產率為31.40%;丙酮作溶劑時,合適的反應溫度是25 ℃左右,反應時間是2 ~3 h,化合物(2)的產率為93.98%。由此丙酮作反應溶劑時,反應收率相對較高,反應速率較快,所需溫度較低,故采用丙酮作溶劑。
2.2 波譜表征
化合物(2)的IR 譜中,2 874 ~2 961 cm-1出現多個較弱的正丙基中C—H 鍵的伸縮振動譜;1 620~1 468 cm-1是芳環和喹啉環的骨架伸縮振動譜;1 313 ~1 373 cm-1是 S O 鍵伸縮振動帶。
1H NMR 中共出現12 組峰:低場區出現8 組峰,苯環上的氫的吸收峰是2 組單峰,喹啉環上的氫的吸收峰是6 組峰。苯環上由于磺酸酯基的吸電子效應的影響,導致與其臨近的碳上的氫吸收峰在較低場(化學位移為8.42)出現一組單峰,而苯環上正丁氧基的供電子效應,導致與其臨近的碳上的氫以單峰的形式出現在較高場(化學位移為6.56);喹啉單元上氮原子鄰位氫的吸收峰的化學位移值是8.77,是dd 峰,耦合常數是4.4 Hz,位移移向低場是因為受氮原子的吸電子效應的影響。氮原子間位和對位的氫的吸收峰的化學位移值是7.74 和8.15。喹啉環的苯環上氧原子鄰位、間位和對位的氫的吸收峰的化學位移值是7.39,7.47,7.53。高場區出現的4 組峰是正丁氧基上4 個碳上的氫的化學位移,證明兩個正丁氧基化學環境完全相同,正丁氧基上氫在譜圖中化學位移為4.17 出現一組三重峰,1.77 ~1.84 和1.49 ~1.59 出現兩組多重峰,0.94出現一組三重峰。這些質子的積分面積的比例分別是2∶1∶2∶2∶2∶2∶2∶1∶4∶4∶4∶6(按化學位移值從高到低的順序),與分子結構中的氫的數目吻合。譜圖上化學位移7.28 的強峰是氘代氯仿的峰,2.19的強峰是水峰。由此可知,化合物(2)的分子結構具有預期的結構。
2.3 紫外光譜性質
溶液配制:以DMF 為溶劑,配制0.1 mmol/L 的化合物(2)的溶液;以二次蒸餾水為溶劑,配制1.0 mmol/L 的硝酸鹽或氯化物的金屬離子溶液(Zn2+,Ca2+,Pb2+,Cu2+,Fe3+,Cd2+,Mn2+,Co2+,Ni2+,Cr3+,Al3+,Ti3+,Ag+,Na+,Ba2+,Bi3+,Sr2+,Hg2+,Sn2+,K+)。紫外光譜測定均在25 ℃。
取濃度為0.1 mmol/L 化合物(2)溶液1 mL,用DMF 定容至10 mL。取3.0 mL 于比色皿中(石英比色皿厚度為1 cm),測定紫外光譜,結果見圖1。
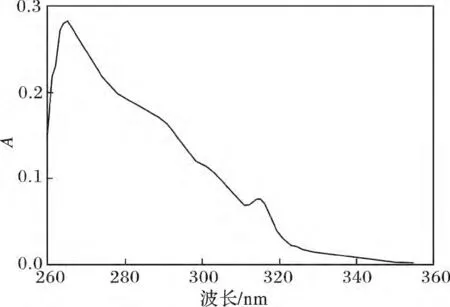
圖1 化合物(2)(10 μmol/L)在DMF 中的紫外吸收光譜Fig.1 UV spectra of compound (2)(10 μmol/L)in DMF
由圖1 可知,化合物(2)的DMF 溶液的最大紫外吸收峰在265 nm 處,是芳環和喹啉環的π→π*躍遷所產生的吸收帶,摩爾吸光系數分別是3.69 ×104L/(mol·cm)。另外,在315 nm 左右處出現的弱的吸收峰是由于磺酸酯基n→π*躍遷所產生的吸收帶。
2.4 對金屬離子的識別性能
取濃度為0.1 mmol/L 的化合物(2)溶液1 mL,1.0 mmol/L的金屬離子溶液0.4 mL,以DMF 定容至10 mL,分別配制含等摩爾量不同金屬離子的混合溶液,利用紫外光譜研究其對不同金屬離子的選擇性識別能力。當分別加入Zn2+、Ca2+、Pb2+、Cu2+、Fe3+、Cd2+、Mn2+、Co2+、Ni2+、Cr3+、Al3+、Ti3+、Ag+、Na+、Ba2+、Bi3+、Sr2+、Hg2+、K+這19 種離子后,主體化合物(2)的紫外吸收光譜最大吸收峰的位置沒有發生明顯的變化,只是吸收強度有不同程度的改變。但是,當將Sn2+加入到化合物(2)的溶液中后,發生了較明顯的變化,化合物(2)在365 nm 處出現了新的吸收峰,原來在紫外光區的最大吸收峰(265 nm)強度有些降低。
配制濃度10 μmol/L 的化合物(2)溶液,濃度為10 ~60 μmol/L 的Sn2+混合溶液,研究不同濃度的Sn2+對化合物(2)紫外吸收的影響,結果見圖2。
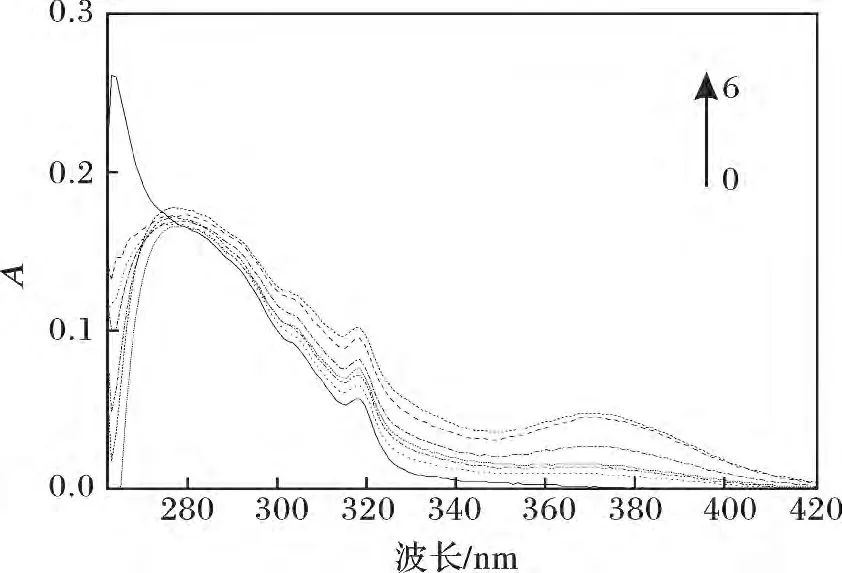
圖2 化合物(2)在加入不同濃度Sn2+后紫外吸收光譜變化曲線Fig.2 UV spectra of compound(2)with different concentrations of Sn2+
由圖2 可知,化合物(2)在365 nm 處出現了新的吸收峰,同時在265 nm 處的吸收峰強度有較大幅度降低,紅移6 ~10 nm,紅移的原因是加入不同量金屬離子時,引入的水的量不同引起的。
取濃度0.1 mmol/L 的化合物(2)溶液1.0 mL,1.0 mmol/L 的Sn2+溶液0. 4 mL,其它金屬 離子0.2 mL(除Sn2+),定容至10 mL,紫外光譜研究其它金屬離子對Sn2+的干擾影響。結果發現,當分別加入Zn2+、Ca2+、Pb2+、Cu2+、Fe3+、Cd2+、Mn2+、Co2+、Ni2+、Cr3+、Al3+、Ti3+、Ag+、Na+、Ba2+、Sr2+、Hg2+、K+等18 種離子后,化合物(2)對Sn2+的紫外光譜吸收峰沒有發生明顯的變化,只是在264 nm左右吸收強度有不同程度的改變,這是因為某些金屬離子如Co2+、Hg2+、Ca2+在264 nm 左右處也有吸收。但是,當將Bi3+加入到化合物(2)和Sn2+的混合溶液后,發生了明顯的變化,365 nm 處的吸收峰消失,在324 nm 處出現了新的吸收峰,原來在紫外光區的最大吸收峰(265 nm)強度有所提高。
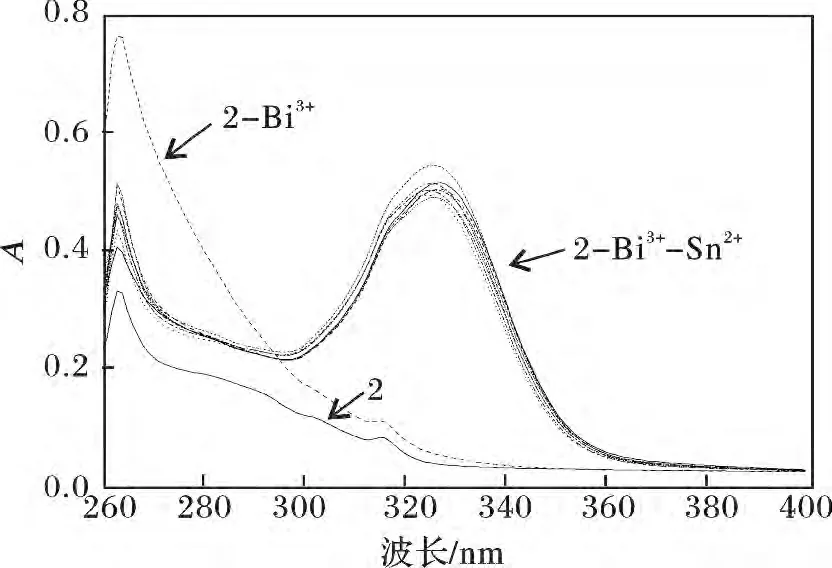
圖3 化合物(2)(10 μmol/L)-Bi3+(40 μmol/L)在加入Sn2+10 ~80 μmol/L 前后紫外吸收光譜變化曲線Fig.3 UV absorption spectra of compound(2)(10 μmol/L)-Bi3+(40 μmol/L)with Sn2+10 ~80 μmol/L
由圖3 可知,將Bi3+加入到化合物(2)中紫外吸收光譜發生了變化,是因為Bi3+最大吸收峰在265 nm左右處,譜圖是兩者吸收峰疊加的結果。因此化合物(2)的吸收峰不隨Bi3+的濃度改變而改變。將Sn2+加入化合物2-Bi3+體系中,紫外吸收光譜在324 nm 左右出現了強吸收峰,并且峰強度基本不受Sn2+濃度影響,此吸收峰是Sn2+和Bi3+協同作用的結果。由此,我們利用紫外吸收光譜在324 nm左右是否出現了強吸收峰作為判斷依據,可將化合物(2)用作Bi3+的選擇性測定,且需在測定體系中加入少量的Sn2+。
以上的結果表明,化合物(2)對Sn2+顯示出一定的選擇性,但這種作用較弱。在化合物2-Sn2+的體系中加入Bi3+,由于Sn2+和Bi3+協同作用的影響,使其在365 nm 處的吸收峰消失,在324 nm 處出現了新的吸收峰,這說明化合物(2)對Bi3+顯示出優于Sn2+的較好選擇性。
3 結論
(1)以4,6-二正丁氧基-1,3-苯二磺酰氯和8-羥基喹啉為原料,三乙胺作縛酸劑,丙酮作溶劑,合成了4,6-二正丁氧基-1,3-二苯磺酸喹啉-8-酯,產率很高。化合物(2)的紫外吸收光譜最大吸收峰在265 nm處,根據朗伯-比耳定律,計算得化合物(2)的摩爾吸光系數是3.69 ×104L/(mol·cm)。
(2)利用紫外光譜法研究了化合物(2)對20 種金屬離子的識別。結果發現,化合物(2)對Sn2+顯示出一定的選擇性,但這種作用較弱。在化合物2-Sn2+的體系中加入Bi3+,由于Sn2+和Bi3+協同作用的影響,使其在365 nm 處的吸收峰消失,在324 nm處出現了新的吸收峰,這說明化合物(2)對Bi3+顯示出優于Sn2+的較好選擇性。
[1] 杜鼎,方建新. 具有生物活性的喹啉類化合物的最新進展[J].有機化學,2007,27(11):1318-1336.
[2] 郝會娟,周鑫,吳學.一種新型喹啉衍生物的合成及其對Hg2+的檢測[J].化學試劑,2011,33(6):551-554.
[3] 趙玉玲,俞天智.8-羥基喹啉類配體及其配合物應用研究[J].材料導報,2007,21(4):21-25.
[4] 歐陽新華,曾和平,謝彥.8-羥基喹啉衍生物及其金屬配合物的合成與光致發光特性[J]. 有機化學,2007,27(3):402-408.
[5] Li Huali,Xu Bing.Synthesis and characterization of 5-substituted 8-hydroxyquinoline derivatives and their metal complexes[J].Tetrahedron,2008,64(9):10986-10995.
[6] 周亞東,曾和平,靖慧蓮,等.5,7’-(亞甲胺基)-二-8-羥基喹啉的合成及其理論研究[J]. 有機化學,2006,26(9):1225-1231.
[7] 周亞東,曾和平,靖慧蓮,等.8-羥基喹啉金屬配合物在電致發光器件中的應用研究進展[J]. 有機化學,2006,26(6):783-792.
[8] He Lan,An Yu,Yuan Lihua,et al.Macrocyclic aromatic tetrasulfonamides with a stable cone conformation[J].Chemical Communications(Cambridge,United Kingdom),2005,30:3788-3790.

