承鋼70t轉爐鐵水提釩的動力學行為
黃偉軍,陳 敏,溫 翰,徐 磊,黃宣輝,范富華
(1.東北大學 材料與冶金學院,沈陽110819;2.承德建龍特殊鋼有限公司,河北 承德067201)
釩是重要的戰略物資,廣泛應用于化學工業、鋼鐵工業、航空航天工業等領域.釩在自然界中主要與鈦、鐵伴生賦存于釩鈦磁鐵礦中[1,2].目前我國多采用轉爐提釩工藝,轉爐提釩根據選擇性氧化原理,通過控制適宜的熱力學和動力學條件,使鐵水中[V]最大限度地氧化進入渣中,同時,抑制熔池中碳的氧化反應,以保證后續煉鋼熱量的需要[3~5].該工藝對釩元素收得率和渣中釩品位及后續煉鋼有直接的影響.良好的動力學條件,有利于提高釩在鐵水中擴散傳質速率,促進[V]的氧化和氧氣利用率的提高.為實現吹煉過程中工藝參數與熔池溫度的有效控制,降低釩渣中(FeO)含量,建立提釩轉爐的控制模型,掌握鐵液中元素的氧化規律尤為重要.趙重陽、梅彬等人對提釩轉爐靜態控制模型進行了研究[6,7],同時甄小鵬、謝兵建立了提釩轉爐界面多元組分耦合反應動力學模型[8],但只實用于渣-金界面.本文以煉鋼轉爐動態模型為基礎,建立了提釩轉爐的動態控制模型,并對其進行了驗證和鐵液中元素氧化機理的分析.
1 頂底復吹提釩轉爐數學模型的建立
提釩轉爐為高溫多相反應,化學反應速率很快,而傳質速率要比化學反應速率慢得多,因此傳質成為了元素化學反應過程的限制環節.本文根據提釩吹煉過程中熱量和質量的平衡,結合反應工程學理論,通過比較吹煉過程中各物質的傳質速率,得出各元素氧化反應的速率方程,建立反應過程中成分與溫度變化的機理模型.注意到提釩轉爐內元素的反應機理和冶煉目的與煉鋼轉爐有所不同,提釩轉爐渣為酸性渣,鐵液中的磷基本不參與反應[9],因此本模型不考慮磷的氧化.提釩過程終點碳質量分數在3.5%左右,所以在整個反應過程中其傳質速率大于氧的傳質速率[8],但是吹煉過程和氧槍的控制機理與煉鋼轉爐基本一致,所以具體模型的建立和模型中參數的計算可借鑒煉鋼轉爐,其內容包括求解沖擊坑氣-液、渣-金界面的反應速率方程及其對應的界面面積,求解冷料的熔解速率方程和冶煉過程熔池的溫度方程[10~13].該模型中熔池主要考慮了[Fe]、[Si]、[C]、[V]、[Cr]、[Mn]、[Ti]等元素,熔渣主要考慮了(FeO)、(SiO2)、(V2O5)、(Cr2O3)、(MnO)、(TiO2)等氧化物,忽略了(CaO)、(P2O5)、(MgO)、(Al2O3)氧化物[8,14].
1.1 求解沖擊坑氣-液界面反應速率方程和反應界面積
沖擊坑界面是氧槍的氧氣射流與金屬液直接接觸的區域,并發生著劇烈的氧化反應:

式中,M 代表金屬中[C],[Ti],[Si],[V],[Cr],[Mn],[Fe].
在沖擊坑界面處,元素的氧化反應過程主要包括氧的傳質(包括氣相和熔池),熔池中元素的傳質,界面的氧化反應,氧化產物的傳質,以及CO和底吹氣體(N2或Ar)的排出等不同環節.其中氧或元素在熔池中的傳質為反應過程的限制環節[10,12].
熔池中氧的傳質速率(RO)為:
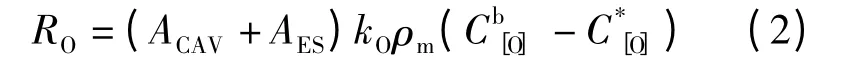
式中,RO為氧在金屬中的傳質速率,mol/s;ACAV,AES為沖擊坑和卷入渣滴的界面積,m2;ρm為鋼液的密度,kg/m3;kO為氧在金屬中的傳質系數,m/s;分別為[O]的本體濃度和界面濃度,mol/m3.
熔池中元素的傳質速率(RM)為:
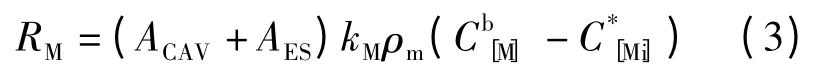
式中,RM為M 元素在金屬中的傳質速率,mol/s;為M 元素在金屬中的傳質系數,m/s,和分別代表熔池中[M]元素的本體濃度和界面濃度,mol/m3.
[M]的氧化速率取決于[O]、[M]在熔池中的傳質速率較小的一方.因此,通過公式(2)~(3)計算熔池中氧和各元素的傳質速率,并進行比較,找出限制環節,進而得出各元素氧化速率方程.由于吹煉終點碳質量分數較高(在3.5%左右),所以吹煉過程RO<RC,脫碳反應的限制環節為氧的傳質.
本模型根據肖興國[15]給出的轉爐沖擊坑氣-液反應界面積的求解方程式,計算不同吹煉條件下的沖擊坑氣-液反應界面積.射流沖擊凹坑形狀的經驗關系式如下:
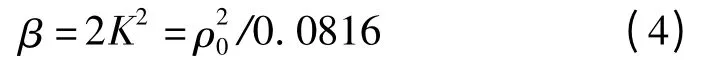
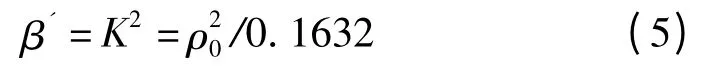
式中,h0為沖擊坑深度,m;L 為頂槍槍位,m;ρ0為氧槍的滯止壓力,Pa.
根據凹坑形狀經驗公式,可計算出硬吹和軟吹時沖擊坑反應界面積[15]:
軟吹時:
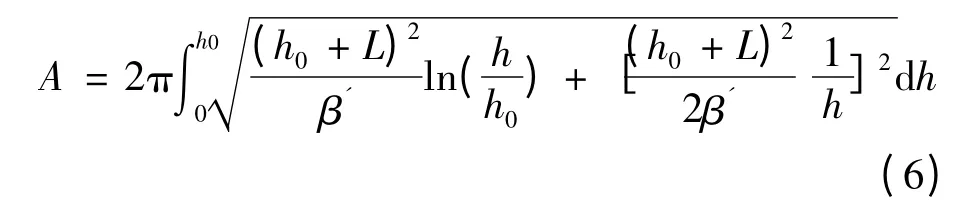
硬吹時:
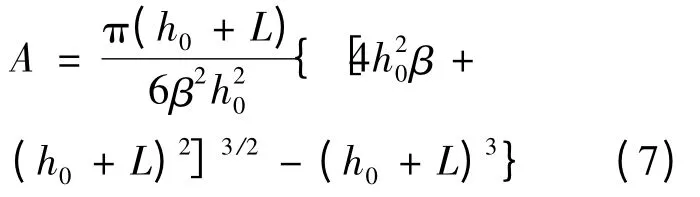
1.2 求解渣-金界面反應速率方程及其反應界面積
提釩轉爐中釩的氧化主要發生在渣-金界面處,因此掌握其界面元素的氧化速率方程對釩元素的提取非常重要.此處主要發生[V]、[Cr]、[Mn]與氧化亞鐵的耦合反應[8,12],反應方程式如下:
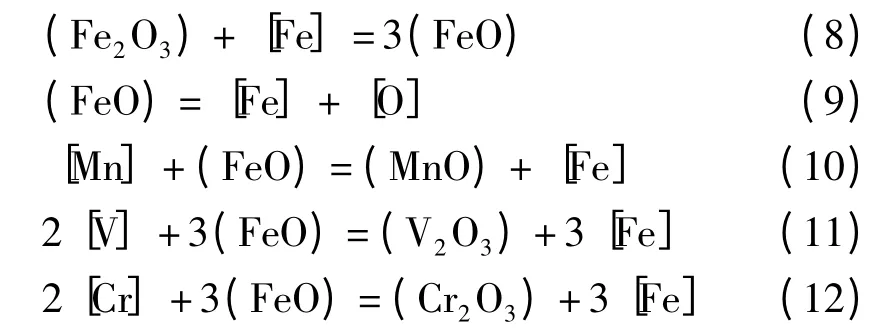
高溫下,化學反應快速達到平衡,而傳質比化學反應慢得多,因此金屬側元素及其對應熔渣側產物的傳質為反應的限制環節[8].其傳質速率分別為:
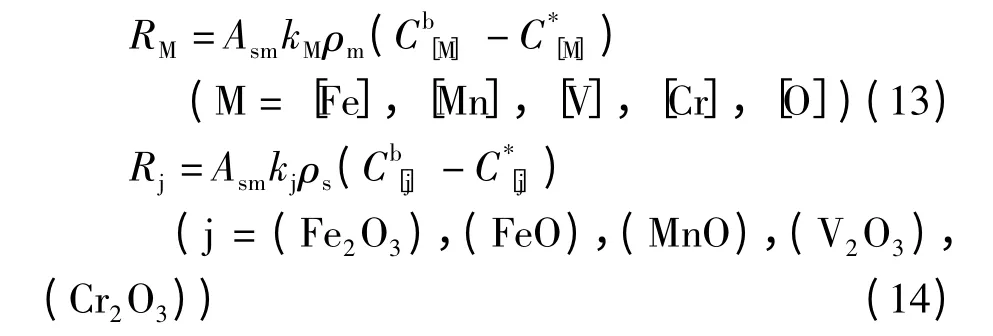
式中,Rj為j 氧化物在熔渣側的傳質速率,mol/s;Asm為渣-金界面積,m2;kj為j 氧化物在熔渣側的傳質系數,m/s;ρs為熔渣的密度,kg/m3.
化學反應(8)~(12)的平衡常數分別為:
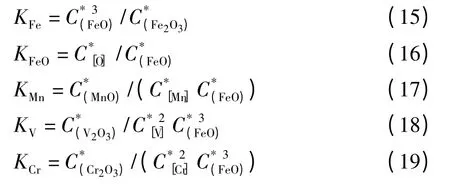
在渣-金界面處,各化學反應處于熱力學平衡,因此各反應物與生成物之間的傳質速率存在如下的關系式:
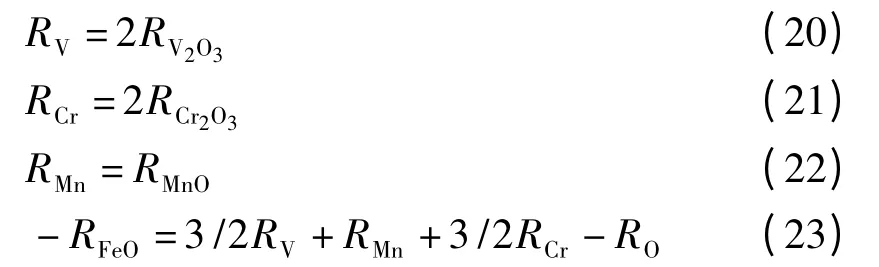
本文假設元素由金屬內向界面,以及氧化產物由界面向熔渣的傳質方向為正.聯立由式(15)至式(23)組成的方程組,可算出,其中,i 分別代表[O],[V],[Cr],[Mn],(Fe2O3),(FeO),(MnO),(V2O3),(Cr2O3).
渣-金界面積對在界面進行耦合反應元素的反應速率影響較大.在頂底復吹過程中,界面快速發生著變化,導致其很難直接測定.本研究根據文獻[12]得到了計算渣-金界面積Asm的一種方法,即:

式中,AEm為乳化液滴的面積,m2;Asm為卷入金屬熔池渣滴的表面積,m2.
1.2.1 求解乳化液滴的表面積
在提釩吹煉過程中,由于氧氣射流沖擊液面形成凹坑,凹坑區域如同一個圓環,圓環的內層是渣側邊界層.同時劇烈運動的鐵液將動能傳遞給凹坑界面上的金屬液滴,當界面金屬液滴的慣性力大于重力和界面力的總和時,液滴脫離金屬液進入渣中形成乳化液滴[16,17].根據文獻[12],乳化液滴面積的計算式:
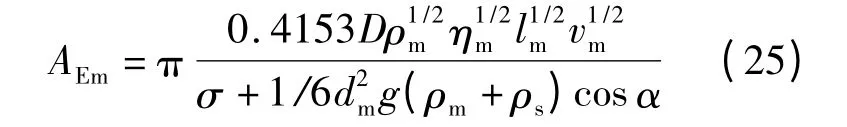
式中,α 為重力與液面之間的夾角,(°);σ 為金屬和熔渣間界面張力,N/m;vm為脫離點處液滴的速度,m/s;dm為液滴直徑,m;g 為重力加速度,9.8 m/s2;l 為流經長度,m;D 為圓環的內徑,m;ηm為鐵液的黏度,Pa·s.
1.2.2 求解卷入熔渣的表面積
在頂底復吹的條件下,由于底吹氣體和產物CO 的排除,使渣液面高于熔池的其他部分,處于下方金屬液的區域被熔渣圍繞如同套在渣環內,圓環的最內層是渣側邊界層,取熔渣環的內徑為D.環內渣-金界面的渣液吸收了排除氣體和金屬液的動能,并劇烈運動,當渣的慣性力大于界面力和浮力總和時,渣層下緣形成渣滴并卷入金屬熔池,形成卷渣[16,17].由以上假設和借鑒乳化液滴表面積的計算公式,可得卷入渣滴表面積為:
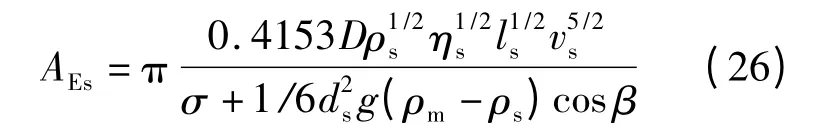
式中,D 為圓環的內徑,m;ηs為熔渣的黏度,Pa·s;β 為浮力與液面方面的夾角,(°);ds為渣滴直徑,m.
1.3 冷卻料熔解速率
1.3.1 生鐵塊、釩渣鐵的熔解速率
生鐵塊和釩渣鐵的主要成分為鐵,其熔解主要是鐵的熔解,屬于固液相變傳熱中的直接接觸固液相變傳熱問題.為簡化問題,生鐵塊和釩渣鐵近似認為是球粒.因其主要成分是Fe-C 合金,其熔點與含碳量有關.由圖1 可以看出,在固液相界面存在溫度梯度和碳的濃度梯度.假定dr 層內碳的質量分數從,而溫度從;鐵熔化部分的溫度和組成與整個熔體相同;t*及的邊界層不斷地向鐵球中心推進,并對界面的熱平衡和質量平衡不產生影響[18~20].
根據以上假設,球體的個數為N(Fe):
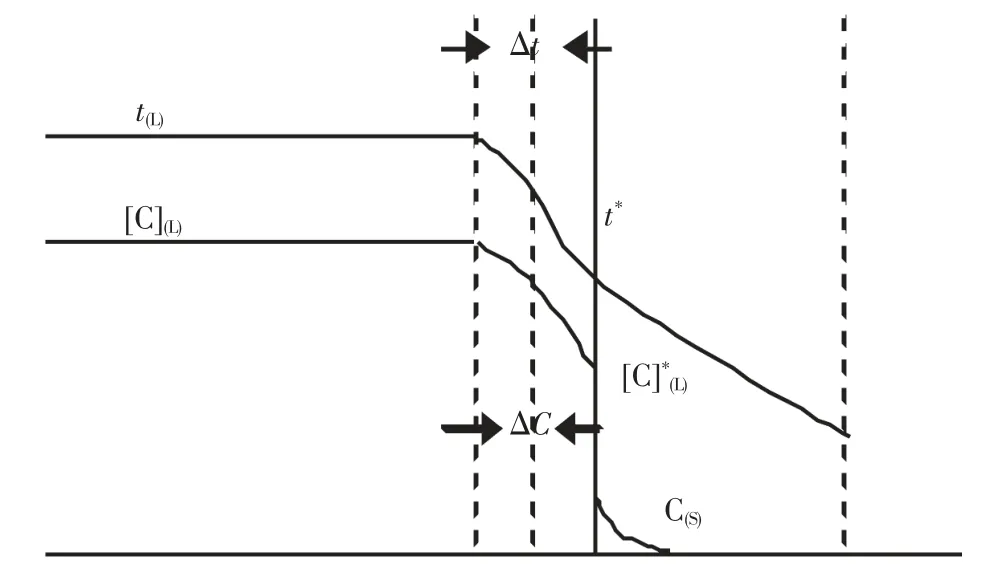
圖1 鐵塊-鐵水界面溫度和碳含量的分布Fig.1 Distribution of temperature and carbon content on interface of the iron block and the molten iron
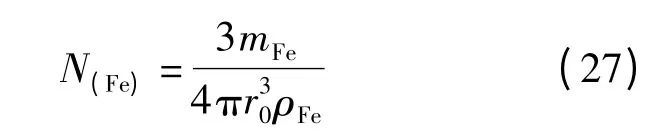
式中,mFe為生鐵塊和釩渣鐵的質量,kg;r0為生鐵塊和釩渣鐵顆粒的初始半徑,m.
根據球粒界面上基元液相層內熱平衡和碳平衡,導出鐵球熔化的速率如下[10]:
熱平衡:

碳平衡:
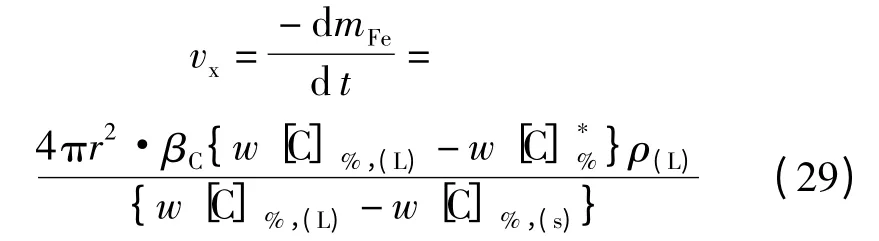
Fe-C 系液相線方程[19]:

式中,vx,v 分別為熱平衡和碳平衡得出的鐵球熔解速率,m/s;分別為熔體內、界面及鐵塊內碳的質量分數,%;t(L)、t*為熔體、界面溫度,℃;a 為傳熱系數,kW/(m2·℃);β 為傳質系數,m/s;q 為鐵塊的熔化潛熱,kJ/kg;為液態金屬的平均熱熔kJ/(kg·℃).
將公式(30)代入公式(28),并令公式(28)和公式(29)相等.則得出的三次方程,然后利用逼近法解出,繼而求解vx的值.
1.3.2 氧化鐵皮和豎爐球的熔解速率
氧化鐵皮和豎爐球中的主要成分為Fe2O3,但是Fe2O3是強氧化性物質并且其熔點高達1 576 ℃,在1 300 ℃有鐵存在的條件下Fe2O3是不可能存在的,會與Fe 反應生成FeO,高溫下此反應進行得很快,不可能成為限制環節,在轉爐中[Fe]的擴散也不可能是其限制環節,所以只有渣中(Fe2O3)的擴散是限制環節,(Fe2O3)的擴散受其熔化的限制,所以最終的限制環節是氧化鐵皮和豎爐球的熔化[18,19].
用FeO-Fe2O3-SiO2三元相圖計算出在提釩渣系中氧化鐵的飽和質量分數w(Fe2O3)sat,建立簡單的氧化鐵皮和豎爐球熔解模型.假設氧化鐵和豎爐球都是等直徑的球粒,由此得到其球粒的個數:
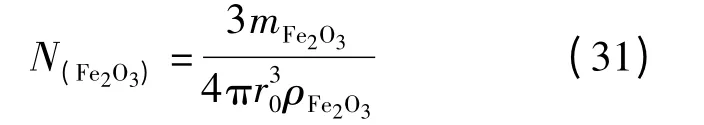
渣中氧化鐵球粒熔解速率為:
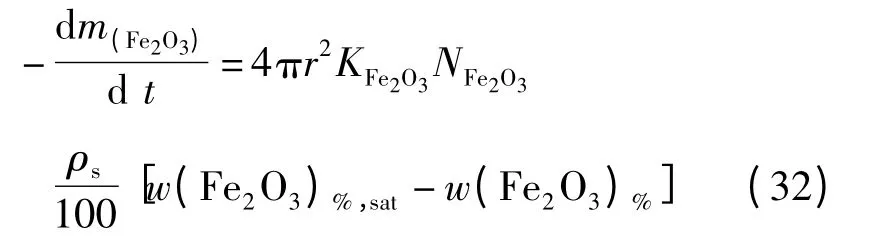
式中,w(Fe2O3)%為渣中Fe2O3的質量分數,%.
1.4 冶煉過程熔池溫度的變化
在提釩冶煉過程中,單位時間熔池的熱量收入主要包括沖擊坑和渣-金界面處各元素氧化反應放熱qL、qsm,以及氧化產物的成渣熱qmix.單位時間熱支出有生鐵塊、釩渣鐵、豎爐球、氧化鐵皮的熔解熱qst、qfz、qsl、qyh,以及底吹氣體(如氮氣)吸熱qN2.對以上單位時間的熱量收支進行平衡計算,可得冶煉過程每一時刻熔池溫度變化率:
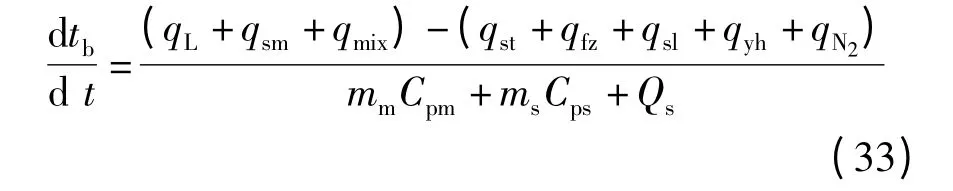
式中,Qs為爐內未熔化的固體冷料含有的總熱量,kJ;mm,ms分別為金屬液質量和熔渣質量,kg;Cpm,Cps分別為金屬液和熔渣的比熱容,kJ/(kg·℃).
2 模型驗證與求解結果分析
2.1 模型驗證
本文為了驗證所建模型的可靠性,結合承德建龍特鋼70 t 復吹提釩轉爐,對半鋼及爐渣成分、熔池溫度進行計算,并結合典型的鐵水成分進行模型驗證,計算結果與現場的數據的對比如表1所示.
由表1 可知,該模型計算結果與實測值吻合較好,其中實測半鋼和實測終渣成分是在半鋼冶煉結束后取樣檢測而得,同時終渣檢測后剔除含量較少的CaO、P2O5、MgO、Al2O3、金屬鐵等組元后對剩余組元含量進行折算,V2O3含量由實測渣中的V2O5和V2O3含量折算得到.
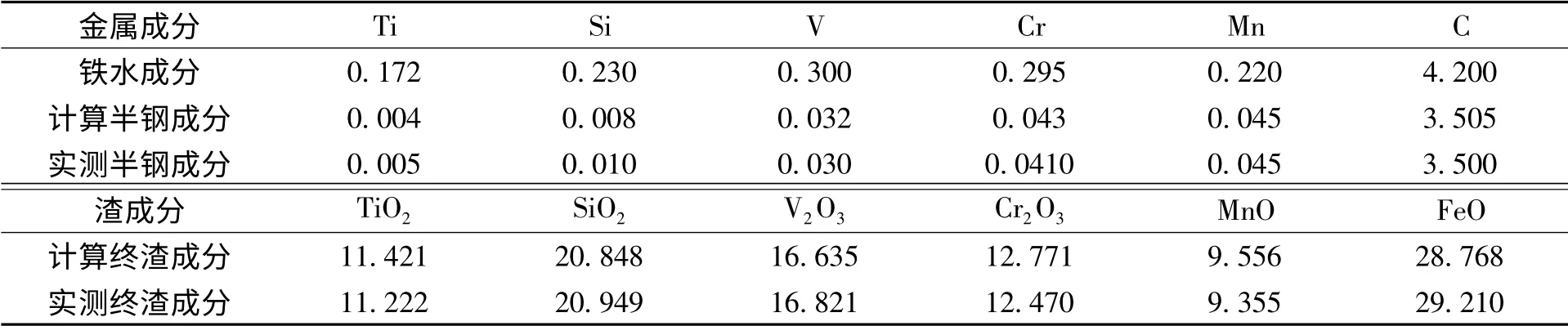
表1 半鋼與釩渣成分(質量分數/%)的計算與實測值對比Table 1 Calculated and measured values for compositions of the semi-steel and the vanadium containing slag %
2.2 結果分析
圖2 是根據表1 鐵液成分進行模型計算的結果.熔池中硅、鈦、釩、鉻、錳、碳組元含量隨吹煉時間的變化如圖2(a)所示.從圖中可以看到,硅、鈦的氧化速率很快,大約吹煉2 min 時硅、鈦的質量分數已基本為零,說明硅、鈦的氧化在吹煉前期已基本結束;吹煉前期,釩的氧化曲線較平滑,說明該時期內,釩氧化速率較小,吹煉2 min 后,曲線斜率迅速增大,釩的氧化速率迅速增加,到4.5 min,曲線斜率減小,接近與橫軸平行,說明在此條件下,釩的氧化已基本結束;鉻和錳的氧化曲線,從2.5 到4.5 min 曲線的斜率較大,說明鉻和錳的氧化速率較大,但在前2.5 min 由于鉻和錳與氧的親和力較其他元素小,故二者氧化速率較小,4.5 min 后氧化速率變小,是由于熔池溫度升高達到了碳錳、碳鉻的氧化還原轉化溫度,因此高溫對錳鉻的氧化不利;碳的氧化曲線從3 min 開始斜率逐漸變大,特別是4.5 min 后斜率最大,這是因為,熔池溫度已經上升到碳與其他元素氧化還原轉化溫度以上,氧槍吹入的氧氣基本用于碳的氧化.
渣中(SiO2)、(TiO2)、(V2O3)、(Cr2O3)、(MnO)和(FeO)組元的含量隨吹煉時間的變化如圖2(b)所示.從圖中可以看到,渣中(SiO2)、(TiO2)和(FeO)的含量在吹煉初期迅速達到各自曲線的最高點,而后隨著吹煉時間的增加曲線平緩下降.這是因為在吹煉初期,由于鐵液中的硅、鈦元素迅速氧化,渣中其他氧化物含量也迅速達到峰值.渣中的氧化亞鐵主要是因為冷料的迅速熔化和鐵水中鐵元素的氧化而來.初渣主要是含二氧化硅、氧化亞鐵較高的酸性、強氧化性渣,隨著吹煉的進行,鐵液中的硅、鈦氧化反應速率逐漸降低,且其他元素氧化反應加快,氧化物進入渣中,導致渣中硅、鈦氧化物含量有所降低.氧化釩、氧化鉻和氧化錳在2 min 后渣中含量開始增加,到4 min 后增加幅度減小,直到吹煉結束達到最大值.
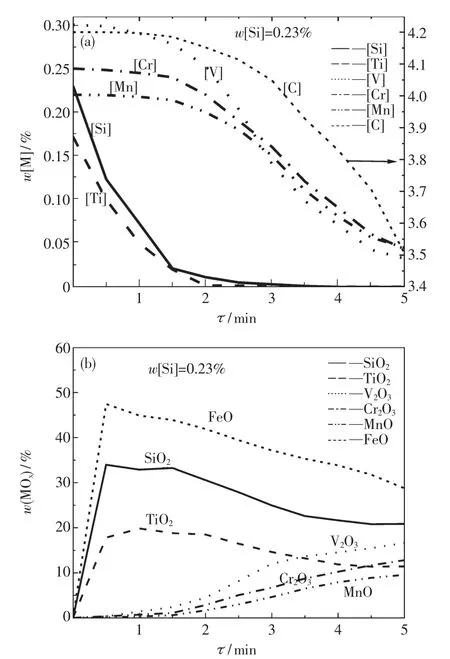
圖2 鐵液、熔渣成分隨吹煉時間的變化Fig.2 Changes of compositions for the hot metal and the slag with the blowing time
圖2 對鐵液中元素和熔渣成分隨時間的變化的分析可得到以下規律:
(1)鐵液中的硅、鈦元素盡可能快地氧化,最好不超過1.5 min.一方面由于硅、鈦的還原性極強,有其大量的存在使釩等其他元素不可能大量的氧化,另一方面硅在前期盡快地氧化不僅有利于促進冷料的熔化,而且可以盡早地形成流動良好的氧化性渣系,以促進鐵液中釩元素的氧化.
(2)降低鐵液中[Cr]、[Mn]的含量有利于中期[V]的氧化.鐵液中硅、鈦氧化結束后,[Cr]、[Mn]、[V]開始氧化,互相之間激烈地爭奪[O],而且放出大量的熱,這對鐵液中[V]的氧化不利.
(3)[C]在中后期開始大量氧化,因此要嚴格控制中后期的溫度,并使后期溫度低于1 390 ℃[6,8],防止溫度過高造成鐵液回釩.

表2 不同鐵水條件下冷料加入量Table 2 Amount of cold materials under different hot metal conditions

圖3 熔池溫度隨吹煉時間的變化Fig.3 Temperature change of molten pool with the blowing time
表2 是在不同鐵水條件下的冷料加入量與供氧制度.圖3 是在表2 條件下的熔池溫度的變化趨勢.由圖3 可以看出在鐵水不同硅含量時,熔池溫度變化的總趨勢基本相同,但在0.5~2 min 有所不同.w[Si]為0.3%、0.23%時,前0.5 min,熔池溫度有小幅上升,0.5 到2 min 時,熔池溫度有小幅下降,這是由于前0.5 min 鈦、硅等元素的氧化放出的熱量超過冷料熔解吸收的熱量,但0.5~2 min 由于冷料大量熔解吸收的熱量超過熔池中元素氧化放的熱,到2 min 時,熔池溫度達到最低值,此時硅和鈦的氧化反應基本結束,2~3 min時,冷料繼續熔解,到3 min 后,冷料熔解已基本結束,熔池溫度迅速上升直到冶煉結束;w[Si]在0.15%時,由于冷料加入量較少,而且冷料大部分是由粒度較大的生鐵塊組成,其熔化速率和熔化吸熱遠小于小粒度的豎爐球,所以冷料熔化吸收的熱量小于元素氧化放出的熱,因此溫度持續上升,不同于w[Si]為0.3%的情況.
從以上分析可得以下結論:0~2 min 隨著鐵中初始硅含量的增加,溫度在1 300 ℃以下的時間在減少,但到2 min 后溫度變化有所不同,在整個吹煉過程中,1 300 ℃以下的時間的長短為:0.23% Si >0.3% Si >0.1% Si.因此,從提釩保碳的角度考慮,高硅和低硅鐵水均不利于冶煉,從熔渣的物理性質考慮硅含量太低熔渣黏度大對冶煉也不利,因此,硅含量有最佳范圍,下面根據現場數據確定硅的范圍.
依據承德建龍特鋼6、7、8 三個月中,不同鐵水Si 含量條件下相應爐次半鋼殘釩量進行了隨機抽取300 爐,并進行統計如圖4.
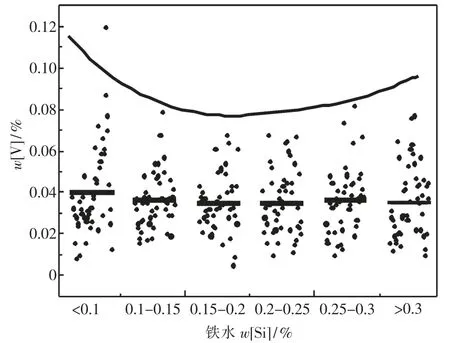
圖4 不同鐵水[Si]含量下半鋼殘釩量w[V]統計值Fig.4 Statistical content of residual vanadium in the emi-steel under different content of[Si]in hot metal
圖4 為不同鐵水[Si]含量下,半鋼殘釩量的統計值.圖中黑色線段為各鐵水w[Si]含量條件下對應的半鋼殘釩量的平均值,黑色曲線為總體殘釩變化趨勢.由圖4 可以看出,半鋼殘釩量隨鐵水[Si]含量的升高呈現出先降低后升高的總體趨勢.鐵水中w[Si]小于0.1%時,對應最高的平均半鋼殘釩量,達到0.04%以上;隨著鐵水[Si]含量的升高,半鋼殘釩量逐步降低,在0.15% <w[Si]<0.20%時,平均殘釩量w[V]降至最低值為0.034%,而且統計各點在平均值附近分布較為集中,也從另一方面說明了在該鐵水[Si]含量內殘釩趨于穩定,有利于操作;鐵水w[Si]>0.25%時,半鋼殘釩量開始升高,在w[Si]>0.3% 以上時,半鋼平均殘釩量w[V]達到0.035%.這由于在低硅含量時,渣量較少,渣中(V2O3)達到飽和所需的量也較少,而且渣中(SiO2)少,渣的黏度較大不利于氧化物的擴散;在高硅時,由于鐵水中硅大量氧化放熱鐵液溫度迅速升高,不利于中后期的保碳,而且鐵液容易回釩.
3 結 論
本文借鑒了煉鋼轉爐控制動力學模型,結合了提釩冶煉過程的特點,建立了描述提釩轉爐冶煉過程的動力學模型,并將模型應用于承德建龍70 t 提釩轉爐冶煉過程的計算.模型的計算結果與現場實測值吻合良好,并分析了轉爐提釩過程中熔池組元、熔渣組成和熔池溫度隨時間的變化規律,得出以下結論:
(1)吹煉初期(0~2 min)鐵液中的[Si]、[V]快速氧化,熔池溫度有小幅上升,有利于盡快形成流動性良好的氧化性渣系.
(2)吹煉中期(2~4.5 min)[V]開始大量氧化及少量[C]的氧化,同時[Cr]、[Mn]的氧化伴隨著整個冶煉的終中后期,尤其中期氧化較為劇烈,因此降低鐵液中[Cr]、[Mn]的含量,有利于中期[V]的氧化.
(3)吹煉后期(4.5~5 min)熔池溫度較高,發生[V]、[C]氧化順序的逆轉,[C]開始大量氧化.因此要嚴格控制后期溫度低于1 390 ℃,防止碳大量氧化和鐵液回釩.
(4)低硅鐵水有利于提釩保碳,同時為了熔渣有良好的物理性質,應控制硅的質量分數在0.15%~0.25%之間.
[1]Li C X,Wei C,Deng Z G,et al.Recovery of vanadium from black shale[J].Transactions of Nonferrous Metals Society of China,2010,20(1):27-31.
[2]付自碧.釩鈦磁鐵礦提釩工藝發展歷程及趨勢[J].中國有色冶金,2011,6(A):30-33.
(Fu Zibi.Development process and trends of vanadium extraction from vanadium-titanium magnetite ore[J].China Nonferrous Metallurgy,2011,6(A):30-33.)
[3]Li X S,Xie B.Extraction of vanadium from calcaium vanadium slag using direct roasting and soda leaching[J].International Journal of Minerals,Metallurgy,and Materials,2012,19(7):595-599.
[4]Zhang S Q,Xie B,Wang Y,et al.Reaction of FeO-V2O5systeMat high temperature[J].Journal of Iron and Steel Research,2012,19(11):33-38.
[5]Howard R L,Richards S R,Welch B J,et al.Vanadium distribution in melts intermediate to ferroalloy production from vanadiferous slag[J].Metallurgical and Materials Transactions B,1994,25(1):27-28.
[6]趙重陽.轉爐提釩靜態控制模型建立與優化的研究[D].重慶:重慶大學,2012:45-50.
(Zhao Chongyang.Establishing and optimizing of static control models for vanadium extraction by converter process[D].Chongqing:Chongqing University,2012:45-50.)
[7]梅彬.轉爐提釩智能控制模型的研究與應用[D].重慶:重慶大學,2002:53-67.
(Mei Bing.The research and application of intelligent control model on oxygen converter devanadium[D].Chongqing:Chongqing University,2002:53-67.)
[8]甄小鵬.轉爐提釩過程中碳、釩氧化的熱力學和宏觀動力學研究[D].重慶:重慶大學,2012:45-55.
(Zhen Xiaopeng.Thermodynamic and macro-kinetic studies on oxidations of carbon and vanadium during vanadium extraction by converter[D].Chongqing: Chongqing University,2012:45-55.)
[9]高圣勇,田志紅,朱立新,等.轉爐鐵水預處理脫磷實驗研究[J].北京科技大學學報,2011,33(1):64-67.
(Gao Shengyong,Tian Zhihong,Zhu Lixin,et al.Study on the dephosphorization of hot metal in converter[J].Journal of University Science and Technology Beijing,2011,33(1):64-67.)
[10]Amaro-Villeda A M,Ramirez-Argaez M A,Conejo A N.Effect of slag properties on mixing phenomena in gas-stirred ladles by physical modeling[J].ISIJ International,2014,54(1):1-8.
[11]許剛,雷洪波,李驚鴻,等.轉爐煉鋼的終點控制技術[J].煉鋼,2011,27(1):66-70.
(Xu Gang,Lei Hongbo,Li Jinghong,et al.End-point control techniques for converter steel-making[J].Steelmaking,2011,27(1):66-70.)
[12]林東,趙成林,張貴玉,等.復吹轉爐煉鋼過程機理模型[J].中國冶金,2006,16(5):31-35.
(Lin Dong,Zhao Chenglin,Zhang Guiyu,et al.Mechanism model steelmaking process in combined blowing converter[J].China Metallurgy,2006,16(5):31-35.)
[13]Wang Z,Chang J,Ju Q P,et al.Prediction model of end-point manganese content for BOF steelmaking process[J].ISIJ International,2012,52(9):1585-1590.
[14]Yu L,Dong Y.Concentrating of vanadium oxide in vanadium rich phase(s)by addition of SiO2in converter slag[J].Ironmaking Steelmaking,2007,34(2):131-134.
[15]肖興國.冶金反應工程學基礎[M].北京:冶金工業出版社,1997:245-247.
(Xiao Xingguo.The base of metallurgical reaction engineering[M].Beijing:Metallurgical Industry Press,1997:245-247.)
[16]Kim S H,Fruehan R J,Guthrie R I L.Physical model studies of slag/metal reactions in gas stirred ladies-determination of critical gas flow rate[J].Iron &Steel Maker,1993,20(11):71-74.
[17]Fabritius T,Riipi J,Jarvinen M,et al.Interfacial phenomena in metal-slag-gas system during AOD process[J].ISIJ International,2010,50(6):797-803.
[18]Gonzalez O J P,Ramirez-Argaez M A,Conejo A N.Mathematical modeling of the melting rate of metallic particles in the electric arc furnace[J].ISIJ International,2010,50(1):9-16.
[19]Arzpeyma N,Widlund O,Ersson M,et al.Mathematical modeling of scrap melting in an EAF using electromagnetic stirring[J].ISIJ International,2013,53(1):48-55.
[20]Qiu X,Xie B,Qing X M,et al.Effects of transition metal oxides on thermal conductivity of mould fluxes[J].Journal of Iron and Steel Research International,2013,20(11):27-32.

