分類解析中考實驗探究題
宋娟


化學實驗探究題是利用化學基礎知識和實驗基本技能知識對化學問題進行實驗探究,旨在考查學生能否使用科學方法來分析和解決實際問題,具有較強的綜合性和靈活性,能力要求較高。縱觀近幾年中考化學試題,化學實驗探究題已逐步成為各省、市中考命題的重點和難點。現對常見中考化學實驗探究題類型歸類解析如下。
一、物質成分的探究
解決此類問題,關鍵是熟練把握物質的性質,特別是酸堿鹽和氧化物類物質的性質,構建起各類物質間反應的結構轉化圖,大膽推測,反復印證。
例1請你閱讀下列短文后,回答有關問題。
“二氧化碳本身沒有毒性,但當空氣中的二氧化碳超過正常含量時,會對人體產生有害影響,所以在人群密集的地方,應該注意通風換氣,保持空氣新鮮。”
(1)根據上述短文,提出一個你想探究的問題: ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 。
(2)對你的問題做出一個比較合理的猜想: ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ?。
(3)請自選用品設計實驗驗證你的猜想,并填寫表1。
表1
操作過程實驗現象結論
思路點撥通過閱讀短文“二氧化碳超過正常含量對人體有害,人群密集地應注意通風換氣”,知道探究目的是“新鮮空氣和人群密集地空氣中二氧化碳含量高低問題”,再根據“人群密集地,應注意通風換氣”提出猜想“人群密集地空氣中二氧化碳含量高”。最后設計如何收集空氣并檢驗空氣中二氧化碳含量的實驗來驗證猜想。
答案:(1)新鮮空氣中的二氧化碳量是否比人群密集的地方中的二氧化碳含量低(其他合理答案也可。但要注意應表述成一個問題,而不是一個肯定的說法,比如“新鮮空氣中的二氧化碳量比人群密集的地方中的二氧化碳含量低”,類似這樣的表述就不符合題意。)
(2)新鮮空氣中的二氧化碳量比人群密集的地方中的二氧化碳含量低。(只要說出合理猜想即可,不必作出解釋。)
(3)(只要學生設計的實驗能夠驗證猜想既可,但要注意應該采用對比的方法進行實驗。)
操作過程實驗現象結論
分別用兩個注射器,在空曠地帶和人群密集地方取兩管氣體,分別注入到盛有澄清石灰水的燒杯中,觀察石灰水變渾濁程度注入在空曠地帶取到的氣體的石灰水,渾濁程度小于注入在人群密集地方取到的氣體的石灰水的渾濁程度新鮮空氣中的二氧化碳量比人群密集的地方中的二氧化碳含量低
二、物質變化條件的探究
該探究是為了研究物質變化的條件和影響物質變化的因素而進行的實驗探究。這里所要探究的物質變化的條件主要有點燃、加熱、催化劑、通電、高溫、高壓等等;而影響物質變化的因素主要是指外界因素(如溫度、濃度、壓強、攪拌、物質的形狀或接觸面積等)。并且,這里的變化既包括物理變化,又包括化學變化。圖1
例2實驗小組欲證明氧化銅能加快氯酸鉀的分解,他們進行了如下實驗:
①稱取x g膽礬晶體,研細后加入10 mL蒸餾水溶解;
②將足量的NaOH溶液與上述溶液充分反應,生成藍色沉淀,過濾后洗滌沉淀;
③將所得沉淀轉移到坩堝中,均勻緩慢加熱至完全變為黑色,研細備用;
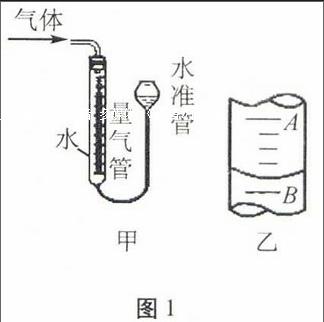
④按表2中的質量混合好固體后,在相同條件下加熱,并與MnO2的催化效果做比較,實驗時間均以生成50 mL氣體為準(見圖1甲),其他可能影響實驗的因素均忽略。
表2
編號KClO3質量(g)其他物質質量(g)待測數據
12.0/
22.0CuO 0.5
32.0MnO2 0.5
回答下列問題:
(1)步驟①中的x應至少稱取g(結果保留1位小數),上述實驗步驟中需要使用玻璃棒的是(填序號)。
(2)表2中的“待測數據”是指。
(3)為了較準確地測量氣體體積,在讀取反應前后量氣管中液面的讀數的過程中,應注意(填字母編號)。
a.視線與凹液面最低處相平;
b.讀數前不能移動量氣管和水準管;c.保持水準管靜止,待水準管中液面不再上升時,立刻讀數;d.讀數前應上下移動水準管,待兩管液面相平再讀數。
(4)若50 mL量氣管中液面的位置如圖1乙所示,A與B刻度間相差1 mL,刻度A為20,則此時氣體的讀數為。
(5)如果要進一步探究CuO在反應中是否起到催化作用,請完成表3后續實驗。(提示:可從催化劑的概念完成實驗。)
表3
實驗步驟設計這一步驟的目的
實驗表明,加入CuO后產生O2的速率比未加入時快得多 CuO能加快KClO3的分解
解析本探究題的目的是證明氧化銅對氯酸鉀的催化作用,過程是先用膽礬通過化學方法制取氧化銅,再讓氧化銅與氯酸鉀混合加熱,并與二氧化錳與氯酸鉀混合加熱比較生成等量氧氣所需的時間,來證明氧化銅對氯酸鉀分解也具有催化作用.計算膽礬的質量應根據需要的氧化銅的質量,可依據銅元素的質量關系進行計算。由于①②③步中有溶解,過濾,轉移固體等操作,所以都要用到玻璃棒,表格中的“待測數據”應是本實驗的關鍵,就是測定反應時間,讀取反應前后量氣管中液面的讀數要準確,方法要規范,如果要進一步探究CuO在反應中是否起到催化作用時,要從催化劑的特點入手,即反應前后催化劑的質量和化學性質都不改變。
解(1)設需要膽礬的質量為x。
CuSO4·5H2O~CuO
250 ? ? ? ? ? 80
x ? ? ? ? ? ?0.5 g
x=1.6 g
由于①②③步中有溶解,過濾,轉移固體等操作,所以都要用的是玻璃棒。
(2)本題的目的是驗證氧化銅的催化作用,關鍵是測定反應時間,所以表格中的“待測數據”就是測定反應時間。
(3)為了較準確地測量氣體體積,在讀取反應前后量氣管中液面的讀數的過程中,視線與凹液面最低處相平,讀數前應上下移動水準管,待兩管液面相平再讀數。
(4)注意量氣管的刻度是上面小,下面大,所以讀數應是20.8 mL。
(5)如果要進一步探究CuO在反應中是否起到催化作用,要從催化劑的特點入手,通過實驗來驗證反應前后催化劑的質量和化學性質都不改變。
答案為:(1)1.6;①②③(2)生成50mL氣體所需時間(3)ad(4)20.8mL
(5)
實驗步驟設計這一步驟的目的
將加熱后殘留的固體溶于足量的水,過濾后稱重CuO的質量CuO的質量在反應前后是否保持不變
將過濾后的CuO重新與KClO3混合加熱,觀察是否依舊能加快KClO3的分解CuO的化學性質在反應前后是否保持不變
三、物質性質的探究
該類探究題要充分利用教材中已有的代表物的性質。在平時的教學中不斷地滲透探究精神,貫穿探究過程,使學生遇到探究性試題有章可循,有方法去突破,找到解題的有效途徑,做到由此及類、一題多解、多題一解的分析問題、解決問題的方法。
例3如圖2是某同學設計的實驗室制取二氧化碳并驗證其性質的實驗裝置圖。
圖2
請回答下列問題:
(1)將A、E裝置連接時,應將A裝置的導管a與E裝置的導管 ? (選填“b”或“c”)相連接。檢驗E裝置中二氧化碳已收集滿的方法是 ? ? 。
(2)將A、B裝置連接,觀察到的現象是 ? ,可驗證二氧化碳的性質是 ? ? ? ? 。
(3)將A、C裝置連接,可驗證二氧化碳與氫氧化鈣反應,該反應的化學方程式為: ? ? 。
(4)用E裝置收集一瓶二氧化碳氣體,取下雙孔橡皮塞,將瓶中的氣體沿D裝置燒杯左側內壁緩慢倒入,觀察到的現象是 ? ? ? ? ? ? ,這些現象說明二氧化碳具有的物理性質 ? ? ? ,化學性質 ? ? ? ? ? , ? ? ? ? ? 。
解析(1)將A、E裝置連接時,應將A裝
置的導管a與E裝置的導管c相連,因為二氧化碳的密度比空氣的密度大,二氧化碳的驗滿方法是:將一根燃著的木條平放在集氣瓶口,木條熄滅,證明滿了;故答案為:c;用燃著的木條靠近E瓶b導管口,木條火焰熄滅。
(2)將A、B裝置連接,觀察到的現象是溶液由紫色變為紅色,因為二氧化碳能與水反應生成碳酸,碳酸能使紫色變紅色,故答案為:溶液由紫色變為紅色;二氧化碳能與水反應生成碳酸。
(3)二氧化碳與氫氧化鈣反應生成碳酸鈣白色沉淀和水,可以用于檢驗二氧化碳氣體的存在,故答案為:Ca(OH)2+CO2CaCO3↓+H2O。
(4)將瓶中的氣體沿D裝置燒杯左側內壁緩慢倒入,觀察到的現象是:燃著的蠟燭由下至上依次熄滅,這些現象說明二氧化碳具有的性質是:二氧化碳的密度比空氣大;不能燃燒,不支持燃燒,故答案為:燃著的蠟燭由下至上依次熄滅;密度比空氣大;不能燃燒;不支持燃燒;
答案:(1) c ? 用燃著的木條靠近E瓶b導管口,木條火焰熄滅。
(2)溶液由紫色變為紅色 ? ? 二氧化碳能與水反應生成碳酸。
(3)Ca(OH)2+CO2CaCO3↓+H2O。
(4)燃著的蠟燭由下至上依次熄滅, 密度比空氣大, 不能燃燒,不支持燃燒。
解化學實驗探究題一定要審好題,明白出題者的考察意圖,思路清晰、層層遞進,把握好推理的思路、方法,注重答題的規范有序;特別是文字敘述一定要簡單明了說明問題即可,同時也要注意書寫的工整,注重卷面的規范,定會取得滿意之效。
(收稿日期:2015-07-15)

