全球醫療器械術語系統(GMDN)應用情況淺析
【作 者】楊婉娟,李 軍,李靜莉
中國食品藥品檢定研究院醫療器械標準管理研究所,北京市,100050
全球醫療器械術語系統(GMDN)應用情況淺析
【作者】楊婉娟,李軍,李靜莉
中國食品藥品檢定研究院醫療器械標準管理研究所,北京市,100050
該文對全球醫療器械術語系統(GMDN)的管理機制、技術架構和全球應用情況進行了梳理,分析了GMDN系統與我國醫療器械產業現狀的協調性,提出應用GMDN系統的建議,為創新我國醫療器械監管手段提供可供借鑒的參考。
醫療器械;全球醫療器械術語系統;應用
規范的醫療器械命名、分類、編碼是醫療器械科學監管的基礎。醫療器械專業跨度大、結構復雜,技術發展快,對層出不窮的新產品進行快速規范命名的難度非常大,一物多名、一名多物現象時有發生,難以進行快速的識別和描述,嚴重影響了注冊、召回等監管效率和醫療管理水平。因此,各國都通過建立產品目錄、命名法等方式來對產品進行描述。
隨著全球化現象日趨升溫,這些結構各異的國家醫療器械術語集逐漸不能適應國際監管需求。各國都在尋找一種“共同語言”,以實現信息互通。建立區域甚至全球通用的命名法或術語集的想法應運而生。2001年歐洲標準委員會(CEN)建成了全球醫療器械術語系統(the Global Medical Device Nomenclature, GMDN)。經過10多年的推廣及發展,GMDN受到了各界關注,很多國家也嘗試應用GMDN來解決注冊、召回、追溯等監管問題。
隨著我國醫療器械進出口規模不斷擴大,科學監管需求的不斷提升,如何認識和參與GMDN的全球協調工作,如何應用GMDN解決我國醫療器械的監管問題,成為目前創新醫療器械監管手段的研究熱點。
1 GMDN管理情況
1.1GMDN的創建
1991年,歐盟、歐洲自由貿易區、加拿大及美國發起全球醫療器械命名協調項目,歐洲標準委員會相繼成立CEN TC/257/SC 1和ISO/TC 210/WG 3(醫療器械符號、編碼和命名法工作組),投入2550,000歐元,集合了來自16個國家約70名醫療器械專家、由一個10人項目委員會、一個6人專家顧問組、一個6人秘書處和若干信息技術人員,于1996年制定出ISO認可的結構標準EN/ISO 15225,并整合各類命名數據庫和新產品信息,于2003年建成GMDN命名法,并授權在英國牛津建立了非營利性機構GMDN機構(GMDN Agency)進行管理維護[1]。
1.2GMDN的管理維護機構
GMDN機構目前有3個部門,其中有6名專職人員(管理、技術各3名):
(1) GMDN機構托管理事會(GMDN BOT) 負責GMDN的運營管理,由6名托管人組成,托管人來自不同的國家和地區,但并不代表任何政府或組織,僅代表個人參與管理。
(2) GMDN政策顧問組(GMDN PAG) 負責對GMDN的管理和術語制定提供建議,由來自GHTF成立國家、AHWP、地區行業和WHO的16位代表組成,以保證國際上主要的法規監管機構、工業界等用戶通過GMDN來協調信息的一致性。
(3) GMDN技術組(GMDN Technical Team) 負責GMDN具體術語的制定,由3名全職專家和2名顧問專家組成。
1.3GMDN的費用政策
GMDN機構以有償會員制度,通過網站或其它方式提供GMDN數據服務及信息產生收益[2]。費用包括會員許可費、代碼申請費、年度審核更新費等。對各國醫療器械監管機構和獲得GMDN機構許可的翻譯機構在許可期間免費,對制造商或經銷商則按不同企業年度營業額規模,收取不同的費用。如年度營業額2~10百萬歐元的企業,會員許可費為1 200歐元,年度更新費為800歐元(含15個),獲取50個代碼費用500歐元。GMDN Agency也可直接向相關國際組織或其它方籌款。
1.4GMDN管理情況分析
GMDN以標準化的形式由多國共同開發,以非營利性質的商業化運作進行管理維護,建立了醫療器械全球流通的“共同語言”,得到國際社會的廣泛關注,但實現全球統一采納GMDN的目標仍需要GMDN機構與各國政府及產業長期的努力:保持持續穩定的維護管理能力;促進各國對GMDN的參與度和話語權的均衡協調,切實反映各方需求;尋求更多的經費支持渠道、探索更易被接受的費用政策;促進GMDN系統與各國數據系統的協調對應,不斷改進完善GMDN的管理。
2 GMDN技術架構
2.1GMDN術語來源
GMDN在早期參考了6個不同的術語集(詳見表1),有的是國家的通用術語集,有的是某領域的專業術語集,術語之間的層次、細化程度、名稱定義的組成及描述方式都有一定差異。GMDN機構通過兩個方式改進:在ISO 9999等有關標準的制定過程中發揮作用,按照GMDN技術流程對有差異的術語進行修正,在對GMDN的長期應用過程中逐步協調各自差異。
2.2GMDN數據結構
GMDN以結構標準ISO 15225為指導,具有三個縱向層次結構的動態體系,每個層次內所定義的術語所表示的器械組的廣度不同,并按順序形成一個相互關聯的結構[4](詳見圖1):17個器械類目(Device Category)、27 570條優選術語(Preferred Term,PT)和超過50萬個器械類型(Device Type)。器械類目是對產品最概括的分類。優選術語是對具有相同或相似預期用途或技術共性的產品的描述。器械類型則指向不同制造商生產的不同規格型號的具體產品。此外還有2 390個集合術語(Collective Term,CT),將具有共同屬性的優選術語進行關聯。
在GMDN網站上,以優選術語為基本構成要素,器械類目、集合術語等作為,建立了網狀數據鏈和檢索系統,各類術語可隨時根據用戶需求不斷更新,構成了市場驅動、快速響應、使用優先的生態型數據系統。用戶可通過術語檢索或分類檢索兩種方式查詢已有產品術語。如無匹配項,可向GMDN機構申請制定新術語。
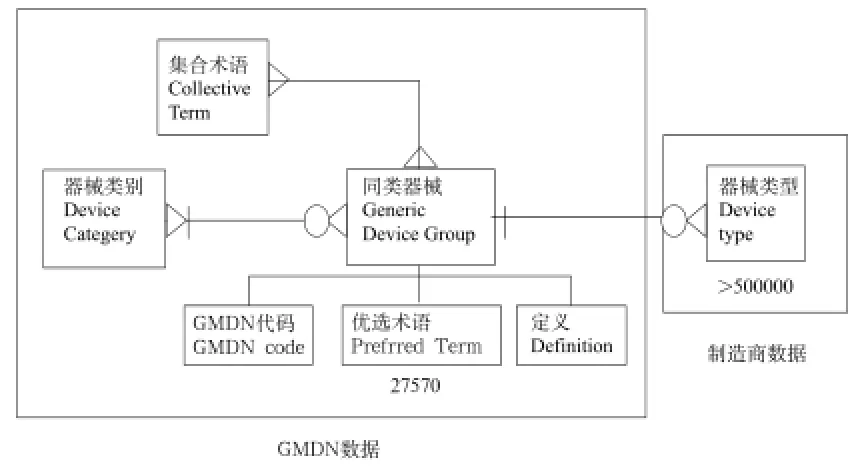
圖1 GMDN數據結構Fig.1 Data structure of GMDN
2.3GMDN技術流程
在GMDN系統中,用以對同類產品進行唯一性識別的是優選術語,由代碼、術語名稱和定義三部分組成。5位流水代碼是識別的核心指標;術語名稱結構包括基本概念和隨附其后的一個或多個限定詞,并用逗號隔開,表示了產品的材質、部位、通用稱謂等,少于120個字符;定義描述了產品的預期用途、使用部位、技術特性及其他強制性特性,少于700個字符。
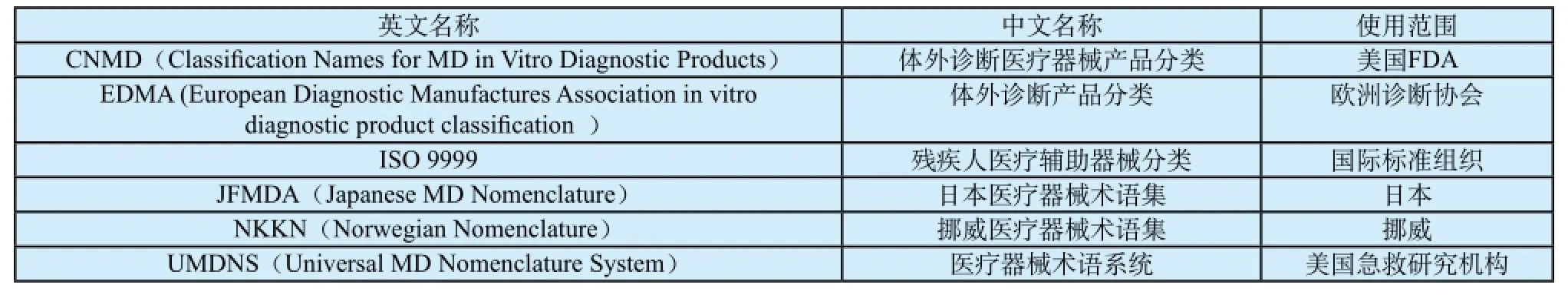
表1 GMDN術語來源Tab.1 The basic source of GMDN
GMDN優選術語制定主要有4項內容,即制定、修訂、廢止、質量控制(詳見圖2),由GMDN 3名技術人員按照標準操作規程制定,必要時組織技術專家論證。GMDN機構每月會接到約50個申請,按照標準流程在3周之內處理完成賦碼、編寫名稱和定義的工作,對于個別的復雜產品,會有30天左右的信息咨詢期。得到授權的機構可以在GMDN網站上在線翻譯GMDN數據,以提供多語言版本,但其術語代碼為翻譯專用4位代碼,并非術語本身的5位代碼。
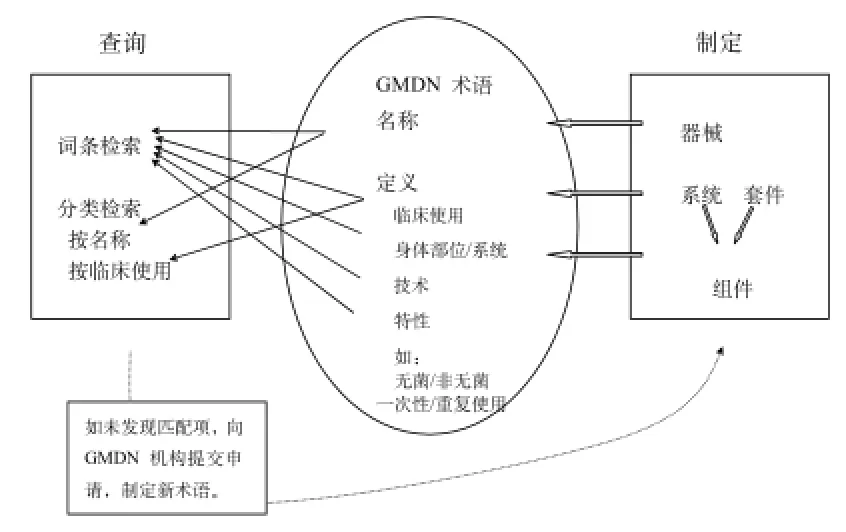
圖2 GMDN術語制定流程Fig.2 GMDN Term Development Overview
2.4GMDN技術架構分析
GMDN是一個基于國際標準而建立的數據庫,由用戶提出術語需求,數據更新快,既可供企業自愿使用,也可在法規的框架下被監管部門所采用,形成法規-標準-數據庫的體系架構,對較為穩定的法規進行補充,滿足技術發展要求。GMDN“代碼—名稱—定義”三位一體的術語結構使用戶對產品的日常管理不再依賴于名稱,企業也不會將此名稱作為產品名稱使用,而是用代碼進行快速識別,并利于消除各國的語言屏障,必要時再查看名稱和定義,對名稱和定義的描述也具有一定規律。這樣的技術理念和架構為醫療器械全球識別提供了可能,不僅在許多跨國企業中得到應用,也得到了多國主管部門的關注。
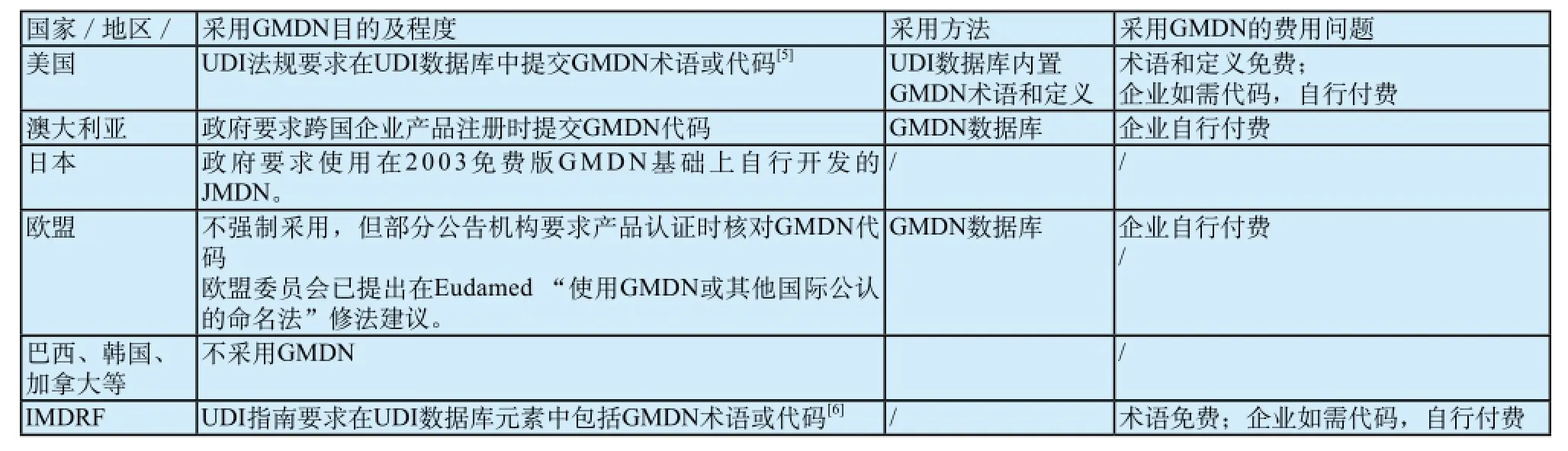
表2 GMDN應用情況Tab.2 The applicaition of GMDN
3 GMDN應用情況
3.1GMDN的功能作用
GMDN并非法規,由各方自愿采用,旨在向監管當局、醫護人員、醫療器械制造商及供應商、合規評估機構及其它相關機構提供能夠維護患者安全的單一術語系統,對同類器械進行識別,進而實現主管當局及其它機構間的數據交換、上市后警戒信息的交換及庫存目的。
GMDN目前主要有兩個方面的實際應用:一是在產品注冊或認證時應用GMDN代碼,使申報、注冊、認證流程更為簡便高效;二是在產品上市后可將GMDN應用于醫療器械警戒系統,還可鎖定特定產品進行稽查、預測警戒數據趨勢、記錄臨床使用情況等;三是在醫療器械唯一標識( UDI)數據庫中使用GMDN,以輔助產品追溯和上市后監管(如產品召回和不良事件分析等)的數據交換和統計分析。GMDN用于成本分析、庫存控制、產品招標、醫保報銷等功能有待進一步探索。
3.2GMDN國外應用情況
GMDN Agency非常重視全球推廣工作,不僅將數據庫向各國監管部門免費開放以供研究,還定期召開PAG會議,聽取監管部門及產業代表意見,致力于制定全球醫療器械識別的“共同語言”。2011年底,GMDN Agency與IHTSDO達成了長期合作協議,將GMDN作為標準臨床術語(SNOMED CT)中的醫療器械部分使用。目前,GMDN已被翻譯為25種文字,全球超過4000個生產企業在使用。但由于監管模式和產業發展程度不同,各國從政府角度采用GMDN的方式也各有差異,詳見表2。
3.3我國參與GMDN工作的情況
全國醫療器械通用標準化技術委員會(SAC TC221)于2003年將GMDN的結構標準《ISO15225:2000 Nomenclature - Specification for a nomenclature system for medical devices for the purpose of regulatory data exchange?》[7]等同轉化為我國的行業標準《YY/T 0468-2003 命名 用于管理資料交流的醫療器械命名系統規范》[8],目前正在對最新版《ISO 15225:2010 Medical devices-Quality management—Medical device nomenclature data structure》[9]進行轉化。我國目前有300多家生產企業為滿足國際貿易需求,自發申請成為GMDN會員,中國醫療器械行業協會也為爭取中國企業的待遇與GMDN機構進行了多次溝通。2006年以來,國家食品藥品監督管理總局作為亞洲協調工作組(Asian Harmonization Working Party,AHWP)的代表參與GMDN PAG工作,共同推進國際法規協調進展。
3.4GMDN應用情況分析
GMDN是一個可以根據用戶需求不斷改進完善的數據系統,政府監管部門如何應用GMDN,將直接影響GMDN發展,因此需要各國在GMDN PAG內不斷發揮作用,根據自己的應用體驗對GMDN整體管理、費用政策、翻譯轉化及術語制定、應用推廣等方面提出需求,例如:如何在不引起注冊問題的情況下,逐步平穩取代不合適的GMDN代碼;如何擴展GMDN除注冊與召回以外的其他功能作用;如何解決在法規中采用收費系統的問題;以什么方式實現GMDN數據系統與各國注冊系統和UDI系統的對接。
4 對我國GMDN相關工作的思考和建議
4.1加深對GMDN 的認識和理解
GMDN中“global”指的是面向全球的產品,而非一個全球組織或全球公認系統;“medical device”指的是健康相關設備,與各國監管部門嚴格意義上的“醫療器械”略有差距;“nomenclature”在國家標準《GB/T 15237.1-2000 術語工作 詞匯 第1部分:理論與應用(ISO 1087.1-2000, EQU)》中表示“術語系統”,GMDN實際上是“按一個國際標準構建的健康相關設備的術語系統”,是全球醫療器械識別的“大字典”。GMDN識別的關鍵指標是優選術語代碼,術語名稱和術語定義是對代碼指向的描述,并非產品名稱。為避免概念混淆,建議在轉化2010年最新版ISO 15225時對2003年版的翻譯做一些調整:將“nomenclature”由“命名系統”改譯為“術語系統”。
4.2持續關注和積極參與GMDN發展
GMDN在構建全球“醫療器械共同語言”方面具有優勢,促進GMDN的應用對醫療器械產業國際化和全球法規協調都有重要意義。但現階段我國對GMDN的認識不夠深入、參與度不足,一些企業對GMDN的應用還停留在對進口國要求的被動合規階段。因此,應進一步發揮中國在IMDRF和GMDN PAG當中的作用,充分反映我國的需求和建議;加快我國的研究步伐,尋求技術方面的交流合作,尤其是在中醫診療設備等特色領域及一些新興領域,不斷提高我國在國際醫療器械命名協調工作中的話語權,共同促進GMDN的發展。
4.3加強對GMDN的應用推廣和技術研究
隨著我國醫療器械進出口規模的不斷擴大,GMDN的應用需求將逐步增加,可從多方面規范和促進GMDN的應用:一可采取法規以外的形式,如轉化標準、制定技術指南或翻譯GMDN數據等技術手段,規范指導企業對GMDN的自發采用;二可借鑒美國UDI實施經驗,進一步研究在醫療器械編碼數據庫中應用GMDN的方式;三是在完善我國醫療器械分類命名體系時充分考慮與《ISO 15225》的協調和與GMDN數據的關聯對應。
感謝GMDN機構Mark Wasmuth、Dr Barry Daniels和歐盟委員會衛生與消費者總司Laurent SELLES、Susanne Hke等提供的幫助,強生公司瞿鐳、潘曄、中國醫療器械有限公司朱學軍、施樂輝公司王宇紅、樂普公司戴燕、奧林巴斯陳東、希森美康蘇靜、TüV SUD中國屈寶鋼、貝朗公司陳燕華等對本文亦有貢獻,一并致謝。
[1] 常永亨. 全球統一醫療器械命名的趨勢[J]. 世界醫療器械, 2013, 19(3): 14-19.
[2] GMDN Agency Ltd. GMDN User Guide version 2012.1[M]. 2012.
[3] 岳偉. 對醫療器械命名規則和分類目錄的見解[J]. 中國醫療器械雜志, 2010, 34(1): 44-46.
[4] 陶立. 醫療器械統一命名[J]. 世界醫療器械, 2013, 19(3): 44-48.
[5] IMDRF UDI Working Group. UDI Guidance: Unique Device Identification (UDI) of Medical Devices[EB/OL]. http://www. imdrf.org/docs/imdrf/final/technical/imdrf-tech-131209-udiguidance.pdf. 2013-12-09.
[6] Food and Drug Administration. the Unique Device Identification System Final Rule[EB/OL]. https://www. federalregister. gov/ articles/2013/09/24/2013-23059/unique-device-identificationsystem. 2013-09-24.
[7] ISO/TC 210. ISO 15225:2000 Nomenclature-Specification for a nomenclature system for medical devices for the purpose of regulatory data exchange[S].
[8] ISO/TC 210. ISO 15225: 2010 Medical devices—Quality management—Medical device nomenclature data structure[S].
[9] 國家食品藥品監督管理局. YY/T 0468-2003 命名 用于管理資料交流的醫療器械命名系統規范[S].
The Analysis on Application of
Global Medical Device Nomenclature(GMDN)
【 Writers 】YANG Wanjuan, LI Jun, LI Jingli
Institute for Medical Device Standardization Administration, NIFDC, Beijing, 100050
The article has reviewed the administration、technical structure and global application of the global medical device nomenclature(GMDN), analyzed the coordination between GMDN and the industry status of medical device in our country, put forward some suggestions on the applicaition of GMDN, provided some reference on raising the management level of medical device in our country。
medical device, GMDN, application
F203
A
10.3969/j.issn.1671-7104.2015.04.011
1671-7104(2015)04-0275-04
2015-04-17
國家食品藥品監督管理總局政策研究課題(H201403)
楊婉娟,E-mail: yangwj@nifdc.org.cn
李靜莉,E-mail: jingli1996@sina.com

