CdTe 量子點熒光猝滅法測定四環素
李娜,李卓然,劉聰,毛永強
(遼寧工程技術大學 理學院,遼寧 阜新 123000)
四環素(TC)是一種廣譜抗生素,在畜牧業生產中曾經作為獸藥或飼料添加劑而廣泛使用。然而四環素容易在畜禽體內殘留,通過食物鏈進而危害人體健康[1]。現有四環素檢測方法主要有微生物法[2]、紫外分光光度法[3]、液相色譜法[4]、液相色譜-質譜聯用法[5]、酶聯免疫法[6]等。量子點(QDs)作為一種熒光納米材料,具有特有的量子尺寸效應和表面效應及其獨特的光學和電學性質,以量子點為熒光探針,已廣泛應用于致病菌[7]、生物毒素[8]、生化藥物[9]和重金屬離子[10]等分析檢測領域。
本文以巰基乙酸為修飾劑水熱法制備水溶性CdTe 量子點,基于四環素對CdTe 量子點的熒光猝滅效應,研究CdTe 量子點熒光猝滅法測定四環素的最適宜條件,建立一種測定四環素含量的熒光分析法。該方法操作簡單、選擇性好、靈敏度高,已成功用于實際樣品中四環素含量的測定。
1 實驗部分
1.1 試劑與儀器
四環素,中國藥品生物制品檢定所;碲粉、硼氫化鈉、巰基乙酸、氯化鎘(CdCl2·2.5H2O)均為分析純;實驗用水為二次蒸餾水。
F-4500 型熒光分光光度計;AUX320 型電子分析天平;pHS-3C 型pH 計;DF-101S 型集熱式恒溫加熱磁力攪拌器;KQ-50DB 型數控超聲波清洗器;DZF-6050 真空干燥箱。
1.2 水溶性CdTe 量子點的制備
參照文獻方法以巰基乙酸為修飾劑制備水溶性CdTe 量子點[11]。準確稱取47 mg 硼氫化鈉和80 mg 碲粉于反應瓶中,加3 mL 蒸餾水溶解,冰水浴中反應8 h,得到淡藍色NaHTe 溶液。在500 mL三口燒瓶中加入0.285 g 氯化鎘,加入200 mL 蒸餾水溶解,磁力攪拌下,加入213 μL 巰基乙酸,用0.5 mol/L NaOH 溶液調節pH 值為11.0,通氮氣30 min 后,加入新制備的NaHTe 溶液;繼續通氮氣30 min 后,100 ℃水浴反應2 h,得到紅色透明的水溶性CdTe 量子點溶液。
1.3 四環素的測定
在5 mL 比色管中依次加入1 mL 的CdTe 量子點溶液、1 mL 的Tris-HCl 緩沖溶液(pH 6.5)和一定量的四環素溶液,用蒸餾水定容到刻度,搖勻。室溫下放置5 min 后,于激發波長λex=330 nm 和發射波長λex=520 nm 處,激發和發射狹縫均為5 nm,測定體系的熒光強度F 和試劑空白的熒光強度F0,計算體系熒光猝滅強度ΔF=F0-F。
2 結果與討論
2.1 CdTe 量子點與四環素相互作用的熒光光譜
考察加入四環素溶液前后CdTe 量子點溶液的熒光光譜性質,結果見圖1。

圖1 不同濃度四環素存在下CdTe 量子點的熒光光譜圖Fig.1 Fluorescence spectra of CdTe QDs in the presence TC with various concentrations
由圖1 可知,巰基乙酸修飾的CdTe 量子點在激發波長330 nm 時,CdTe 量子點的熒光發射峰位于520 nm 處;當四環素加入CdTe 量子點溶液后,其熒光強度明顯被猝滅,且CdTe 量子點熒光強度隨著四環素濃度的增加而逐漸降低,這構成熒光法測定四環素含量的基礎。
2.2 最佳實驗條件選擇
2.2.1 反應介質及pH 值的選擇 考察不同pH 值下NaH2PO4-Na2HPO4緩沖溶液、Tris-HCl 緩沖溶液及其濃度對體系熒光猝滅強度ΔF 的影響。結果表明,當pH 值6.5 的Tris-HCl 緩沖溶液達到5.0 ×10-3mol/L 時,ΔF 達到最大且相對穩定。因此實驗選擇pH 值6.5 的5.0 ×10-3mol/L 的Tris-HCl 溶液作為反應緩沖體系。
2.2.2 CdTe 量子點濃度的選擇 考察CdTe 量子點濃度對體系熒光猝滅強度ΔF 的影響。結果表明,隨著CdTe 量子點濃度的增加,ΔF 逐漸增大;當CdTe 量子點濃度為8.0 ×10-6mol/L 時,ΔF 達到最大;但繼續增加其濃度,ΔF 基本趨于不變。因此實驗選擇CdTe 量子點濃度為8.0 ×10-6mol/L。
2.2.3 反應時間的選擇 考察反應時間對體系熒光猝滅強度ΔF 的影響。結果表明,當四環素溶液加入CdTe 量子點溶液5 min 后,ΔF 達到最大且趨于穩定。因此實驗選擇反應5 min 后測定體系熒光強度。
2.2.4 共存物質的影響 在最佳實驗條件下,當四環素濃度為1.0 μg/mL、相對誤差為±5.0%時,考察常見共存物質對四環素測定的影響。結果表明,500 倍的K+、Na+、Mg2+、Ca2+、Zn2+、NO3-、Cl-、對測定無影響;但Cu2+、Hg2+、Ag+濃度較高時會對測定產生干擾,可采用巰基棉處理來消除其干擾。
2.3 工作曲線和檢出限
在最佳實驗條件下,分別取不同濃度四環素溶液加入到一定濃度的CdTe 量子點溶液中,考察四環素與CdTe 量子點相互作用的熒光光譜,并以體系熒光猝滅強度ΔF 對四環素濃度c 繪制工作曲線,結果見圖2。
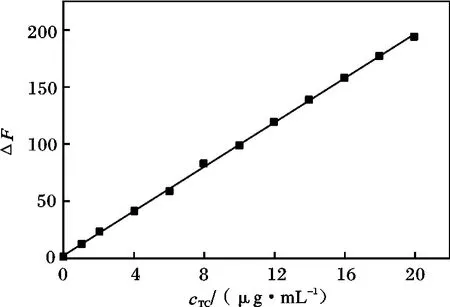
圖2 標準曲線Fig.2 Standard curve
由圖2 可知,四環素濃度在1.0 ~20.0 μg/mL范圍內與體系熒光猝滅強度ΔF 呈良好的線性關系,工作曲線為ΔF =2.308 2 +9.679 3c(μg/mL),相關系數r 為0.999 5,檢出限為0.025 μg/mL(按3SD/斜率計算,其中SD 為11 份空白溶液的標準偏差)。
2.4 樣品測定
取四環素膠囊,研成粉末后準確稱取適量,用0.01 mol/L 稀鹽酸溶解并過濾,用蒸餾水定容于100 mL 容量瓶中。移取處理后樣品溶液用巰基棉處理后,按實驗方法對樣品中四環素進行測定,同時進行加標回收實驗,結果見表1。
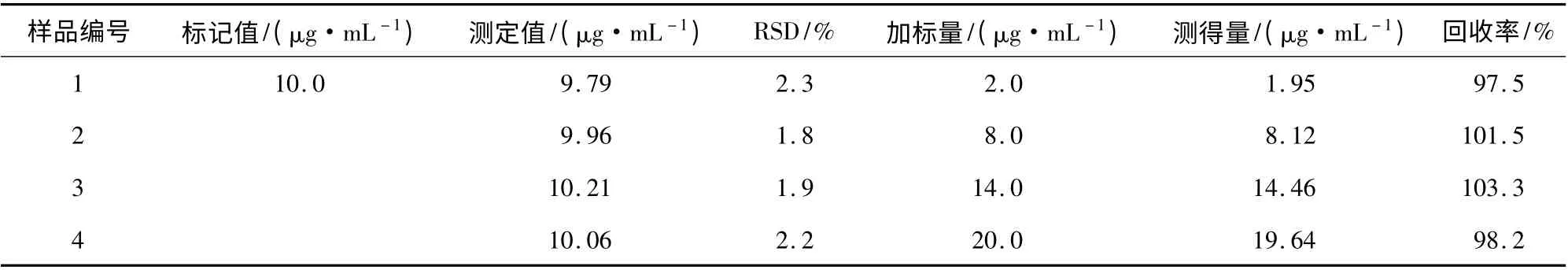
表1 樣品測定結果Table 1 Determination results of samples
由表1 可知,所測樣品的相對標準偏差(RSD)<2.3%,加標回收率在97.5% ~103.3%,表明該方法可用于藥物中四環素含量的定量測定。
3 結論
以巰基乙酸為修飾劑制備水溶性CdTe 量子點,基于四環素對CdTe 量子點的熒光猝滅作用,建立一種測定四環素含量的熒光分析法。在最佳實驗條件下,體系的熒光猝滅強度與四環素濃度在1.0 ~20.0 μg/mL 范圍內呈良好的線性關系。該方法操作簡便、選擇性好、靈敏度高,可用于藥物中四環素含量的測定。
[1] 張憲,張坤.PMoA/CS/P25 納米復合光催化劑的制備及光催化降解鹽酸四環素[J].應用化工,2014,43(5):791-794.
[2] Kanda M,Kusano T,Osanai T,et al.Rapid determination of residues of 4 tetracyclines in meat by a microbiological screening,HPLC and LC/MS/MS[J].Journal of the Food Hygienic Society of Japan,2008,49(1):37-44.
[3] 馮學忠,吳廣輝,方炳虎,等.紫外分光光度法測定長效四環素注射液含量方法的建立[J].動物醫學進展,2009,30(9):65-68.
[4] 王敏,馬玉龍,馬琳,等.高效液相色譜法同時檢測藥渣中四環素及其衍生物[J].湖北農業科學,2014,53(6):1411-1414.
[5] 鐘冬蓮,丁明,湯富彬,等.高效液相色譜-電噴霧串聯質譜法測定畜禽糞便中四環素類抗生素[J].分析科學學報,2014,30(3):433-436.
[6] 國占寶,武玉香,田文禮,等.食品中四環素類殘留的酶聯免疫檢測試劑盒的研制[J].食品科學,2011,32(2):333-337.
[7] 王洪江,柳婷,謝躋,等.CdS 量子點制備與單增李斯特菌抗體偶聯的研究[J].分析化學,2010,38(5):632-637.
[8] 楊淑平,金鑫,鄭佳,等.高性能CdTe/CdS 核殼型量子點的制備及應用于小麥面粉中嘔吐毒素的熒光免疫檢測研究[J].化學學報,2011,69(6):687-692.
[9] 周曉燕,李在均,王光麗,等.手性CdTe 量子點制備及在藥物青霉胺對映體檢測中的應用[J].分析試驗室,2013,32(9):1-5.
[10]杜保安,劉澄,曹雨虹,等.ZnS ∶Mn 量子點作磷光探針定量檢測微量汞[J].光譜學與光譜分析,2014,34(4):1070-1074.
[11]梁佳然,鐘文英,于俊生.高質量CdTe 量子點的水相快速合成[J].高等學校化學學報,2009,30(1):14-18.

