植物葉片中硫含量測定方法研究
楊璐,依麗米努爾,朱苗苗,李宏*
(1.新疆林業科學院,新疆 烏魯木齊 830002;2.新疆農業大學 林學與園藝學院,新疆 烏魯木齊 830052)
硫是植物生長必需的礦質營養元素之一,是繼氮、磷、鉀之后第四位植物生長必需的營養元素[1],幾乎所有蛋白質都有含硫氨基酸,因此硫在植物細胞的結構和功能中都有著重要作用。硫不僅是蛋白質和氨基酸的組成成分,而且參與許多酶、輔酶和硫胺類等生理活性物質的組成,參與有氧呼吸作用、氮素代謝、脂肪代謝、淀粉合成和生物固氮作用等重要生理生化過程[2]。研究表明,硫能促進豆科作物形成根瘤,參與固氮酶的形成[3];硫元素能提高氨基酸、蛋白質含量,進而提升農產品品質[4]。同時,植物對一定濃度范圍內的大氣污染物不僅具有一定程度的抵抗力,而且具有一定程度的吸收凈化能力,通過植物葉片中的含硫量檢測大氣環境中二氧化硫的濃度[5-7]。因此,硫的測定對于環境科學和生態學的研究均有重要意義。本文采用單因素實驗對硫酸鋇比濁法測定植物葉片中的硫含量進行了系統的研究,旨在建立一種簡便、快捷測定植物葉片中硫含量的方法。
1 實驗部分
1.1 試劑與儀器
Na2SO4、BaCl2均為優級純;Na2CO3、硝酸、鹽酸、甘油、無水乙醇、丙酮、吐溫80 均為分析純。
UV-2600 紫外可見光分光光度計;F6020C-33-80 馬弗爐;DHG-9053A 烘箱;C-MAG HP10 電熱板;TW20 水浴鍋;C-MAG HS4 磁力攪拌器;TP-214 萬分之一天平。
1.2 實驗方法
1.2.1 樣品處理 對從現場采集的新鮮植物葉片樣品立即用自來水洗2 ~3 次,去除葉面塵埃及附著物,再用去離子水沖洗2 次,自然晾干后置于鼓風干燥箱中在70 ℃下烘30 min,然后105 ℃下烘至恒重。將烘干的樣品用電動粉碎機粉碎,過60 ~80 mm 篩孔,得到粉末狀樣品,備用。
樣品處理參考吳名劍等[8]的方法,略有改動。精確稱取適量樣品1.000 g 于瓷坩堝中,加入2 mL 5% Na2CO3溶液,攪拌均勻,調節溫度300 ℃烘干至完全炭化,然后移入馬弗爐中先調節溫度300 ℃1 h 后逐步升溫至600 ℃,灰化2 h 后取出,冷卻后加入10 mL 2%鹽酸,電熱板100 ℃加熱20 min,過濾,濾液至于25 mL 容量瓶中,用去離子水稀釋至刻度,搖勻,即得供試品溶液。
1.2.2 樣品測定 取2 mL 供試品溶液,置于25 mL 容量瓶中,加入2 mL 甘油-乙醇(1 ∶1)保護劑,加入少量去離子水稀釋,搖勻,加入10 mg/mL BaCl2溶液2 mL,再加入25% HCl 溶液2 mL,用去離子水稀釋至刻度,搖勻后靜置3 min,倒入1 cm 石英比色皿中,以試劑空白作參比,在波長470 nm 下測定其吸光度,并計算樣品中的硫含量。
2 結果與討論
2.1 吸收波長的選擇
取樣品濃度16 μg/mL 的硫標準溶液,按照實驗方法在200 ~600 nm 進行波長掃描,其吸收曲線顯示,在450 ~475 nm 該體系吸收值較穩定,在470 nm波長處體系有最大吸收峰,故實驗選擇470 nm 為測量波長。
2.2 加入不同酸的穩定性實驗
取硫標準溶液,分三組,a 組不加任何酸,b 組加HCl(體積比1 ∶3)1 mL、c 組加HNO3(體積比1 ∶3)1 mL,按文獻方法,以相應的試劑空白作參比,測定吸光度值觀察30 min,每5 min 記錄1 次,結果見圖1。
由圖1 可知,不加酸的一組測定的吸光度不穩定,忽高忽低,變異系數為9.2%。加酸的兩組吸光度均較為穩定,隨著時間的延長略有下降。加HCl組吸收值比加HNO3組的吸光度值大,且較穩定,因此,選擇在比色體系中加入HCl。
溶液酸度的高低即是H+濃度的高低,它對沉淀反應有一定的影響[9],當溶液中酸度較低或較高時均會影響吸光度的穩定性,需在合適的酸度范圍內進行沉淀反應,才能使形成的懸濁液測得的吸光度高而穩定[6,10]。進一步對HCl(體積比1 ∶3)用量進行考察。取硫標準溶液,加入0.50,1.00,1.50,2.00,3.00,4.00,5.00 mL 的HCl(體積比1 ∶3)溶液,按實驗方法,以相應的試劑空白作參比,測定吸光度見圖2。
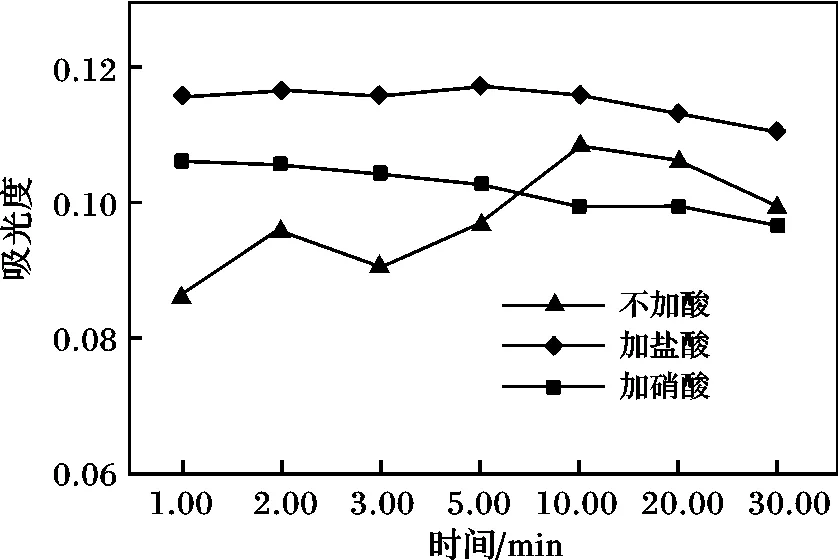
圖1 加入不同酸的穩定性實驗Fig.1 The stability test of different acid
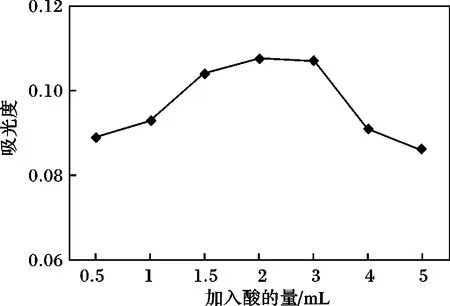
圖2 鹽酸用量對吸光度的影響Fig.2 The influence on the absorbance of different amount of hydrochloric acid
由圖2 可知,當鹽酸(體積比1 ∶3)加入量為2 mL 時吸光度值最高。
2.3 膠體保護劑的選擇
2.3.1 不加任何膠體保護劑時不同SO2-4 濃度的穩定性實驗 分別取0.00,1.00,3.00,4.00,5.00,6.00,8.00 mL 硫標準溶液,至25 mL 容量瓶中,用文獻實驗方法[11],以相應的試劑空白作參比,靜置1 min 后立刻倒入l cm 石英比色皿中,在波長470 nm下測定其吸光度,觀察45 min,前10 min 每2 min記錄1 次,之后每5 min 記錄1 次,見圖3。
由圖3 可知,不加任何有機試劑時,BaSO4膠體吸光度值在8 min 內較穩定,8 min 后除濃度為4 μg/mL 外其它各個濃度的吸光度值均逐漸下降,濃度越大,吸光度下降越快,是由于BaSO4膠體顆粒沉降造成的。在未添加膠體保護劑的條件下,BaSO4膠體的穩定性較弱,因此需要加入適當的穩定劑。
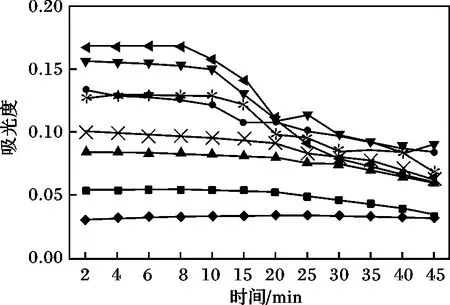
圖3 不加保護劑的穩定性實驗Fig.3 The stability test without stabilizer
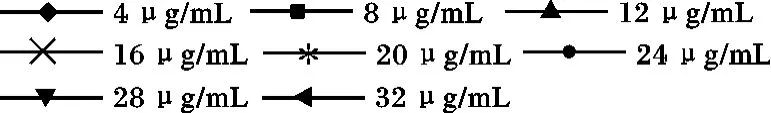
2.3.2 加入不同有機試劑作保護劑的穩定性實驗
膠體穩定劑能控制生成BaSO4晶粒的大小,增加膠粒的親水性,同時增加介質的粘度,以利于分散相的穩定防止BaSO4膠體顆粒的沉淀,使其在體系中分散均勻、穩定時間長,使測得的吸光度穩定可靠[9]。取4 mL 硫標準溶液,分別加入甘油、丙酮、無水乙醇、吐溫80、甘油-乙醇(1 ∶1)各2 mL,按實驗方法,以相應的試劑空白作參比,測定吸光度,觀察45 min,前5 min 每1 min 記錄1 次,之后每5 min 記錄1 次,見圖4。
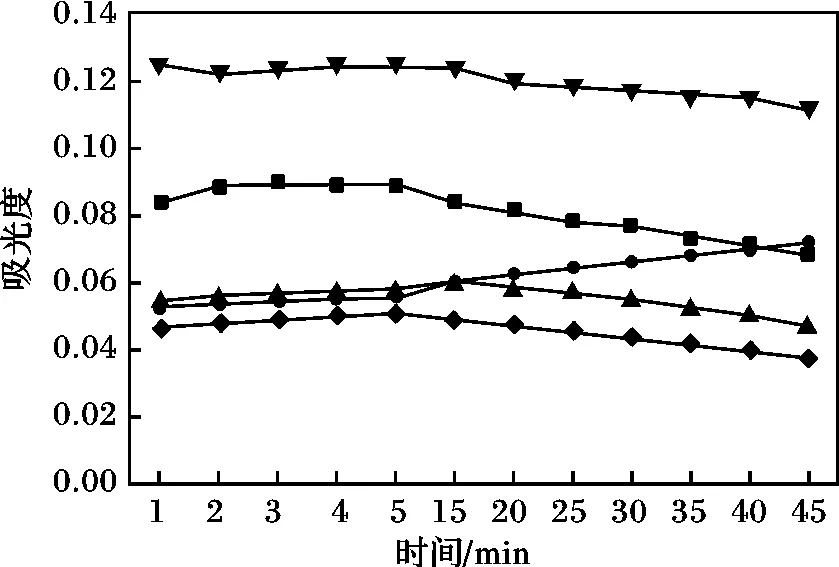
圖4 保護劑的選擇Fig.4 The test of choice stabilizer

由圖4 可知,加入丙酮等有機試劑后,膠體吸光度值穩定時間至少達45 min。但不同的保護劑有不同的效果:加丙酮、甘油、無水乙醇、吐溫80、甘油-乙醇(1 ∶1)穩定劑均較穩定,但是加甘油-乙醇(1 ∶1)的吸光度值最大且穩定性較好,所以選擇甘油-乙醇(1 ∶1)作保護劑。
進一步對膠體保護劑的用量進行考察。取硫標準溶液濃度16 μg/mL 時,分別加入0.5,1.0,2.0,3.00,4.00,5.00 mL 保護劑,按照實驗方法,以相應的試劑空白作參比,測定吸光度,見圖5。添加保護劑的用量要在適宜的范圍內體系才較為穩定,保護劑含量過低使體系穩定性降低,保護劑含量過高使體系不易澄清影響比色。
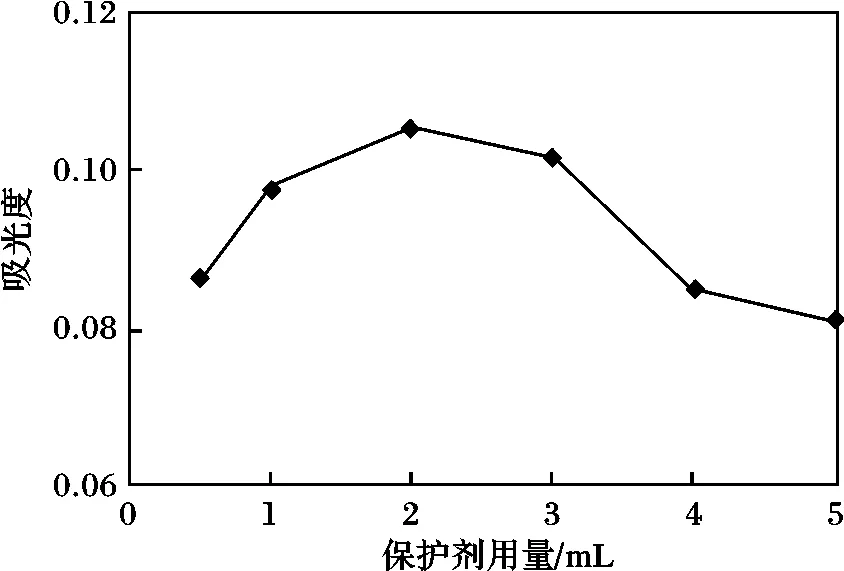
圖5 保護劑用量對吸光度的影響Fig.5 The influence on the absorbance of different amount of stabilizer
由圖5 可知,在加入保護劑2 mL 時體系有最大的吸光度值,因此確定保護劑用量為2 mL。
進一步對加入膠體保護劑后不同SO2-4濃度的穩定性進行考察。以甘油-乙醇(1 ∶1)作為膠體保護劑,在不同SO2-4濃度時的穩定性實驗,按實驗方法,以相應的試劑空白作參比,測定吸光度,觀察45 min,前5 min 每1 min 記錄1 次,之后每2 min 記錄1 次,到10 min 后每5 min 記錄1 次,見圖6。
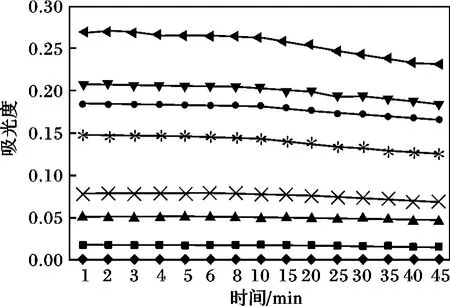
圖6 加保護劑后不同SO2-4 濃度的穩定性Fig.6 The stability test of stabilizer

由圖6 可知,在體系中加入2 mL 甘油-乙醇(1 ∶1)作為膠體保護劑,在不同SO2-4濃度下體系的穩定性較好。
2.4 BaCl2 形態及劑量影響
目前普遍使用的方法是將BaCl2·H2O 晶體研細,過篩0.25 ~0.5 mm 后使用,本實驗選用此方法和配制成10%BaCl2溶液作為實驗條件進行對比,見圖7。
由圖7 可知,加入10% BaCl2溶液作為實驗條件的穩定性較好,變異系數為0.82%。加入BaCl2·H2O 晶體顆粒的穩定性較差,變異系數為7.5%。在沉淀的形成過程中,加入液體BaCl2則為液-液反應,此時溶液中的微小顆粒相互發生反應,反應速度較快。當加入一定粒級范圍內均勻的固體BaCl2時則為固-液反應,不利于BaSO4的形成和均勻懸浮,在30 min 內吸光度呈持續上升趨勢。

圖7 氯化鋇形態的選擇Fig.7 The test of form of BaCl2
2.5 BaCl2 溶液用量考察
取標準品濃度16 μg/mL 時,加入2 mL 甘油-乙醇(1 ∶1)保護劑,用去離子水稀釋到20 mL 左右,分別加入0.5,1.00,1.50,2.00,3.00,4.00,5.00 mL 10 mg/mL BaCl2溶液,再加入2 mL 25% HCl 溶液,用去離子水稀釋至刻度,搖勻,靜置3 min,傾入1 cm玻璃比色皿中,以試劑空白作參比,在波長470 nm下測定其吸光度,見圖8。
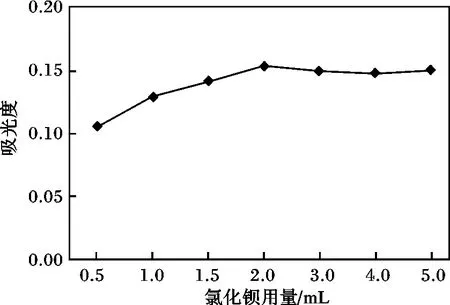
圖8 氯化鋇用量的選擇Fig.8 The test of content of BaCl2
由圖8 可知,BaCl2溶液用量在2 ~5 mL 吸光度最大且穩定。
當溶液中BaSO4的結晶速度大于溶解速度時,溶液中BaSO4晶體顆粒數逐漸增加,吸光度逐漸上升,當體系達到平衡時吸光度最高。如果繼續加入BaCl2,體系中Ba2+濃度遠遠超過其沉淀反應所需要的量,導致部分沉淀聚沉并且使沉淀溶解度增大,因此BaCl2加入量需在適量范圍內,根據實驗結果選擇BaCl2加入量2 mL 為宜。
2.6 溫度選擇
取標準品濃度16 μg/mL 時,按照實驗方法,分別在20,30,40,50,60,70,80,90 ℃下加熱10 min,冷卻,測量吸光度值,分析溫度對吸光度的影響。由圖9 可知,加熱溫度20 ~40 ℃吸光度值較穩定,加熱溫度超過50 ℃后吸光度值呈逐漸下降趨勢。溫度對硫酸鋇比濁法的吸光度的影響有正反兩方面,一方面,溫度升高可以縮短沉淀的陳化時間加速轉化為晶體大顆粒使吸光度增大;另一方面,溫度升高使沉淀的溶解度增大吸光度下降。結合本實驗的結果,為測定方法簡單易行且穩定性好,選擇在室溫下進行。
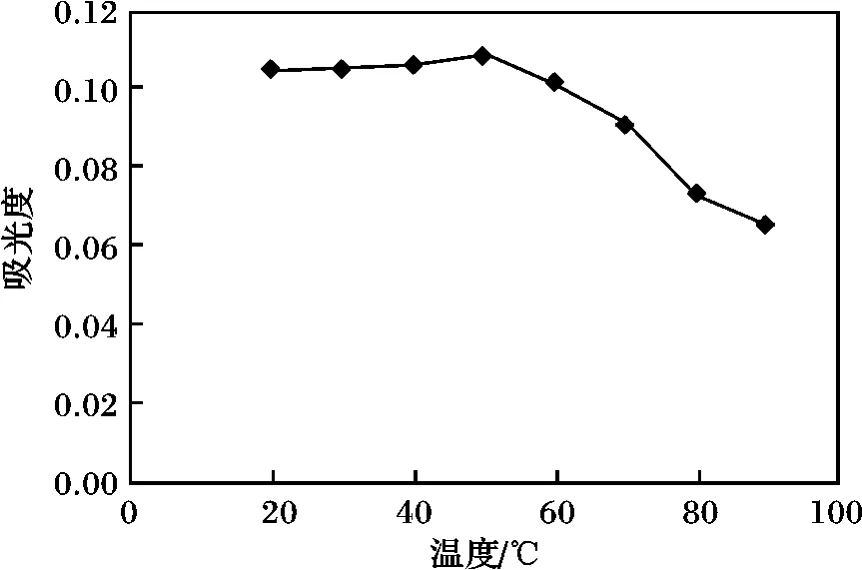
圖9 溫度的選擇Fig.9 The test of choose different temperature
2.7 標準曲線
準確稱取0.369 7 g 烘至恒重的Na2SO4,去離子水定容至250 mL 容量瓶中,得含量為1.0 mg/mL的儲備液,取10 mL 到100 mL 容量瓶中去離子水定容,即稀釋了10 倍,得0.1 mg/mL 的標準溶液。在9 個25 mL 容量瓶中,分別加入0.00,1.00,2.00,3.00,4.00,5.00,6.00,7.00,8.00 mL 硫標準溶液,濃度分別為:0.00,4,8,12,16,20,24,28,32 μg/mL,按照選定的樣品測定方法測定吸光度,并根據各標準溶液的濃度及相應的吸光度繪制工作曲線(圖10),其線性回歸方程為:y =0.006 3x-0.000 2,R2=0.998 4。

圖10 標準曲線Fig.10 The results of sulfur standard curve
2.8 樣品量的考察
精密吸取處理好的葡萄樣品供試品溶液,分別加入1,2,3,4,5 mL,用選定的方法,測定吸光度,選定樣品的量,見圖11。
由圖11 可知,加入樣品2 mL 后吸光度值為0.111,在標準曲線的12 ~20 μg/mL,較合適。
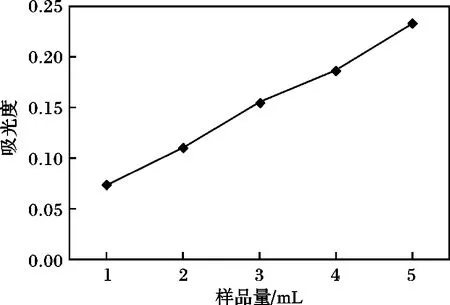
圖11 樣品量的考察Fig.11 The test of sample amount
2.9 重復性和加樣回收率
取同一份樣品供試品溶液,用選定的方法,樣品平行處理6 次,測定吸光度,計算吸光度值A 的相對標準偏差,RSD 為1.32%,表明該實驗方法的重復性良好。
精密稱取6 份樣品各1 g,分成3 組,各組分別加入對照品溶液,按實驗方法測定吸光度,并計算加樣回收率和相對標準偏差,結果見表1,平均回收率為99.17%,RSD 為1.89%,符合方法要求的回收率,表明該測定方法可用于植物葉片中硫含量的測定。
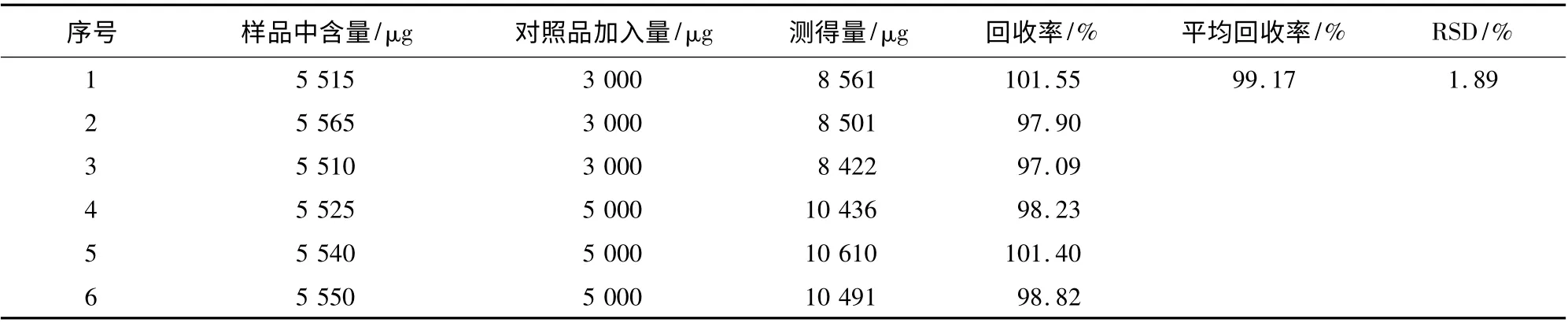
表1 回收率實驗結果Table 1 The results of recovery experiment
3 結論
在植物中的硫有兩種存在形式:有機硫和無機硫,大部分的有機硫以蛋白質形式出現,形態和含量比較穩定;無機硫多以SO2-4的形式在細胞中,含量隨著硫素供應水平的變化存在很大的差異。植物從土壤中吸收硫素主要是以SO2-4的形式逆濃度梯度的主動吸收過程進入植物體內,然后通過代謝合成為有機硫固定在細胞中,也可以轉移到其他部位被再次利用[1]。同時,植物可以吸收大氣中的硫化氫、二氧化硫等供生長發育的需要。植株中SO2-4可作為硫素診斷的指標[12]。
由于不同研究文獻中硫酸鋇比濁法的比色條件有一定的差異,對于不同的樣品材料會產生比較大的誤差[8]。本文采用單因素實驗對硫酸鋇比濁法對測定植物葉片硫含量進行系統的研究,在硫濃度為0 ~32 μg/mL 內與其吸光值有良好的線性關系(r=0.998 4);檢測波長經實驗測定為470 nm,葡萄葉片提取液2 mL 在甘油-乙醇(1 ∶1)2 mL,10 mg/mL BaCl2溶液2 mL,25% HCl 溶液2 mL,常溫下反應的條件下,測定其470 nm 處的吸光值,平均回收率為99.17%,RSD 為1.89%。該法具有操作簡單、速度快、準確性高、精密度高、穩定性和重現性好、設備要求低等優點,是檢測植物葉片中硫含量可靠方法。
[1] 謝瑞芝,董樹亭,胡昌浩.植物硫素營養研究進展[J].中國農學通報,2002,18(2):65-69.
[2] Rennenberg H,Herschbach C,Haberer K,et al.Sulfur metabolism in plants:Are trees different?[J].Plant Biology,2007,9:620-637.
[3] 李金鳳.大豆硫素營養及硫肥肥效研究[D].沈陽:沈陽農業大學,2003.
[4] 王東,于振文,樊廣華,等.硫素對冬小麥品質和產量的影響[J].山東農業科學,2000,6:10-12.
[5] 郭雪艷,關慶偉,劉暢,等.園林綠化樹種香樟葉片的含硫量動態分析[J].城市環境與城市生態,2012,25(4):19-21.
[6] 傅嬌艷,丁振華,吳彥慜,等.硫酸鋇分光光度比濁法測定高硫環境樣品[J].廈門大學學報:自然科學版,2007,46(6):880-883.
[7] 洪淵,黃俊華,張冬鵬.深圳市園林植物葉片含硫量的特點[J].生態科學,2007,26(2):122-125.
[8] 吳名劍,孫賢軍,雷啟福,等.硫酸鋇溶膠比濁法測定煙草中的硫[J].煙草科技,2005(1):24-26.
[9] 丁根娣,吳杰,許志遂.硫酸鋇吸光比濁法測定機理的探討[J].理化檢驗-化學分冊,2001,37(3):111-112.
[10]宋金如,劉淑娟,朱霞萍.測定水中硫酸根方法的概述[J].華東地質學院學報,2002,25(2):64-68.
[11]梁運獻.硫酸鋇比濁法測定土壤全硫的改進[J].廣西農業科學,2002,4:186-187.
[12]洪淵,張冬鵬,黃俊華.硫污染對9 種園林植物葉片硫含量與葉綠素熒光參數的影響[J].生態科學,2006,25(6):558-560.

