腹腔鏡巨脾切除術的臨床療效分析*
鄭佳隆,黃鶴光,陳燕昌,陸逢春,林賢超,林榮貴,楊媛媛
(福建醫科大學附屬協和醫院,福建 福州,350001)
自1991年我國第一例腹腔鏡手術[1]成功開展,經過二十余年的發展,腹腔鏡手術發生了巨大的變化,其創傷小、術后康復快、住院時間短等優點使其在全國絕大多數醫院得到廣泛開展,且為外科醫生普遍接受。而腹腔鏡脾臟切除也已普及,目前腹腔鏡脾切除術(laparoscopic splenectomy,LS)已成為特發性血小板減少性紫癜(idiopathic thrombocytopenic purpura,ITP)、遺傳性球形紅細胞增多癥、地中海貧血等血液病、原發或繼發性脾臟腫瘤及其他原因引起的脾功能亢進等脾臟疾病的常規術式。既往巨脾(≥20 cm)是LS 的絕對禁忌證,但隨著腹腔鏡技術的不斷發展及手術器械、設備的不斷改進,腹腔鏡巨脾切除術也已在臨床得到開展[2]。本文現對我院開展的腹腔鏡巨脾切除術進行臨床分析。
1 資料與方法
1.1 臨床資料 2008年5月31日至2014年10月9日我院施行LS 77 例,以脾臟長徑是否≥20 cm 分為非巨脾組(n=64)與巨脾組(n=13)。非巨脾組中男25 例,女39 例;10~68 歲;巨脾組男5 例,女8 例;14~75 歲。同時回顧了同期施行的74 例開腹巨脾切除的臨床資料,歸為開腹組(n =74)。將各組病種分為血液病(ITP、自身免疫性溶血性貧血、地中海貧血、白血病等)、腫瘤類(脾臟淋巴管瘤、脾臟炎性假瘤、脾臟淋巴瘤等)、肝硬化及其他(Evan 綜合征、脾臟硬化性血管瘤樣結節性轉化及原因不明等)四種。其手術方式主要根據術者對患者病情分析的臨床經驗及患者的要求進行選擇。巨脾組與非巨脾組性別、年齡、疾病、聯合手術等方面差異無統計學意義。巨脾組與開腹組年齡、性別差異無統計學意義,而巨脾組疾病種類以血液病為主,開腹組以肝硬化為主,兩者差異有統計學意義。開腹組聯合賁門周圍離斷術較多,與巨脾組差異有統計學意義。3組患者性別、年齡、疾病、聯合手術等方面的對比見表1、表2。
表1 巨脾組與非巨脾組患者基本資料的比較(±s)
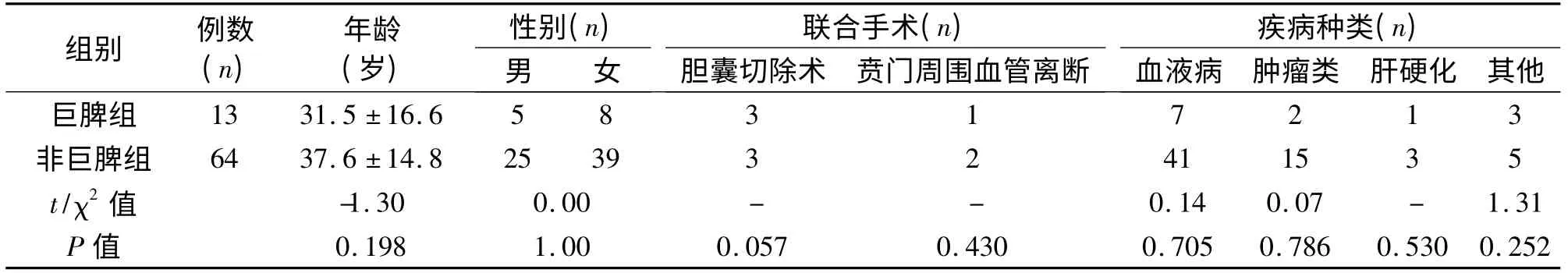
表1 巨脾組與非巨脾組患者基本資料的比較(±s)
注:-表示應用Fisher 的精確檢驗,不存在χ2 值。
?
表2 巨脾組與開腹組患者基本資料的比較(±s)
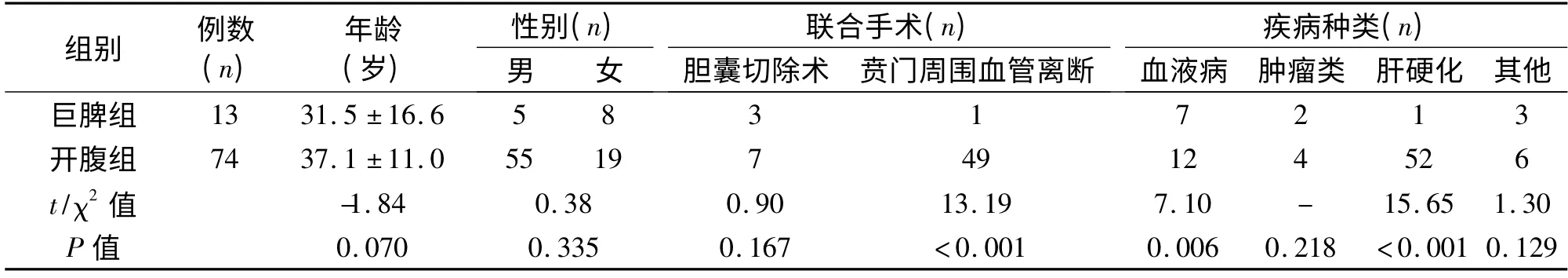
表2 巨脾組與開腹組患者基本資料的比較(±s)
注:-表示應用Fisher 的精確檢驗,不存在χ2 值。
?
1.2 手術方法 氣管內插管靜脈復合麻醉,常規導尿。麻醉成功后患者取平臥位,常規消毒鋪巾,術者及持鏡者立于患者右側,助手立于患者左側。下腹正中偏右取10 mm 切口做觀察孔,建立氣腹,壓力維持在12~14 mmHg,穿刺一次性10 mm Trocar,置入腹腔鏡,探查腹腔情況,直視下根據脾臟大小選擇另外4 個操作孔(于右中腹取2 個5 mm 切口,左下腹取5 mm、10 mm 小切口,分別穿刺相應Trocar),置入超聲刀、抓鉗、吸引器,再次仔細探查腹腔情況。挑起脾臟下極,用超聲刀于脾臟下極分離脾結腸韌帶,將脾臟向內翻轉,向上分離脾腎韌帶至脾臟上極,并分離脾膈韌帶。助手用抓鉗將胃牽拉至右上方,暴露脾胃韌帶,用超聲刀自胃大彎中上部逐步分離脾胃韌帶至脾臟上極(圖1),用Hem-o-lok 夾閉胃短血管胃側端,顯露脾蒂。用超聲刀初步分離脾蒂,離斷脾蒂周圍組織(圖2),將胰尾從脾門后方游離。分別采用非解剖脾蒂離斷或解剖脾蒂離斷兩種方法離斷脾門,非解剖脾蒂離斷法即游離出脾蒂后不解剖其血管及分支,用腔鏡直線型切割閉合器切割釘合脾蒂;解剖脾蒂離斷法即顯露脾蒂后,在腔鏡直視下解剖脾動靜脈二級分支,分別用Hem-o-lok或鈦夾夾閉脾動靜脈二級分支及主干后超聲刀離斷脾蒂(圖3、圖4)。完全游離脾臟后將脾臟裝入標本袋,取繞臍切口長3~4 cm,逐層入腹,取出脾臟(圖5),關閉切口。用溫生理鹽水沖洗腹腔,仔細檢查有無活動性出血,清點器械紗布無誤,脾窩常規放置中號硅管引流(見圖6),退出腔鏡器械及Trocar,依次縫合各手術切口。
1.3 觀察指標 記錄各病例手術時間、術中出血量、術后恢復進食時間、術后住院時間及術后并發癥。
1.4 統計學處理 將巨脾組、非巨脾組及同期開腹組的臨床資料進行比較。用SPSS 13.0 統計軟件包進行數據分析,計量資料(脾臟長徑、手術時間、術中出血、術后恢復進食時間、術后出院時間)采用t 檢驗、計數資料(并發癥、中轉開腹)采用χ2檢驗進行組間比較。
2 結 果
本研究中三組均無死亡病例。與非巨脾組相比,巨脾組手術時間長、術中出血多、術后住院時間長。與開腹組相比,巨脾組術后恢復進食時間及術后住院時間短。見表3、表4。巨脾組5 例患者發生并發癥,其中肺炎4 例(30.8%),繼發性血小板增多癥1 例(7.7%);非巨脾組13 例患者發生并發癥,其中肺炎10例(15. 6%),腹腔感染1例(1.6%),繼發性血小板增多癥2 例(3.1%);開腹組33 例患者出現并發癥(其中有的患者出現多項并發癥),其中肺炎27 例(36.5%),腹腔感染1 例(1.4%),泌尿系感染1 例(1.4%),切口感染3 例(4.1%),繼發性血小板增多癥2 例(2.7%),脾靜脈血栓2 例(2.7%),胰瘺1 例(1.4%),術后出血2例(2.7%)。三組術后并發癥發生率均較高,其中巨脾組與非巨脾組(χ2=1.10,P =0.294)及巨脾組與開腹組(χ2=0.012,P =0.914)的術后并發癥發生率差異均無統計學意義,而非巨脾組與開腹組(χ2=8.046,P =0.005)相比,術后并發癥明顯降低,差異有統計學意義。
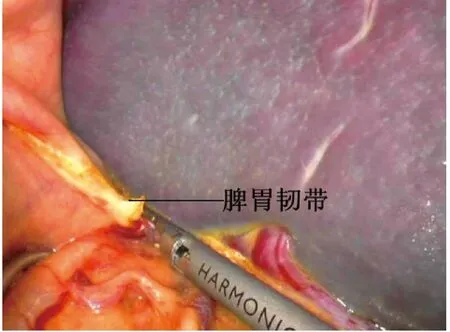
圖1 用超聲刀分離脾胃韌帶至脾臟上極
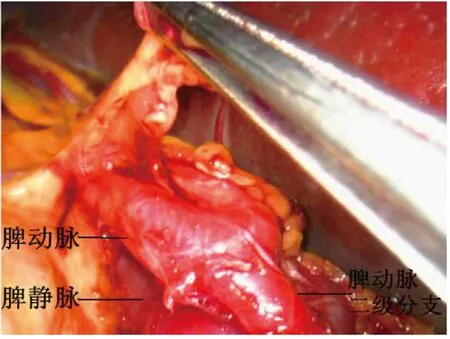
圖2 分離脾周組織顯露脾蒂
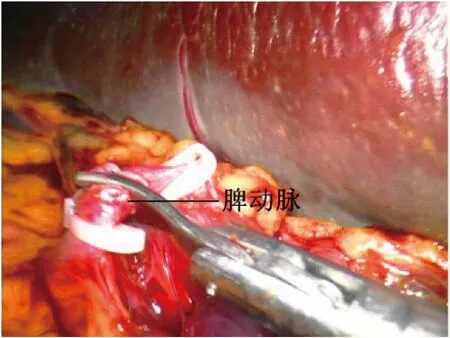
圖3 預先斷扎脾動脈
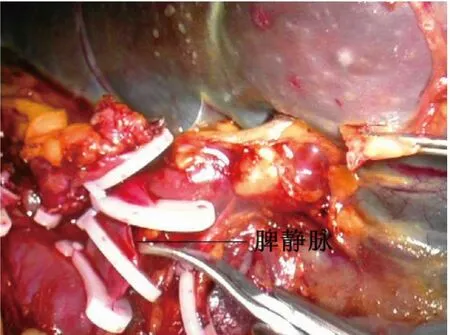
圖4 解剖脾蒂斷扎脾靜脈
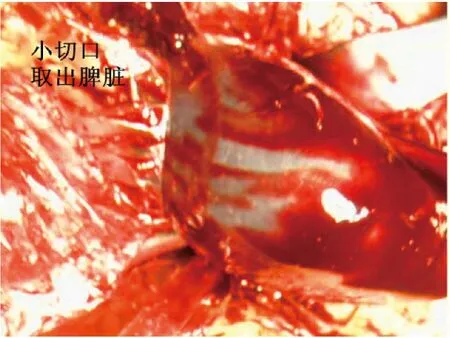
圖5 小切口取出脾臟組織
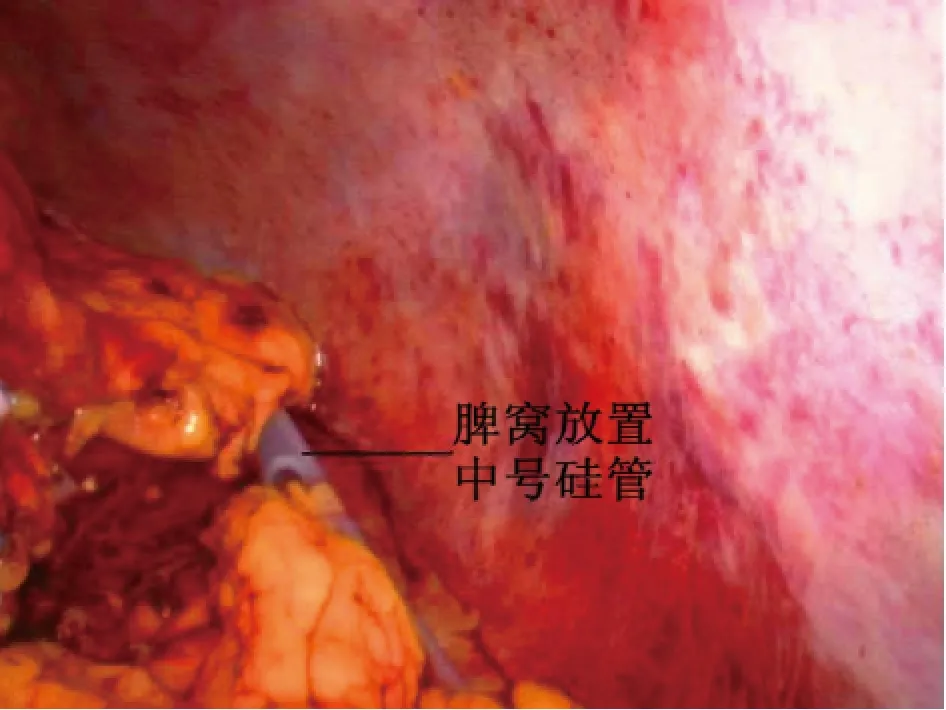
圖6 脾窩放置中號硅管
表3 巨脾組與非巨脾組患者臨床結果的比較(±s)
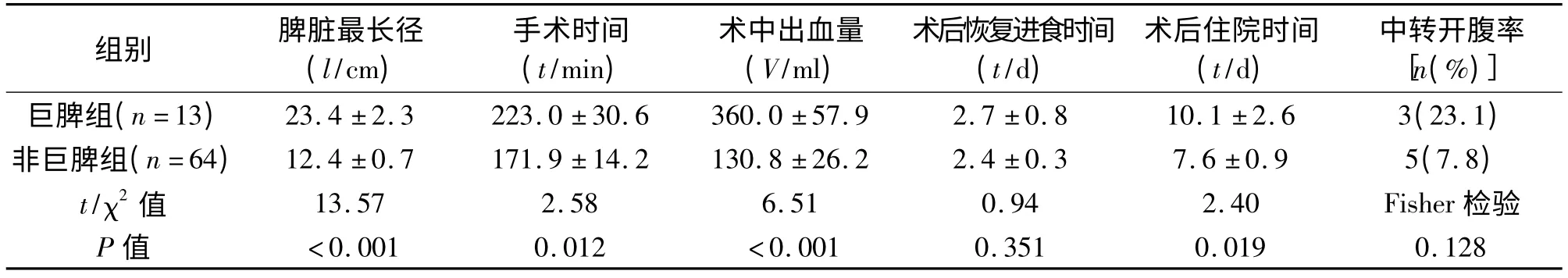
表3 巨脾組與非巨脾組患者臨床結果的比較(±s)
?
表4 巨脾組與開腹組患者臨床結果的比較(±s)
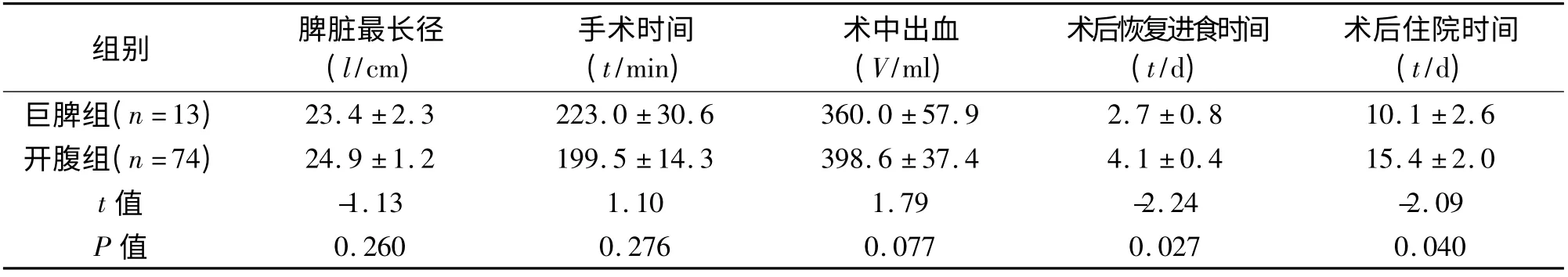
表4 巨脾組與開腹組患者臨床結果的比較(±s)
?
3 討 論
自1992年Delaitre 等[3]首次報道LS 以來,創傷小、術后康復快、住院時間短等優點使其成為血液病脾切除的金標準,也是原發或繼發性脾臟腫瘤及其他原因引起的脾功能亢進等非巨脾疾病的常規術式。
巨脾[4](脾臟長徑≥20 cm 或質量>1 000 g 的脾臟,由于臨床切脾過程中脾臟組織及脾臟血液的流失導致對脾臟質量的估計偏小,因此一般以脾臟的長徑≥20 cm 為依據)曾被認為是LS 的絕對禁忌證,但隨著腹腔鏡技術的不斷發展及手術器械、設備的不斷改進,腹腔鏡巨脾切除術已陸續開展,并取得不錯的效果。
3.1 可行性與安全性 本研究中,巨脾組手術時間及術中出血與開腹組相比差異無統計學意義,術后進食時間及術后出院時間較開腹組短,差異有統計學意義,切口并發癥存在明顯優勢。從臨床結果可見,與開腹巨脾切除相比,腹腔鏡巨脾切除切口小、術后恢復進食快,術后住院時間短,無死亡病例,手術時間及術中出血差異無統計學意義,可見其可行性、安全性及療效是令人滿意的。
3.2 中轉開腹 本研究中,巨脾組中轉開腹3 例(23.1%),非巨脾組中轉開腹5 例(7.8%),中轉開腹的主要原因為術中大出血及脾蒂分離困難。由于巨脾患者具有腹腔操作空間小,脾臟張力大、質地脆,脾門及周圍血管曲張、病理血管多等特點,腹腔鏡巨脾切除術中大出血的風險往往較非巨脾患者高。在游離脾臟周圍韌帶時,暴力牽拉或抓持脾臟容易引起脾被膜撕裂及脾臟實質損傷出血,因此操作時必須輕柔,使用無損傷鉗“抬、撥”脾臟,避免暴力“抓、拉”。解剖脾蒂時避免用力牽拉,造成脾靜脈壁撕裂出血,仔細分離脾蒂,用Hem-o-lok 或鈦夾夾閉分支血管,避免損傷側支血管引起出血。如使用直線切割吻合器處理脾蒂,盡量避免直線切割閉合器反復試插脾蒂,以免損傷周圍側支血管,并防止脾蒂組織厚薄不均導致切割閉合不滿意從而出血;避免損傷胰腺,以免造成胰腺出血及術后胰瘺等相關并發癥[5]。脾蒂周圍粘連嚴重、分離困難也是中轉開腹的主要原因之一,對于這種情況如強行于腔鏡下分離,導致術中大出血的危險性將大大增加,因此術中需在腔鏡下探查清楚,根據患者病情、術中所見及術者手術技巧而選擇術式,嚴格掌握其適應證,避免出現不必要的被動局面。
3.3 術后并發癥及預防 脾切除術常見的并發癥有感染(肺部感染、腹腔感染、切口感染等)、術后出血、胰瘺、門靜脈系統血栓(portal vein thrombosis,PVT)、繼發性血小板增多癥等[6]。
本研究中,三組患者最常見的并發癥均為感染,其中最常見的為術后肺部感染(非巨脾組15.6%,巨脾組30. 8%,開腹組36. 5%),考慮主要由于:(1)部分脾臟疾病(ITP、脾亢、肝硬化、自身免疫性疾病等)導致患者免疫力降低;(2)部分患者經過長期激素治療后免疫力降低;(3)均為氣管插管,且手術時間較長,術中出血相對較多,為易感因素。因此術前做好患者肺部評估、提高免疫力、改善營養狀況、術前禁煙(>2 周),術后常規予化痰與霧化治療、勤咳痰、早期下床活動,對于預防肺部感染至關重要。非巨脾組與巨脾組均未出現切口感染,開腹組出現3 例切口感染(4.1%),主要由于開腹巨脾切除手術切口大、創傷大,切口愈合慢,導致切口感染率增高,這也體現了腔鏡手術的優點。腹腔感染常系術后腹腔積液積膿、引流不暢所致,因此術中防止胰腺損傷、止血徹底、引流管位置放置準確、術后保持引流管通暢是關鍵。泌尿系感染則主要系術后留置尿管時間過長所致,因此術后早期鍛煉膀胱、盡早拔除尿管是防止泌尿系感染發生的主要手段。
術后出血也是脾切除術較常見的并發癥之一,其主要原因包括患者的自身因素與手術因素,ITP、淋巴瘤等血液病患者大多貧血或血小板減少,門脈高壓脾功能亢進患者本身存在凝血功能障礙,可引起切口或脾窩創面滲血,這是患者術后出血的自身因素;而手術因素一般為術中止血不徹底。對于患者自身因素的預防要點為:(1)建議PLT >50 ×109/L時手術,如果病情緊急或術前PLT 低難以糾正時,可于手術前1日輸注血小板,并在手術當日備血小板;(2)術前積極糾正凝血功能,必要時輸注新鮮冰凍血漿,以改善凝血功能;(3)術中脾窩放置止血材料,防止滲血;(4)術后常規予去氨加壓素預防出血。手術因素主要為術中止血不徹底,因此關腹前需再次仔細探查,確認有無滲血。PVT[7]是腹腔鏡巨脾切除、開腹巨脾切除術共有的并發癥之一,主要與患者脾臟切除術后門靜脈屬支系統靜脈血流增加,局部形成渦流及繼發性血小板增多有關,好發于脾靜脈。對此術后需密切監測患者血小板,如血小板持續升高,可予以阿司匹林等抗凝,必要時可予以低分子肝素,避免血小板凝集、血栓形成。而胰瘺的防治主要依賴于術中避免損傷胰腺,尤其直線切割吻合器離斷脾蒂時避免損傷胰尾。
綜上所述,腹腔鏡巨脾切除術是安全、可行的,相對于開腹巨脾切除術,具有手術切口小、術后康復快、住院時間短等優點。相對于非巨脾而言,腹腔鏡巨脾切除術手術難度高,術中出血較多,手術時間較長,且中轉開腹率較高,因此對于術者的腔鏡技術要求較高,且術前需做好手術評估,嚴格掌握適應證。LS 的并發癥發生率尤其切口相關并發癥明顯低于開腹巨脾切除,而對于降低肺部感染等并發癥仍有賴于術前做好充分的準備。相信隨著臨床經驗的積累、腔鏡技術的提高及相關器械的發展,腹腔鏡巨脾切除術會取得更大的突破。
[1]荀祖武,方登華,方榮新,等.電視腹腔鏡膽囊切除術100 例報道[J].中華外科雜志,1991,29(10):616-617.
[2]Owera A,Hamade AM,Bani Hani OI,et al.Laparoscopic versus open splenectomy for massive splenomegaly:a comparative study[J].J Laparoendosc Adv Surg Tech A,2006,16(3):241-246.
[3]Delaitre B,Maignien B.Splenectomy by the laparoscopic approach.Report of a case[J].Presse Med,1991,20(44):2263.
[4]Smith L,Luna G,Merg AR,et al.Laparoscopic splenectomy for treatment of splenomegaly[J].Am J Surg,2004,187(5):618-620.
[5]Chand B,Walsh RM,Ponsky J,et al. Pancreatic complications following laparoscopic splenectomy[J]. Surg Endosc,2001,15(11):1273-1276.
[6]Targarona EM,Espert JJ,Bombuy E,et al. Complications of laparoscopic splenectomy[J]. Arch Surg,2000,135(10):1137-1140.
[7]Targarona EM.Portal vein thrombosis after laparoscopic splenectomy:the size of the risk[J].Surg Innov,2008,15(4):266-270.

