德國(guó)藥品參考價(jià)格體系對(duì)構(gòu)建我國(guó)醫(yī)保支付標(biāo)準(zhǔn)的啟示
常 峰 崔鵬磊 夏 強(qiáng) 張艦云
中國(guó)藥科大學(xué)國(guó)際醫(yī)藥商學(xué)院 江蘇南京 211198
?
·醫(yī)藥服務(wù)價(jià)格·
德國(guó)藥品參考價(jià)格體系對(duì)構(gòu)建我國(guó)醫(yī)保支付標(biāo)準(zhǔn)的啟示
常 峰*崔鵬磊 夏 強(qiáng) 張艦云
中國(guó)藥科大學(xué)國(guó)際醫(yī)藥商學(xué)院 江蘇南京 211198
明確醫(yī)保支付標(biāo)準(zhǔn)制定的程序、依據(jù)和方法等規(guī)則,是藥品最高零售限價(jià)放開(kāi)后價(jià)格管理工作的重點(diǎn)和難點(diǎn)。1989年德國(guó)率先在其法定醫(yī)療保險(xiǎn)系統(tǒng)中實(shí)施藥品參考價(jià)格制度,主要目的在于控制藥品費(fèi)用的持續(xù)上漲,提高藥品價(jià)格管理工作的科學(xué)性和透明性。本文系統(tǒng)梳理了德國(guó)參考價(jià)格體系,包括參考價(jià)格體系概述、參考價(jià)格組劃分準(zhǔn)則、參考價(jià)格形成機(jī)制和藥品部分負(fù)擔(dān)四方面內(nèi)容,以期對(duì)我國(guó)醫(yī)保支付標(biāo)準(zhǔn)的實(shí)施提供借鑒。并指出我國(guó)可率先在非處方藥市場(chǎng)或慢性病市場(chǎng)中基于參考價(jià)格建立醫(yī)保支付標(biāo)準(zhǔn),在合理劃分參考價(jià)格組的基礎(chǔ)上,依據(jù)市場(chǎng)價(jià)格制定和調(diào)整醫(yī)保支付標(biāo)準(zhǔn),并通過(guò)完善部分負(fù)擔(dān)機(jī)制來(lái)規(guī)避患者和醫(yī)療機(jī)構(gòu)的道德風(fēng)險(xiǎn)行為,保障醫(yī)保基金的合理配置。
藥品參考價(jià)格體系; 參考價(jià)格組; 共付費(fèi)用; 支付標(biāo)準(zhǔn)
2015年5月5日,國(guó)家發(fā)展改革委等七部委聯(lián)合發(fā)文,決定推進(jìn)藥品價(jià)格改革,取消絕大部分藥品政府定價(jià),逐步建立以市場(chǎng)為主導(dǎo)的藥品價(jià)格形成機(jī)制,最大限度減少政府對(duì)藥品價(jià)格的直接干預(yù)。政策的出臺(tái)表明我國(guó)未來(lái)將通過(guò)銜接招標(biāo)采購(gòu)和醫(yī)保控費(fèi)政策,建立醫(yī)保支付標(biāo)準(zhǔn)來(lái)深入推進(jìn)藥品價(jià)格改革。而依據(jù)參考價(jià)格體系來(lái)制定醫(yī)保支付標(biāo)準(zhǔn)早已在多數(shù)國(guó)家和地區(qū)付諸實(shí)踐,且被證明是一種行之有效的支付標(biāo)準(zhǔn)管理方式。德國(guó)作為世界上首個(gè)建立參考價(jià)格體系的國(guó)家,其參考價(jià)格體系科學(xué)成熟,設(shè)計(jì)精辟完備,眾多國(guó)家紛紛效仿。因此,本文對(duì)德國(guó)參考價(jià)格體系進(jìn)行系統(tǒng)性梳理,以期對(duì)構(gòu)建我國(guó)醫(yī)保支付標(biāo)準(zhǔn)提供借鑒。
1 參考價(jià)格體系概述
德國(guó)于1883年制定了《醫(yī)療保險(xiǎn)法》,建立了法定醫(yī)療保險(xiǎn)制度,旨在向民眾提供補(bǔ)償范圍廣且低廉的醫(yī)療服務(wù),降低被保險(xiǎn)者的醫(yī)療負(fù)擔(dān),但這不可避免地刺激了醫(yī)藥費(fèi)用的增長(zhǎng)。為了有效控制醫(yī)藥費(fèi)用的過(guò)快增長(zhǎng),德國(guó)相繼實(shí)施了價(jià)格折扣、參考價(jià)格、醫(yī)藥費(fèi)用分擔(dān)等制度,并取得了顯著成效。[1]其中,為達(dá)到長(zhǎng)期控制藥品費(fèi)用的目標(biāo),德國(guó)于1989年實(shí)施《醫(yī)療改革法案》,率先在其法定醫(yī)療保險(xiǎn)系統(tǒng)中構(gòu)建了融合定價(jià)與補(bǔ)償?shù)闹Ц稑?biāo)準(zhǔn)制定方法——參考價(jià)格體系。該體系對(duì)降低藥品價(jià)格起到了積極作用,并隨后在荷蘭、丹麥、瑞典、西班牙、比利時(shí)、意大利、澳大利亞、新西蘭和加拿大等國(guó)廣為應(yīng)用。
參考價(jià)格體系通過(guò)限制藥品補(bǔ)償水平進(jìn)而間接控制藥品價(jià)格,其設(shè)計(jì)的主要理念為一方面增加患者和醫(yī)生對(duì)藥品價(jià)格的敏感程度以提高藥品價(jià)格的需求彈性,降低需方對(duì)藥品的需求量,避免道德風(fēng)險(xiǎn)行為;另一方面促使供方為避免失去市場(chǎng)份額而自覺(jué)限制藥品價(jià)格,增強(qiáng)供方市場(chǎng)的競(jìng)爭(zhēng),最終降低保險(xiǎn)者支付的藥品費(fèi)用。[2]參考價(jià)格體系有5個(gè)顯著特點(diǎn):(1)依據(jù)生物等效性或治療等價(jià)性對(duì)藥品進(jìn)行分組;(2)參考價(jià)格是每組藥品補(bǔ)償上限;(3)參考價(jià)格根據(jù)藥品市場(chǎng)價(jià)格分布狀況制定;(4)廠(chǎng)商自由定價(jià);(5)如果廠(chǎng)商定價(jià)高于參考價(jià)格,患者需支付差額。[3]在德國(guó)參考價(jià)格制定過(guò)程中,首先由聯(lián)邦聯(lián)合委員會(huì)(G-BA)依據(jù)分組標(biāo)準(zhǔn)將藥品劃分為不同的參考價(jià)格組并確定藥品限定日劑量和比較大小(VG),然后由聯(lián)邦醫(yī)療保險(xiǎn)基金協(xié)會(huì)(GKV-SV)制定各分組的最高補(bǔ)償額并由德國(guó)醫(yī)學(xué)文獻(xiàn)和信息研究所(DIMDI)將參考價(jià)格信息在網(wǎng)上公布,便于相關(guān)主體進(jìn)行查閱與監(jiān)督。[4]目前德國(guó)藥品市場(chǎng)上大約75%的處方藥[5]和部分非處方藥受到參考價(jià)格體系的管理。
2 參考價(jià)格組劃分準(zhǔn)則
2.1 參考價(jià)格組藥品范圍
德國(guó)在制定藥品價(jià)格過(guò)程中充分體現(xiàn)了分類(lèi)管理的思想。首先將藥品劃分為不予補(bǔ)償?shù)乃幤泛涂裳a(bǔ)償藥品。其中不予補(bǔ)償藥品由廠(chǎng)商自由定價(jià),可補(bǔ)償藥品依據(jù)有無(wú)創(chuàng)新性劃分為創(chuàng)新藥品和非創(chuàng)新藥品。創(chuàng)新藥品依據(jù)藥品的附加效益程度由保險(xiǎn)者與廠(chǎng)商協(xié)商制定價(jià)格,如果協(xié)商不能達(dá)成共識(shí),則交由仲裁機(jī)構(gòu)(包括基金協(xié)會(huì)代表、廠(chǎng)商代表、中立成員)裁決。非創(chuàng)新藥品則納入?yún)⒖純r(jià)格體系,由廠(chǎng)商自由定價(jià),但受到參考價(jià)格的約束。因此參考價(jià)格體系包括了絕大多數(shù)的可補(bǔ)償藥品以及不具備創(chuàng)新性的專(zhuān)利藥品。
可補(bǔ)償藥品——絕大多數(shù)納入?yún)⒖純r(jià)格體系。德國(guó)實(shí)施負(fù)面清單(negative list)制度,一般而言,獲得上市許可的藥品都可獲得補(bǔ)償,除非藥品被納入負(fù)面清單。負(fù)面清單包括四種藥品類(lèi)型:(1)用于治療輕微癥狀的藥品;(2)“無(wú)效益”(inefficient)的藥品;(3)“l(fā)ife-style”藥品,主要用于改善生活品質(zhì);(4)非處方藥品(部分除外)。其中第一類(lèi)藥品于1983年未納入補(bǔ)償,第二類(lèi)藥品于1991年未納入補(bǔ)償,“l(fā)ife-style”藥品及非處方藥于2004年被列為不予補(bǔ)償藥品。[6]
專(zhuān)利藥品——無(wú)療效改善的藥品將納入?yún)⒖純r(jià)格體系。2004年德國(guó)實(shí)施《健康保險(xiǎn)現(xiàn)代化法案》規(guī)定可以將專(zhuān)利藥品納入?yún)⒖純r(jià)格體系中,但不包括那些與現(xiàn)有治療方案相比具有療效改善的藥品。2011年實(shí)施的《醫(yī)藥行業(yè)改革法案》(AMONG),將創(chuàng)新藥品的附加效益劃分為6個(gè)等級(jí),規(guī)定如果藥品附加效益不被接受,則將該藥劃入?yún)⒖純r(jià)格組,附加效益的判斷標(biāo)準(zhǔn)包括全因死亡率、發(fā)病率、健康相關(guān)生命質(zhì)量和不良反應(yīng)4個(gè)指標(biāo)。同時(shí)《社會(huì)法典》第五部(SGB V)規(guī)定只有專(zhuān)利藥品的參考價(jià)格組應(yīng)至少應(yīng)包括3種藥品。
2.2 參考價(jià)格組劃分流程
參考價(jià)格組的劃分流程包括4個(gè)步驟:(1)GKV-SV向G-BA提議建立新的參考價(jià)格組或?qū)F(xiàn)有藥品納入已有參考價(jià)格組;(2)G-BA藥品小組委員會(huì)負(fù)責(zé)討論并審核提議,然后召集基金會(huì)代表、專(zhuān)家、患者等多方參與人舉行聽(tīng)證會(huì),做出初步?jīng)Q定;(3)G-BA辦公室對(duì)藥品小組委員會(huì)的決策進(jìn)行評(píng)估,根據(jù)SGB V第91條的規(guī)定編制和匯總草案,包括文件摘要、決策理由和最終決定,并提交至聯(lián)邦衛(wèi)生部;(4)聯(lián)邦衛(wèi)生部如果無(wú)異議,則發(fā)布聯(lián)邦公告,公開(kāi)信息,確定參考價(jià)格組。如果存在異議,則交由藥品小組委員會(huì)重新討論和審核提議。[7]
2.3 參考價(jià)格組制定標(biāo)準(zhǔn)
在制定參考價(jià)格組的過(guò)程中,主要考慮以下標(biāo)準(zhǔn):(1)解剖學(xué)治療學(xué)及化學(xué)分類(lèi)系統(tǒng)(Anatomical Therapeutic Chemical,ATC)。在參考價(jià)格系統(tǒng)中,依據(jù)ATC-3、ATC-4、ATC-5將藥品劃分為3個(gè)級(jí)別。(2)生物等效性和治療結(jié)果相似性。如果藥品包含相同的活性物質(zhì),同時(shí)能夠以相同的速度和強(qiáng)度被身體吸收,此類(lèi)藥品形成的參考價(jià)格組稱(chēng)為學(xué)名藥參考價(jià)格組,由過(guò)專(zhuān)利期的品牌藥及其被證明的具有生物等效性的學(xué)名藥組成。如果藥品不具有生物等效性,但常用于治療相同的疾病和癥狀,也能形成相應(yīng)的參考價(jià)格組,即“療效參考價(jià)格組”,組中的藥品具有相似的治療效果但不具備相同活性成分。[8](3)藥品屬性。不同屬性的藥品需要進(jìn)行分組處理,如根據(jù)給藥途徑(口服、注射、直腸、經(jīng)皮等)不同,劃分為不同亞組,依據(jù)藥理動(dòng)力學(xué)分為正常釋放制劑和控釋制劑等,依據(jù)劑型形態(tài)分為固態(tài)、液態(tài)等。然而對(duì)于藥理動(dòng)力學(xué)與制劑形態(tài)上存在差異,但藥品療效不存在顯著差異,則不作為劃分標(biāo)準(zhǔn)。

表1 ATC分類(lèi)系統(tǒng)舉例
2.4 參考價(jià)格組劃分結(jié)果
根據(jù)參考價(jià)格組劃分流程與標(biāo)準(zhǔn),最終將藥品劃分為3個(gè)級(jí)別。其中級(jí)別1是具有相同活性成分藥品。其中活性成分可以是單一物質(zhì),也可由不同活性成分以固定比例組合而成。級(jí)別2是藥理上和治療上具有相當(dāng)活性成分的藥品,特別是化學(xué)結(jié)構(gòu)類(lèi)似的藥品。級(jí)別3為具有同等治療效果的藥品,特別是復(fù)方制劑。截至2015年4月15日,參考價(jià)格體系中劃分了438個(gè)參考價(jià)格組,包括因藥品屬性不同所形成的不同亞組,覆蓋了33 840種藥品包裝(表2)。[9]

表2 參考價(jià)格組劃分結(jié)果
3 參考價(jià)格形成機(jī)制
3.1 標(biāo)準(zhǔn)包裝的選擇及參考價(jià)格制定
制定參考價(jià)格前,GKV-SV應(yīng)首先確定參考價(jià)格組中藥品的標(biāo)準(zhǔn)包裝。標(biāo)準(zhǔn)包裝是由大多數(shù)廠(chǎng)商在市場(chǎng)上銷(xiāo)售的藥品,依據(jù)藥品規(guī)格與包裝大小兩個(gè)方面來(lái)確定。例如對(duì)于阿昔洛韋片劑,當(dāng)市場(chǎng)中同時(shí)存在200mg/25片、400mg/35片、800mg/35片等多種規(guī)格與包裝大小組合時(shí),應(yīng)選擇大多數(shù)廠(chǎng)商都能提供的組合。如果存在多種組合大多數(shù)廠(chǎng)商均能提供,則選擇處方量最大的組合為標(biāo)準(zhǔn)包裝。[10]
確定標(biāo)準(zhǔn)包裝后,需制定標(biāo)準(zhǔn)包裝的參考價(jià)格。然而德國(guó)法律對(duì)于參考價(jià)格的制定,并沒(méi)有詳細(xì)的規(guī)則,只進(jìn)行了概括的描述。即參考價(jià)格應(yīng)充分反映藥品價(jià)值,保證藥品的安全、有效、經(jīng)濟(jì)與質(zhì)量可控。參考價(jià)格制定時(shí)應(yīng)充分利用企業(yè)經(jīng)濟(jì)利潤(rùn),引發(fā)市場(chǎng)的充分競(jìng)爭(zhēng),促使廠(chǎng)商提供較為廉價(jià)的藥品,減輕患者和政府費(fèi)用負(fù)擔(dān)。SGB V第35條第5段闡明了參考價(jià)格的制定原則:(1)標(biāo)準(zhǔn)包裝的參考價(jià)格不得超過(guò)最高價(jià)與最低價(jià)所形成價(jià)格區(qū)間的下三分位數(shù);(2)同組藥品中參考價(jià)格下至少應(yīng)涵蓋20%的處方量。同時(shí)市場(chǎng)份額小于1%的藥品,不納入計(jì)算范圍。[11]為了適應(yīng)不斷變化的市場(chǎng)狀況,參考價(jià)格每年至少審查一次。參考價(jià)格計(jì)算如圖1所示。

圖1 標(biāo)準(zhǔn)包裝參考價(jià)格的制定
3.2 非標(biāo)準(zhǔn)包裝參考價(jià)格的制定
非標(biāo)準(zhǔn)包裝參考價(jià)格制定的理念在于藥品價(jià)格受到規(guī)格和包裝大小兩個(gè)因素的影響,其中規(guī)格越大或包裝數(shù)量越多,則價(jià)格越高,但價(jià)格與規(guī)格和包裝大小的關(guān)系并不滿(mǎn)足簡(jiǎn)單線(xiàn)性關(guān)系,而更適合于指數(shù)函數(shù)形式。[12]因此,對(duì)于非標(biāo)準(zhǔn)包裝的參考價(jià)格需要由下面回歸方程計(jì)算的結(jié)果乘以標(biāo)準(zhǔn)包裝的參考價(jià)格得到。
p=a×wb×pkc
(1)
其中p代表相對(duì)價(jià)格;w代表規(guī)格(級(jí)別1)和效力比較大小、效力等同因子(級(jí)別2和級(jí)別3)、效力比較因子(級(jí)別3);pk為包裝大小;a表示倍增因子,b表示效力指數(shù),c表示包裝大小指數(shù)。回歸系數(shù)a、b、c的計(jì)算是由非標(biāo)準(zhǔn)包裝的市場(chǎng)價(jià)格除以標(biāo)準(zhǔn)包裝的市場(chǎng)價(jià)格獲得相對(duì)價(jià)格p,然后將p、w、pk帶入公式ln(p)=ln(a)+b×ln(w)+c×ln(pk),運(yùn)用最小二乘法計(jì)算得到指數(shù)a、b、c。同組藥品中回歸系數(shù)是固定的。
對(duì)于級(jí)別2和級(jí)別3的藥品,由于活性成分不同,不能直接將規(guī)格代入(1)中,而是應(yīng)針對(duì)不同活性成分的限定日劑量進(jìn)行換算,得出效力比較大小wvg、效力等同因子w?f和效力比較因子wvf替代w代入(1)中。計(jì)算公式如下:
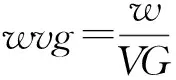


其中VG表示比較大小,由聯(lián)邦聯(lián)合委員會(huì)制定,F(xiàn)和VF由聯(lián)邦醫(yī)師和健康保險(xiǎn)委員會(huì)制定。在制定參考價(jià)格時(shí),根據(jù)參考價(jià)格組中有無(wú)非處方藥,回歸分析時(shí)基礎(chǔ)價(jià)格的選擇存在差異。對(duì)于有非處方藥的參考價(jià)格組,基于藥房零售價(jià)格(AVP)(包括增值稅)進(jìn)行回歸分析;對(duì)于只有處方藥的參考價(jià)格組,2012年1月1日前形成的參考價(jià)格組,基于藥房購(gòu)買(mǎi)價(jià)格(AEP)進(jìn)行回歸分析,2012年1月1日后形成的參考價(jià)格組,基于廠(chǎng)商銷(xiāo)售價(jià)格(APU)進(jìn)行回歸分析。
3.3 市場(chǎng)參考價(jià)格的形成


表3 可補(bǔ)償非處方藥流通環(huán)節(jié)利潤(rùn)率

圖2 銷(xiāo)售終端參考價(jià)格形成方式
4 參考價(jià)格下患者部分負(fù)擔(dān)機(jī)制
參考價(jià)格體系下的藥品,患者需承擔(dān)藥品市場(chǎng)價(jià)格高于參考價(jià)格的差額,同時(shí)需承擔(dān)部分共付費(fèi)用。德國(guó)根據(jù)患者年齡和藥品適應(yīng)癥劃分為3個(gè)補(bǔ)償類(lèi)別,首先12歲以下的患者使用的處方藥和非處方藥可獲得100%的補(bǔ)償,其次12~18歲的患者使用的處方藥和治療特定適應(yīng)癥的非處方藥同樣可獲得100%的補(bǔ)償,最后對(duì)于超過(guò)18歲的患者根據(jù)藥品藥房零售價(jià)格(包括增值稅)pi劃分為4種共付方式。[11](表4)

表4 患者藥品部分負(fù)擔(dān)
同時(shí)法定醫(yī)療保險(xiǎn)規(guī)定的以下情況可免除部分負(fù)擔(dān):(1)保險(xiǎn)人的部分負(fù)擔(dān)已超過(guò)其年收入的2%;(2)慢性病患者治療慢性疾病的部分負(fù)擔(dān)超過(guò)其年收入的1%;(3)18歲以下的兒童;(4)病人購(gòu)買(mǎi)的藥品價(jià)格低于參考價(jià)格30%;(5)基金協(xié)會(huì)與廠(chǎng)商簽訂了免除部分負(fù)擔(dān)合約。同時(shí)如果基金協(xié)會(huì)拒絕補(bǔ)償某項(xiàng)服務(wù),患者可以向法院控訴基金協(xié)會(huì),如果患者能夠證明這種服務(wù)對(duì)于他而言是充分的、適當(dāng)?shù)暮透咝У模敲淳涂梢垣@得補(bǔ)償。[14]如果醫(yī)師開(kāi)具的藥品價(jià)格高于參考價(jià)格時(shí),醫(yī)師有責(zé)任將此信息告知患者,并考慮可供替換的藥品。
5 啟示與建議
5.1 探索建立基于參考價(jià)格的醫(yī)保支付標(biāo)準(zhǔn)形成機(jī)制
德國(guó)參考價(jià)格體系在降低藥品價(jià)格方面發(fā)揮了顯著作用,其中Pavcnik通過(guò)實(shí)證分析1986—1996年間抗糖尿病和抗?jié)儍蓚€(gè)治療領(lǐng)域的藥品價(jià)格數(shù)據(jù),證明參考價(jià)格體系使品牌藥和學(xué)名藥的價(jià)格均產(chǎn)生較大幅度下降。[15]同時(shí)在DIMDI網(wǎng)站上公開(kāi)價(jià)格信息有利于消除藥品市場(chǎng)的信息不對(duì)稱(chēng),保證患者、醫(yī)療機(jī)構(gòu)和醫(yī)保機(jī)構(gòu)間信息完全,便于利益相關(guān)主體的監(jiān)督。因此在我國(guó)放開(kāi)藥品價(jià)格管理的背景下,可參照德國(guó)模式,從明確支付標(biāo)準(zhǔn)制定部門(mén)、劃分參考價(jià)格組、制定參考價(jià)格、進(jìn)行價(jià)格公示以及完善部分負(fù)擔(dān)機(jī)制5個(gè)方面進(jìn)行制度設(shè)計(jì)來(lái)構(gòu)建醫(yī)保支付標(biāo)準(zhǔn)。但由于藥品市場(chǎng)具有不適用于患者“購(gòu)者自慎”原則、復(fù)雜的信息不對(duì)稱(chēng)關(guān)系、價(jià)格需求彈性低等特點(diǎn),對(duì)藥品市場(chǎng)采用“一刀切”的支付標(biāo)準(zhǔn)制定方式并不是最優(yōu)的,需進(jìn)一步依據(jù)患者價(jià)格判斷能力、藥品治療領(lǐng)域、藥品質(zhì)量、是否需要處方等因素進(jìn)行市場(chǎng)細(xì)分,針對(duì)性的選取醫(yī)保支付標(biāo)準(zhǔn)制定方法。因此可首選非處方藥市場(chǎng)或慢性病市場(chǎng)等接近于完全競(jìng)爭(zhēng)的市場(chǎng),依據(jù)參考價(jià)格體系來(lái)制定醫(yī)保支付標(biāo)準(zhǔn),降低藥品市場(chǎng)特殊性和參考價(jià)格局限性對(duì)患者的影響。
5.2 科學(xué)確定參考價(jià)格組劃分準(zhǔn)則
德國(guó)基于ATC分類(lèi)系統(tǒng)、生物等效性和治療結(jié)果相似性、藥品屬性3個(gè)標(biāo)準(zhǔn)將參考價(jià)格體系范圍中的藥品劃分為3個(gè)等級(jí)和不同亞組,包含了專(zhuān)利藥與非專(zhuān)利藥,處方藥與非處方藥。但客觀存在的問(wèn)題是不同藥品間存在異質(zhì)性,尤其是不同活性成分藥品間異質(zhì)性更為明顯,例如級(jí)別2和級(jí)別3同組藥品間有較大的療效差異,這意味著患者需要在經(jīng)濟(jì)負(fù)擔(dān)和健康風(fēng)險(xiǎn)間進(jìn)行抉擇。[2]因此在我國(guó)實(shí)施參考定價(jià)過(guò)程中,在ATC分類(lèi)標(biāo)準(zhǔn)的基礎(chǔ)上,應(yīng)綜合考慮藥品生物等效性、劑型、給藥途徑、質(zhì)量層級(jí)等多種因素對(duì)藥品進(jìn)行分組,鑒于藥品異質(zhì)性問(wèn)題,可首先依據(jù)ATC-5劃分參考價(jià)格組,保證患者用藥的公平性。
5.3 依據(jù)市場(chǎng)實(shí)際交易價(jià)格制定和調(diào)整醫(yī)保支付標(biāo)準(zhǔn)
德國(guó)依據(jù)藥品市場(chǎng)價(jià)格分布情況來(lái)制定標(biāo)準(zhǔn)包裝的參考價(jià)格,同時(shí)每年至少審查一次參考價(jià)格,對(duì)降低藥品價(jià)格,及時(shí)反應(yīng)市場(chǎng)價(jià)格起到了積極的作用。在制定我國(guó)醫(yī)保制度標(biāo)準(zhǔn)時(shí),同樣應(yīng)采集藥品市場(chǎng)價(jià)格,運(yùn)用科學(xué)合理的方法,比如選擇中位數(shù)、平均數(shù)、調(diào)和平均值、下四分位數(shù)等方式來(lái)制定藥品支付標(biāo)準(zhǔn),對(duì)于非代表品,由于我國(guó)對(duì)于不同劑型、規(guī)格和包裝的藥品制定了差比價(jià)規(guī)則,因此近期仍可采用差比價(jià)規(guī)則計(jì)算非代表品支付標(biāo)準(zhǔn),長(zhǎng)期則可依據(jù)回歸模型制定支付標(biāo)準(zhǔn)。同時(shí)需構(gòu)建長(zhǎng)效動(dòng)態(tài)調(diào)整機(jī)制,明確支付標(biāo)準(zhǔn)調(diào)整原則、調(diào)整方法、調(diào)整周期及信息公開(kāi)等內(nèi)容,進(jìn)而保證支付標(biāo)準(zhǔn)能及時(shí)反映市場(chǎng)信息,減少藥品市場(chǎng)價(jià)格與支付標(biāo)準(zhǔn)的價(jià)格差異,提高支付標(biāo)準(zhǔn)管理的科學(xué)性和透明性。
5.4 完善部分負(fù)擔(dān)機(jī)制以規(guī)避道德風(fēng)險(xiǎn)行為
根據(jù)OECD數(shù)據(jù)顯示,從2001—2012年德國(guó)藥品費(fèi)用占衛(wèi)生總費(fèi)用的比值穩(wěn)定在13%~15%,并且近年來(lái)呈下降趨勢(shì),表明參考價(jià)格體系結(jié)合部分負(fù)擔(dān)機(jī)制以及其它配套機(jī)制,對(duì)于控制德國(guó)藥品費(fèi)用起到顯著的效果。我國(guó)基本醫(yī)療保險(xiǎn)制度對(duì)醫(yī)藥費(fèi)用起付標(biāo)準(zhǔn)、最高支付限額和報(bào)銷(xiāo)比例進(jìn)行了明確規(guī)定,由于醫(yī)療保險(xiǎn)減免了個(gè)人所需支付的醫(yī)療費(fèi)用,患者傾向于獲取比自付全部醫(yī)療費(fèi)用時(shí)更多的消費(fèi)量,致使藥品需求彈性下降,在一定程度上影響了醫(yī)保基金的合理配置。因此在構(gòu)建醫(yī)保支付標(biāo)準(zhǔn)過(guò)程中,需進(jìn)一步完善部分負(fù)擔(dān)機(jī)制,結(jié)合定率負(fù)擔(dān)和定額負(fù)擔(dān),明確醫(yī)保—醫(yī)院,醫(yī)保—患者的費(fèi)用結(jié)算方式,合理制約醫(yī)保、醫(yī)院和患者三方的行為,均衡各方利益,進(jìn)而規(guī)避患者和醫(yī)療機(jī)構(gòu)道德風(fēng)險(xiǎn)行為,提高藥品價(jià)格需求彈性。
[1] 董文勇. 德國(guó)社會(huì)醫(yī)療保險(xiǎn)用藥費(fèi)用控制制度及其對(duì)中國(guó)的啟示[J]. 環(huán)球法律評(píng)論, 2006, 28(2): 208-217.
[2] 常峰, 張子蔚. 國(guó)外藥品參考定價(jià)研究綜述[J]. 河海大學(xué)學(xué)報(bào): 哲學(xué)社會(huì)科學(xué)版, 2009, 11(2): 51-54, 92.
[3] 常峰, 張子蔚, 趙雪松. 國(guó)內(nèi)外藥品價(jià)格規(guī)制政策述評(píng)[J]. 價(jià)格理論與實(shí)踐, 2009, 29(4): 49-50.
[4] G-BA. Reference prices and how they are set [EB/OL]. [2015-01-23]. https://www.g-ba.de/institution/themenschwerpunkte/arzneimittel/festbetrag/
[5] G-BA. Decisions on Healthcare Benefits[EB/OL]. [2014-10-23]. http://www.english.g-ba.de/structure/
[6] Paris V, Docteur E. Pharmaceutical pricing and reimbursement policies in Germany[R]. Organisation for Economic Co-operation and Development, 2008.
[7] G-BA. Arzneimittel-Richtlinie[EB/OL]. [2015-03-11]. https://www.g-ba.de/informationen/richtlinien/anlage/7/
[8] Petkantchin V. Economic effects of Germany’s reference pricing policy for drugs[J]. Institut économique Molinari, Brussels, 2006: 1-20.
[9] DIMDI. Arzneimittel-Festbetr?ge[EB/OL]. [2015-04-15]. http://www.dimdi.de/static/de/amg/festbetraege-zuzahlung/festbetraege/index.htm
[10] 姚東寧, 邵蓉. 德國(guó)藥品參考定價(jià)制度對(duì)我國(guó)的啟示[J]. 價(jià)格理論與實(shí)踐, 2014, 34(9): 58-60.
[11] Herr A, Suppliet M. Pharmaceutical prices under regulation: Tiered co-payments and reference pricing in Germany[M]. DICE Discussion Paper, 2012.
[12] Danzon P M, Ketcham J D. Reference pricing of pharmaceuticals for Medicare: evidence from Germany, The Netherlands, and New Zealand[C]//Forum for Health Economics & Policy. 2004.
[13] G-BA.Arzneimittelpreisverordnung(AMPreisV)[EB/OL]. [2014-03-27]. http://www.gesetze-im-internet.de/ampreisv/BJNR021470980.html
[14] European Commission, Health and Consumer Protection Directorate-General and Austrian Ministry of Health, Family and Youth. Germany Pharma Profile[R]. Pharmaceutical Pricing and Reimbursement Information, 2008.
[15] Pavcnik N. Do pharmaceutical prices respond to potential patient out-of-pocket expenses?[J]. RAND Journal of Economics, 2002, 33(3): 469-487.
(編輯 薛云)
Medicine reference price system in Germany and its implication for healthcare payment standard in China
CHANGFeng,CUIPeng-lei,XIAQiang,ZHANGJian-yun
SchoolofInternationalPharmaceuticalBusiness,ChinaPharmaceuticalUniversity,NanjingJiangsu211198,China
It is significantly important but difficult to establish healthcare payment standard system in case our country has cancelled government and government guidance prices. In 1989, Germany was the first country to introduce the medicine reference price system in Statutory Health Insurance. It does not only aim to regulate the medicine prices, but also defines a reimbursement level for a cluster of products considered to be therapeutically equivalent, and has a good influence on lowering the price of medicine. This paper systematically reviews the medicine reference price system in Germany, including four aspects: the reference price system overview, the reference price groups’ determination procedure, the reference prices calculation and the co-payment mechanisms. Based on the Germany reference price system, we can establish healthcare payment standard in over-the-counter or chronic market first, then scientifically divide the reference price groups, formulate and adjust payment standard based on the market price, and perfect the co-payment mechanism to avoid moral hazard.
Medicine reference price system; Reference price groups; Co-payment; Payment standard
中央高校基本科研業(yè)務(wù)費(fèi)專(zhuān)項(xiàng)資金(2015PT065)
常峰,男(1972年—),副教授,主要研究方向?yàn)樗幤穬r(jià)格、醫(yī)療保障和醫(yī)藥流通規(guī)制。 E-mail:cpucf@163.com
崔鵬磊。E-mail:cuipenglei1991@163.com
R197
A
10.3969/j.issn.1674-2982.2015.07.009
2015-05-18
2015-06-25
- 中國(guó)衛(wèi)生政策研究的其它文章
- 英國(guó)NICE衛(wèi)生技術(shù)評(píng)估研究決策轉(zhuǎn)化機(jī)制及對(duì)我國(guó)的啟示
- 我國(guó)老年人醫(yī)療衛(wèi)生支出影響因素研究
- 藥品價(jià)格指數(shù)的方法學(xué)綜述
- 德國(guó)長(zhǎng)期照護(hù)保險(xiǎn)制度:緣起、規(guī)劃、成效與反思
- 全球環(huán)境與衛(wèi)生的關(guān)聯(lián)性:政策響應(yīng)與制度構(gòu)建
- 全球環(huán)境與衛(wèi)生的關(guān)聯(lián)性:科學(xué)認(rèn)知的深化

