N2O5/HNO3硝解烏洛托品制備RDX的機理
王志鑫,楊紅偉,伍 波,呂春緒,程廣斌
(南京理工大學化工學院,江蘇南京210094)
?
N2O5/HNO3硝解烏洛托品制備RDX的機理
王志鑫,楊紅偉,伍波,呂春緒,程廣斌
(南京理工大學化工學院,江蘇南京210094)
摘要:利用13C NMR譜監測了烏洛托品(HA)在N2O5/HNO3和N2O5/HNO3/CH2Cl2硝化體系中硝解反應的歷程,根據實驗13C NMR譜和計算13C NMR譜的解析結果,并結合HA硝解反應過程中可能存在中間體和副產物的13CNMR理論計算結果,提出了硝解歷程中可能存在的中間體與副產物的結構,推測了HA在N2O5/HNO3體系中的硝解歷程為:HA首先與兩分子HNO3結合生成烏洛托品二硝酸鹽(HADN);HADN再經環三亞甲基硝胺母體逐步降解為黑索今(RDX)。
關鍵詞:有機化學;烏洛托品;HA;N2O5/HNO3;RDX;硝解機理;13C NMR
引言
黑索今(RDX)是一種性能優良的高能炸藥,在軍事領域得到廣泛應用[1-2]。目前,RDX的生產工藝主要有直接硝解法和無水醋酸法等[3-5],我國主要采用直接硝解法生產RDX。關于硝酸直接硝解烏洛托品(HA)制備RDX的反應機理,國內外學者進行了大量研究,其機理一般分為兩種:一是逐步降解機理,Dunning等[6]通過對比研究HA在濃硝酸中硝解的放熱率與RDX的生成速率,認為從HA硝解到RDX的反應分為兩個階段,第1階段是生成帶有兩個氮硝基的氮雜六元環(RDX母體),該階段反應快、放熱多;第2階段是生成含3個氮硝基的RDX,該階段反應較慢,為速度控制步驟;二是小分子環合機理,方志杰等[7-10]用核磁共振的方法監測了直接硝解法(濃硝酸硝化體系)和K法硝解法(濃硝酸/硝酸銨硝化體系)制備RDX的硝解反應進程,提出了小分子環合機理。
20世紀80年代,出現了采用N2O5/HNO3體系作為硝化劑的新型硝化技術,其硝化能力可調,反應選擇性好,氧化副產物少,并用于HMX、CL-20等含能材料的制造中[11-12]。以N2O5/HNO3體系作為硝化劑硝解HA制備RDX的工藝已有較多的研究[12-14]。John等[13]考察了反應溫度、反應時間、N2O5用量、HNO3用量對硝解反應的影響,并得到N2O5/HNO3硝解HA制備RDX的最佳反應條件;石煜等[15]提出了HA在N2O5/HNO3體系中可能的硝解歷程,但未對該硝解歷程進行驗證研究。
本實驗利用13C NMR監測了HA在N2O5/HNO3和N2O5/HNO3/ CH2Cl2體系中的硝解反應過程,并對硝解過程中可能存在中間體的13C NMR譜進行了理論計算,在解析核磁共振碳譜的基礎上,推測了HA在N2O5/HNO3體系中可能的硝解機理,以期為N2O5/HNO3硝解HA制備RDX的生產提供參考。
1實驗
1.1試劑與儀器
烏洛托品,AR、發煙硝酸(質量分數95%),南京化學試劑有限公司;五氧化二磷,AR,西隴化工股份有限公司;二氯甲烷,AR,上海凌峰化學試劑有限公司;HNO3(質量分數100%)、N2O5,自制。
JB50-D型增力電動攪拌機,上海標本模型廠;85-2型磁力攪拌器,上海司樂儀器有限公司;DFY-5型低溫恒溫反應浴,南京科爾儀器設備有限公司;SHB-D(III)循環水式多用真空泵,鄭州長城科工貿有限公司;Bruker Avance 300核磁共振儀,瑞士Bruker公司;InVia 激光顯微拉曼光譜儀,英國Renishaw公司。
1.2N2O5/HNO3硝解HA制備RDX
將一定濃度的N2O5/HNO3硝化液(0.75g N2O5和15g HNO3)倒入三口燒瓶中,劇烈攪拌,保持溫度0℃,將1.5g HA緩慢加入到上述硝化體系中,控制加料溫度為0~5℃,加料完畢后在0℃反應1h。反應結束后,向反應液中滴加一定量的去離子水使體系硝酸質量分數降為40%左右,氧化結晶20~30min,有大量白色晶體析出。減壓抽濾,并將得到的濾餅用熱水煮洗,降溫后過濾再水洗至水洗液呈中性,60℃真空干燥10h即可得到產品RDX。
在硝解反應過程中,取0.25mL加料結束的硝解混合液與0.5mL DMSO-d6混合,并用13C NMR測試,取0.25mL反應結束的硝解混合液與0.5mL DMSO-d6混合,并用13C NMR測試。
1.3N2O5/HNO3/CH2Cl2硝解HA
配制100mL的N2O5/ HNO3/CH2Cl2硝解混合液(HNO3濃度為10mol/L),其中HNO3和N2O5的質量比為20∶1,硝解液低溫避光保存。取10mL上述N2O5/HNO3/CH2Cl2硝解混合液倒入三口燒瓶中,劇烈攪拌,保持體系溫度0℃,將0.7g HA(5mmol)緩慢加入到上述硝化體系中,控制加料溫度為0~5℃,加料完畢后,在0℃反應1h。
在硝解反應過程中,取0.25mL加料結束的硝解混合液與0.5mL DMSO-d6混合,并用13C NMR測試;取0.25mL反應結束的硝解混合液與0.5mL DMSO-d6混合,并用13C NMR測試。
取0.7g HA(5mmol)分散于一定體積的CH2Cl2中,在充分攪拌下體系呈懸浮狀,緩慢滴加一定體積的N2O5/HNO3/CH2Cl2硝解混合液(HNO3濃度為10mol/L的),控制加料溫度為0~5℃,加料完畢后,取0.25mL硝解混合液與0.5mL DMSO-d6混合并用13C NMR測試。
2結果與討論
2.1N2O5/HNO3體系硝解HA制備RDX過程中的13C NMR分析
N2O5/HNO3體系加料結束和反應結束時的13C NMR譜圖如圖1所示。
如圖1所示,加料結束和反應結束兩個階段的譜圖信息基本一致,這是由于加料方式采用的是將HA緩慢加入到N2O5/HNO3體系中,硝解反應速率快,加入的HA迅速反應至反應終點狀態。將譜圖中13C信號的化學位移與RDX的13C化學位移對比,可以確定硝解反應終點時各副產物的結構。反應結束時,δ為63.95處的13C信號遠高于其他13C信號,歸屬為RDX的13C信號峰,這與實測的RDX標準物的13C化學位移61.72和理論計算所得RDX的13C化學位移60.42基本一致。根據文獻[7-10]可知,δ為75.25處較高的13C信號峰歸屬為O2NN(CH2OH)2;δ為91.89處較高的13C信號峰歸屬為CH2(ONO2)2,這與兩種化合物理論計算所得13C化學位移(δ為76.23和94.27)基本一致。
2.2N2O5/HNO3/CH2Cl2體系硝解HA過程中的13C NMR分析
根據對N2O5/HNO3體系硝解HA反應液的13C信號監測結果可知,N2O5/HNO3體系硝解HA的反應速率快,通過13C NMR監測雖可以確定該硝解反應終點時各產物的結構,但是無法準確監測反應進程來進行機理研究。因此,實驗過程中改變加料方式,采用惰性有機溶劑CH2Cl2與N2O5/HNO3混合,將HA分散于一定體積的CH2Cl2中,并將N2O5/HNO3/CH2Cl2硝解混合液緩慢滴加到HA和CH2Cl2的混合物中,改變HNO3和HA的物質的量比,利用13C NMR監測反應進程。通過研究隨著硝解劑N2O5/HNO3中HNO3物質的量的增加,硝解反應液中13C化學位移的變化,可以推測N2O5/HNO3體系硝解HA制備RDX的反應機理。
N2O5/HNO3/CH2Cl2體系加料結束和反應結束時的13C NMR譜圖如圖2所示。
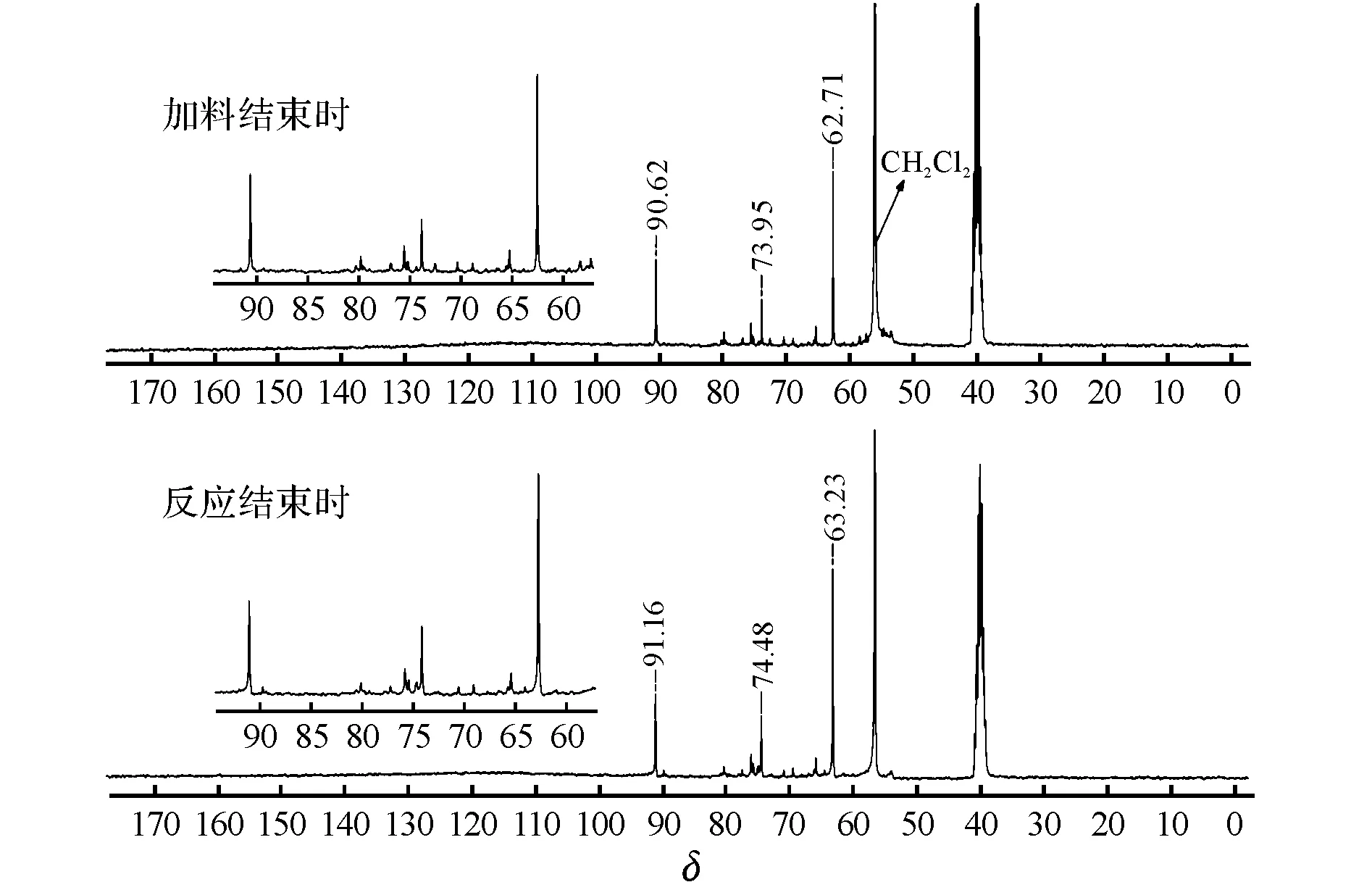
圖2 N2O5/HNO3/CH2Cl2體系的13C NMR譜圖Fig.2 13C NMR spectra of N2O5/HNO3/CH2Cl2nitrating system
通過對比N2O5/HNO3體系和N2O5/HNO3/CH2Cl2體系硝解反應過程中同一階段的碳譜(圖1與圖2加料結束時;圖1與圖2反應結束時),發現反應過程同一階段的碳譜基本一致,因此認為CH2Cl2的加入可能僅是作為惰性有機溶劑存在,并未參與到硝解反應過程中,對實驗結果沒有影響。
當HA與HNO3物質的量比分別為1∶1、1∶2、1∶3、1∶4、1∶6、1∶7、1∶8、1∶9、1∶10、1∶11、1∶13、1∶18時,監測硝解反應液所得到的13C NMR譜圖如圖3~圖5所示,其中HNO3與N2O5的質量比20∶1。
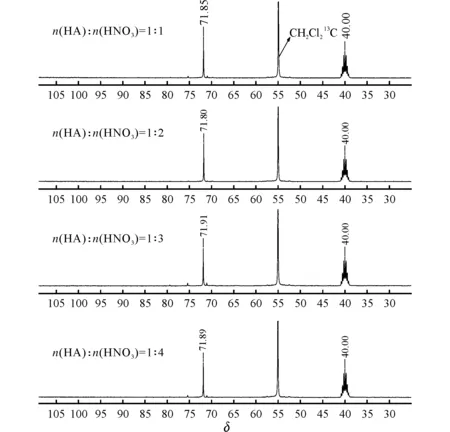
圖3 HA與HNO3物質的量比為1∶1、1∶2、1∶3、1∶4時的13C NMR譜圖Fig.3 13C NMR spectra of HA and HNO3with themolar ratio of 1∶1,1∶2,1∶3,1∶4
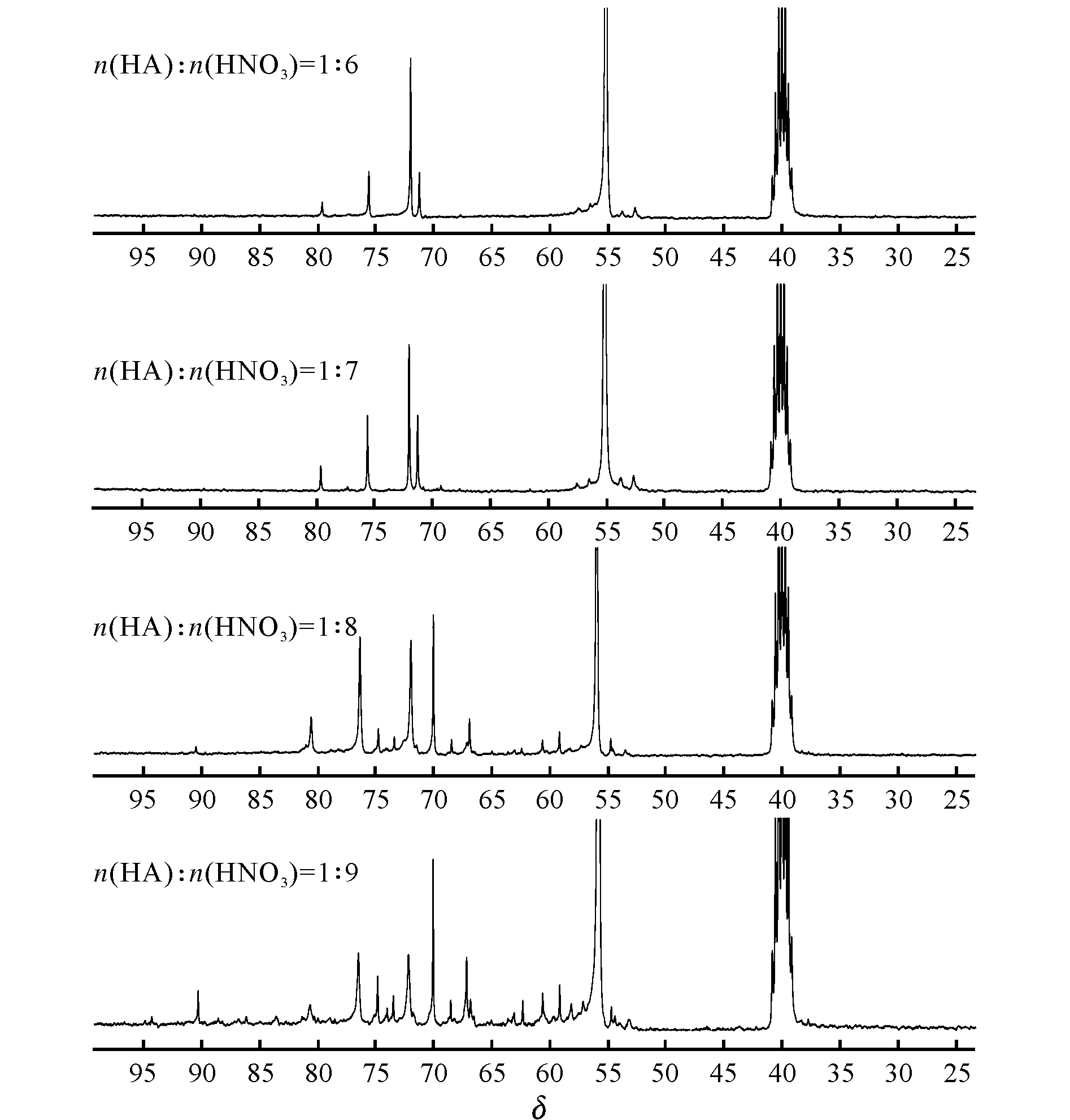
圖4 HA與HNO3物質的量比為1∶6、1∶7、1∶8、1∶9時的13C NMR譜圖Fig.4 13C NMR spectra of HA and HNO3with themolar ratio of 1∶6,1∶7,1∶8,1∶9
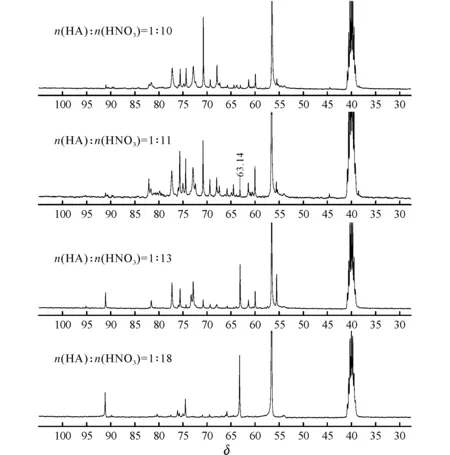
圖5 HA與HNO3物質的量比為1∶10、1∶11、1∶13、1∶18時的13C NMR譜圖Fig.5 13C NMR spectra of HA and HNO3with the molar ratio of 1∶10,1∶11,1∶13,1∶18
由圖3可知,當HA與HNO3物質的量比為1∶1時,δ為72左右最強的13C信號峰可歸屬為烏洛托品一硝酸鹽(HAMN)的13C信號;當HA與HNO3物質的量比為1∶2、1∶3、1∶4時,δ為72左右最強的13C信號峰可歸屬為烏洛托品二硝酸鹽(HADN)的13C信號,即硝解劑N2O5/HNO3較少時,HA與硝解劑N2O5/HNO3反應的主要產物為HADN。
由圖4可知,隨著硝解劑N2O5/HNO3加入量的增加,HADN逐漸開環降解。
由圖5可知,當HA與HNO3物質的量比為1∶10時,HADN的13C信號消失,HADN完全開環降解。當HA與HNO3物質的量比為1∶11時,譜圖中δ為63附近出現明顯的13C信號,在HA與HNO3物質的量比為1∶11時,硝解劑N2O5/HNO3的量已經能夠將開環中間體進一步硝解得到RDX,此時,硝解液中大部分仍為開環中間體,只含有少量RDX。進一步增加硝解劑N2O5/HNO3的加入量,會使得硝解液中更多的開環中間體硝解為RDX,使得RDX的生成量增加。隨著硝解劑N2O5/HNO3加入量的增加,譜圖中RDX的13C信號峰的相對峰高也隨之增高,即硝解液中RDX的含量也在增加。當HA與HNO3物質的量比為1∶18時,該譜圖中RDX與副產物的相對含量與圖1所示的N2O5/HNO3硝解HA反應終點時的譜圖信息基本一致。
2.3硝解過程中可能存在中間體的13C NMR理論計算
在使用N2O5/HNO3體系硝解HA制備RDX的過程中,由于很多中間體和副產物穩定存在于強酸環境中,難以將其從反應體系中離析出來確定其結構,因此對硝解過程中可能存在中間體的13C NMR圖譜進行了理論計算[16],并將計算結果、實驗結果和相關文獻[7-10]數據進行了對比,結果如表1所示。所有計算內容均在Gaussian 09程序[17]中完成,并采用B3LYP/6-311+G**[18]的方法對部分中間體與副產物的結構進行優化并計算了相應的13C化學位移。
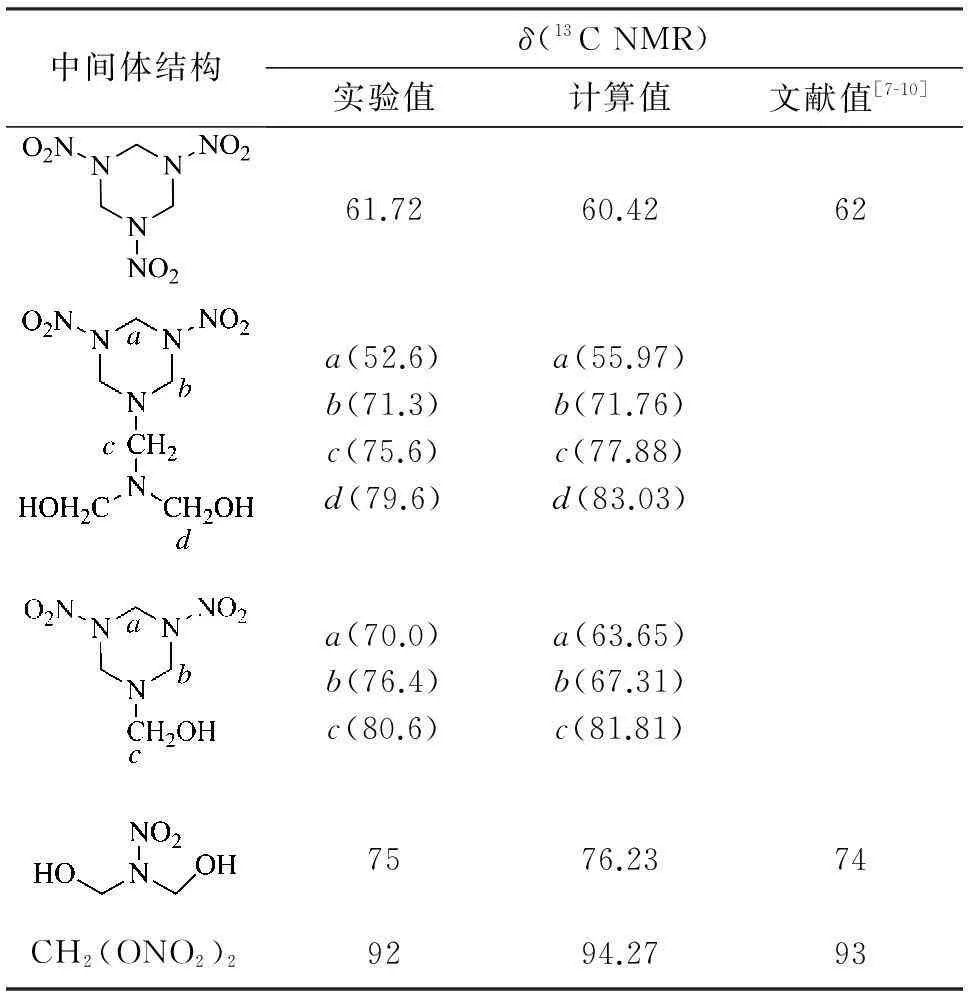
表1 目標產物與中間體的13C NMR實驗值、
由表1可知,中間體化合物13C化學位移的理論計算值與實驗值基本一致,因此,可以確定中間體化合物的結構。
2.4鍵參數的理論計算[19]
為研究HA、HAMN和HADN的穩定性,計算了這幾個化合物中各化學鍵的鍵離解能;HA、HAMN和HADN的結構如圖6所示,HA、HAMN和HADN中各化學鍵的鍵參數計算結果如表2所示。由表2可知,HADN中CH2NH+-CH2的鍵離解能最弱(242.48kJ/mol),同時其鍵長也最長,最易發生斷裂。因此,認為HA在N2O5/HNO3體系中首先形成的是HADN而不是HAMN。
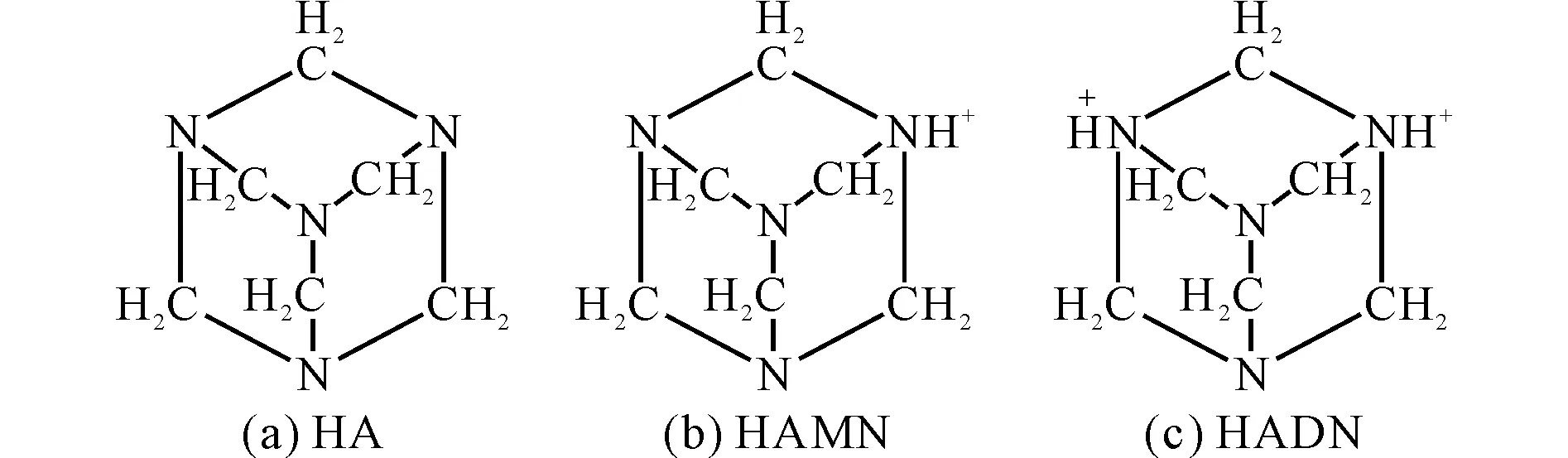
圖6 HA、HAMN和HADN的結構Fig.6 Structures of HA, HAMN and HADN
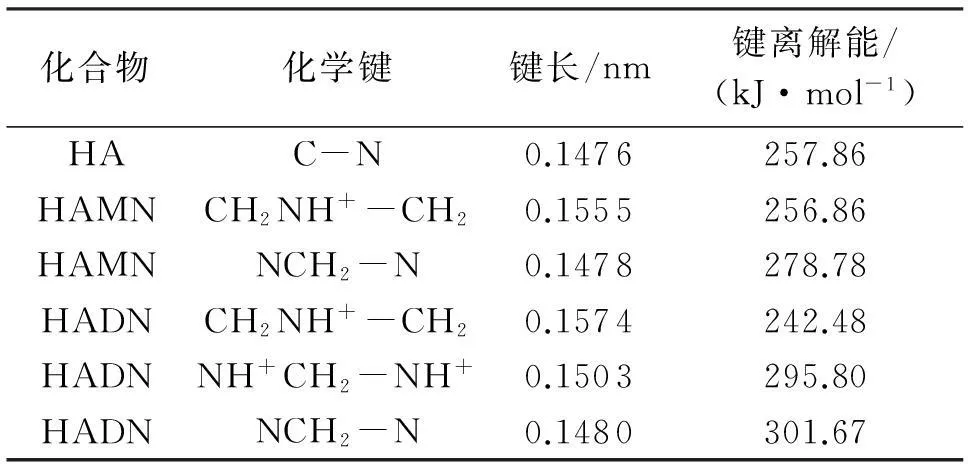
化合物化學鍵鍵長/nm鍵離解能/(kJ·mol-1)HAC-N0.1476257.86HAMNCpNH+-Cp0.1555256.86HAMNNCp-N0.1478278.78HADNCpNH+-Cp0.1574242.48HADNNH+Cp-NH+0.1503295.80HADNNCp-N0.1480301.67
2.5硝解機理分析

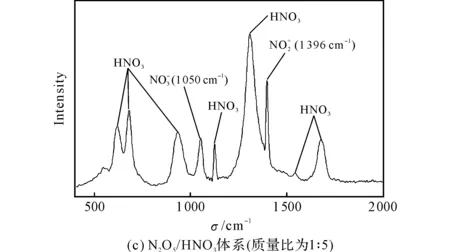
圖7 HNO3及N2O5/HNO3體系的拉曼光譜圖Fig.7 Raman spectra of HNO3and N2O5/HNO3system
綜上所述,通過利用13C NMR監測HA在N2O5/HNO3和N2O5/HNO3/CH2Cl2體系中的硝解反應進程,并根據對硝解過程中碳譜的解析,部分中間體的13C NMR理論計算結果和HA、HAMN、HADN的穩定性計算結果,認為HA在N2O5/HNO3體系中可能主要經歷了如圖8所示的硝解歷程。
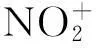
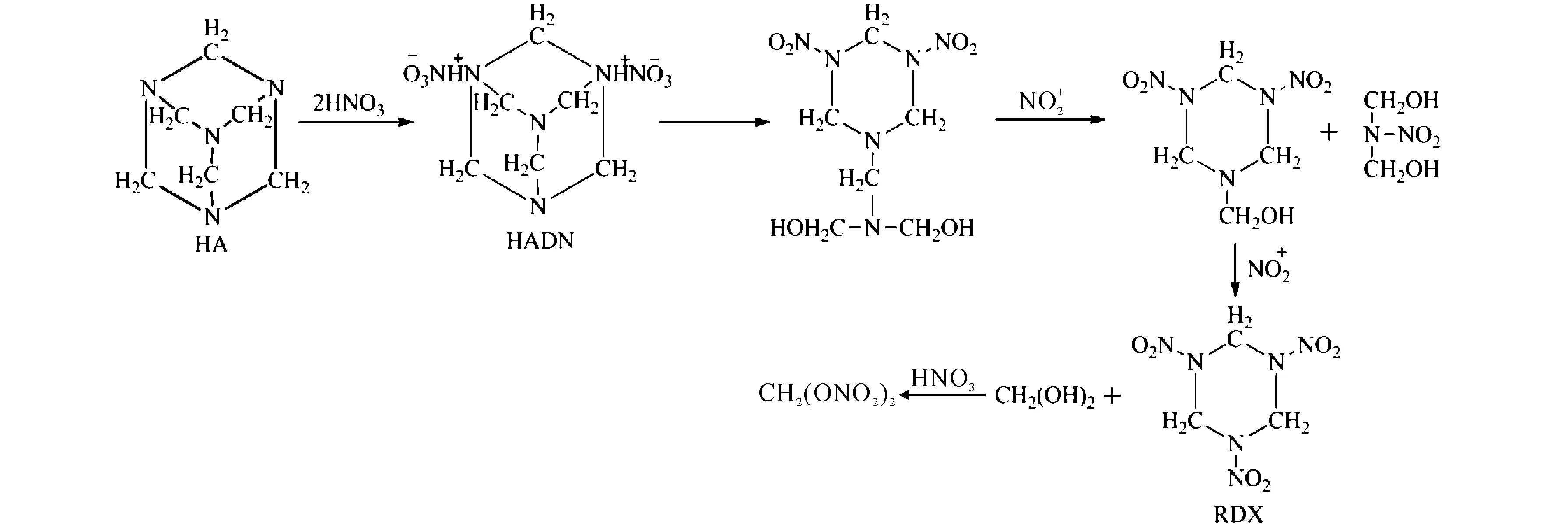
圖8 HA在N2O5/HNO3體系中生成RDX的主要途徑Fig.8 The main approach of the formation of RDX from HA in the N2O5/HNO3system
3結論
(1)用13C NMR監測了HA在N2O5/HNO3體系中的硝解反應進程,并確定硝解反應過程中生成了O2NN(CH2OH)2和CH2(ONO2)2等副產物與中間體。
(2)推測N2O5/HNO3體系硝解HA制備RDX的反應過程是HA首先與兩分子HNO3反應生成HADN,HADN再逐步降解形成RDX的途徑。
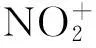
參考文獻:
[1]Olah G A, Squire D R. Chemistry of energetic materials[M]. SanDiego: Academic Press Inc., 1991.
[2]周敬, 楊麗俠, 陳曉明, 等. RDX基高能發射藥的抗撞擊損傷性能[J]. 火炸藥學報, 2013, 36(6): 86-90.
ZHOU Jing, YANG Li-xia, CHEN Xiao-ming, et al. Anti-impact fracture property of RDX-based high-energy gun propellants[J]. Chinese Journal of Explosives and Propellants, 2013, 36(6): 86-90.
[3]曹端林, 曹明保, 李永祥. 綠色硝解技術合成RDX酮[J]. 火炸藥學報, 2004, 27(1): 12-15.
CAO Duan-lin, CAO Ming-bao, LI Yong-xiang. Synthesis of keto-RDX using dinitrogen pentoxide as the nitrating agent[J]. Chinese Journal of Explosives and Propellants, 2004, 27(1): 12-15.
[4]George H C. The nitration of hexamethylenetetramine[J]. Journal of the American Chemical Society, 1925, 47(11): 2754-2763.
[5]Bachmann W E, John S C. A new method of preparing the high explosive RDX[J]. Journal of the American Chemical Society, 1949, 71(5): 1842-1845.
[6]Dunning W J, Millard B, Nutt C W. The heat of nitrolysis of hexamie in nitric acid[J]. Journal of the Chemical Society, 1952: 1264-1269.
[7]FANG Zhi-jie, LI Chen, WANG Shao-fang, et al. Study on the nitrolysis of hexamethylenetetramine by NMR spectrometry[J]. Propellants, Explosives, Pyrotechnics, 1995, 20(2): 83-86.
[8]FANG Zhi-jie, LI Chen, WANG Shao-fang, et al. Study on the nitrolysis of hexamethylenetetramine by NMR spectrometry II. some new evidences of the intermediate of HOCH2NHNO2as a possible precursor to RDX[J]. Propellants, Explosives, Pyrotechnics, 1997, 22(2): 78-80.
[9]FANG Zhi-jie, JU Chen, LI Fu-ping. Study on the nitrolysis of hexamethylenetetramine by NMR spectrometry. Part III: the NMR spectral data of some products and intermediates from the nitrolysis of HA[J]. Propellants, Explosives, Pyrotechnics, 1997, 22(6): 314-316.
[10]FANG Zhi-jie, WANG Shao-fang, LI Fu-ping. Study on the nitrolysis of hexamethylenetetramine by NMR-spectrometry. Part IV: a novel mechanism of the formation of RDX from HA[J]. Propellants, Explosives, Pyrotechnics, 1998, 23(6): 317-319.
[11]何志勇. 離子液體催化N2O5硝解反應制備HMX及硝解機理研究[D]. 南京:南京理工大學,2012.
HE Zhi-yong. Synthesis of HMX by nitrolysis with dinitrogen pentoxide catalyzed by acidic ionic liquid and study on the nitrolysis mechanism[D]. Nanjing: Nanjing University of Science and Technology, 2012.
[12]錢華, 葉志文, 呂春緒. N2O5/HNO3硝化硝解TAIW制備CL-20[J]. 應用化學, 2008(3): 378-380.
QIAN Hua, YE Zhi-wen, Lü Chun-xu. Nitration and nitrolysis of TAIW with N2O5/HNO3to synthesize CL-20[J]. Chinese Journal of Applied Chemistry, 2008(3): 378-380.
[13]John F W, Ronald A L. Direct preparation of 1,3,5-triaza-1,3,5-trinitrocyclohexane from hexamethylenetetramine [J]. Organic Preparations and Procedures International, 1986, 18(4): 281-283.
[14]覃光明, 葛忠學. 含能化合物合成反應與過程[M]. 北京: 化學工業出版社,2011.
[15]石煜. 黑索今的合成工藝研究[D]. 南京:南京理工大學,2010.
SHI Yu. Study on synthetic process of RDX [D]. Nanjing: Nanjing University of Science and Technology, 2010.
[16]張穎. 密度泛函方法在NMR理論計算中的系統研究[D]. 廈門:廈門大學,2008.
ZHANG Ying. Systematic study on DFT prediction of NMR properties[D]. Xiamen: Xiamen University, 2008.
[17]Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 09[CP/CD]. Wallingford CT: Gaussian, Inc., 2009.
[18]John P A, Stephen B J, Rolf S. Theoretical models incorporating electron correlation[J]. International Journal of Quantum Chemistry, 1976, 10(S10): 1-19.
[19]WU Qiong, ZHU Wei-hua, XIAO He-ming. Molecular design of tetrazole- and tetrazine-based high-density energy compounds with oxygen balance equal to zero[J]. Journal of Chemical and Engineering Data, 2013, 58(10): 2748-2762.
[20]Goddard D R, Hughes E D, Ingold C K. Chemistry of nitronium salts. Part I: isolation of some nitronium salts[J]. Journal of the Chemical Society, 1950, 4: 2559-2575.
The Mechanism for the Preparation of RDX from the Nitrolysis of
Hexamethylenetetramine with N2O5/HNO3
WANG Zhi-xin, YANG Hong-wei, WU Bo, Lü Chun-xu, CHENG Guang-bin
(School of Chemical Engineering, Nanjing University of Science and Technology, Nanjing 210094, China)
Abstract:The reaction mechanism for the nitrolysis of hexamethylenetetramine (HA) in the nitrating system of N2O5/HNO3and N2O5/HNO3/CH2Cl2was monitored by using13C NMR spectroscopy. Based on the analytical result of the13C NMR spectrum, and combined the result of calculated13C NMR of the possible intermediates and by-products in the nitrolysis reaction process of HA, the structures of the possible intermediates and by-products in the nitrolysis reaction process of HA were presented. A possible mechanism for the nitrolysis of HA in the nitrating system of N2O5/HNO3was speculated. In the first step, hexamethylenetetramine dinitrate (HADN) was formed via one molecular HA and two molecular HNO3. And then, HADN gradually degrades to RDX via cyclotrimethylenenitramine matrix.
Keywords:organic chemistry; hexamethylenetetramine; HA; N2O5/HNO3; RDX ; nitrolysis mechanism;13C NMR
通訊作者:程廣斌(1967-),男,教授,從事含能材料的合成與應用研究。
作者簡介:王志鑫(1991-),男,碩士研究生,從事含能材料的合成。
基金項目:國家自然科學基金資助(21376121)
收稿日期:2015-07-03;修回日期:2015-10-23
中圖分類號:TJ55; TQ203
文獻標志碼:A
文章編號:1007-7812(2015)06-0045-06
DOI:10.14077/j.issn.1007-7812.2015.06.009

