結構化學中的VSEPR理論與八隅體規則
路慧哲 杜鳳沛
(中國農業大學理學院應用化學系 北京 100193)
結構化學中的VSEPR理論與八隅體規則
路慧哲 杜鳳沛
(中國農業大學理學院應用化學系 北京 100193)
介紹在新型晶體結構中出現的不符合八隅體規則的現象,討論了結構化學教學中VSEPR理論與八隅體規則的相關問題,幫助學生客觀準確地理解相關理論及應用。
結構化學 VSEPR理論 八隅體規則
物質的新結構一直是科學工作者的興趣所在。2013年,美國《科學》雜志發表了在高壓物理領域的最新研究成果《鈉氯間反常計量比化合物》[1],通過理論預測并實驗驗證了在Na-Cl體系中,高壓下存在不符合八電子規則(即八隅體規則)的反常計量比化合物。文中用結構化學的VSEPR理論解釋了這一不符合八隅體規則的情況。
1 VSEPR理論
VSEPR理論即價層電子對互斥理論(valence shell electron pair repulsion theory, VSEPR),以簡單的電子對互斥判斷多原子分子的幾何結構。VSEPR 理論認為:原子周圍各個價電子對之間由于相互排斥,在鍵長一定的條件下,相互間距離愈遠愈穩定。
關于VSEPR理論的發展首先要追溯到1940 年,Sidgwick和Powell[2]分析當時已知的分子結構, 提出了只有單鍵結合的分子, 外層或價電子對盡可能遠離的觀點。其中的價電子對包括成鍵電子對(bond pairs,BP)和孤電子對(lone pairs,LP)。他們認為電子對作用相等, 所有電子對都占有一定的空間, 而且所有的電子對都相互排斥, 稱為Sidgwick-Powell理論。1957年,Gillespie和Nyholm[3]發展了Sidgwick-Powell理論,進一步預測和解釋了一些分子的結構;此后,Gillespie擴充完備了上述觀點,提出了VSEPR理論[ 4-6]。
VSEPR理論忽略了許多次要因素,抓住價層電子對相互排斥這一主要因素,結合簡單的幾何知識對整個分子的構型進行預測。該理論不考慮中心原子的雜化軌道的形狀,僅僅考慮價層電子對的數目,多用于對分子構型的預測,方法簡便而準確。因此,VSEPR 理論已經同經典價鍵理論、雜化軌道理論以及分子軌道理論一并成為大學化學價鍵理論體系的核心內容。
2 VSEPR理論的應用
VSEPR理論能解釋許多化合物的幾何構型[7],是一種簡捷快速地預測多原子分子幾何構型的方法,對于以A為中心的ABn型分子,根據中心原子A的價電子數和成鍵情況,確定其成鍵電子對BP數目(每形成一個BP,原子A貢獻一個價電子,另一個價電子由原子B貢獻) 及孤電子對LP數目的總和。根據電子對盡量遠離的原則,確定分子構型。VSEPR理論認為,成鍵電子對的中心在以A為球心的球面上等距離分布,當成鍵電子對數為2時,其兩中心點是通過球心的直徑兩端,分子為直線形;當成鍵電子對數為3時,其三中心點是通過球心的內接三角形頂點,分子為三角形;當成鍵電子對數為4時,分子為四面體形;當成鍵電子對數為5時,分子為三角雙錐形;當成鍵電子對數為6時,分子為八面體形。以上規則在許多分子的結構分析中得到驗證,簡便而準確。例如:BeCl2,中心原子Be的價電子數為2,與Cl形成兩個成鍵電子對,分子為直線形;BF3,中心原子B的價電子數為3,與F形成3個成鍵電子對,分子為平面三角形;CCl4有4個成鍵電子對,分子為正四面體形;PCl5有5個成鍵電子對,分子為三角雙錐形。

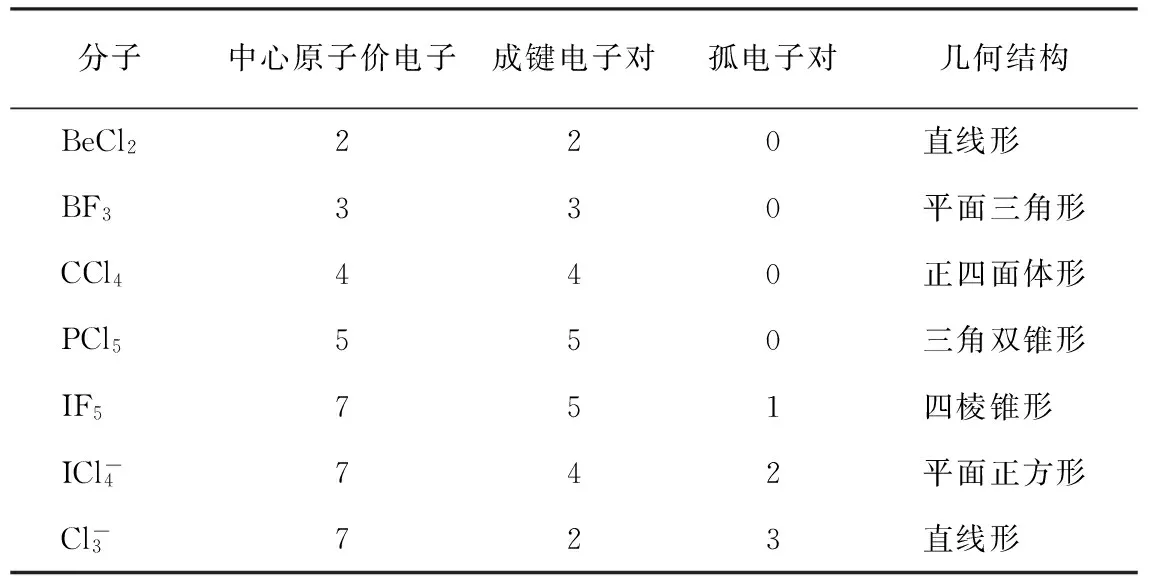
表1 若干分子(或離子)的電子結構與幾何結構

圖1 表1中分子(或離子)的結構示意圖[1,8]


3 VSEPR理論與八電子規則
八電子規則即八隅體規則(octet rule)。1916年,Lewis[9]提出了8電子規則;后來,Langmuir將此規則表述為八隅體規則(octet rule)[10]。
八隅體規則是化學中一個經典而簡單的經驗規則,對于主族元素特別是碳族元素、氮族元素、氧族元素和鹵素元素的化合物,如碳、氮、氧、鹵素、鈉、鎂,由于其價電子構型為s軌道和3個p軌道,各個原子組合成分子時,各電子的價層趨向于都擁有8個電子,與惰性氣體擁有相同的電子排列,即滿足八隅體規則。


4 結語
在學科發展過程中,有些規則的提出確實抓住了事物或現象的客觀規律與某些特征,但同時也往往存在局限性。八隅體規則就是這樣的規則,此規則也是學生在學習基礎化學時的一個基本規則,因此印象深刻。VSEPR理論是結構化學課程中一個簡單而又有效的理論規則,其中不少結構都與八隅體規則不符。本文就新發現的晶體結構,對比了VSEPR理論與八隅體規則中的特殊分子或離子,以期使學生能對這兩個規則有更全面的認識,并加深對學科發展規律的理解。
[1] Zhang W W,Artem R O,Alexander F G,etal.Science,2013,342:1502
[2] Sidgwick N V,Powell H M.ProcRoySocA,1940,176:153
[3] Gillespie R J,Nyho lm R S.QuantRevChemSoc,1957,11:339
[4] Gillespie R J.JChemEdu,1963,40:295
[5] Gillespie R J.InorgChem,1966,5(6):1634
[6] Bader R F W,Gillespie R J,MacDougall P J,etal.JAmChemSoc,1988,110(22):7329
[7] 周公度,段連運.結構化學基礎.第4版.北京:北京大學出版社,2008
[8] 李炳瑞.結構化學.北京:高等教育出版社,2011
[9] Lewis G N.JAmChemSoc,1916,38(4):762
[10] Langmuir I.Science,1921,54(1386):59
VSEPR Theory and Octet-rule in Structural Chemistry
Lu Huizhe Du Fengpei
(CollegeofScience,ChinaAgriculturalUniversity,Beijing100193,China)
By introducing the exceptions to the octet-rule, VSEPR theory and the related problems about octet-rule were discussed in the Structural Chemistry course, helping students understand the related theory and applications.
Structural chemistry; VSEPR theory; Octet-rule
10.3866/pku.DXHX20150675
O6; G64

