來曲唑促排卵在卵巢低反應患者中的應用
徐楗熒,楊桂艷,楊嫦玉,鄭煜麗
(珠海市婦幼保健院生殖中心,珠海 519000)
來曲唑(LE)是高選擇性芳香化酶抑制劑,通過抑制芳香化酶有效地抑制雄激素向雌激素轉化,降低雌激素水平而消除雌激素對腫瘤生長的刺激作用,主要用于乳腺癌患者[1]。因其解除雌激素對下丘腦-垂體-卵巢軸的負反饋作用,使促性腺激素(Gn)分泌增多,促進卵泡募集及發育,近10年其已廣泛用于不育癥患者的促排卵治療[2]。本研究回顧性分析LE用于體外受精-胚胎移植(IVF-ET)促排卵,探討其對不育癥患者子宮內膜、卵母細胞質量及妊娠結局的影響。
資料與方法
一、研究對象
選擇2012年2月至2013年4月在本生殖中心接受IVF-ET助孕的不育癥患者124個周期,隨機分為兩組:A組(62個周期)應用來曲唑促排卵,符合卵巢低反應(POR)標準;B組(62個周期),應用短效促性腺激素釋放激素激動劑(GnRH-a)降調后促排卵的長方案,為對照組,按病例對照研究入選標準為:年齡>35歲、基礎FSH升高,但不符合POR標準。POR按照2011年歐洲人類生殖與胚胎學會(ESHRE)推薦診斷標準[3]:(1)年齡≥40歲或POR(傳統控制性促排卵治療下獲卵數≤3枚)其他危險因素;(2)既往POR;(3)卵巢儲備功能檢驗異常(竇卵泡計數<5~7枚),滿足上述3個條件中的任意兩條。所有患者不育原因包括輸卵管阻塞、子宮內膜異位癥和(或)男方少弱畸形精子癥等。
二、研究方法
1.促排卵方案:(1)A組:月經來潮第3天開始口服LE(江蘇恒瑞醫藥)2.5mg/d,連續服用5d,并于月經第5天后肌注尿人絕經期促性腺激素(HMG,珠海麗珠)150U/d。(2)B組:于前1月經周期黃體期皮下注射短效 GnRH-a 0.1mg/d(博福-益普生,法國),月經第3天后給予基因重組卵泡刺激素(rFSH,默克雪蘭諾,德國)和/或HMG行控制性促排卵,根據患者情況及卵泡長勢調整劑量。兩組患者均于用藥期間行陰道超聲監測卵泡發育,并測定血清黃體生成素(LH)、雌二醇(E2)及孕酮(P)水平。當至少有1個主導卵泡直徑≥18mm時,肌肉注射人絨毛膜促性腺激素(HCG,珠海麗珠)10 000U。
2.取卵及移植:注射后34~36h陰道超聲引導下取卵。卵母細胞培養3~6h后行體外受精,受精16~20h觀察受精卵原核形成情況,孵箱中繼續培養,定期觀察胚胎卵裂情況,取卵后第3天行胚胎移植。
3.妊娠判定:兩組患者均于取卵后每天肌注60mg黃體酮注射液(湖北制藥)行黃體支持。胚胎移植后第14天測定血清中HCG水平,判定是否妊娠,妊娠者繼續黃體支持。移植后第28~35天行陰道超聲檢查見到胎芽及胎心血管搏動者為臨床妊娠。
三、統計學分析
結 果
一、兩組一般情況比較
兩組患者平均年齡分別為(36.9±5.1)歲和(37.6±1.1)歲;兩組不育年限最長者為20年。兩組患者的平均年齡、不育年限、基礎FSH值3項指標相比較,差異均無統計學意義(P>0.05)。A組Gn治療時間及總劑量均低于B組,差異具有統計學意義(P<0.01);A組 HCG日子宮內膜厚度、E2及P水平均低于B組,LH水平高于B組,差異均具有統計學意義(P<0.01)(表1)。
表1 兩組一般情況比較(±s)
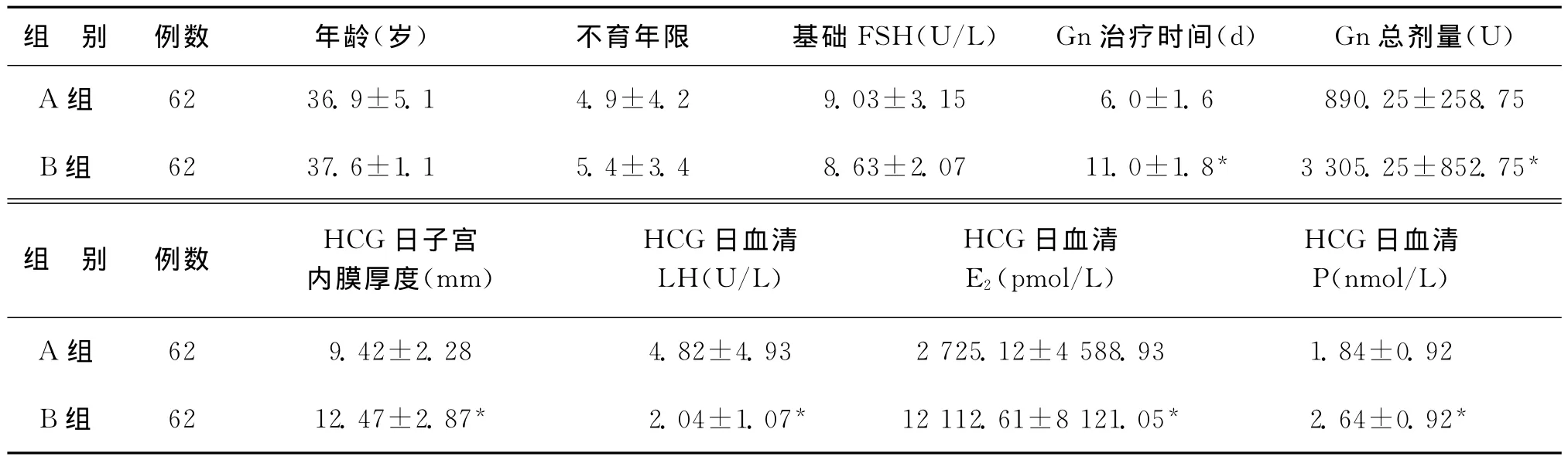
表1 兩組一般情況比較(±s)
注:與A組比較,*P<0.01
組 別 例數 年齡(歲) 不育年限 基礎FSH(U/L) Gn治療時間(d) Gn總劑量(U)A組 62 36.9±5.1 4.9±4.2 9.03±3.15 6.0±1.6 890.25±258.75 B組 62 37.6±1.1 5.4±3.4 8.63±2.07 11.0±1.8* 3 305.25±852.75*組 別 例數 HCG日子宮內膜厚度(mm)HCG日血清LH(U/L)HCG日血清E2(pmol/L)HCG日血清P(nmol/L)A組 62 9.42±2.28 4.82±4.93 2 725.12±4 588.93 1.84±0.92 B組 62 12.47±2.87* 2.04±1.07* 12 112.61±8 121.05* 2.64±0.92*
二、兩組獲卵及受精情況比較
A組中有10例未獲卵,穿刺卵泡數為1~3個;B組均獲卵,兩組未獲卵周期率相比較,差異有統計學意義(P<0.01)。A組平均獲卵數及可移植胚胎數均低于B組,差異均有統計學意義(P<0.01),但受精率及卵裂率兩組比較,差異無統計學意義(P>0.05)(表2)。
三、兩組妊娠結局情況比較
A組中有22例取消周期,B組有4例取消周期,取消周期率分別為35.5%和6.5%,差異有統計學意義(P<0.01);取消周期原因為未獲卵、無正常受精或移植日無優質胚胎。A組臨床妊娠率/取卵周期低于B組,差異具有統計學意義(P<0.01);但兩組的臨床妊娠率/移植周期相比較,差異無統計學意義(P>0.05)。A組胚胎種植率及流產率均高于B組,但差異無統計學意義(P>0.05)(表3)。
表2 兩組獲卵及受精情況比較±s),%]

表2 兩組獲卵及受精情況比較±s),%]
注:與 A組比較,*P<0.01
組62 16.1 2.5±2.2 75.2 84.4 1.2±1.4 B組 62 0* 9.2±3.6* 74.3 78.5 3.4±2.5例數 未獲卵周期率 平均獲卵數 受精率 卵裂率 可移植胚胎數A組別*

表3 兩組妊娠結局情況比較(%)
討 論
隨著IVF-ET技術在臨床的廣泛應用,促排卵方案逐步發展并完善,常用方案有長方案、短方案及拮抗劑方案。在促排卵過程中,有些高齡、基礎FSH升高及卵巢竇狀卵泡數少的患者對藥物反應性差,用較大劑量的Gn也不能獲得滿意的卵母細胞數,POR的發生率為9%~24%[4]。
對于POR,微刺激方案近幾年已較多用于臨床[5]。克羅米芬(CC)及LE是微刺激方案常用藥物,適用于反復IVF-ET失敗、常規促排卵未獲卵及POR患者[6]。CC自1962年用于無排卵性不孕癥患者的促排卵治療,因其有抗雌激素的作用,妊娠率較低。與CC相比,LE有很短的半衰期(48h),能夠快速地從體內清除,并且沒有雌激素受體降調節發生,雌激素靶器官沒有受到不良影響[7]。本中心前期研究顯示,LE用于POR患者,能夠獲得比CC高的種植率和臨床妊娠率,并且對子宮內膜的影響小(P<0.01)[8]。
LE用于促排卵的理論依據有[9-11]:(1)通過抑制雄激素向雌激素轉化而降低雌激素水平,解除雌激素對性腺軸的負反饋作用,使內源性Gn分泌增多;(2)卵巢內雄激素的短暫蓄積,刺激胰島素樣生長因子-1(IGF-1)的表達,促進FSH 受體的表達,增強卵巢對FSH的敏感性,減少Gn使用劑量,尤其是POR的患者;(3)卵巢內高雄激素能促使卵巢更早更多的募集早期卵泡。
IVF-ET中獲得高質量卵母細胞和優質胚胎是良好妊娠結局的基礎。本研究顯示,LE聯合Gn促排卵后受精率(75.2%)和卵裂率(84.4%)能夠獲得與同期行短效GnRH-a降調后促排卵長方案相近的結果;但是,Gn使用時間及總劑量均顯著降低(P<0.01)。由于LE不占據雌激素受體,且半衰期短,對子宮內膜影響小;而且子宮內膜胞飲突較自然周期豐富,白血病抑制因子(LIF)、金屬蛋白酶組織抑制劑-3(TIMP-3)及整合素等表達與自然周期無差異,為胚胎著床提供了較為合適的內環境[12-13]。本研究顯示,LE促排卵后HCG日子宮內膜厚度、胚胎種植率(37.7%)和臨床妊娠率/移植周期(43.6%)也與對照組結果相近。LE促排卵平均獲卵數及可移植胚胎數顯著低于對照組(P<0.01),43.6%患者行單胚移植,對照組移植胚胎個數為2~3枚。因此,LE組胚胎種植率略高于對照組,但差異無統計學意義(P>0.05)。
LE主要適用于IVF-ET助孕中POR患者,在不影響卵母細胞、胚胎質量及臨床妊娠率的前提下能減少Gn使用劑量,降低患者治療費用。但是,LE促排卵作用并不優于短方案。本中心前期研究提示,短效GnRH-a降調后促排卵長方案用于IVFET患者,能夠獲得多枚高質量的胚胎及較高的種植率[14]。因此,LE促排卵不建議用于正常卵巢儲備的患者。
綜上所述,LE促排卵獲得卵母細胞數目少,但其受精及卵裂情況較好,而且對子宮內膜影響小,適宜受精卵著床,更適合POR的IVF-ET患者。LE促排卵后患者的流產率相對較高,可能與患者年齡大、胚胎染色體異常發生率高有關,對胚胎染色體進行檢測是有必要的。
[1]Glück S,von Minckwitz G,Untch M.Aromatase inhibitors in the treatment of elderly women with metastatic breast cancer[J].Breast,2013,22:142-149.
[2]Mitwally MF,Casper RF.Use of an aromatase inhibitor for induction of ovulation in patients with an inadequate response to clomiphene citrate[J].Fertil Steril,2001,75:305-309.
[3]Ferraretti AP,La Marca A,Fauser BC,et al.ESHRE consensus on the definition of ‘poor response’to ovarian stimulation for in vitro fertilization:the Bologna criteria[J].Hum Reprod,2011,26:1616-1624.
[4]Tarlatzis BC,Zepiridis L,Grimbizis G,et al.Clinical management of low ovarian response to stimulation for IVF:a systematic review[J].Hum Rerod Update,2003,9:61-76.
[5]Heijnen EM,Eijkemans MJ,De Klerk C,et al.A mild treatment strategy for in-vitro fertilisation:a randomised noninferiority trial[J].Lancet,2007,369:743-749.
[6]匡延平 .輕刺激-從克羅米芬到來曲唑[J].生殖醫學雜志,2008,17:431-434.
[7]Mitwally MF,Casper RF.Aromatase inhibition reduces gonadotrophin dose required for controlled ovarian stimulation in women with unexplained infertility[J].Hum Reprod,2003,18:1588-1597.
[8]蔡桂豐,許偉標,楊桂艷 .來曲唑和克羅米芬微刺激方案在卵巢功能低下患者助孕結局比較[J].中國婦幼保健,2013,28:3312-3314.
[9]Mukherjee S,Sharma S,Chakravarty BN.Letrozole in a lowcost in vitro fertilization protocol in intracytoplasmic sperm injection cycles for male factor infertility:A randomized controlled trial[J].J Hum Reprod Sci,2012,5:170-174.
[10]Goswami SK,Das T,Chattopadhyay R,et al.A randomized single-blind controlled trial of letrozole as a low-cost IVF protocol in women with poor ovarian response:apreliminary report[J].Hum Reprod,2004,19:2031-2035.
[11]Verpoest WM,Kolibiankis E,Papanikolaou E,et al.Aromatase inhibitors in ovarian stimulation for IVF/ICSI:a pilot study[J/OL].Reprod Biomed Online,2006,13:166-172.
[12]Wallace KL,Johnson V,Sopelak V,et al.Clomiphene citrate versus letrozole:molecular analysis of the endometrium in women with polycystic ovary syndrome[J].Fertil Steril,2011,96:1051-1056.
[13]Cortínez A,De Carvalho I,Vantman D,et al.Hormonal profile and endometrial morphology in letrozole-controlled ovarian hyperstimulation in ovulatory infertile patients[J].Fertil Steril,2005,83:110-115.
[14]蔡桂豐,許偉標,阮永銘,等 .體外受精-胚胎移植中影響胚胎著床的因素分析[J].生殖醫學雜志,2013,22:190-193.

