不同麻醉藥物對肺癌根治術患者全麻蘇醒期躁動的影響
孫建國
肺癌根治術患者全麻蘇醒期躁動是常見的不良反應之一,主要表現為躁動、興奮和定向力障礙并可合并語無倫次、呻吟或哭喊、無理性言語、無意識動作和妄想思維等[1],其興奮和躁動掙扎可影響患者的預后、增加蘇醒期風險,使用鎮靜藥和鎮痛藥為臨床常使用的抑制蘇醒期躁動的方法,常用藥物芬太尼、曲馬多、異丙酚和咪達唑侖等均可在一定程度上減低了術后躁動的發生,但也易引起蘇醒延遲、呼吸抑制等不良反應。地佐辛為μ受體拮抗藥,具有脊髓鎮痛作用和鎮靜作用,不良反應少。右美托咪定為腎上腺素能受體α2受體激動藥,作用于中樞系統,具有中樞鎮靜作用,且具有一定鎮痛作用,并且無呼吸抑制不良反應[2]。本研究擬比較地佐辛和右美托咪定單獨或聯合使用對肺癌根治術患者全麻蘇醒期躁動的影響,探討患者術后躁動治療的合理化用藥方案。
1 資料與方法
1.1 研究對象
選擇2013年1月-2013年12月在我院擇期全麻下行肺癌根治術患者84例,性別不限,ASA分級Ⅰ或Ⅱ級,年齡36~63歲,所有患者術前均未接受放療、化療,術前無嚴重心、肝、腎功能損害。將患者隨機分為4組(n=21):生理鹽水對照組(C組),地佐辛組(D1組),右美托咪定組(D2組),右美托咪定聯合地佐辛組(D3組)。本研究已獲本院醫學倫理委員會批準,并與患者或家屬簽署知情同意書。
1.2 麻醉方法
患者術前均未用藥。入室后常規監測心電圖(ECG)、血壓(BP)及脈搏氧飽和度(SpO2)。建立上肢靜脈通路,局麻下行橈動脈穿刺監測有創動脈壓。麻醉誘導:靜脈注射咪達唑侖0.05 mg/kg,芬太尼2 μg/kg,異丙酚2 mg/kg和維庫溴銨0.15 mg/kg,插入雙腔支氣管導管,經纖維支氣管鏡定位后,行機械通氣。麻醉誘導后行中心靜脈穿刺置管。術中應用七氟醚復合瑞芬太尼、間斷靜脈注射維庫溴銨維持麻醉,維持BIS值40~60。麻醉誘導前15 min至關胸時,D2組和D3組靜脈輸注右美托咪定0.5 μg/kg·h,C組和D1組輸注等容量生理鹽水;開始關胸,D1組和D3組靜脈注射地佐辛0.1 mg/kg,C組和D2組靜脈注射等容量生理鹽水。術畢待患者自主呼吸恢復后,給予新斯的明1 mg和阿托品0.5 mg拮抗肌松,拔除氣管導管,送至PACU。術畢2組患者行舒芬太尼PCIA,PCIA配置:舒芬太尼2 μg/kg+生理鹽水至100 ml,負荷量2 ml,持續輸注量2 ml/h,PCA量1 ml,鎖定時間15 min。
1.3 觀察指標
分別于麻醉誘導前15 min(T1)、氣管導管拔除前15 min(T2)、氣管導管拔除即刻(T3)和氣管導管拔除后15 min時(T4),采集患者血樣測定血漿中IL-10、TNF-α和C-反應蛋白(CRP)濃度。
鎮靜程度采用Ramsay評分法[3]。1分:焦躁不安、焦慮或兩者兼有;2分:合作、安靜、定力正常;3分:僅對指令有反應;4分:入睡,但對強聲刺激或對擊眉間有敏感反應;5分:入睡,但對強聲刺激或對擊眉間反應遲鈍;6分:無反應。躁動程度評價[4]。無:安靜合作;輕度:無行為反應但被詢問時主訴不適;中度:主動并頻繁表示不適;重度:有行為反應且頻繁,四肢亂動,咬導尿管等。重度躁動患者需給予0.5 mg/kg丙泊酚治療。
1.4 統計學方法
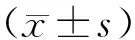
2 結果
4組患者年齡、體重、性別比例、手術時間、術中輸液量及出血量比較差異無統計學意義(P>0.05),見表1。

表1 4組患者一般情況各指標的比較
與T1時比較,T2-T4時C組、D1和D2組血漿IL-10、TNF-α和CRP濃度均升高,D3組血漿IL-10濃度升高(P<0.05);與C組比較,D1、D2和D3組T2-T4時血漿IL-10濃度升高,TNF-α和CRP濃度下降(P<0.05);與D3組比較,C、D1和D2組T2-T4時血漿IL-10濃度下降,TNF-α和CRP濃度升高(P<0.05),見表2。與C組比較,D1、D2和D3組Ramsay評分升高,躁動發生率降低(P<0.05);與D3組比較,C、D1和D2組Ramsay評分降低,躁動發生率升高(P<0.05),見表3。
3 討論
肺癌根治術患者術后蘇醒期躁動是常見的蘇醒期并發癥之一,其對腦血管疾病及心功能不全的患者存在著較大的風險,導致蘇醒期躁動的主要原因為疼痛。
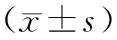
表2 4組患者圍手術期血漿IL-10、TNF-α和CRP濃度比較
注:a為與T1比較,P<0.05;b為與C組比較,P<0.05;c為與D3組比較,P<0.05。

表3 4組患者圍手術期Ramsay評分及躁動情況比較/例
注:a為與C組比較,P<0.05;b為與D3組比較,P<0.05。
臨床常采用抑制蘇醒期躁動的藥物如芬太尼、曲馬多、異丙酚和咪達唑侖等均具有呼吸抑制等不良反應,對患者預后不良[5]。本研究采用地佐辛和右美托咪定來抑制患者蘇醒期躁動。
在臨床上,右美托咪定鎮靜的負荷劑量為1.0 μg/kg,0.2~0.5 μg/kg·h為其維持劑量,本研究采用維持劑量0.5 μg/kg·h,而地佐辛通過預實驗結果和參考臨床劑量最后采用劑量為0.1 mg/kg。
外科手術可引起組織損傷,激活固有免疫系統,導致外周炎癥因子和血細胞因子釋放,中樞神經系統炎癥反應被激活。而炎癥因子、NO、三磷酸腺苷和興奮性氨基酸等可使膠質細胞活化,所以膠質細胞的激活可由中樞神經炎癥反應引起,膠質細胞的激活,引起小膠質細胞和星形膠質細胞釋放大量前列腺素、NO等神經活化因子和TNF、IL-6、IL-1等前炎性細胞因子,作用于突觸前終末,進一步促使興奮性氨基酸和傷害性神經遞質P物質的釋放,作用于與突觸后的背角痛覺傳遞神經元,使其反應性和敏感性增強而處于敏化狀態,最終導致中樞敏化。皮層和皮層下神經環路異常可能為躁動不安的原因[6]。全麻后患者蘇醒過快,皮質下中樞抑制作用解除而大腦皮質尚處于抑制狀態,從而導致局部中樞敏化,大腦皮質和皮質下層功能不平衡導致患者對感覺的反應和處理能力失衡,臨床上表現為躁動[7]。本研究表明,無論單用地佐辛、右美托咪定還是兩者聯合使用,都有效地緩解患者躁動的程度和發生率,且兩者合用抑制躁動效果更佳(P<0.05)。
IL-10是由巨噬細胞、T細胞等產生的抑炎因子,其與促炎因子TNF-α相互作用可調控機體的炎癥反應[8]。TNF-α在感染或者創傷后迅速升高,為敏感的細胞因子在炎癥早期表達,并可啟動炎癥連鎖反應從而引起全身炎癥反應。CRP為1種急性期蛋白,在組織損傷早期顯著升高[9]。本研究中,地佐辛聯合右美托嘧定組患者T2-T4時血漿中的IL-10濃度比T1時明顯升高(P<0.05);地佐辛組、右美托嘧定組患者T2-T4時血漿中的IL-10濃度均明顯比對照組高,而TNF-α和CRP的濃度均明顯比對照組低(P<0.05);與地佐辛聯合右美托嘧定組比較,對照級、地佐辛組、右美托嘧定組T2-T4時血漿IL-10濃度降低,TNF-α和CRP濃度升高(P<0.05)。說明地佐辛和右美托咪定有效地抑制了手術過程中引起的炎癥反應,減少炎癥因子的釋放和增加抑炎因子的釋放,有利于控制炎癥因子反應等引起的蘇醒期躁動。
研究表明,預防患者蘇醒期躁動的一積極處理處理方式為鎮痛,且阿片類藥物的使用有效地降低患者蘇醒期躁動,這些都說明了蘇醒期躁動與疼痛有關[10]。地佐辛為μ受體拮抗藥,且不產生μ受體依賴,其也是κ受體激動藥。因地佐辛具有阿片類受體拮抗劑和激動劑兩種作用,比可待因和嗎啡等具有更強的鎮痛作用。因其不產生μ受體依賴作用,可松弛胃腸道平滑肌,降低惡心嘔吐的發生率和其他不良反應。地佐辛還具有一定的鎮靜作用[11]。本研究中,使用地佐辛的患者的躁動程度和發生率較對照組明顯下降,且具有明顯的鎮靜效果。右美托咪定作用于中樞和外周α2腎上腺素能受體,可產生鎮痛、鎮靜和交感神經活性抑制作用,其作用于腦干藍斑α2受體,激動腎上腺素能受體,產生擬非動眼睡眠狀態的鎮靜作用,并且無呼吸抑制等不良反應。同時可降低肺癌手術應激而引起的心率加快、心律失常、和降低血壓異常升高和術中心肌缺血等心血管事件的發生,有效提高患者拔管的安全[12]。本研究中,使用地佐辛的患者的躁動程度和發生率較對照組明顯下降,且具有明顯的鎮靜效果。而單用地佐辛和右美托咪定的效果不如兩者聯用效果佳,推測兩者合用與減少躁動誘發因素、充分鎮靜鎮痛有關,起到更好地消除中樞敏化的作用。而本研究中,單用地佐辛和右美托咪定或者兩者聯合使用都能夠抑制患者的炎癥反應,可能與藥物在減弱外周炎癥反應的同時,也減輕了中樞炎癥反應,消除中樞敏化作用有關,從而降低躁動發生率。
綜上所述,地佐辛、右美托咪定可有效降低肺癌根治術患者全麻蘇醒期躁動發生率及抑制炎癥反應的發生,且兩種藥物聯合應用效果優于單獨使用。
[1] Yucel A,Begec Z,Ozgul U,et al.The effect of magnesium on emergence agitation in children undergoing adenotonsil lectomy under sevoflurane general anesthesia:a prospective randomised clinical trial〔J〕.Health Med,2012,6(5):11-12.
[2] 萬永靈,陳學鈞,林 濤,等.右美托咪定啶聯合地佐辛對剖胸手術后拔管期血流動力學及鎮痛鎮靜的影響〔J〕.中國藥房,2013,24(38):3616-3618.
[3] Kim YH,Yoon SZ,Lim HJ,et al.Prophylactic use of midazolam or propofol at the end of surgery may reduce the incidence of emergence agitation after sevoflurane anaesthesia〔J〕.Anaesth Intensive Care,2011,39(5):904-908.
[4] 曾兆東,程明華,林樹勇,等.地佐辛與曲馬多術后早期鎮痛效果的比較〔J〕.中國醫藥,2011,6(6):698-699.
[5] 張國生,趙錦芳,朱合波,等.瑞芬太尼對腹腔鏡膽囊切除術病人血液動力學和應激反應的影響〔J〕.中國生化藥物雜志,2010,31(3):210-211,217.
[6] 張 燕,劉雪婷.全麻手術患者蘇醒期躁動原因分析及護理〔J〕.中國醫藥指南,2013,11(3):291-292.
[7] Chen J,Li W,Hu X,et al.Emergence agitation after cataract surgery in children:a comparison of midazolam,propofol and ketamine〔J〕.Paediatr Anaesth,2010,20(9):873-879.
[8] Mizuno J,Nakata Y,Morita S,et al.Predisposing factors a-
nd prevention of emergence agitation〔J〕.Masui,2011,60(4):425-435.
[9] Qihong Z,Ying Z,Mei M.The effects of dezocine on the emergence agitation in patients subjected radical operation for esophageal cancer after propofol-remifentanil anesthesia〔J〕.Anhui Medical Journal,2012,3:16.
[10] Thung A K.Handbook of Pediatric Chronic Pain〔M〕.Spr-
inger:New York,2011:359-374.
[11] 巢齊放,王 強.地佐辛在全麻蘇醒期的應用〔J〕.中國醫學創新,2011,8(19):55-56.
[12] 蔡 暢,郭建榮.右美托咪啶用于全麻術后蘇醒期患者鎮靜的研究〔J〕.中國臨床藥理學與治療學,2011,16(9):1047-1051.

