組織蛋白酶D對CD11b+髓系來源細胞體外增殖、遷徙和侵襲的影響及侵襲機制
孫萬里,周家華
(東南大學附屬中大醫院 肝膽外科,江蘇 南京 210009)
腫瘤患者的預后與腫瘤的侵襲和轉移密切相關[1],遠處轉移已經成為提高患者生存率的主要障礙。有一種新的假說,在腫瘤細胞到達靶器官之前,預轉移小生境(the pre- metastatic niche)會釋放出一些腫瘤相關的可溶性因子,激活一些骨髓來源的細胞(bone marrow- derived cells,BMDCs),這些細胞先于腫瘤細胞而到達靶器官,在那里營造一個適宜腫瘤細胞生存的微環境來迎接腫瘤細胞的到來[2]。Erler等[3]研究認為,原發乳腺腫瘤釋放的、缺氧誘導的賴氨酸氧化酶(lysyl oxidase,LOX)可能是乳腺癌肺轉移中關鍵的可溶性因子。結腸癌釋放的環氧合酶2(cyclooxygenase- 2,COX- 2)在結腸癌定向肝預轉移中可以招募腫瘤相關的巨噬細胞進入預轉移位點,形成預轉移小生境[4]。
胰腺癌是常見的消化道腫瘤,患者死亡的主要原因是胰腺癌引起的轉移性疾病,最常見的轉移部位是肝臟[5],但是,關于在肝轉移過程中胰腺癌通過分泌何種可溶性因子誘導BMDCs至預轉移小生境的研究甚少。我們在前期的研究中證明了組織蛋白酶D前體(組織蛋白酶D precursor,pCath- D)組織蛋白酶D(cathepsin D)是人胰腺癌分泌的促進定向肝轉移的可溶性因子[6]。本單位實驗觀察了胰腺癌分泌的組織蛋白酶D對于CD11b+髓系來源細胞生物學行為的影響,并初步探討其作用機制。
1 材料和方法
1.1 材料
胰腺癌細胞株L3.6pl、L3.6pl- s以及Colo357由本單位實驗室保存。L3.6pl- s細胞是由組織蛋白酶D特異性sh- RNA重組慢病毒感染L3.6pl細胞后,組織蛋白酶D表達明顯下降的細胞株。Transwell小室(8 μm)購自美國Corning公司,基質蛋白膠購自美國BD公司,超濾離心管(截留相對分子質量10 000)購自德國Millipore公司。抗鼠組織蛋白酶D抗體、FITC- anti- CD11b購自美國Biolegend公司。
1.2 方法
1.2.1 細胞培養、條件培養基的收集(conditioned media,CM)及細胞分泌蛋白質的提取 L3.6pl、L3.6pl- s以及Colo357在含有10%胎牛血清的RPMI 1640培養基中培養。當細胞融合至80%~90%時棄去培養中基,用PBS輕柔沖洗4~5次后加入無血清、無酚紅的RPMI 1640培養基置于培養箱中培養24 h后收集。細胞分泌蛋白質的提取采取之前[6]的方法。
1.2.2 裸鼠胰腺癌原位瘤建立 具體實驗方法見文獻[7]。
1.2.3 流式細胞術檢測 種植原位瘤后第3、7天收集肝臟和骨髓的全血細胞,用紅細胞裂解液裂解紅細胞,離心獲得細胞,按照1×106個·μg-1的濃度加入FITC- anti- CD11b避光冰上孵育30 min。PBS洗滌細胞2次,重懸于500 ml PBS中,上機檢測。
1.2.4 組織蛋白酶D表達的測定 蛋白質印跡法檢測胰腺癌細胞系L3.6pl、L3.6pl- s以及Colo357細胞培養上清中組織蛋白酶D的表達。取3組細胞濃縮的分泌蛋白樣品,進行聚丙烯酰胺(SDS- PAGE)凝膠電泳,將蛋白質電轉移至聚偏二氟乙烯膜(PVDF膜)并將膜封閉(封閉液為含5%脫脂奶粉的TBST),封閉結束后,加入適量的一抗組織蛋白酶D抗體(一抗用封閉液1∶1 000稀釋),4 ℃過夜。將膜與辣根過氧化物(HRP)結合的二抗(二抗用封閉液1∶3 000稀釋),室溫下搖蕩孵育1.5 h,然后用TBST充分洗膜,漂洗3次,每次5~10 min。將配置好的顯影液加到PVDF膜上,避光室溫放置1~2 min,稍瀝干顯影液,將膜置于保鮮膜上并將膜包好(盡量避免氣泡)。GAPDH作內參。最后用Image J軟件分析其蛋白相對表達量。
1.2.5 CD11b+髓系來源細胞的分離培養 取3只健康的4~6周齡清潔級BALB/C小鼠,常規獲得骨髓的全血細胞后裂解紅細胞,離心獲得骨髓細胞, PBS離心洗滌細胞2次(800 r·min-1,5 min)。棄上清,以含有青鏈雙抗的少量PBS重懸,并與適量的熒光標記的FITC- anti- CD11b抗體結合。避光冰上孵育30 min后,用流式細胞儀分選,以含15%胎牛血清的RPMI 1640接種至25 cm2的塑料培養瓶中,加入GM- CSF 50 ng·ml-1,置于37 ℃、5%CO2培養箱中培養。
1.2.6 MTT比色法檢測細胞增殖水平 將CD11b+髓系來源細胞分別用含有L3.6pl- CM、Colo357- CM、L3.6pl- CM+抗組織蛋白酶 D、鼠組織蛋白酶D(10 ng·ml-1)、L3.6pl- s- CM的15%胎牛血清RPMI 1640重懸,對照組以單獨含有15%胎牛血清RPMI 1640重懸。調整細胞密度為10 000個·孔-1接種于96孔板中,每組設5個復孔。分別培養48 h后,每孔加入20 μl的MTT后繼續置入培養箱4 h,去上清后加入150 μl二甲基亞砜(DMSO)低速振蕩10 min使用酶標儀檢測,以570 nm波長處的光吸收值代表細胞活力,每組實驗重復3次。
1.2.7 Transwell小室實驗 (1) CD11b+髓系來源細胞遷徙實驗:每個小室上室面(直徑8 μm)加入50 μl含10 ng·ml-1BSA的無血清RPMI 1640,37 ℃放置30 min,然后加入無血清CD11b+髓系來源細胞懸液100 μl(5×105個·ml-1),將小室的上室面置入含有不同腫瘤上清的下室中,在37 ℃、5%CO2條件下孵育24 h。棉球擦盡上室表面細胞后用乙醇固定和0.2%結晶紫染色10 min,顯微鏡下觀察穿入膜內細胞。(2) CD11b+的髓系來源細胞侵襲實驗:預先將基質蛋白膠在4 ℃過夜,變成液態后加入無血清培養液配成基質蛋白膠混合液(基質蛋白膠∶培養基=1∶8)。在加入細胞懸液前,中間微孔膜表鋪被200 μl 基質蛋白膠混合液,置于細胞培養箱4 h后吸盡成膠表面的液體,其余操作同細胞遷徙實驗。
1.2.8 基質金屬蛋白酶(MMP- 2)蛋白表達的測定 蛋白質印跡法檢測分別經過L3.6pl- CM、Colo357- CM、L3.6pl- CM+抗組織蛋白酶D、鼠組織蛋白酶D(10 ng·ml-1)、L3.6pl- s- CM處理的CD11b+髓系來源細胞中MMP- 2的表達。按照常規方法,分組加入蛋白裂解液提取總蛋白,制備樣品進行SDS- PAGE凝膠電泳,余具體方法同前。一抗MMP- 2抗體用封閉液稀釋(1∶400)。
1.3 統計學處理
2 結 果
2.1 流式細胞術檢測CD11b+髓系來源細胞比例
L3.6pl荷瘤鼠第3天、第7天肝臟中CD11b+細胞比例(33.44%±0.029%、38.15%±0.017%)明顯高于Colo357荷瘤鼠肝臟中的細胞比例(5.19%±0.009 %,6.76%±0.013%),差異均有統計學意義(均P<0.05)。
2.2 蛋白質印跡法檢測胰腺癌細胞培養上清中組織蛋白酶D的表達
蛋白質印跡法檢測結果顯示,L3.6pl- CM中組織蛋白酶D的表達明顯高于L3.6pl- s- CM和 Colo357- CM中的表達,見圖1。

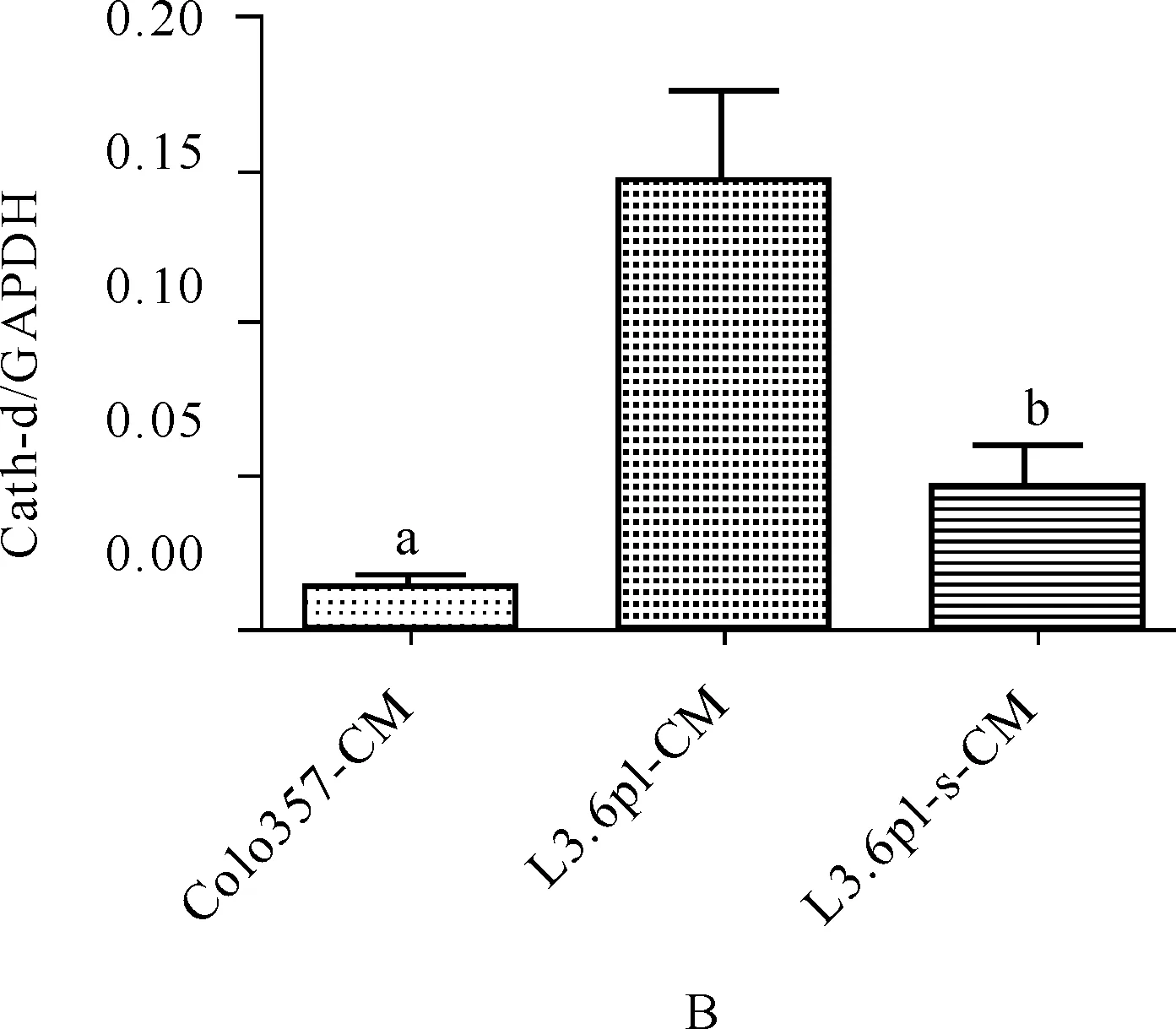
與L3.6pl- CM和L3.6pl- s- CM比較,aP<0.05;與L3.6pl- s- CM比較,bP<0.05
圖1腫瘤細胞上清液組織蛋白酶D的表達A.腫瘤細胞上清液組織蛋白酶D電泳圖;B.腫瘤細胞上清液組織蛋白酶D半定量統計圖
Fig1TheexpressionofCathepsinDoftumorconditionedmedia
2.3 MTT檢測組織蛋白酶D對CD11b+髓系來源細胞增殖的影響
CathepsinD促進CD11b+髓系細胞的增殖,含有重組鼠組織蛋白酶D(0.267±0.034)對細胞的增殖相比于在含有L3.6pl- s- CM組(0.158±0.012)、Colo357- CM組(0.153±0.005)明顯增加(P<0.05),而添加了阻斷劑之后,則增殖明顯受到抑制(0.166±0.008)(P<0.05)。
2.4 Transwell小室實驗
Anti- 組織蛋白酶D抑制CD11b+髓系細胞的遷徙和侵襲。在遷徙實驗中,培養24 h后,含有重組鼠 組織蛋白酶D組遷徙到膜內的細胞數量(36.666±4.932)明顯高于L3.6pl- s- CM組(19.333±1.527)及Colo357- CM組(13.778±3.065)(P<0.05),而在CathepsinD被阻斷后遷徙細胞數量明顯減少(26.333±3.511,P<0.05)。
在侵襲實驗中,培養24 h之后,含有重組鼠組織蛋白酶D組細胞侵襲進入微孔膜的數量(19.333±4.725)明顯多于含有L3.6pl- s- CM組(9.778±3.055)和Colo357- CM組(4.333±1.154)(P<0.05),而在組織蛋白酶D被阻斷后細胞侵襲數量(14.66±2.561)明顯減少(P<0.05)。
2.5 CD11b+髓系細胞中MMP- 2蛋白變化的表達
見圖2。
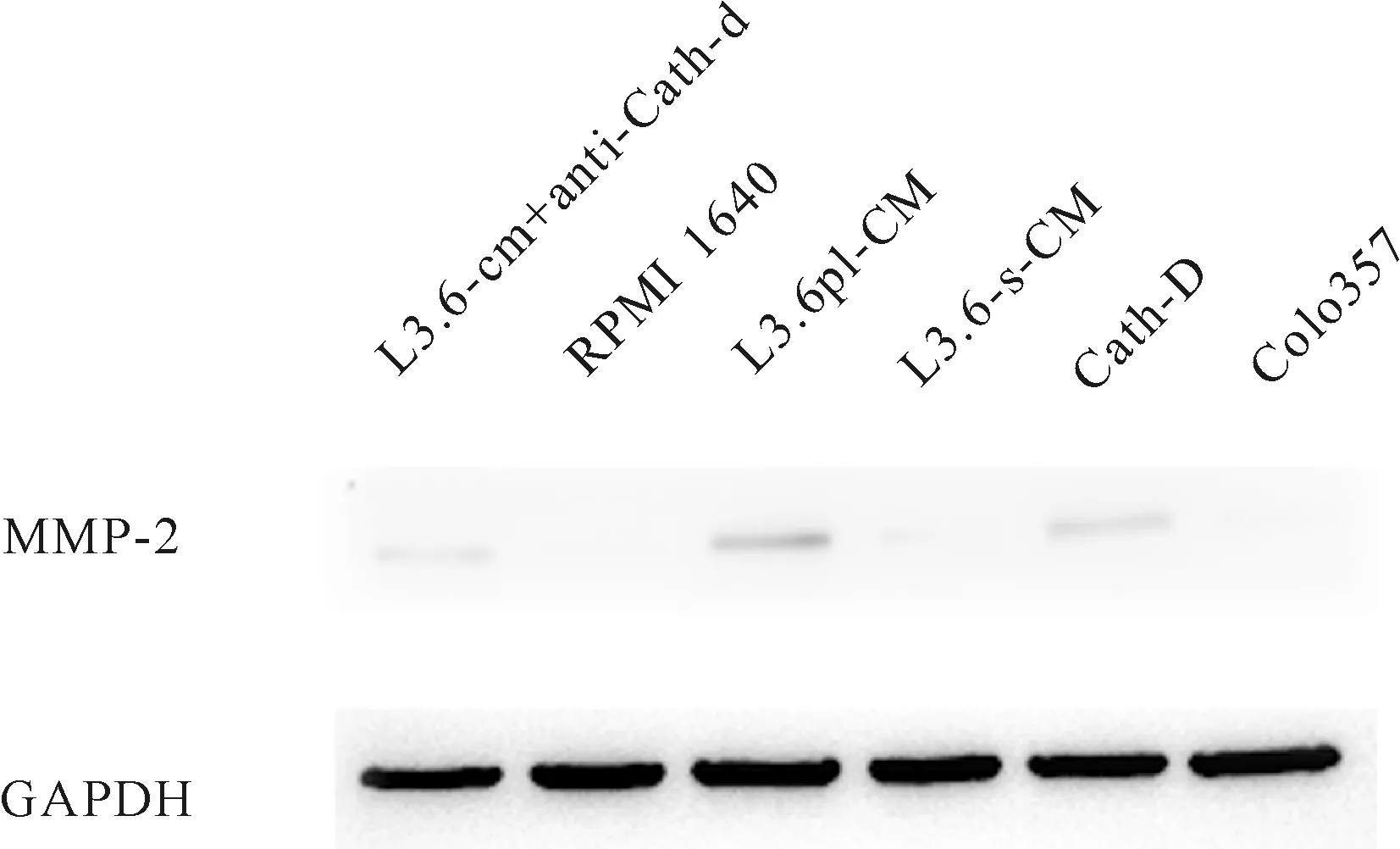
圖2CD11b+髓系細胞MMP- 2蛋白表達
Fig2TheexpressionofMMP- 2proteininCD11bpositivebonemarrowderivedcells
3 討 論
目前的研究表明,表達血管內皮生長因子受體- 1、CD11、CD34的造血祖細胞以及CD11b+的髓系來源細胞在腫瘤細胞到達前就預先到在轉移位點形成了預轉移小生境[2]。在腫瘤目標性轉移器官中,CD11b+細胞被大量招募[8]。CD11b+細胞可以通過多種方式、途徑促進腫瘤的增長和轉移。研究者認為,CD11b+髓系來源細胞的招募在預轉移小生境的形成中起到了主要的作用[9]。在本實驗中觀察到預轉移期內L3.6pl原位移植瘤模型骨髓和肝臟中CD11b+髓系來源細胞的比例明顯增加,且明顯高于Colo357原位移植瘤模型骨髓和肝臟中此細胞的比例。這個結果表明,在胰腺癌肝轉移中大量的CD11b+髓系來源細胞被動員并招募到預轉移的器官,構成預轉移小生境。
在體內預轉移小生境的形成過程中,腫瘤分泌特殊的可溶性因子發揮著重要的作用。在先期研究中發現,p 組織蛋白酶D / 組織蛋白酶D是人胰腺癌分泌的促進定向肝轉移的可溶性因子。本實驗也證明了人胰腺癌細胞株L3.6pl所分泌的組織蛋白酶D明顯高于人胰腺癌細胞株Colo357所分泌的組織蛋白酶D(見圖1)。組織蛋白酶D是一種廣泛存在于各種組織細胞中的一種溶酶體蛋白酶,其在許多腫瘤中表達增高,它不但可以促進腫瘤細胞的增生,而且可以促進腫瘤的浸潤和轉移[10]。本研究探討胰腺癌分泌的可溶性因子組織蛋白酶D是否對CD11b+髓系來源細胞的體外生物學行為有影響。用流式細胞儀分選出小鼠骨髓中的CD11b+細胞用于體外培養并進行下一步的研究。在MTT增殖實驗中看到,組織蛋白酶D對CD11b+髓系細胞的增殖具有很明顯的促進作用,阻斷組織蛋白酶D后則促增殖的作用明顯受到抑制。通過流式分析儀可以觀察到,在裸鼠自身肝臟中含有著很少量的CD11b+的細胞,而荷瘤裸鼠肝臟中CD11b+的細胞明顯增多,預轉移小生境中的髓系細胞是由骨髓、外周血以及原發腫瘤中遷移而來的,而從后面的細胞增殖實驗的結果我們發現,組織蛋白酶D對于CD11b+髓系來源細胞有一定的促增殖作用,我們猜想預轉移小生境的髓系細胞的組成一部分是遷徙而來的,另一部分則是由遷徙來的骨髓細胞增殖而成的。這是我們后續關注的一個方面。骨髓細胞的遷徙是預轉移小生境形成的一個關鍵性環節。本實驗以Transwell小室為模型,觀察組織蛋白酶D在CD11b+髓系來源細胞的遷徙實驗中發揮的作用,發現組織蛋白酶D能夠顯著地提高CD11b+髓系來源細胞的遷徙能力,阻斷它后遷徙的細胞數量明顯下降,同樣也發現L3.6pl- CM對遷徙的影響大于單純含有組織蛋白酶D的影響。骨髓細胞是通過擴增、遷徙和侵襲一步步地定植到預轉移器官。我們觀察到組織蛋白酶D對CD11b+髓系來源細胞侵襲能力是有影響的,同樣通過Transwell小室模型,我們觀察到組織蛋白酶D對CD11b+髓系來源細胞侵襲力有一定的促進作用。Coussens等[11]認為,BMDCs的侵襲力的增加與MMPs激活相關。通過蛋白質印跡法觀察到,組織蛋白酶D對于CD11b+髓系來源細胞MMP- 2的激活有重要作用。Erler等通過研究發現,LOX可以增強CD11b+髓系來源細胞MMP- 2的活性,從側面證實MMP- 2在CD11b+髓系來源細胞的侵襲中發揮了一定的作用。組織蛋白酶D參與惡性腫瘤的浸潤和轉移,目前主要認為是其活性肽AP片段發揮著重要的作用。已有研究認為,腫瘤以及免疫細胞產生一些在CD11b+髓系來源細胞的募集及擴增中發揮著重要作用的因子,包括血管內皮生長因子、COX、粒細胞、巨噬細胞集落刺激因子(GM- CSF)、IL- 4和IL- 6。Deng等[12]認為,髓系細胞中S1PR1- STAT3信號途徑在預轉移小生境的形成中發揮著重要的作用。但是組織蛋白酶D與髓系細胞中STAT3和JAK直接激活的相關性研究未見報道,也不清楚AP片段是否與其有關,故組織蛋白酶D是如何動員并遷徙CD11b+髓系來源細胞的機制還未闡釋清楚。
從上述實驗結果中觀察到,純化的組織蛋白酶D能獨立誘導CD11b+髓系來源細胞動員,但與L3.6pl- CM組的結果比較發現,其誘導CD11b+髓系來源細胞動員的能力低于L3.6pl- CM,可能的原因是L3.6pl- CM中蘊含有其他的可溶性因子,同樣可以誘導CD11b+髓系來源細胞,或這些可溶性因子對組織蛋白酶D的誘導作用有協同效應,能促進組織蛋白酶D對CD11b+髓系來源細胞的動員。目前的研究中高轉移性的胰腺癌細胞系L3.6pl- CM中有很多的可溶性因子,包括有血管內皮生長因子和COX,這在一定程度上解釋了L3.6pl- CM動員并遷徙CD11b+髓系來源細胞的能力強于單純的組織蛋白酶D的動員能力。
綜上所述,我們發現,在胰腺癌肝轉移模型中CD11b+髓系來源細胞大量招募到肝臟中并參與形成預轉移小生境,體外實驗中組織蛋白酶D可以促進CD11b+髓系來源細胞的增殖、遷徙,并且通過增強MMP- 2來促進它的侵襲。本實驗僅僅是從體外實驗說明了組織蛋白酶D能動員CD11b+髓系來源細胞,而缺乏在體內方面的研究,我們將在后續的實驗中對此進一步完善明確。
[1] CAIRNS R A,KHOKHA R,HILL R P.Molecular mechanisms of tumor invasion and metastasis:an integrated view[J].Curr Mol Med,2003,3(7):659- 671.
[2] KAPLAN R N,RIBA R D,ZACHAROULIS S et al.VEGFR1- positive haematopoietic bone marrow progenitors initiate the pre- metastatic niche[J].Nature,2005,12:820- 827.
[3] ERLER J T,BENNEWITH K L,COX T R,et al.Hypoxia- induced Lysyl Oxidase is a critical mediator of bone marrow cell recruitment to form the premetastatic niche[J].Cancer Cell,2009,15:35- 44.
[4] YAMAMOTO M,KIKUCHI H,OHTA M,et al.TSU68 prevents liver metastasis of colon cancer xenografts by modulating the premetastatic niche[J].Cancer Res,2008;68(23):9754- 9762.
[5] YACHIDA S,IACOBUZIO- DONAHUE C A.The pathology and genetics of metastatic pancreatic cancer[J].Arch Pathol Lab Med,2009,133(3):413- 422.
[6] 胡方方,周家華.胰腺癌肝轉移相關分泌蛋白質的篩選[J].東南大學學報:醫學版,2010,29(4):367- 372.
[7] 余澤前,周家華.紅色熒光蛋白標記的胰腺癌裸鼠原位移植瘤轉移模型的建立[J].中華外科雜志,2009,47(14):1092- 1095.
[8] HIRATSUKA S,WATANABE A,ABURATANI H,et al.Tumour- mediated upregulation of chemoattractants and recruitment of myeloid cells predetermines lung metastasis[J].Nat Cell Biol,2006,8(12):1369- 1375.
[9] GIL- BERNABé A M,FERJANCIC S,TLALKA M ,et al.Recruitment of monocytes/macrophages by tissue factor- mediated coagulation is essential for metastatic cell survival and premetastatic niche establishment in mice[J].Blood,2012,119(13):3164- 3175.
[10] VASHISHTA A,OHRI S S,PROCTOR M,et al.Ribozyme- targeting procathepsin D and its effect on invasion and growth of breast cancer cells:an implication in breast cancer therapy[J].Int J Oncol,2007,30(5):1223- 1230.
[11] COUSSENS L M,WERB Z.Inflammation and cancer[J].Nature,2002,420(6917):860- 867.
[12] DENG J,LIU Y,LEE H,et al.S1PR1- STAT3 signaling is crucial for myeloid cell colonization at future metastatic sites[J].Cancer Cell,2012,21(5):642- 654.

