2型糖尿病患者輕度認知功能障礙與血尿酸的相關性
周 穎 王愛民 譚 紅
(長沙市第一醫院神經內科,湖南 長沙 410005)
許多資料顯示,糖尿病患者中有60-70%存在輕中度認知功能障礙,空腹血糖受損或糖尿病的婦女認知功能損害的風險增加了將近一倍〔1〕。但目前對2型糖尿病引起的認知功能障礙的病因及發病機制尚不十分清楚。以往研究提示氧化應激損傷、炎癥反應和脂質代謝紊亂等與MCI的發病具有相關性〔2,3〕。人體內存在抗氧化劑-促氧化劑尿酸鹽氧化還原系統,血尿酸(UA)在一定范圍內具有抗氧化特性,對人體具有保護作用;但血UA水平過高時,UA變得具有促氧化特性,便成為致病因素。目前,UA在糖尿病認知功能障礙中的作用未見報道。本研究探討2型糖尿病合并輕度認知功能障礙(MCI)與血UA水平的關系。
1 對象與方法
1.1研究對象 選擇2009年8月至2011年12月在我科住院的2型糖尿病患者105例,男58例,女47例,平均年齡(62.32±6.68)歲。分為無MCI組50例和MCI組55例。兩組間性別、年齡等一般資料間無顯著差異。見表1。糖尿病診斷依據1999年世界衛生組織(WHO)發表的診斷標準。MCI的診斷符合國際MCI工作組標準和歐洲阿爾茨海默并聯合會MCI工作組標準〔4,5〕,包括:①認知功能下降;②日常基本能力正常,復雜的工具性日常能力可以有輕微損害;③無癡呆。排除標準:①有相關精神疾病史、焦慮抑郁癥、服抗抑郁藥物、甲狀腺功能減退、嚴重心肺功能不全、2型糖尿病急性并發癥;②有其他引起中樞神經損傷的疾病史,如腫瘤、感染、CO中毒、中樞神經脫髓鞘疾病、正常壓力性腦積水和變性疾病等;③嚴重視、聽功能障礙和失語(RVR<6分)而不能參與檢查者;④排除服用利尿劑和其他影響UA代謝藥物的患者。
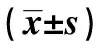
表1 兩組2型糖尿病患者的一般情況
1.2方法
1.2.1資料收集 記錄患者一般資料,包括性別、年齡、身高、體重、受教育程度、病程、現病史、用藥史、既往史和家族史等。
1.2.2調查工具 ①認知功能篩查:采用簡易智力狀態檢查表(MMSE)對認知功能進行評分,最高分30分,MCI:中學以上25~27分,小學21~24分,文盲18~21分。②日常生活能力評定量表(ADL)對日常基本生活能力和工具性日常能力評分(20項版本),MCI:<26分。所有量表評分1次完成,調查過程患者及家屬共同參與。
1.2.3血液樣本收集和測定 所有患者均于晨起空腹抽取靜脈血5 ml,檢測FPG、HbAlc、血UA、血SCr、LDL、hs-CRP。
1.3統計學方法 應用SPSS12.0統計學軟件,兩組間計量資料數據檢驗用方差分析,計數資料數據檢驗用Kolmogorov-Smirnov檢驗;采用逐步多元線性回歸法對糖尿病認知功能的相關因素進行分析。
2 結 果
以MMSE評分為因變量,用逐步多元回歸分析法在回歸方程中引入年齡、性別、受教育年限、冠心病、高血壓、腦血管病、吸煙、FPG、HbA1c、血UA、血SCr、LDL、hs-CRP。建立回歸方程:Y=32.645-0.017X1+0.204X2-0.368X3-0.668X4。見表2。

表2 MMSE影響因素的回歸分析
3 討 論
MCI泛指認知功能下降但沒有達到癡呆的人群,是介于正常衰老和癡呆的中間狀態,其發展為癡呆的危險性是正常老人的10倍〔6〕,部分患者是癡呆的前期階段。因此,對于MCI的早期發現以及明確MCI的危險因素并進行有效控制是防止MCI發生發展的重要環節。
在發展中國家2型糖尿病存在某些方面的認知障礙,特別是其學習、記憶能力受損,比普通人群認知功能障礙的風險增加〔7〕。目前,許多研究表明影響2型糖尿病患者認知功能的危險因素包括年齡、基因、病程、血糖、血壓、藥物、HbA1c、胰島素抵抗等〔8,9〕。本研究結果提示高UA水平可能與2型糖尿病認知功能障礙有關。在多元回歸分析結果提示UA水平和血糖控制情況、糖尿病的腦血管并發癥較其他因素對糖尿病患者發生MCI的影響更大。
目前研究認為UA在認知功能障礙中的可能作用機制是氧化應激損傷〔10〕和血管病變〔11,12〕。高水平的血UA可導致微炎癥狀態及氧化應激,使血管內皮功能發生紊亂,進而導致微血管病變及小動脈玻璃樣變,大血管硬化等改變〔11〕。在腦組織處于缺血缺氧狀態時,缺血缺氧可造成海馬神經元膜磷脂代謝障礙,自由基過量生成,興奮性氨基酸大量釋放,細胞內鈣離子超載等病理生理改變,最終導致海馬膽堿能神經元死亡及膽酰乙酰轉移酶活性下降,造成患者出現認知功能障礙〔12〕。Schretlen等〔13〕在對96例健康老年人的臨床研究發現,生理范圍內處于中等偏高UA水平者比偏低者在三個認知域中的測試評分要低,包括運算速度、執行能力和語言記憶方面。然而,也有研究表明阿爾茨海默病(AD)和血管性癡呆(VD)患者的血尿酸水平較對照組低,提示UA可以降低癡呆發生發展的風險,本研究的結果與此不一致,原因可能為UA具有抗氧化和促氧化雙重性質,在細胞外和體外環境中UA可清除氧自由基抗氧化損傷;在細胞內UA可誘導內皮損傷、自由基產生、炎癥反應從而促進氧化損傷〔14,15〕。
因此,2型糖尿病患者中UA水平增高導致認知功能障礙的可能機制為:①首先2型糖尿病患者可能存在胰島素抵抗,一方面胰島素抵抗使血漿胰島素水平升高,從而引起腎排出UA減少;一方面胰島素抵抗影響糖酵解中間產物轉移,促進血UA生成;另一方面胰島素抵抗可增加肝臟脂肪的合成,導致嘌呤代謝紊亂,引起血UA升高;②糖尿病患者多存在大血管和微血管病變,腎微血管病變可導致腎血流下降,而致血UA增高;③UA在一定高水平條件下,可通過一系列反應生成自由基,增加脂質的氧化作用,介導多種氧化前體對血管內皮的損傷,減少NO生成從而導致血管內皮功能失調,促進動脈粥樣硬化及腦白質缺血,促使認知功能減退。所以,在2型糖尿病中,高水平UA和血管病變互為因果,進一步加重了MCI發生的危險。
綜上,高水平血UA與2型糖尿病患者認知功能下降有關,血UA水平與認知功能相關性的深入研究將有利于認知功能的早期診斷和合理治療。
4 參考文獻
1Allen KV,Frier BM,Strachan MW.The relationship between type 2 diabetes and cognitive dysfunction:longitudinal studies and their methodological limitations〔J〕.Eur J Pharmacol,2004;490(1-3):169-75.
2Ana F,Masaki T,Umeno Y,etal.Correlations between homocysteine levels and atherosclerosis in Japanese type 2 diabetic patients〔J〕.Metabolism,2007;56(10):1390-5.
3李 浩,吳 敏,姚明江,等.老年輕度認知功能障礙與氧自由基代謝、乙酰膽堿酯酶、血脂及炎癥介質的關系〔J〕.臨床神經病學雜志,2008;21(3):201-3.
4Petersen RC,Morris JC.Mild cognitive impairment as a clinical entity and treatment target〔J〕.Arch Neurol,2005;62(7):1160-3.
5Winblad B,Palmer K,Kivipelto M,etal.Mild cognitive impairment-beyond controversies,towards a consensus:report of the International Working Group on Mild cognitive Impairment〔J〕.J Intern Med,2004;256(3):240-6.
6Bozoki A,Giordani B,Heidebrink JL,etal.Mild cognitive impairments predict dementia in nondemented elderly patients with memory loss〔J〕.Arch Neurol,2001;58(3):411-6.
7Ebady SA,Arami MA,Shafigh MH.Investigation on the relationship between diabetes mellitus type 2 and cognitive impairment〔J〕.Diabetes Res Clin Pract,2008;82(3):305-9.
8Alencar RC,Cobas RA,Gomes MB.Assessment of cognitive status in patients with type 2 diabetes through the mini-mental status examination:a cross-sectional study〔J〕.Diabetol Metab Syndr,2010;1(2):10.
9Liang XC,Gou SS,Hagino N.Current status of clinical and experimental researches on cognitive impairment in diabetes〔J〕.Chin J Integr Med,2006;12(1):68.
10Kim TS,Pac CU,Yoon SJ,etal.Decreased plasma antioxidants in patients with Alzheimer′s disease〔J〕.Int J Geriatr Psychiatry Apr,2006;21(4):344-8.
11Khosla UM,Zharikov S,Finch JL,etal.Hyperuricemia induces endothelial dysfunction〔J〕.Kidney Int,2005;67(5):1739-72.
12Matsumoto K,Murakami Y.Neuronal damage and decrease of central acetylcholine level following permanent occusion of bilateral common carotid arteries in rat〔J〕.Brain Res,1995;673(2):290-6.
13Schretlen DJ,Inscore AB,Jinnah HA,etal.Serum uric acid and cognitive function in community-dwelling older adults〔J〕.Neuropsychology,2007;21(1):136-40.
14Imaram W,Gersch C,Kim KM,etal.Radicals in the reaction between peroxynitrite and uric acid identified by electron spin resonance spectroscopy and liquid chromatography mass spectrometry〔J〕.Free Radic Biol Med,2010;49(2):275-81.
15Yu MA,Sanchez-Lozada LG,Johnson RJ,etal.Oxidative stress with an activation of the rennin-angiotensin system in human vascular endothelial cells as a novel mechanism of uric acid-induced endothelial dysfunction〔J〕.J Hypertens,2010;28(6):1234-42.

