創傷后應激障礙大鼠模型的建立及其有效性探討
晉 翔,王 文,王化寧,譚慶榮,鄭 紅
創傷后應激障礙(post trauma stress disorder,PTSD)是一種創傷后心理失衡狀態,臨床表現包括反復重現創傷性體驗、情感麻木、回避、警覺過強所致持續性焦慮、驚恐逃避以及易激惹癥狀等癥候群[1]。多數研究認為應激強度與PTSD的發病率存在“劑量-效應”關系,應激強度越高患病的可能性越大[2]。由于缺少合適的動物模型使PTSD的研究受到很大的限制,因此對其神經生物學致病機制研究及臨床治療帶來很大的困難。單次延長應激(single prolonged stress,SPS)動物模型由心理應激(束縛應激)和生理應激(強迫游泳、乙醚麻醉)構成。本實驗采用SPS的方法建立PTSD大鼠模型,現報道如下。
1 材料與方法
1.1 材料
1.1.1 實驗動物 成年雄性SD大鼠24只,第四軍醫大學動物實驗中心提供,體質量(200±20)g,光亮/黑暗周期為12 h/12 h,光照時間7:00—19:00,環境溫度為22~24℃,相對濕度60%,正常攝食攝水,飼養1周開始實驗。實驗動物的操作和處理按照《第四軍醫大學關于利用實驗動物開展研究的規定》執行。
1.1.2 實驗藥物及器材 乙醚(分析純,中國醫藥集團上海化學試劑公司),松下微型攝像機(HDCSD10,日本),Morris 水迷宮(Morris water maze,MWM)視頻分析系統(上海吉量軟件科技有限公司),自制束縛器、游泳缸。
1.2 方法
1.2.1 實驗設計
1.2.1.1 實驗分組 SD大鼠隨機分為空白對照組(control組,n=12)、單次延長應激組(SPS組,n=12),分組當天完成模型組單次延長應激實驗。
1.2.1.2 實驗流程 SPS組和control組大鼠不受打擾飼養15 d,第16天行曠場(open-field,OF)和高架十字迷宮(elevated plus maze,EPM)實驗;第16天起行連續6 d的MWM實驗,其中5 d為空間學習能力測試,最后1 d為記憶能力測試。
1.2.2 應激方法 首先將大鼠置于束縛器束縛2 h,隨后將其放入23~25℃水溫的游泳缸(直徑24 cm,高50 cm)強迫游泳20 min;游泳缸側面置一數碼攝像頭,動態記錄大鼠在強迫游泳裝置中游泳的錄像資料;設定分析參數,進行在線或離線數據分析。休息15 min后乙醚麻醉失去知覺。麻醉后將大鼠置于通風處至自然蘇醒,后放回飼養籠不受打擾飼養15 d。
1.2.3 觀察指標
1.2.3.1 利用EPM、OF實驗觀察動物的高警覺性、焦慮/抑郁、恐懼行為
(1)EPM 實驗:參照 Cohen等[3]的方法,利用不透明有機玻璃制成0.5 m高的高架十字迷宮,中間為8 cm×8 cm的平臺。將大鼠放于EPM的中央平臺上,鼠頭統一朝向同一方向,10 s適應后,記錄其行動5 min,記錄大鼠在開臂停留時間以及大鼠進入開臂的次數等行為學指標。然后采用高架十字迷宮視頻分析系統分析動物的各項行為指標。
(2)OF實驗:參照 kalynchuk等[4]的方法,在直徑47 cm×47 cm的黑暗曠場上用攝像頭監視大鼠的活動情況,采集視頻后分析各項行為指標。具體方法:將大鼠放于曠場行為觀察箱中,10 s適應后,開始記錄大鼠行為15 min,分析大鼠的活動次數、水平運動距離。
1.2.3.2 利用MWM實驗觀察動物的學習、記憶能力MWM為一直徑120 cm、高55 cm的圓形水池,水池內壁被漆為黑色,池內水深42 cm,水溫保持在(22±2)℃,房間內光照恒定,無光線直射在水池內。池壁上以4個等距離點將水池分為4個象限,在靶象限(設為第一象限)內距離池壁35 cm處放有一個直徑為8 cm、高40 cm的圓形黑色站臺,站臺位于水面下2 cm。池壁內貼有不同形狀及顏色的標記物。迷宮上方安置連接攝像機,同步記錄大鼠運動軌跡。采用MWM視頻分析系統進行信息處理,提供大鼠上臺潛伏期、靶象限活動時間百分比、穿臺次數等多個指標。
(1)定位航行實驗:實驗前任意選定一個目標象限將大鼠置于站臺上適應20 s,隨后將大鼠隨機從不同位置(靶象限除外)面壁置入池內。大鼠登上站臺5 s后終止記錄,最長記錄時間為60 s,若大鼠在60 s內不能上臺,引導其登上站臺適應10 s,最后將大鼠擦干放入鼠籠。如此將大鼠置入游泳池4次。測量平均上臺潛伏期,以評判大鼠的空間學習能力。在第1~5天分別重復上述步驟。
(2)空間探索實驗:在第6天撤掉水面下的站臺,然后將大鼠面壁置入池內1次,記錄大鼠在60 s內游泳軌跡并進行分析,最后將大鼠擦干放入鼠籠。記錄穿臺次數并計算大鼠在靶象限活動時間的百分比,評判大鼠的空間記憶能力。
1.3 統計學處理 采用SPSS 14.0統計軟件對數據進行方差分析,數據用均數±標準差(±s)表示,各組動物之間的均數采用最小顯著差異法(least significant difference,LSD)檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 SPS應激后對大鼠EPM行為的影響 SPS組開臂進入次數的百分比(23.55±3.79)%和開臂停留時間百分比(11.45±2.77)%顯著低于control組[(37.83±4.07)%,(17.85±3.45)%],差異具有統計學意義(P<0.05,表1)。提示單次延長應激有明顯的長時間致焦慮效應。
2.2 SPS應激后對大鼠OF行為的影響 應激15 d后,兩組大鼠5 min內水平活動距離、中央停留時間存在差異(P<0.05),SPS組大鼠的水平活動距離[(4 557.35)mm、中央停留時間(37.12±4.10)s]均較 control組[(8 775.85)mm,(22.65±1.54)s]明顯減少(表1)。提示單次延長應激導致大鼠活動性和探索性抑制,警覺水平、焦慮狀態增強。
2.3 SPS應激后對大鼠MWM空間學習能力及空間記憶能力的影響
2.3.1 SPS應激后對大鼠MWM空間學習能力的影響 SPS組與control組第1~5天隨著時間的延長上臺潛伏期逐漸縮短。SPS組第1~5天的上臺潛伏期分別為(49.27±2.78)、(33.04±3.85)、(29.18±3.51)、(20.98±2.76)、(19.67±2.66)次;control組第1~5天的上臺潛伏期分別為(44.6±5.46)、(25.59±4.76)、(13.21±2.68)、(10.23±1.08)、(9.63±0.94)次。SPS組與control組相比第3~5天上臺潛伏期明顯延長,差異有統計學意義(P<0.05,圖1),提示其學習和記憶的獲得與鞏固過程受到顯著影響。
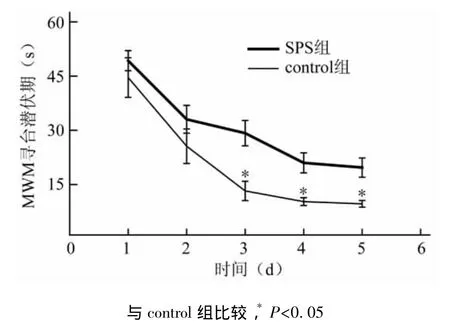
圖1 SPS應激后對大鼠Morris水迷宮空間學習能力的影響
2.3.2 SPS應激后對大鼠MWM空間記憶能力的影響 SPS組在Morris水迷宮4個象限無目的漫游,在靶象限花費時間的百分比(32.15±2.82)%和穿臺次數(1.15±0.26)次與control組靶象限花費時間的百分比(51.68±4.38)%和穿臺次數(2.87±0.35)次相比均明顯減少,差異具有統計學意義(P<0.05,表1)。提示單次延長應激記憶的讀出或提取受到顯著損害。
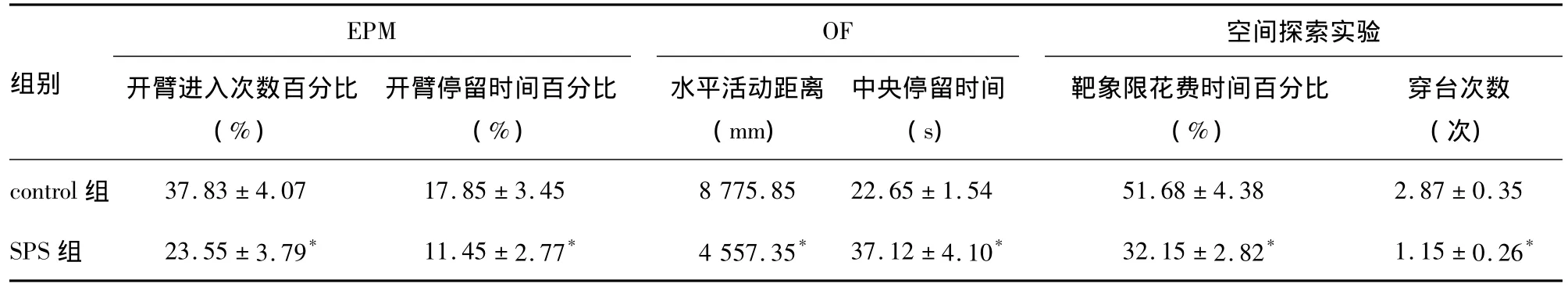
表1 大鼠EPM、OF、空間探索實驗數據
3 討論
PTSD是一組與應激密切相關的精神疾病,突發性、威脅性或災難性生活事件是引發PTSD的首要因素。無論是人類或其他生物在面臨不適于其生存的重大應激時,必然產生緊張、焦慮、恐懼、抑郁的情緒反應。但目前無理想的動物模型復制PTSD用以機制及藥物干預研究,因此建立標準的PTSD的動物模型有重要的基礎研究及應用價值。
EPM實驗是利用動物對新異環境的探究性,以及對高懸開臂的恐懼感而形成矛盾沖突狀態來評價實驗動物焦慮素質特征[5]。SPS大鼠在EPM實驗中表現為開臂進入次數的百分比和開臂停留時間百分比較空白對照組顯著降低(P<0.05)。說明受到單次延長應激后的大鼠被置于EPM的中央區時,探究、好奇的天性減弱,與外界相通的開臂對其帶來的威脅性增強,焦慮、恐懼水平明顯增高,大鼠很快從中央區逃跑,離開開臂退縮到閉臂中。而空白對照組大鼠則在開臂停留更多的時間,對開臂的探究次數也相對較多。提示SPS可致大鼠較長時間的焦慮反應,大鼠探究行為抑制、回避和恐懼、焦慮水平增高。
OF實驗是檢測動物焦慮、恐懼水平的經典方法,用來評定動物的警覺水平、焦慮狀態和環境適應能力[6-7]。如果大鼠的焦慮、恐懼水平高則傾向于停留在外周區,對中央區的探究次數及時間就會減少;反之,對中央區的探究次數及時間就會增多。SPS大鼠在OF實驗中表現為水平活動度、活動次數、中央停留時間明顯減少。說明SPS大鼠對中心區域的恐懼水平明顯增高,較快退避至相對安全的外周區。
MWM通過測量動物的空間學習、記憶能力,可以更全面地了解動物空間認知的加工過程[8-9],觀察應激的影響作用。在MWM實驗中SPS大鼠的尋臺時間明顯延長,而在靶象限花費時間的百分比和穿臺次數明顯減少。提示SPS可以引發大鼠長期的學習和記憶能力受損,與臨床PTSD患者存在的長期認知功能受損頗為相似。
從進化的角度講,SPS大鼠所表現的防御反應是人類恐懼和焦慮反應的原始成分。因此,本實驗中SPS大鼠所表現的對環境探究行為的抑制、回避反應與人類經歷重大應激事件后的焦慮、恐懼反應是相似的。人類的焦慮反應主要表現為逃避現實、逃跑行為、警覺性提高,同樣的行為反應也可從本實驗SPS大鼠身上觀察到。本模型成功模擬了PTSD的系統癥狀,如明顯和較長時間對SPS的恐懼、高警覺性、逃跑行為、環境適應能力下降以及焦慮行為、空間學習記憶能力障礙。模型制作過程中,單次足夠強度的應激源及不可預測性是模型成功的關鍵,多種不可預測的應激因子聯合應用可產生理想的效果[10]。本研究通過SPS成功誘發了動物多種PTSD樣精神和行為異常表現。該模型與PTSD有相似的致病因素與發生過程,效應持久,為進一步研究PTSD發病機制及藥物干預提供了必要條件。
[1]Fortuna LR,Porche MV,Alegría M.A qualitative study of clinicians'use of the cultural formulation model in assessing posttraumatic stress disorder[J].Transcult Psychiatry,2009,46(3):429-450.
[2]Wang M,Armour C,Li X,et al.The factorial invariance across gender of three well-supported models:further evidence for a five-factor model of posttraumatic stress disorder[J].J Nerv Ment Dis,2013,201(2):145-152.
[3]Cohen H,Matar MA,Buskila D,et al.Early post-stressor intervention with high-dose corticosterone attenuates posttraumatic stress response in an animal model of posttraumatic stress disorder[J].Biol Psychiatry,2008,64(8):708-717.
[4]Kalynchuk LE,Pinel JP,Meaney MJ.Serotonin receptor binding and mRNA expression in the hippocampus of fearful amygdala-kindled rats[J].Neurosci Lett,2006,396(1):38-43.
[5]Golub Y,Mauch CP,Dahlhoff M,et al.Consequences of extinction training on associative and non-associative fear in amousemodelofPosttraumaticStressDisorder(PTSD)[J].Behav Brain Res,2009,205(2):544-549.
[6]Rubin DC,Berntsen D,Bohni MK.A memory-based model of posttraumatic stress disorder:evaluating basic assumptions underlying the PTSD diagnosis[J].Psychol Rev,2008,115(4):985-1011.
[7]Yamamoto S,Morinobu S,Takei S,et al.Single prolonged stress:toward an animal model of posttraumatic stress di-sorder[J].Depress Anxiety,2009,26(12):1110-1117.
[8]Unceta N,Barrondo S,Ruiz de Azúa I,et al.Determination of fluoxetine,norfluoxetine and their enantiomers in rat plasma and brain samples by liquid chromatography with fluorescence detection[J].J Chromatogr B Analyt Technol Biomed Life Sci,2007,852(1/2):519-528.
[9]Pinna G,Rasmusson AM.Up-regulation of neurosteroid biosynthesis as a pharmacological strategy to improve behavioural deficits in a putative mouse model of post-traumatic stress disorder[J].J Neuroendocrinol,2012,24(1):102-116.
[10]Yu H,Watt H,Kesavan C,et al.Lasting consequences of traumatic events on behavioral and skeletal parameters in a mouse model for post-traumatic stress disorder(PTSD)[J].PLoS One,2012,7(8):e42684.

