胰腺癌術后腸內營養護理的應用
王廣勝
湖北省宜昌市中心人民醫院普外科,湖北宜昌 443000
胰腺癌患者常伴有不同程度的營養不良和免疫功能下降,術后死亡率及感染率較高[1]。營養支持重要的護理內容,正確有效的飲食護理可以增加患者營養,改善胃癌患者術后的機體營養狀態,促進機體功能恢復,減少術后并發癥[2]。研究表明,腸內營養比胃腸外營養更為安全,應用腸內營養支持可以及時預防并糾正營養不良的發生,并且可以更有效地減少并發癥的發生[3]。本研究對20例胰腺癌術后患者早期采用腸內營養,并加強護理,取得了較好的效果,現報道如下:
1 資料與方法
1.1 一般資料
選取2011年1月~2012年8月宜昌中心人民醫院(以下簡稱我院)40例胰腺癌患者,所有病例均經臨床、影像學和病理檢查確診,無肝腎功能異常,無糖尿病患者,近期內為接受或免疫制劑及激素治療。排除近期患有功能性胃腸病、甲狀腺功能減退、結締組織病、術后發生嚴重合并癥及認知功能障礙者。其中,男24例,女16例;年齡42~70歲,平均(55.9±2.5)歲;病理類型:高分化腺癌16例,中分化腺癌13例,導管細胞癌11例。將所有患者根據術后營養方式的不同分為觀察組和對照組,每組各20例。兩組患者在年齡、性別、病理類型等方面比較差異無統計學意義(P>0.05),具有可比性。
1.2 方法
1.2.1 營養方式 兩組手術方法相同,但術后營養方式不同。但兩組患者能量供應按146.3 kJ/kg 計算,非蛋白熱量/氮為564.3 kJ/kg[5]。①對照組:采用腸外營養,建立靜脈通道,將一定量的葡萄糖、電解質、氨基酸、維生素脂肪乳劑通過微量泵從周圍靜脈或深靜脈勻速輸入到患者的體內。其余均混勻在3 L 聚乙烯袋中進行滴注(抗生素單獨滴注)。②觀察組:采用腸內營養支持,由我院營養科按患者情況進行勻漿膳的配置,其中包括雞蛋、牛奶、米粉、奶粉、香菇、白糖、紅棗、油、鹽等,早期將勻漿膳通過鼻胃十二指腸管注入。其中每天為維持氮平衡,增強患者的免疫功能,滿足機體的需要,應給的蛋白質>2 g/kg[4]。過多的蛋白質可增加腎臟的負擔,出現氮質潴留,并可能導致腹瀉,因此,在腸內營養時,蛋白質的供給控制在總熱量的20%。初次胃腸道輸入者,從1000 kcal/d 開始,2~3 d 后逐漸增加至人體需要量[6]。
1.2.2 腸內營養的護理 ①由于是鼻插管的不適感,使患者不易接受,甚至產生抵觸情緒,因此,在鼻飼前護理人員將腸內營養高的意義,方法和醫患如何配合都向患者和家屬詳細的進行說明,取得患者的配合[7]。②鼻飼前首先吸凈咽喉部的分泌物,取右側臥位,使用前端帶有側孔的5~6 F軟質硅膠胃管,胃管的下端用液狀石蠟潤滑胃管,右手持胃管用拇、食指夾持胃管由一側鼻孔緩緩插入胃管,插入到胃部,胃管長度以耳垂-鼻尖-劍突間距離為準[8]。插入時無阻力,則快速向下插入所需長度。插管操作一定要輕柔,切忌暴力推進,以免損傷黏膜。當胃管的插入深度達到標記時,取左側臥位,可用抽吸胃液法或用聽診器在胃部聽氣過水聲等方法確定胃管在胃內[9]。以貼膠將胃管妥善固定后可開始緩慢注入患者所需營養液。③鼻飼期間環境應保持整潔、安靜、無強光刺激,認真精細的護理患者,鼻飼前30 min 不宜翻身或進行其他操作。固定胃管用的膠布寬度以1.5~2.0 mm 為宜,膠布要保持干燥,注意檢查膠布處皮膚是否出現損傷,更換時須先以溫水沾濕以防損傷患者皮膚[10]。每次鼻飼前后用2~3 mL 的溫開水沖洗營養管,嚴格掌握如真的溫度和濃度,溫度為38~40℃,以防止引起患者腹瀉或腹痛。每次鼻飼前先抽吸患者胃內容物[11]。④鼻飼結束后將胃管末端的蓋子蓋好,以紗布包裹好,待下次鼻飼時打開。做好口腔護理,每周更換鼻飼管。在輸注營養液的過程中,護士應嚴密觀察患者胃腸耐受情況,注意有無嘔吐、腹脹、腹瀉、明顯胃潴留現象,并觀察患者大便的顏色、性狀及量。若明顯腹脹、胃潴留、反復呼吸暫停,應停止鼻飼,采用靜脈高營養積極預防感染,嚴格遵守無菌操作規程。并注意觀察營養液有無污染,及時排除低蛋白血癥引起的腹瀉。加強巡視,預防少量的營養液反流可引起呼吸暫停甚至窒息,及時發現,及時處理。準確記錄24 h出入量,嚴密監測患者的水、電解質、血糖變化。
1.3 評價指標
比較兩組患者術后7 d 時的胃腸功能情況(反流、腹瀉、腹脹、便秘等)、營養學指標變化、免疫功能情況,并發癥(吸入性肺炎、消化道出血、感染等)的發生率及術后3個月的生活質量。①營養學指標:包括血漿白蛋白、血漿前白蛋白和血紅蛋白。采集患者清晨空腹肘靜脈血2 mL,放入-40℃冰箱保存,統一進行檢測。檢測儀器為日本生產的日立7170A 自動生化分析儀。②免疫功能:檢測患者術前、術后7 d 免疫功能主要檢測患者傷后7 d 的CD4+、CD4+/CD8+、IgM、IgG 的變化。采用由美國貝克曼公司生產的用于IMMAGE 800 儀器,測試方法為免疫比濁法。③生活質量:采用生活質量綜合評定問卷(GQOLI-74)進行調查兩組患者出院前的生活質量。共包括四個維度,軀體功能、心理功能、社會功能、物質生活狀態,前三個維度有5個因子,最后一個維度有4個因子,每個項目評分采用5級(1~5級)。
1.4 統計學方法
采用SPSS 16.0 統計軟件,計量資料采用均數±標準差(±s)表示,組間比較采用t檢驗,計數資料采用百分率表示,組間對比采用χ2檢驗。以P<0.05 為差異有統計學意義。
2 結果
2.1 兩組術后7 d 胃腸功能及并發癥比較
觀察組術后7 d 的胃腸功能顯著優于對照組(χ2=3.89,P<0.05),并發癥顯著少于對照組,差異有統計學意義(χ2=3.85,P<0.05)。見表1。

表2 兩組術后7 d時胃腸功能及并發癥比較(例)
2.2 兩組患者術后7 d 時的營養學指標變化
營養支持7 d 時的血漿白蛋白、血漿前白蛋白和血紅蛋白,觀察組均顯著優于對照組,差異有統計學意義(P<0.05)。見表2。
表2 兩組患者營養相關生化指標分析(±s)
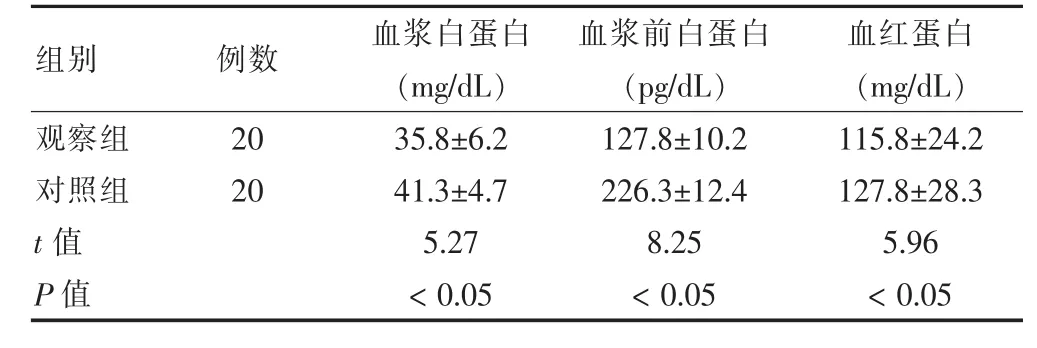
表2 兩組患者營養相關生化指標分析(±s)
組別例數 血漿白蛋白(mg/dL)血漿前白蛋白(pg/dL)血紅蛋白(mg/dL)觀察組對照組20 20 t 值 P 值35.8±6.2 41.3±4.7 5.27<0.05 127.8±10.2 226.3±12.4 8.25<0.05 115.8±24.2 127.8±28.3 5.96<0.05
2.3 兩組患者術后7d 時的免疫功能學指標比較
營養支持 7 d 的 CD4+、CD4+/CD8+、IgA、IgG, 觀察組均顯著高于對照組,差異有統計學意義(P<0.05)。見表3。
表3 兩組患者免疫功能比較(±s)
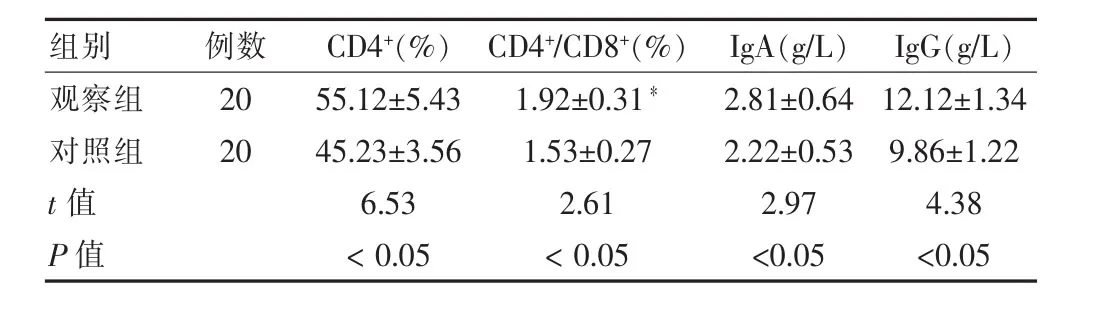
表3 兩組患者免疫功能比較(±s)
組別例數 CD4+(%) CD4+/CD8+(%) IgA(g/L) IgG(g/L)觀察組對照組20 20 t 值 P 值55.12±5.43 45.23±3.56 6.53<0.05 1.92±0.31*1.53±0.27 2.61<0.05 2.81±0.64 2.22±0.53 2.97<0.05 12.12±1.34 9.86±1.22 4.38<0.05
2.4 兩組術后3個月的生活質量比較
觀察組術后3個月時在軀體功能、心理功能、社會功能、物質生活狀態方面的生活質量評分顯著高于對照組,差異有統計學意義(P<0.05)。見表4。
3 討論
手術是治療胰腺癌的重要方法,但手術使胃的結構發生了變化,正常生理功能受到了影響,出現胃納不佳,餐后飽脹,消化吸收功能紊亂等癥狀,容易發生蛋白質-能量營養不良[12]。營養是維持生命、保持健康的物質基礎,在很大程度上飲食對機體的功能和狀態有著重要的影響。營養支持作為其中的一個重要部分,對其轉歸具有十分重要的意義。因此,必須采用必要的護理手段改善患者的飲食狀況,增加營養,以減少并發癥的發生,提高機體免疫能力。胃腸外營養是常用的營養支持方式,但往往不能滿足患者的營養需求,患者一旦營養不良住院期間就更容易并發肺炎及其他部位的感染,甚至胃腸道出血。腸內營養在近年來發展迅速,能有效改善患者的營養狀態,食物可促進胃腸道激素增多,促進腸道屏障功能恢復且維持全身臟器功能,減輕應激狀態下腸黏膜萎縮、降低腸道通透性、改善黏膜的免疫功能[3],還可防止菌群失調,降低腸道內膜屏障功能的損害和細菌內毒素的易位,預防由細菌或內毒素吸收而導致腸源性感染。還能刺激消化液和胃腸道激素的分泌,促進腸蠕動,增加內臟血液循環[13]。此外,食物中的葡萄糖還能促進巨噬細胞和單核細胞、T 淋巴細胞的增生和分化,增加機體防御能力。
表4 兩組術后3個月的生活質量比較(分,±s)
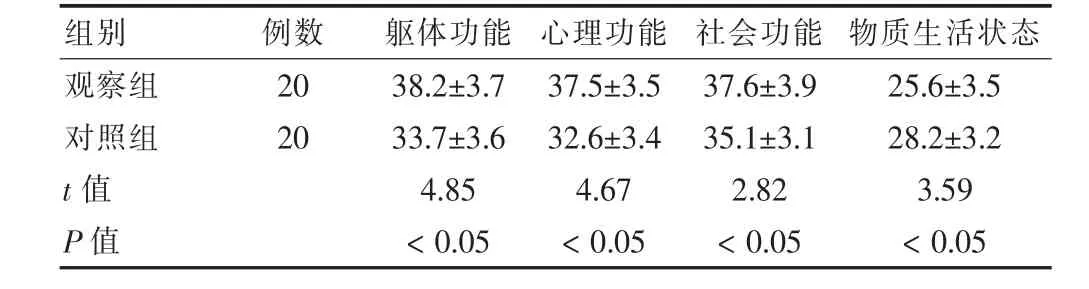
表4 兩組術后3個月的生活質量比較(分,±s)
組別例數 軀體功能 心理功能 社會功能 物質生活狀態觀察組對照組20 20 t 值 P 值38.2±3.7 33.7±3.6 4.85<0.05 37.5±3.5 32.6±3.4 4.67<0.05 37.6±3.9 35.1±3.1 2.82<0.05 25.6±3.5 28.2±3.2 3.59<0.05
本研究結果顯示,采用早期腸內應用的觀察組術后7 d的胃腸功能顯著優于對照組,并發癥顯著少于對照組(P<0.05);營養支持7 d 時的血漿白蛋白、血漿前白蛋白和血紅蛋白,觀察組均顯著優于對照組(P<0.05);營養支持7 d 的CD4+、CD4+/CD8+、IgA、IgG, 觀察組均顯著高于對照組 (P<0.05);這提示腸內應用能夠較好的改善胰腺癌患者術后的胃腸功能,增加營養,提高患者的免疫功能。結果還顯示,觀察組術后3個月時在軀體功能、心理功能、社會功能、物質生活狀態方面的生活質量評分顯著高于對照組(P<0.05)。
綜上所述,對胰腺癌患者術后早期采用腸內應用可改善患者的體液免疫情況和營養學指標,增加抵抗力,減少并發癥的發生。同時患者營養素平衡全面,安全價廉,合理方便,有利于提高術后生活質量。
[1]林麗華,楊觀德,吳家園.腸內營養對胰腺癌患者術后營養支持的探討[J].中國實用醫藥,2009,4(15):19-20.
[2]Komunm S,Nelwon KA,Wahh D,et al.Gastrointestinal symptom-samong inpatients with advance cancer [J].Am J Hosp pattiar Care,2002,9(5):351-355.
[3]李慶林,李寶平,賈仙.早期腸內營養對胃癌胰腺癌術后免疫功能的影響[J].山東醫藥,2007,47(30):96-98.
[4]Hadden JW.Immunode ciencv and cancer:prospects for correction[J].Int Immu opharmac,2003,12(3):1061-1071.
[5]趙亮,于永福,李慧.腸內營養支持治療在肺癌化療病人中的臨床應用[J].腸外與腸內營養,2011,18(5):281-283.
[6]邵燕.食管癌術后早期腸內營養支持的護理[J].齊齊哈爾醫學院學報,2005,26(1):111.
[7]鄭家駒.腸內營養的實施與進展[J].臨床內科雜志,2005,22(2):13.
[8]王慶喜.早期腸內營養在胃癌、胰腺癌術后的應用及護理[J].當代護士:專科版,2009,12(5):59-60.
[9]馬玲,朱丹.早期腸內營養在急性重度胰腺炎中的應用及護理[J].護理學雜志,2005,20(4):81-82.
[10]李愛霞,張葉鋒,張轉玲.胰腺癌術后早期腸內營養治療的護理體會[J].當代醫學,2011,17(1):120-121.
[11]楊勇,全志偉,沈定豐,等.術后早期腸內免疫營養對老年胰腺癌、胃癌患者免疫的影響[J].胰腺病學,2008,2(3):155-158.
[12]囝瑞君.急性重癥胰腺炎早期腸內營養的應用[J].中國醫藥導報,20l0,7(31):164-165.
[12]蘇惠芳.龐旭峰,李艦.胰腺癌術后腸內營養護理[J].實用醫藥雜志,2010,27(8):719-720.
[13]許文華.對重癥急性胰腺炎患者髓內營養護理研究[J].中國醫藥導報,2011,8(11):101-102.

