吡格列酮對腦缺血/再灌注損傷大鼠NF-kB和PARP表達的影響
劉 洋 祝慧慧 馮春梅 俞 波
吡格列酮對腦缺血/再灌注損傷大鼠NF-kB和PARP表達的影響
劉 洋1祝慧慧1馮春梅1俞 波2
目的探討吡格列酮對大鼠腦缺血/再灌注梗死區炎癥介質NF-κB和PARP表達的影響。方法采用線栓法建立大鼠大腦中動脈缺血/再灌注模型,動物分為假手術組、模型組、尼莫地平組和吡格列酮組。觀察各組大鼠的神經功能損害NSS評分,應用RT-qPCR檢測梗死區NF-κB和PARP基因的表達。結果吡格列酮組較模型組NSS評分顯著降低(P<0.05),梗死區NF-κB和PARP mRNA表達顯著下降(P<0.05)。結論吡格列酮可能通過下調炎癥介質NF-κB和PARP表達抑制炎癥反應,促進腦缺血損傷神經功能恢復。
吡格列酮;腦缺血/再灌注;NF-κB;PARP
吡格列酮是過氧化物酶體增殖物激活受體(Peroxisome proliferators activated receptor γ, PPARγ)的合成激動劑,是新一代噻唑烷二酮類代表性藥物,其作為胰島素敏感因子[1],已廣泛應用于2型糖尿病的臨床治療,療效顯著。近年來有研究者發現[2,3],吡格列酮還可用于腦血管疾病的治療,White等[2]通過meta分析發現在許多大鼠腦梗死模型實驗中,經靜脈注射或腦室內注射吡格列酮能夠顯著降低腦梗死體積,促進腦神經功能恢復,但其具體作用機制尚不清楚。炎癥轉錄因子NF-κB和DNA修復酶PARP能夠協同調節多種炎癥因子轉錄,在腦缺血損傷炎癥反應中發揮重要作用。因此,本研究通過觀察吡格列酮對腦梗死后炎癥因子NF-κB和PARP基因表達的影響,探討吡格列酮促進腦梗死后神經功能恢復的機制。
1 材料與方法
1.1 主要試劑鹽酸吡格列酮片(煙臺方正制藥有限公司,國藥準字H20070229),尼莫地平注射液(河北永豐藥業有限公司,國藥準字H13021882)。反轉錄試劑盒、Trizol和Taq酶購自Takara公司,引物合成購自大連寶生物公司,NF-κB上游引物:AAGAAGCGAGACCTGGA,下游引物CCGGAACA CAATGGCCA;PARP上游引物:CCAGGGTCTTCG GATAG,下游引物GCGTGCTTCAGTTCATACA;β-actin上游引物GGGTATGGGTCAGAAGGA,下游引物GCTGGGGTGTTGAAGGTC。
1.2 動物造模及分組健康成年SD大鼠,體重160~180g,由哈醫大動物中心提供[SCXK(黑)許可證號:2007D200]。線栓改良法制備大腦中動脈缺血大鼠模型,大鼠隨機分為4組,每組9只,分別為假手術組、模型組、尼莫地平組(20mg/kg)、吡格列酮組(20mg/kg)。尼莫地平組、吡格列酮組從造模前7d開始每日一次灌胃給藥,假手術組、模型組給予等體積生理鹽水。根據Culman等[3]的報道,本研究采用吡格列酮為最大有效劑量。
1.3 NSS法檢測再灌注96h后,依據NSS評分標準評價大鼠運動功能和感覺功能,功能缺損最嚴重時得分為22分,無功能損傷為0分。
1.4 RT-qPCR檢測提取各組腦組織內總RNA,參照PrimeScript? RT-PCR說明書進行反轉錄、PCR檢測及熒光定量分析。通過2-ΔΔCt方法進行樣本相對定量比較。
1.5 統計學分析采用SPSS 11.5軟件進行分析,結果以(±s)表示,各組間比較用LSD分析,P<0.05有統計學意義。
2 結果
2.1 神經功能損害評分與假手術組[(0)分]比較,模型組[(11.22±1.06)分]、尼莫地平組[(9.25±0.79)分]和吡格列酮組[(7.72±0.94)分]NSS評分顯著增加,差異有顯著性(P<0.01)。與模型組和尼莫地平組比較,吡格列酮組NSS評分顯著降低(P<0.05),差異有統計學意義(F=91.27,P<0.05)。
2.2 RT-qPCR檢測模型組PARP和NF-κB mRNA相對表達較假手術組顯著增多(P=0.000,P=0.000),模型組PARP和NF-κB mRNA相對表達均與尼莫地平組無統計學差異(P=0.124,P=0.598)。與模型組比較,吡格列酮組PARP和NF-κB mRNA相對表達均顯著降低(P=0.000,P=0.000),差異有統計學意義(見表1)。
表1 梗死區PARP和NF-κB mRNA相對表達(2-ΔΔCt值,±s,n=9)
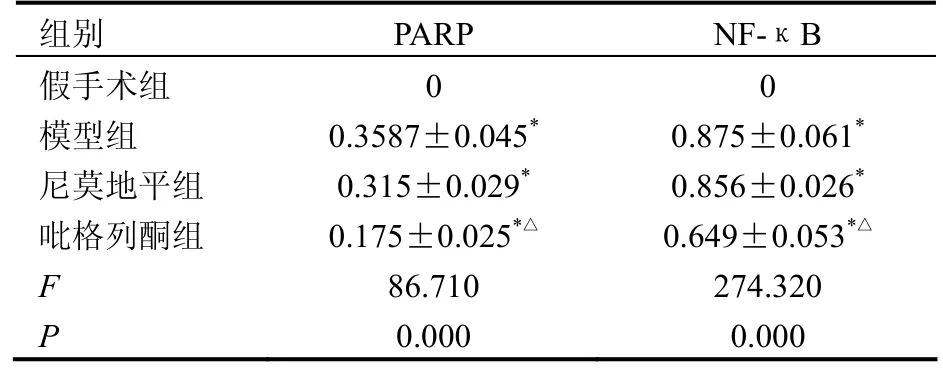
表1 梗死區PARP和NF-κB mRNA相對表達(2-ΔΔCt值,±s,n=9)
注:*與假手術組比較,P<0.01;△與模型組比較,P<0.01
組別 PARP NF-κB假手術組 0 0模型組 0.3587±0.045*0.875±0.061*尼莫地平組 0.315±0.029*0.856±0.026*吡格列酮組 0.175±0.025*△0.649±0.053*△F86.710 274.320P0.000 0.000
3 討論
噻唑烷二酮類(Thiazolidinediones, TZDs)是PPARγ合成激動劑,PPARγ是核內受體超家族中的配體激活轉錄因子,在調控細胞增殖、分化和炎性反應中發揮重要作用。吡格列酮、羅格列酮和曲格列酮[1]均為噻唑烷二酮類代表性藥物,吡格列酮作為胰島素敏感因子已廣泛應用于臨床2型糖尿病的治療。臨床研究發現[3],吡格列酮治療能顯著降低心肌梗塞、腦梗死和2型糖尿病的死亡率及并發癥的發生,吡格列酮還能夠促進糖尿病合并腦梗死患者的神經功能恢復,其在短期內即可顯效,且無心力衰竭、水腫和體重增加等副作用。研究發現吡格列酮治療能夠顯著降低大鼠腦梗死體積,促進腦梗死后神經功能恢復,且其治療無時間依賴性。White等[2]發現腦缺血后吡格列酮治療組在任何時間點與對照組比較,收縮期和舒張期的血壓、心率和其它生理學變量均無顯著差異,在體內未表現明顯毒性,安全可靠。本研究發現與模型組和對照組比較,吡格列酮組NSS評分顯著降低,再次證實了吡格列酮能夠促進腦梗死后神經功能恢復。
研究發現,炎癥轉錄因子NF-κB能夠啟動腦缺血后炎癥反應,影響炎癥級聯反應,放大炎癥效應。而DNA修復酶PARP是NF-κB的共活化物,兩者在炎癥趨化過程中發揮協同促進作用,誘導靜止的小膠質細胞轉化為活化的小膠質細胞,促進粒細胞和巨噬細胞向腦梗死區遷移,加劇早期腦缺血的局部損傷,導致梗死區神經細胞的死亡。本實驗發現與假手術組比較,模型組梗死區NF-κB和PARP基因表達顯著增高,而使用吡格列酮可顯著下調NF-κB和PARP基因表達,提示吡格列酮能夠抑制與NF-κB和PARP相關的炎癥反應。從而推測其機制可能與吡格列酮通過PPARγ途徑抑制NF-κB和PARP等前炎癥因子的轉錄有關[3]。
綜上所述,吡格列酮治療能促進腦缺血損傷后大鼠神經功能恢復,其作用機制可能與吡格列酮下調腦梗死區PARP和NF-κB的表達,抑制炎癥反應有關。
[1] Kataoka Y, Yagi N, Kokubu N, et al. Effect of pretreatment with pioglitazone on reperfusion injury in diabetic patients with acute myocardial infarction [J]. Circ J, 2011,75(8):1968-1974.
[2] White A, Murphy A.Administration of thiazolidinediones for neuroprotection in ischemic stroke: a pre-clinical systematic review[J]. J.Neurochem, 2010,115(10):845-853.
[3] Culman J, Nguyen-Ngoc M, Glatz T, et al. Treatment of rats with pioglitazone in the reperfusion phase of focal cerebral ischemia:A preclinicalstroke trial[J]. Exp Neurol, 2012,238(2): 243-253.
R743
A
1673-5846(2013)01-0211-02
1 黑龍江牡丹江醫學院,黑龍江牡丹江 157011
2 浙江省諸暨市中醫院胸外科,浙江紹興 311800

