自身免疫性胰腺炎二例報道并文獻分析
徐梅梅,高福來,李 莉,謝長順,鄭 岳
自身免疫性胰腺炎(AIP)是胰腺將自身成分作為抗原由CD4陽性輔助細胞產生免疫應答而造成的胰腺炎癥性病變,是以胰腺腫大、胰管不規則狹窄為特征的特殊類型的胰腺炎。AIP多以黃疸為首發癥狀,臨床上較少見,發病率較低,我科2011—2013年收治2例AIP患者,現將診治過程報道如下。
1 病例簡介
患者1,男性,69歲,干部,主因“腹脹2個月,發現皮膚、鞏膜黃染3 d”入院。患者緣于3個月前無明顯誘因出現餐后上腹部脹滿不適,間斷性發作,伴大便習慣改變(4~6次/d,成型黃色大便),3 d前出現小便黃染,呈醬油色,大便呈白陶土色,并逐漸出現全身皮膚、鞏膜黃染,無皮膚瘙癢,伴乏力,食欲差,我院門診以胰腺炎收入院。自發病以來,體質量下降5 kg。家族史:患者兩兄弟均曾因可疑胰腺癌而行手術,術后均未發現癌細胞。入院時查體:意識清楚,全身皮膚、鞏膜黃染,淺表淋巴結無腫大,心肺無異常,腹平軟,無壓痛,肝脾未觸及。移動性濁音陰性,腸鳴音正常。胰腺磁共振成像(MRI)、磁共振胰膽管造影(MRCP)、十二指腸乳頭及膽總管異常改變,考慮為炎癥;胰腺異常改變,考慮為胰腺炎(見圖1~3)。實驗室檢查結果,肝功能示丙氨酸氨基轉移酶(ALT):695 U/L,天冬氨酸氨基轉移酶(AST):464 U/L,總膽紅素:103.7 μmol/L,直接膽紅素:68.4 μmol/L,間接膽紅素:35.3 μmol/L,球蛋白:47.3 g/L,谷氨酰轉肽酶(GGT):843 U/L,免疫球蛋白G(IgG):24.7 g/L;自身免疫肝病,抗核抗體-IF(-),抗線粒體抗體(-),抗潤盤抗體(-),抗橫紋肌抗體(-),抗平滑肌抗體(-),抗肝-腎微粒體抗體(-),血清淀粉酶正常;腫瘤標志物,CA-199:104.8 U/L,IgG4:24.7 g/L,且患者CA-199明顯升高,不能除外胰腺癌。行胰腺活檢病理報:胰腺腺泡萎縮,小導管增生,間質大量纖維增生,炎細胞浸潤。液基薄層細胞學檢查:未見惡性細胞。患者經口服胰酶及熊去氧膽酸治療膽紅素下降,CA-199正常。最終診斷為自身免疫胰腺炎。
患者2,男性,70歲,農民,主因“間斷皮膚、鞏膜黃染10 d”入院。入院前10 d無明顯誘因出現皮膚、鞏膜黃染,伴陶土樣便,惡心、嘔吐,為胃內容物,隨時間延長黃疸進行性加重伴明顯消瘦,就診于中國人民解放軍281醫院:B超示:膽囊增大,胰腺增大。我院門診MRCP示:胰腺彌漫性病變侵及膽總管。患者后就診于中國人民解放軍總醫院(301醫院)和北京協和醫院,并在兩院行病理檢查(結果未回報),為進一步診治,門診以梗阻性黃疸收入我院。既往體健,有青霉素過敏史,無煙酒嗜好。查體:意識清楚,全身皮膚、鞏膜黃染,淺表淋巴結無腫大,心肺無異常,腹平軟,無壓痛,反跳痛,腹部無包塊,肝脾未觸及。移動性濁音陰性,腸鳴音正常,4次/min。胰腺MRI及MRCP示:胰腺異常改變及繼發膽管擴張,胰腺彌漫性病變侵及膽總管,肝內多發異常信號影,考慮肝囊腫(見圖4)。實驗室檢查:肝功能示ALT 109 U/L,AST 123 U/L,總膽紅素:170.1 μmol/L,直接膽紅素:120.5 μmol/L,清蛋白:27.6 g/L,球蛋白:58 g/L,谷氨酰轉肽酶:224 U/L,堿性磷酸酶:220 U/L,紅細胞沉降率:89 mm/h,CA-199:612 U/ml,血清淀粉酶正常,IgG1:11 500 mg/L,IgG2:4 760 mg/L,IgG:3 591 mg/L,IgG4>58 700 mg/L。入院后經內鏡逆行性胰膽管造影術(ERCP)示:膽總管下段狹窄(見圖5);十二指腸乳頭病理檢查示:黏膜組織慢性炎。患者為中老年男性,>50歲,以黃疸為主要癥狀,球蛋白及IgG4明顯升高,影像學檢查示:胰腺增大,肝內外膽管擴張,膽總管下端狹窄。十二指腸乳頭病理檢查示:黏膜組織慢性炎,膽總管擴張,考慮為AIP。給予口服潑尼松40 mg,1次/d治療后黃疸癥狀逐漸改善。
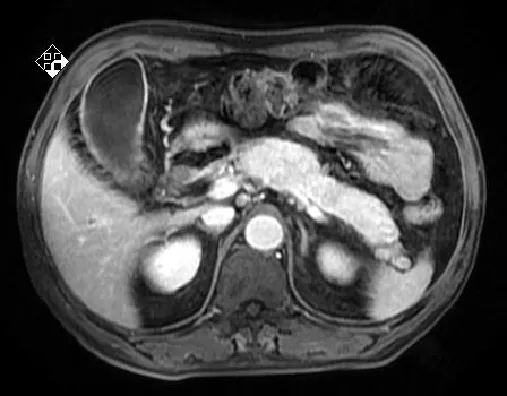
圖1 胰腺彌漫性腫大
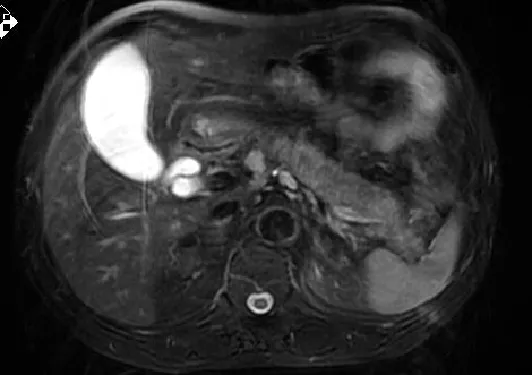
圖2 胰腺彌漫性腫大
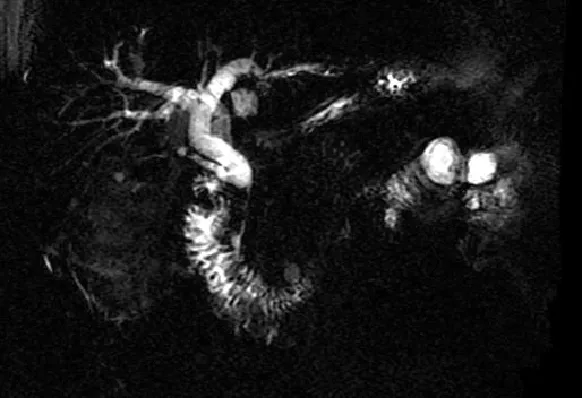
圖3 膽總管下端狹窄
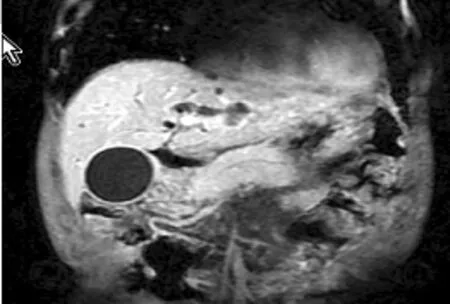
圖4 胰腺異常改變及繼發膽管擴張,胰腺彌漫性病變侵及膽總管
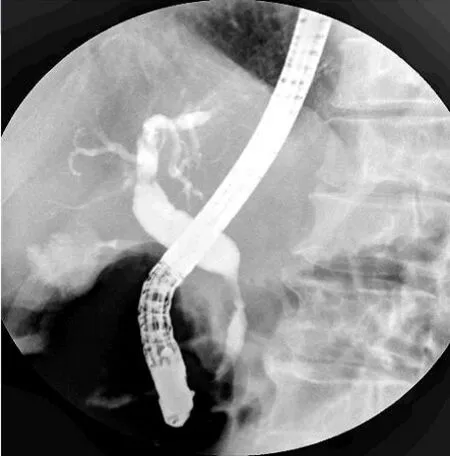
圖5 膽總管下端狹窄,膽總管上端擴張
2 討論
AIP是一種以自身免疫性炎癥過程為表現的慢性胰腺炎,以胰腺大量淋巴細胞浸潤伴纖維化為特征[1]。多以黃疸為首發癥狀,腹痛常不明顯,主要以胰腺腫大,胰管不規則狹窄為特征。該病在人群中發病率尚不清楚,在東西方不同國家AIP在慢性胰腺炎所占比例相似,為3.92%~6.00%,AIP發病率可能與種族、地理環境無明顯關系。AIP是疑似為胰腺癌而行外科手術切除術最常見的良性病變,占所有胰腺切除術的2.2%~2.5%。Abramham等[2]報道442例手術中有47例為良性病變,其中11例為AIP,術前診斷均為胰腺癌,因此本病很容易誤診。
AIP發病機制尚未明確,目前考慮自身免疫因素是此病的基礎[3]。AIP患者常伴有高γ球蛋白血癥,血清IgG、IgG4水平升高,自身抗體陽性,同時伴有干燥綜合征、類風濕性關節炎、潰瘍性結腸炎等,以上均提示其與自身免疫異常有關。我科收治的2例患者球蛋白明顯升高,提示與免疫系統疾病有關。
AIP主要臨床特征表現為:中老年男性(>50歲),起病隱匿,臨床極少有急性胰腺炎表現,約2/3的患者有梗阻性黃疸,多為輕中度,也可為重度,可呈進行性或間歇性,約2/5的患者有非特異性的輕度上腹痛或上腹部不適。
AIP實驗室檢查:10%~100%患者自身抗體陽性,常有高γ球蛋白血癥和(或)IgG4增高,特別是IgG4水平升高在AIP診斷中具有重要作用。Hamano等[4]報道:IgG4水平升高診斷AIP的敏感度為95%,特異度為97%。約半數患者血清淀粉酶輕度升高,但升高3倍以上者少見。白細胞計數基本正常,嗜酸粒細胞、IgE水平可升高,2/3的患者膽紅素升高,轉氨酶異常。
AIP影像學檢查:典型的彌漫性AIP在X線電子計算機斷層掃描(CT)和MRI上顯示為臘腸樣改變,密度降低,部分患者胰周出現低密度包膜樣緣包圍胰腺,而不累及鄰近系膜及系帶,此緣界限清晰、平整胰腺鈣化和假性囊腫形成罕見[5]。
AIP病理特點:胰腺腫大及淋巴細胞、漿細胞浸潤以及胰腺組織纖維化,很少出現胰腺鈣化,胰管結石,或胰腺假性囊腫。
AIP治療:口服糖皮質激素療效顯著,可使癥狀顯著緩解。常用劑量為潑尼松口服,開始劑量30.0~40.0 mg/d,每2周減5.0 mg,至15.0 mg時改為每4~8周減2.5 mg,維持劑量為2.5~5.0 mg/d[6]。除糖皮質激素外,Tsubakio等[7]報道熊去氧膽酸能較好地治療AIP,使其并發的肝功能損害明顯改善,胰腺體積縮小,有望成為激素的替代藥物,可以避免因長期應用激素引起的不良反應。
AIP診斷尚未統一,日本和韓國提出的亞洲標準:影像學(2條必備):(1)胰腺實質影像學:腺體彌漫性/局限性/局灶性增大;(2)胰膽管影像學:彌漫性/局限性、局灶性胰管狹窄,伴有膽管狹窄。
血清學(必備1條):(1)血清IgG或IgG4水平升高;(2)其他自身抗體陽性。
組織學:發現胰腺淋巴細胞、漿細胞浸潤以及纖維化,有大量IgG4陽性細胞浸潤。
可選擇的診斷標準:對激素的反應。
本研究2例患者均以黃疸為主要臨床表現,無明顯腹部疼痛等表現,實驗室檢查結果均為IgG水平升高,影像學檢查患者1 MRI示,胰腺彌漫性腫大,成臘腸樣改變,膽總管上段擴張,胰腺段狹窄。曾懷疑為急性胰腺炎,不除外胰腺癌,但最終行胰腺病理活檢后診斷為AIP,經口服熊去氧膽酸有效。患者2影像學檢查可見胰腺彌漫性腫大,懷疑胰腺癌,行ERCP可見膽總管胰段狹窄,膽總管上段擴張,十二指腸乳頭病理檢查示,炎性改變,且實驗室檢查示,IgG4水平升高,考慮為AIP,經激素治療有效最終診斷為AIP。
綜上,分析我院發現并確診的2例AIP患者的診治經過,雖然AIP少見,臨床容易誤診,但只要認識AIP實驗室檢查及影像學表現的特點,臨床中能懷疑到此病的可能性,再進一步完善相關檢查,也可行診斷性治療,就能明確診斷AIP。
1 Finkeberg DL,Sahani D,Deshpande V,et al.Autoimmune pancreatitis[J].N Engl J Med,2006,355(1):2670-2676.
2 Abraham SC,Wilentz RE,Yeo CJ,et al.Pancreaticoduodenectomy(Whipple Resection)in patients without malignancy:are they all chronic pancreatitis?[J].Am J Surg Pathol,2003,27(3):110-120.
3 Chari ST,Echelmeyer S.Can histopathology be the "Gold STandard" for dignosing autonommune pancreatitis?[J].Gastroenterology,2005,129(6):2118-2120.
4 Hamano H,Kawa S,Horiuchi A,et al.High serum IgG4 concentrations in patients with sclerosing pancreatitis [J].N Engl J Med,2001,344(4):732-738.
5 Wakabayashi T,Kawaura K,Satomura Y,et al.Clinical and imaging features of autoimmune pancreatic with focal pancreatic awelling or mass formation:comparison with so-called tumor-forming pancreatitis and pancreatic carcinoma[J].Am J Gastroenterol,2003,98(6):2679-2687.
6 Takayoshi N,Fummitake T,Hiroyasu O,et al.Long-term outcome of autoimmune pancreatitis after oral prednisolone therapy[J].Internal Medicine,2006,45(8):497.
7 Tsubakio K,Kiriyama K,Matsushima N,et al.Autoimmune pancreatitis successfully treated with ursodeoxycholic acid[J].Intern Med,2002,41(12):1142.

