DC-CIK生物治療聯合肝動脈灌注化療治療肝癌的短期臨床觀察
尤振宇 蘇曉輝 劉洋
原發性肝癌是最常見的惡性腫瘤之一,因其惡性程度高,進展快,預后常較差。研究證明,DC-CIK能夠顯著提高抗腫瘤活性及IFN-γ的分泌,增加 CD3(+)CD56(+)細胞和 CD3(+)CD8(+)細胞的比率,并促進細胞分化[1]。2009年6月至2012年1月,采用介入治療及DC-CIK生物治療晚期肝癌236例。其中,單純介入治療118例,介入+DC-CIK生物治療118例。取得一定療效,報告如下。
1 資料與方法
1.1 一般資料 2009年6月至2012年1月中國人民解放軍202醫院腫瘤介入科所收治診斷為原發性肝癌患者。隨機分為試驗組(介入治療+DC-CIK生物治療)和對照組(介入治療)。隨機分組方法:將符合納入標準的患者按入院順序自動排序,得到序號;在每個序號數字之后生成一個隨機數,函數是=RAND();將隨機數按從小到大順序進行重新排序,得到新序號。在新序號中位于奇數位置的患者分在實驗組,位于偶數位置的患者分在對照組。符合納入標準者244例,其中8例失訪,隨訪完整的236例臨床資料特征。見表1。

表1 2組患者臨床特征 n=118,例
1.2 納入標準 (1)原發性肝癌臨床診斷明確。診斷及分期參照2001年9月廣州第八屆全國肝癌會議所制定標準:①AFP≥400 μg/L,能排除妊娠、生殖系胚胎源性腫瘤、活動性肝病及轉移性肝癌,并能觸及腫大、堅硬及有大結節狀腫塊的肝臟或影像學檢查有肝癌特征的占位性病變者。②AFP<400 μg/L能排除妊娠、生殖系胚胎源性腫瘤、活動性肝病及轉移性肝癌,并有兩種影像學檢查有肝癌特征的占位性病變或有兩種肝癌標志物陽性及一種影像學檢查有肝癌特征的占位性病變者。③有肝癌臨床表現并有肯定的肝外轉移病灶(包括肉眼可見的血性腹水或在其中發現癌細胞),并能排除轉移性肝癌者。(2)
臨床分期為ⅡB期以下,無外科手術指征。(3)CT檢查示肝內病灶數不超過4個病灶,邊界較清楚;(4)肝功能Child-Pugh分級為A或B級。(5)年齡不超過70歲,卡氏評分不小于70。(6)治療前血常規、凝血功能及肝、腎功基本正常,且無其他介入治療、化療禁忌證。病例排除標準:(1)彌漫性肝癌;(2)一般狀態差,不能耐受介入治療者;(3)DSA造影顯示中重度肝動脈-門靜脈瘺或肝動脈一肝靜脈瘺者。
1.3 方法
1.3.1 介入化療:患者接受2~4次肝動脈化療栓塞術,治療間隔30~45 d。插管和造影技術按常規操作執行。術中化療用藥為:奧沙利鉑100~160 mg用于化療灌注,表柔比星20~40 mg與超液化碘油(用量為10~20 ml)做成乳劑栓塞。
1.3.2 DC-CIK 治療方案:分離血細胞經培養后第 4、8、12、16天回輸CIK,第8、12天皮下注射DC。肝動脈灌注治療每兩周期之間應用生物治療。
1.4 評價標準
1.4.1 病灶改變:2000年美國國立癌癥研究所推出的實體瘤反應評價標準,即RECIST。由于此標準沒有考慮到腫瘤活性變化,2008年美國肝病學會采納了存活腫瘤的概念,并提出了改良RECIST標準,用于評估肝癌治療療效[2],其內容為:CR:所有靶病灶動脈期強化消失;PR:同基線相比,所有靶病灶存活腫瘤最大徑總和縮小30%以上;PD:靶病灶存活腫瘤最大徑總和增加20%以上或出現新病灶;SD:病灶縮小未達PR或增加未至PD。研究證明:RECIST標準低估原發性肝癌化療栓塞術局部治療的效果[3]。改良RECIST標準與EASL(歐洲肝病學會標準)對療效評價一致性程度,且改良RECIST標準在臨床實踐中更簡便易行。
1.4.2 2組AFP下降大于20 ng/ml患者比率:臨床受益率采用與治療前比較,Karnofsky評分改善大于20分,體重變化增加5%,疼痛變化緩解50%以上的患者比率。其中疼痛為腫瘤所致疼痛。疼痛評價標準為數字疼痛分級法:0為無痛,10為最劇烈疼痛,讓患者自己圈出最能代表其疼痛程度的數字。
1.4.3 免疫學評價:T淋巴細胞 rDNA轉錄活性分析:Ag-NORs為RNA聚合酶的亞單位,反映rRNA的轉錄效率和淋巴細胞活性。I.S=核仁積分面積/細胞核積分面積×100%。
1.5 統計學分析計數資料采用χ2檢驗,計量資料以表示,采用t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 2組近期療效比較 試驗組有效率和疾病控制率分別為42.4%和78.0%。對照組有效率和疾病控制率分別為32.2%和71.2%。2組差異無統計學意義(P>0.05)。見表2。
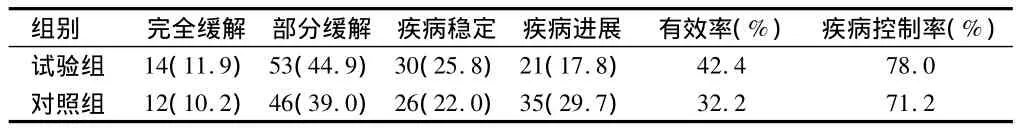
表2 2組近期療效 n=118,例(%)
2.2 毒性反應 試驗組1級骨髓抑制19例(19.2%),2級骨髓抑制4例(1.3%);對照組1級骨髓抑制22例(20.5%),2級骨髓抑制6例(2.6%),2組差異無統計學意義(P>0.05)。試驗組胃腸道反應34例(24.4%),對照組38例(25.6%)。2組差異無統計學意義(P>0.05)。
2.3 腫瘤標記物檢測 經治療,試驗組腫瘤標記物AFP下降>20 ng/ml 94例(79.7%),對照組 78 例(66.1%)。2 組比較差異有統計學意義(P<0.05)。
2.4 生活質量變化 治療后與治療前比較,試驗組Karnofsky評分增加大于20分98例(83.1%),對照組80例(67.8%);試驗組體重增加大于5%的57例(48.3%),對照組為41例(34.7%);試驗組疼痛減輕大于50%者78例(66.1%),對照組61例(51.7%)。這三項指標2組差異有統計學意義(P<0.05)。
2.5 免疫學評價 試驗組 Ag-NORs的 I.S均值為(5.76±0.14),對照組為(4.84 ±0.09),2 組差異有統計學意義(P<0.05)。
3 討論
肝癌在我國發病率高,是第二位的腫瘤致死原因。由于起病隱匿,大半的原發性肝癌就診時已進入中晚期,手術切除率低。經導管肝動脈化療栓塞術由于其創傷小,超選灌注,局部藥物濃度高等優點成為當前主要的治療手段。但單一采取TACE的局限性在于腫瘤較大或乏供血則難以完全栓塞病灶。
近年來DC-CIK免疫治療已成為較成熟的腫瘤新療法。樹突狀細胞(DC)是體內抗原遞呈細胞,處于啟動、調控并維持免疫應答的中心環節。利用負載腫瘤抗原的DC作為瘤苗,能有效打破機體對腫瘤的耐受,激活T淋巴細胞,殺傷并清除腫瘤細胞。細胞因子活化的殺傷細胞(CIK)可以直接殺傷腫瘤細胞,與DC共同發揮著免疫治療作用,有臨床應用作為術后預防腫瘤復發的治療[4]。
本研究采用肝動脈灌注化療聯合DC-CIK生物治療,有效率達到42.4%,疾病控制率達到78.0%。按統計學分析,不優于單純灌注化療組。聯合治療組有效率有疾病控制率均較單純介入化療組略高,說明DC-CIK生物治療在與其他治療聯合時可能起到一定的協同抗腫瘤作用,但是從短期療效上對比,加用DC-CIK生物治療并未提高短期療效。
徐永茂等[5]研究表明,DC-CIK治療有預防腫瘤復發的療效。對比本文研究結果,似乎療效相差很大。分析可能原因是術后患者腫瘤負荷非常小,而本文所涉及患者,其腫瘤負荷較大。DC-CIK生物治療可能對腫瘤負荷較大者短期療效不明顯。研究發現,聯合治療比單純介入化療臨床受益率高,Karnofsky評分增加大于20分占83.1%,而對照組為67.8%,體重增加超過5%者占47.5%,而對照組為34.7%,疼痛減輕較原來大于50%者占66.1%,而對照組為51.7%。DC-CIK治療實體腫瘤,患者的腫瘤標記物和免疫功能明顯改善[6]。本研究中,AFP下降試驗組高于對照組。Ag-NORs 2組差異顯著。Ag-NORs為RNA聚合酶的亞單位,反映rRNA的轉錄效率,間接反映機體免疫狀態,對腫瘤療效及預后具有重要意義[7]。其他研究也證實了DC-CIK生物治療是可行的[8],可以增加患者的免疫能力[9]。聯合DC-CIK生物治療后,對患者無不良反應。研究中,骨髓抑制和胃腸道反應2組差異無統計學意義。惡性腫瘤經化療后免疫力降低,應用DC-CIK細胞治療,可以提高惡性腫瘤患者的免疫功能[10]。本研究證實兩者聯合治療具有很好的安全性。
綜上所述,DC-CIK生物治療聯合介入化療不能提同肝癌患者短期療效,但從患者生活質量提高上可起到積極作用。介入化療聯合DC-CIK生物治療治療晚期肝癌具有可行性和較好的應用前景。因研究未進行長期的療效觀察,還需進一步研究觀察其遠期效果。
1 QiJing Wang,Hui Wang,Ke Pan,et al.Comparative study on antitumor immune response of autologous cytokine-induced killer(CIK)cells,dendritic cells CIK(DC-CIK),and semi-allogeneic DC-CIK.Chinese Journal of Cancer,2010,29:641-648.
2 Llovet JM,Di Bisceglie AM,Bruix J,et al.Design and endpoints of clinical trials in hepatocellular carcinoma.J Natl Cancer Inst,2008,100:698-711.
3 余文昌,張孔志,陳示光,等.實體瘤反應評價標準、歐洲肝病學會和改良實體瘤反應評價標準評價原發性肝癌化療栓塞效果一致性的比較.中華放射學雜志,2011,45:766-769.
4 高岱清,劉淑貞,趙鵬,等.惡性腫瘤術后DC聯合CIK治療的臨床觀察.中華腫瘤防治雜志,2009,16:222-225.
5 徐永茂,徐冬云,張南征,等.NP方案化療同步放療并序貫過繼免疫細胞治療非小細胞肺癌的臨床研究.中華腫瘤防治雜志,2011,18:1032-1035.
6 Tao Yang,Ying Xiang,Yucheng Li,et al.Clinical Study of co-treatment with DC-CIK cells for advanced solid carcinomas.Chinese-German Journal Clinical Oncology.2011,10:354-359.
7 宗登偉,郭晨陽,黎海亮,等.肝動脈化療栓塞加灌注治療胃癌肝轉移療效評價.河北醫藥,2011,33:2301-2303.
8 Mesiano G,Todorovic M,Gammaitoni L,et al.Cytokine-induced killer(CIK)cells as feasible and effective adoptive immunotherapy for the treatment of solid tumors.Expert Opin Biol Ther,2012,12:673-84.
9 Zhou P,Liang P,Dong B,et al.Phase Ⅰ clinical study of combination therapy with microwave ablation and cellular immunotherapy in hepatocellular carcinoma.Cancer Biol Ther,2011,11:450-456.
10 吳寶英,周紅霞,韓俊杰,等.肝動脈灌注栓塞術治療肝癌的護理.中國基層醫藥,2012,19:306-308.

