MnO2·0.5H2O的固相法制備及其對Li+的吸附動力學
石西昌,張志兵,周喜誠,周定方,肖 湘,陳白珍
(中南大學 冶金科學與工程學院,長沙 410083)
鋰離子電池[1?2]作為一種新型可充放電和高能量密度電源廣泛應用于人們生活的各個方面,例如手機、手提電腦、照相機和電動汽車等。因此,鋰被稱作“21世紀的能源元素”[3]。自然界中鋰資源的分布主要賦存于花崗巖偉晶型礦床、地熱水、海水以及鹽湖鹵水中。據統計,鹽湖鹵水資源約占世界鋰資源總儲量的66%和基礎儲量的80%以上[4]。自20世紀50年代以來,科學家們一直致力于尋求一種能從海水和鹽湖鹵水中提鋰的方法,如今已逐漸成為世界鋰鹽生產的主攻方向[5]。
關于Li+吸附劑的研究始于20世紀80年代,其中,MnO2·xH2O(x=0.31,0.5,…,摩爾分數)是被研究最多的化合物之一,它以選擇性高、穩定性高、吸附容量大及對環境友好等優點獲得了迅速的發展[6?7]。其中,MnO2·0.5H2O是目前鋰錳氧化物吸附劑中對鋰吸附容量最大的吸附劑,它具有化學穩定性高、吸附容量大和循環壽命長等優點,是從海水、鹽湖鹵水提鋰最有前途的吸附劑之一[8?9]。MnO2·0.5H2O 是通過其前軀體 Li1.6Mn1.6O4經酸洗而獲得的,因此制備Li1.6Mn1.6O4是獲得MnO2·0.5H2O的關鍵步驟。鋰錳氧化物 Li1.6Mn1.6O4是完全不同于傳統富鋰尖晶石錳氧化物系列 Li1+xMn2?xO4(0≤x≤0.33)的新型離子篩前軀體。它具有更高的鋰含量,其鋰錳摩爾比達到 1,遠高于傳統富鋰尖晶石系列中 LiMn2O4的 0.5及Li1.33Mn1.67O4中的0.8。Li1.6Mn1.6O4不能通過傳統的固相反應直接處理鋰錳化合物一步得到,僅能通過常用的幾個軟化學合成方法如前軀物法、溶膠?凝膠法及水熱法等[10]制備。溶膠?凝膠法具有燒結溫度相對較低、晶相較純、產物形態規整及粒度均勻等優點,但同時也存在操作要求高、反應步驟長和不易控制等不足。CHITRAKAR等[11]將 LiOH溶液與市售的γ-MnOOH混合,然后120 ℃水熱法處理1 d后合成了前軀體Li1.6Mn1.6O4,由于γ-MnOOH需要通過比較繁瑣的方法制備獲得,在制備過程中不可避免地會生成Mn3O4或 MnO2等雜質,從而影響所合成鋰錳氧化物前軀體的純度。液相法通常涉及到高壓、強堿和強酸等,對設備的要求比較高,同時占地面積相對較大,產量較低,難以實現大批量生產;而固相法則有工藝流程簡單、操作方便、生產效率高及設備腐蝕小等優點。僅靠液相法來生產離子篩前軀體遠遠不能滿足未來鹽湖資源開發需求,因此,開發固相合成方法顯得尤為重要。目前,關于直接采用全固相反應制備Li1.6Mn1.6O4的工藝還未見報道。
本文作者首先通過兩步固相法(先固相制備LiMnO2,再將其空氣中焙燒)制備前軀體Li1.6Mn1.6O4,再用 HCl溶液進行洗脫獲得離子篩 MnO2·0.5H2O,探索一條固相合成 MnO2·0.5H2O的新工藝路線,方法簡單可行,有利于吸附劑 MnO2·0.5H2O今后的工業化生產及應用推廣;采用相關動力學模型等對MnO2·0.5H2O吸附機理進行深入的探討;最后研究離子篩對鹽湖鹵水中各主要金屬離子的分離特性及其循環吸附性能。
1 實驗
1.1 鋰離子篩前軀體Li1.6Mn1.6O4的制備
經查閱大量文獻得知,不能通過一步固相或液相反應直接獲得前軀體Li1.6Mn1.6O4。本研究采用兩步固相法制取Li1.6Mn1.6O4,即先制備鋰錳氧化物LiMnO2,然后再將 LiMnO2置于一定溫度下焙燒制得Li1.6Mn1.6O4。LiMnO2是以 Mn2O3和 LiOH·H2O 為原料(n(Li)/n(Mn)=1.03),在氮氣氣氛中于600 ℃焙燒8 h制得,其XRD譜如圖1所示。
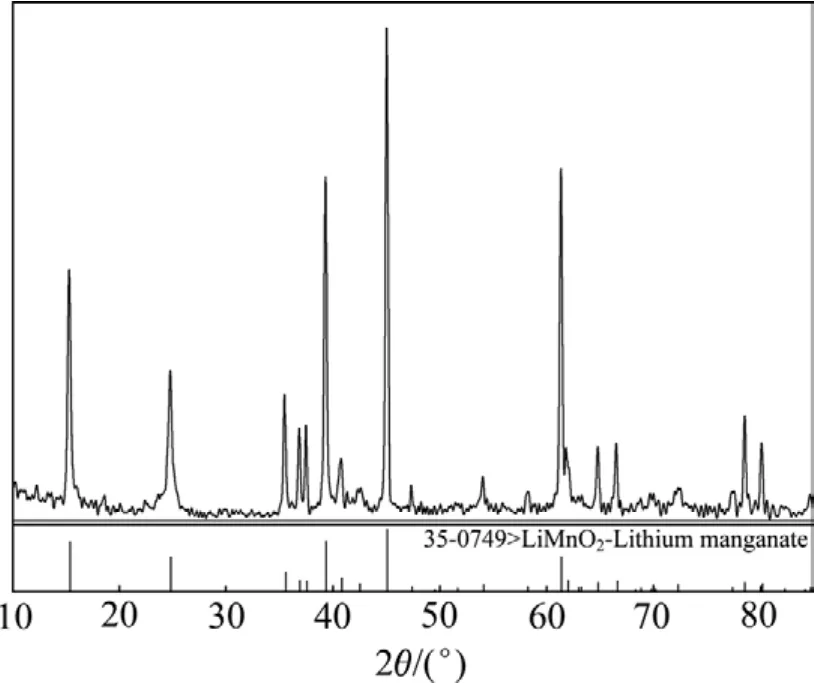
圖1 自制LiMnO2原料的XRD譜Fig.1 XRD pattern of self-made LiMnO2
將 LiMnO2置于箱式程控爐中焙燒,考察焙燒溫度和焙燒時間對合成的鋰離子篩前軀體 Li1.6Mn1.6O4結構和性質的影響。
1.2 前軀體酸洗制備MnO2·0.5H2O
取適量以上優化條件下制備的離子篩前軀體Li1.6Mn1.6O4置于過量的0.5 mol/L HCl溶液中進行酸洗9 h制取鋰離子篩MnO2·0.5H2O;然后對樣品的結構及吸附性能進行 XRD、粒度、吸附動力學等相關分析。
1.3 pH值對MnO2·0.5H2O吸附Li+性能的影響
分別稱取適量MnO2·5H2O置于含Li+均約為250 mg/L,pH分別為0.52、1.38、3.05、4.96、7.31、9.75、11.67和13.04的各溶液中進行吸附實驗。此實驗的前提是務必使離子篩吸附達到飽和,所以吸附時間必須要足夠長,結合前面的吸附實驗結果,吸附時間都控制為24 h,此實驗目的是考察pH值對離子篩吸附容量和錳溶損率的影響。
1.4 離子篩在含鋰溶液中的動力學
將適量離子篩置于250 mg/L Li+溶液中進行各溫度下吸附容量隨時間變化的吸附實驗,然后應用偽一級動力學、偽二級動力學、Langmuir和Freundlich吸附等溫方程等對吸附數據進行擬合,探討MnO2·0.5H2O 對 Li+的吸附機理。根據偽二級動力學方程并結合阿羅尼烏斯公式作出ln k2—T?1圖,求出吸附過程的表觀活化能。最后,應用動邊界模型對吸附過程的控制步驟進行探討。
1.5 離子篩對鹽湖鹵水中 Li+的選擇性及其循環吸附性能
由于鹽湖老鹵鹵水成分比較復雜,含有許多種金屬離子與非金屬離子,為了能有效地從復雜鹵水體系中提取鋰,離子篩對Li+的特定選擇性是決定鋰離子篩的性能與實用價值的關鍵指標。同時離子篩的循環吸附性能也至關重要,直接決定著離子篩能否實現其經濟價值。故本文作者從對鹽湖中主要金屬離子的選擇性及其在鹵水中的循環吸附兩個方面來考察離子篩的性能。
2 結果與討論
2.1 MnO2·0.5H2O 的制備
MnO2·0.5H2O是通過將Li1.6Mn1.6O4在酸中洗脫而獲得的,因此如何制取合格的前軀體Li1.6Mn1.6O4是獲得離子篩的關鍵步驟。
2.1.1 Li1.6Mn1.6O4的制備
焙燒時間和溫度等條件是影響Li1.6Mn1.6O4結構、形貌和性能的主要因素,故分別考察焙燒時間和溫度對所合成前軀體結構和性能的影響,以選定合適的焙燒溫度和時間。
2.1.1.1 焙燒溫度對前軀體Li1.6Mn1.6O4合成的影響
分別將 LiMnO2樣品置于空氣中于 390、410、430、450、470、490和510 ℃下焙燒4 h,考察焙燒溫度對前軀體合成的影響。所得各樣品的 XRD譜如圖2所示。
從圖2可以看出,在各個溫度下都能獲得較純的Li1.6Mn1.6O4,峰基底都比較平滑,但峰強略有變化。470 ℃以下時,隨著焙燒溫度的升高,所得樣品特征峰強度逐漸增高,峰形變窄,晶體結構越趨完整,而470 ℃以上隨著溫度的升高,樣品特征峰強度逐漸變弱,峰形變寬。這表明470 ℃附近可能是晶相轉變點,470 ℃以上,結構發生了部分坍塌,溫度越高,坍塌越嚴重,故樣品的峰強逐漸變弱。470 ℃所得的樣品峰形最為尖銳,晶體結構較為完整,所以,制備前軀體Li1.6Mn1.6O4的焙燒溫度應選擇470 ℃為宜。

圖2 LiMnO2原料在空氣中各溫度下焙燒所得樣品的XRD譜Fig.2 XRD patterns of LiMnO2 roasted at different temperatures in air
2.1.1.2 焙燒時間對合成Li1.6Mn1.6O4的影響
將LiMnO2在空氣中于470 ℃下分別焙燒2、4、6、8和10 h,考察焙燒時間對合成前軀體結構形貌的影響。所得樣品XRD譜如圖3所示。

圖3 LiMnO2原料在空氣中焙燒不同時間所得樣品的XRD譜Fig.3 XRD patterns of LiMnO2 roasted with different times in air
從圖3可知,隨著焙燒時間的延長,樣品的衍射峰逐漸變強,但到了6 h后,隨著時間的延長,衍射峰的強度基本未發生變化,這說明焙燒時間為6 h后得到的樣品晶型結構已趨于完整,形貌已達到最佳狀態。故樣品的焙燒時間選擇6 h為宜。
2.1.2 前軀體酸洗制備MnO2·0.5H2O
將在空氣中于 470 ℃下焙燒 6 h所得前軀體Li1.6Mn1.6O4用0.5 mol/L HCl溶液進行酸洗9 h,獲得鋰離子篩 MnO2·0.5H2O,酸洗前后樣品的 XRD譜如圖4所示。

圖4 前軀體Li1.6Mn1.6O4酸洗前后XRD譜Fig.4 XRD patterns of precursor Li1.6Mn1.6O4 before(a)and after(b)pickling
從圖4可以看出,前軀體酸洗前后樣品的衍射特征峰強度基本未發生變化,只是衍射角略微向高角度方向偏移,這說明在酸洗過程中樣品的結構未發生太大變化,只是晶胞略微變小,這是因為酸洗過程中酸中的H+與前軀體中的Li+進行離子交換反應,樣品的基本骨架保持不變,但晶胞發生了略微收縮。
2.2 pH值對MnO2·0.5H2O吸附Li+性能的影響
將0.2 g左右的離子篩MnO2·0.5H2O分別置于70 mL不同pH值、含有過量Li+溶液(LiCl,用LiOH和HCl調整pH值,溶液約含Li+250 mg/L)于50 ℃并在適量攪拌條件下吸附24 h,考察溶液pH值對離子篩吸附容量和錳溶損率的影響,結果如圖5所示。

圖5 溶液pH值對鋰離子篩吸附容量和錳溶損率的影響Fig.5 Influence of pH value on adsorption capacity and manganese dissolution loss rate of lithium ion-sieve
從圖5可以看出,離子篩對Li+的吸附容量開始隨著溶液pH值的升高緩慢增加,但pH值到10以后吸附容量顯著增加,吸附容量由 pH=0.52時的?4.39 mg/g(離子篩發生了解吸)增加到pH=13.04時的29.75 mg/g。可見,堿性越強,離子篩的吸附容量越大。這是因為離子篩吸附Li+發生如下離子交換反應[12]:S—OH+Li+→S—OLi+H+,pH值越高,OH?中和H+的能力就越強,促進反應向右移動,也即促進了離子篩對Li+的吸附。另外,離子篩的錳溶解損失率(簡稱錳溶損率)開始卻是隨著溶液 pH值增大急劇減小,當 pH值到3以后錳溶損率緩慢減小,變化比較平緩,但pH值到10以后又有略微增大的趨勢。在強酸性溶液中,離子篩會發生部分溶解,酸性越強,溶解損失越嚴重,同時在非常強的堿性溶液中離子篩中的錳也會與OH?反應生成絡合物,從而造成離子篩的損失。因此,離子篩對Li+的吸附pH值應控制在一定的范圍內。
2.3 MnO2·0.5H2O在含鋰溶液中的吸附動力學2.3.1 吸附動力學模型
動力學的研究有助于理解反應的歷程和機理,關于吸附反應的動力學模型已有不少報道,目前偽一級動力學模型(式(1))和偽二級動力學模型(式(2))被廣泛用來研究吸附機理[13?15],確定吸附反應的速率常數。

式中:qe(mg/g)和qt(mg/g)分別為在吸附平衡與吸附時間為 t(h)時吸附劑對 Li+的吸附容量;k1(h?1)和k2(g/(mg·h))分別為偽一級動力學模型和偽二級動力學模型的吸附速率常數。
分別采用上述偽一級動力學方程和偽二級動力學方程對離子篩在pH=12.99、含Li+約250 mg/L的溶液中于 50 ℃各時間下的吸附數據進行線性擬合,擬合結果如圖6所示。
從圖6可以看出,由偽二級動力學方程擬合的線性相關系數比偽一級動力學方程擬合的線性相關系數大,擬合更好,且相關系數R2達0.998以上。因此,可以認為離子篩對 Li+的吸附過程符合偽二級動力學方程,為化學吸附過程。
2.3.2 吸附等溫方程
鋰離子篩對Li+的吸附可以通過Langmuir吸附等溫方程(式(3))[16]和 Freundlich吸附等溫方程(式(4))[17]來擬合:

圖6 50 ℃下離子篩在含鋰溶液中吸附Li+的偽一級動力學和偽二級動力學線性擬合圖Fig.6 Linear fitting figures of lithium ion-sieve adsorbing Li+ at 50 ℃ with pseudo-first-order(a)and pseudo-second-order rate equation(b)
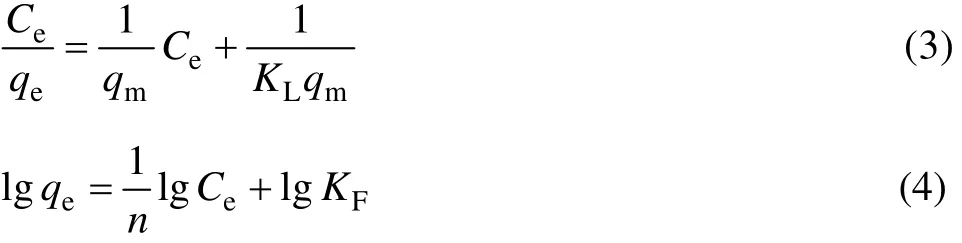
式中:Ce是吸附平衡后溶液中 Li+的濃度,mg/L;qm是最大吸附容量,mg/g;qe是平衡吸附容量,mg/g;KL是Langmuir實驗常數,L/mg;KF和n是與吸附速率和吸附容量有關的Freundlich常數。
分別應用Langmuir和Freundlich吸附等溫方程對離子篩MnO2·0.5H2O在不同Li+濃度溶液中于50 ℃吸附24 h的數據進行線性擬合,其擬合結果如圖7所示。
由圖7可以看出,用Langmuir吸附等溫方程擬合所得直線的線性相關系數比用Freundlich吸附等溫方程擬合的線性相關系數大得多,其相關系數達 0.993以上。故可以認為離子篩在不同Li+濃度溶液中的等溫吸附過程遵循Langmuir吸附等溫方程,從而可得離子篩對Li+的吸附是單層吸附。
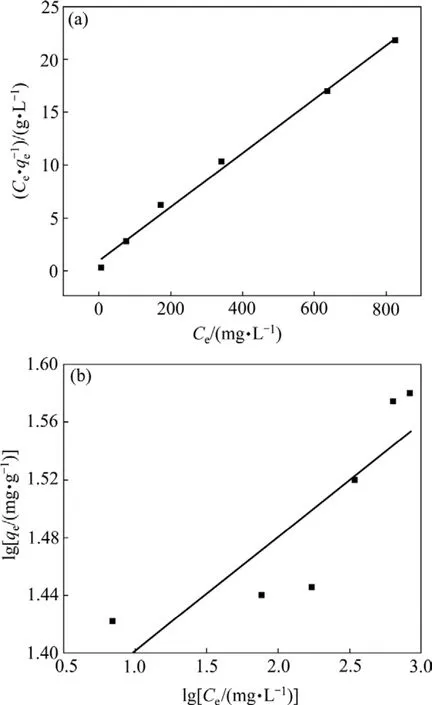
圖7 離子篩在不同 Li+濃度溶液中吸附的 Langmuir和Freundlich吸附等溫擬合圖Fig.7 Fitting lines of ion-sieve adsorbing in different Li+-concentrations solutions with Langmuir(a)and Freundlich(b)models
2.3.3 溫度對吸附動力學過程的影響及表觀吸附活化能的計算
表1所列為利用偽二級動力學方程對不同溫度下鋰離子篩吸附 Li+的動力學曲線擬合的結果,Li+的初始濃度為250 mg/L。結果顯示,隨著吸附溫度的升高,離子篩的吸附速率加快,吸附容量也稍微增加,這表明吸附過程為吸熱反應過程,這也與反應動力學的基本原理一致。
根據阿累尼烏斯(Arrhenius)公式[18]:

式中:k為反應速率常數;R為摩爾氣體常數,8.314 J/(mol·K);Ea為表觀活化能,kJ/mol;A 為常數。
利用表1中的數據作ln k2—T?1線性擬合圖(見圖8),通過直線斜率求得此吸附反應的表觀活化能Ea=26.71 kJ/mol。Ea為正值,說明升高溫度有利吸附,且由Ea>24 kJ/mol可知,吸附過程并不是簡單的物理吸附過程,而是離子交換或化學反應過程。
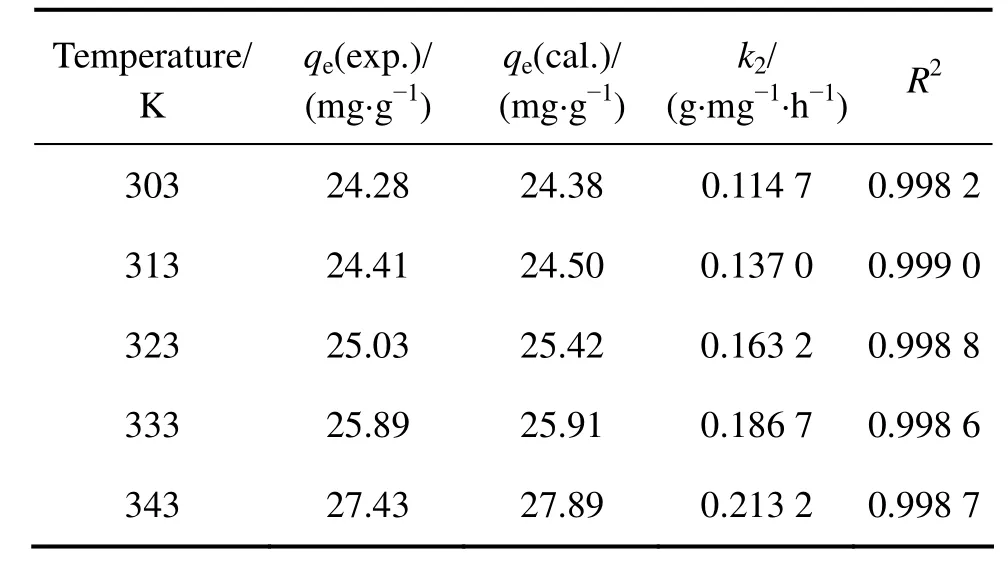
表1 離子篩在不同溫度下吸附 Li+的偽二級動力學方程擬合參數Table 1 Fitting parameters of ion-sieve adsorbing Li+ at different temperatures according to pseudo-second-order dynamic equation
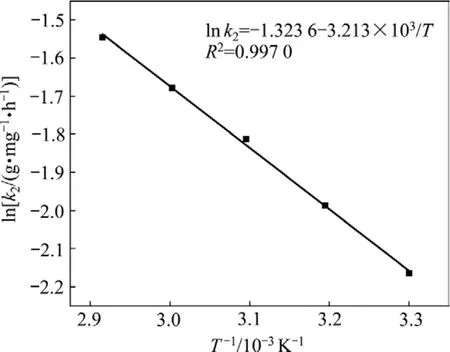
圖8 偽二級動力學方程所得ln k2對T ?1作圖的擬合結果Fig.8 Fitting results of plot of ln k2 to T ?1 according to pseudo-second-order dynamic equation
2.3.4 吸附過程控制步驟
目前,動邊界模型[19?21]廣泛用于描述離子交換行為。離子交換的過程大致可以分為3個步驟:1)金屬離子由溶液經液膜擴散到離子篩表面;2)金屬離子由離子篩表面向內部擴散;3)金屬離子在離子篩內部活性基位置發生表面絡合反應。即離子交換過程受液膜擴散、顆粒擴散和化學反應3個步驟的影響,其中速度最慢的步驟為整個過程的控制步驟。動邊界模型方程式分別表示為

式中:F為離子交換度,且F=qt/qe;k為反應速率常數。
將離子篩在 50 ℃吸附的數據用動邊界模型進行擬合,其擬合結果如表2所列。從表2可以看出,擬合的結果都不是很理想,說明吸附過程比較復雜,并不是由單一過程步驟所控制,而是幾個過程共同作用的結果。

表2 動力學邊界模型線性回歸擬合結果Table 2 Linear regression fitting results with dynamic boundary models
2.4 離子篩對鹽湖鹵水中 Li+的選擇性及其循環吸附性能
2.4.1 離子篩對鹵水中的主要金屬離子的分離特性
離子篩對各金屬離子分離性能通常用分配比D(式(9))和分離系數 β(式(10))來表示。分配比大小反映溶質在兩相中的遷移能力及分離效能,而分離系數表示某一分離流程將兩種不同物質分離的程度,反映兩組分分離的難易程度。

式中:D為某金屬離子的分配系數,L/g;C0為吸附前溶液中金屬離子的濃度,mg/L;V為溶液的體積,L;m為離子篩質量,g;Ce為吸附后溶液中金屬離子的濃度,mg/L;DM1和 DM2分別是金屬離子 M1和 M2的分配系數。
將一定量的離子篩置于適量的鹽湖老鹵鹵水中于60 ℃下吸附16 h后,然后測定鹵水吸附前后各主要成分的含量(見表3),在本研究中,主要考察Li+、Mg2+、K+和 Na+等主要金屬離子的分配比及 Li+對其他離子的分離系數,實驗結果分別如表4和5所列。

表3 老鹵鹵水吸附前后各主要成分含量的變化Table 3 Content changes of main ingredients in brine before and after adsorption

表4 離子篩對鹵水中各主要金屬離子的分配系數Table 4 Distribution coefficients of ion-sieve for main metal ions in brine (mL/g)
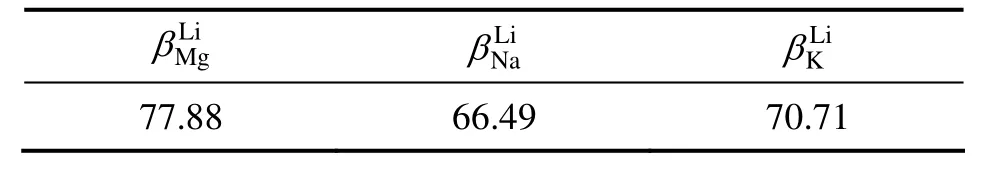
表5 鹵水中Li+對其他主要金屬離子的分離系數Table 5 Separation coefficients of Li+ to other main metal ions in brine
從表4中可以看出DLi>>DNa>DK>DMg,即離子篩對各金屬離子吸附的優先順序為 Li+、Na+、K+、Mg2+。同時從表5可知,Li+對 Mg2+、K+和 Na+的分離系數都遠遠大于 1,表明離子篩對 Li+與 Mg2+、K+和 Na+有較好的分離性能,對 Li+有較好的特定選擇性。
2.4.2 離子篩在鹵水中的循環吸附性能
稱取一定量的離子篩前軀體不斷進行酸洗—吸附—洗脫—吸附的循環吸附實驗,考察離子篩的循環吸附性能。酸洗洗脫控制條件:酸洗溫度70 ℃,攪拌速率500 r/min,酸洗時間24 h,鹽酸濃度0.5 mol/L,液固比(質量比)400:1。鹵水吸附實驗控制條件:吸附溫度60 ℃,吸附時間16 h,液固比(質量比)350:1,攪拌速率500 r/min。

圖9 離子篩吸附/解吸量隨循環次數的變化Fig.9 Change of quantity of adsorption/desorption of ion-sieve with cycle times
圖9所示為離子篩的吸附量/解吸量隨循環次數的變化。從圖9可以看出,第1次循環時離子篩的解吸量非常高,每克離子篩釋放出67.37 mg Li+。這是因為第1次循環酸洗洗脫時使用的離子篩為實驗固相法制備的離子篩前驅體,其理論含鋰量為68.13 mg/g。同時還可看出,第 1次循環時離子篩的吸附容量只有18.37 mg/g,遠低于第 1次循環洗脫步驟時的 67.37 mg/g,但離子篩的吸附容量還是比較穩定的,經8次循環吸附實驗后,吸附容量僅從 18.37 mg/g降低到16.39 mg/g,且第2次循環以后離子篩的解吸量與吸附量基本持平。這表明離子篩具有比較優異的循環吸附性能,但是離子篩實際的吸附容量小于其理論吸附容量的1/3,離子篩始終未達到飽和吸附狀態,這可能是因為離子篩在四面體間隙位的能壘低于八面體間隙位的能壘,吸附鋰時比較容易在四面體間隙位發生鋰的嵌入/脫嵌反應,而在八面體間隙位不發生或者很難發生鋰的嵌入/脫嵌反應。
3 結論
1)通過兩步固相法制備了鋰離子篩前軀體Li1.6Mn1.6O4,然后用一定濃度HCl溶液對前軀體進行洗脫,從而獲得了對Li+有特定吸附作用的一種新型離子篩 MnO2·0.5H2O,且其基本骨架與前軀體的差異不大。
2)一般情況下,溶液pH值的升高有利于離子篩對Li+的吸附,堿性越強,其吸附容量越大,但在較強的堿性溶液中離子篩的溶損也相應增加。
3)MnO2·0.5H2O對 Li+的吸附動力學遵循偽二級動力學方程,其擬合相關系數達0.998以上,表明離子篩對Li+的吸附為化學吸附過程。
4)離子篩對不同濃度含 Li+溶液的吸附過程與Langmuir吸附等溫方程的擬合比較好,相關系數達0.993以上,從而可知離子篩對Li+的吸附為單層吸附。
5)根據偽二級動力學方程式作出了ln k2—T?1的線性擬合圖,再通過求其斜率,并結合阿累尼烏斯公式計算出吸附過程的活化能為 26.71 kJ/mol。離子篩對 Li+吸附過程的控制步驟并不由單一過程決定,而是幾個過程共同作用的結果。
6)離子篩對Li+與Mg2+、K+和Na+具有較好的分離性能,對Li+有較好的特定選擇性。同時第2次循環以后,離子篩的解吸量與吸附量基本持平,且吸附容量隨循環次數的增加衰減比較緩慢,離子篩具有較好的循環吸附性能。
[1]CHEN C H, LIU J, STOLL M E, HENRIKSENA G, VISSERSA D R, AMINEA K.Aluminium-doped lithium nickel cobalt oxide electrodes for high-power lithium-ion batteries[J].J Power Sources, 2004, 128: 278?285.
[2]NAZRI G A, PISIOIA O.Lithium batteries: Science and technology[M].Norwell: Kluwer Academic Publishers, 2003:113?114.
[3]李明慧, 鄭綿平.鋰資源的分布及其開發利用[J].科技導報,2003(12): 38?39.LI Ming-hui, ZHENG Mian-ping.Distribution and development of lithium resource[J].Science and Technology Review,2003(12): 38?39.
[4]封國富, 張 曉.世界鋰工業發展格局的變化和對中國鋰工業的影響和對策[J].稀有金屬, 2003, 27(1): 57?61.FENG Guo-fu, ZHANG Xiao.Variation in feature of world lithium industry and its influence on lithium industry in China[J].Chinese Journal of Rare Metals, 2003, 27(1): 57?61.
[5]HAMZAOUI A H, M’NIF A, HAMMI H, ROKBANI R.Contribution to the lithium recovery from brine[J].Desalination,2003, 158: 221?224.
[6]綦鵬飛, 朱桂茹, 王 鐸, 高從堦.鋰離子篩的制備及其吸附性能研究[J].功能材料, 2010, 41(3): 856?861.QI Peng-fei, ZHU Gui-ru, WANG Duo, GAO Cong-jie.Preparation and adsorption properties of lithium ion sieve[J].Journal of Functional Materials, 2010, 41(3): 856?861.
[7]董殿權, 吳延方, 劉維娜.溶膠?凝膠法制備尖晶石型鋰離子篩[J].青島科技大學學報: 自然科學版, 2007, 28(z1): 11?13.DONG Dian-quan, WU Yan-fang, LIU Wei-na.Sol-gel synthesis of lithium ion sieve with spinel structure[J].Journal of Qingdao University of Science and Technology: Natural Science Edition,2007, 28(z1): 11?13.
[8]蒙麗麗, 韋 華, 李士霞, 文衍宣.尖晶石型錳酸鋰鋰離子篩的合成研究[J].無機鹽工業, 2009, 41(3): 37?39.MENG Li-li, WEI Hua, LI Shi-xia, WEN Yan-xuan.Synthesis of spinel lithium manganate as lithium ion sieve[J]. Inorganic Chemicals Industry, 2009, 41(3): 37?39.
[9]王 祿, 馬 偉, 韓 梅, 孟長功.高效鋰離子篩吸附劑MnO2·0.5H2O 的軟化學合成及吸附性能研究[J].化學學報,2007, 65(12): 1135?1139.WANG Lu, MA Wei, HAN Mei, MENG Chang-gong.Soft chemical synthesis and adsorption properties of MnO2·0.5H2O, a high performance ion sieve for lithium[J].Acta Chimica Sinica,2007, 65(12): 1135?1139.
[10]張克力, 孫聚堂, 袁良杰.無機合成化學[M].武漢: 武漢大學出版社, 2004: 127?128.ZHANG Ke-li, SUN Ju-tang, YUAN Liang-jie.Inorganic synthesis chemistry[M].Wuhan: Wuhan University Press, 2004:127?128.
[11]CHITRAKAR R, KANOH H, MIYAI Y, OOI K.Recovery of lithium from seawater using manganese oxide adsorbent(H1.6Mn1.6O4)derived from Li1.6Mn1.6O4[J].Industrial and Engineering Chemistry Research, 2001, 40(9): 2054?2058.
[12]張碧泉.MnO2的離子交換行為及其離子篩法提取鋰[J].應用化學, 1998, 15(5): 98?100.ZHANG Bi-quan.Ionic-exchange behaviour of MnO2and selective adsorption of lithium ions by MnO2ionic sieve[J].Chinese Journal of Applied Chemistry, 1998, 15(5): 98?100.
[13]ZHOU Li-min, WANG Yi-ping, LIU Zhi-rong, HUANG Qun-wu.Characteristics of equilibrium, kinetics studies for adsorption of Hg(Ⅱ), Cu(Ⅱ), and Ni(Ⅱ)ions by thiourea-modified magnetic chitosan microspheres[J].Hazardous Materials, 2009, 161(2):995?1002.
[14]BARKAT M, NIBOU D, CHEGROUCHE S, MELLAH A.Kinetics and thermodynamics studies of chromium(Ⅵ)ions adsorption onto activated carbon from aqueous solutions[J].Chemical Engineering and Processing, 2009, 48(1): 38?47.
[15]BENHAMMOU A, YAACOUBI A, NIBOU L, TANOUTI B.Adsorption of metal ions onto moroccan stevensite: Kinetic and isotherm studies[J].Colloid and Interface Science, 2005, 282(2):320?326.
[16]LANGMUIR I.The adsorption of gases on plane surfaces of glass, mica and platinum[J].Journal of the American Chemical Society, 1918, 40(9): 1361?1403.
[17]WANG Lu, MENG Chang-gong, HAN Mei, MA Wei.Lithium uptake in fixed-pH solution by ion sieves[J].Colloid and Interface Science, 2008, 325(1): 31?40.
[18]傅獻彩, 沈文霞, 姚天楊.物理化學[M].北京: 高等教育出版社, 1999: 236?237.FU Xian-cai, SHEN Wen-xia, YAO Tian-yang.Physical chemistry[M].Beijing: Higher Education Press, 1999: 236?237.
[19]李 響, 魏榮卿, 劉曉寧, 方 碩.新型弱堿性陰離子交換樹脂對 Cr(Ⅵ)的吸附性能[J].環境科學與技術, 2008, 31(10):9?12.LI Xiang, WEI Rong-qing, LIU Xiao-ning, FANG Shuo.Adsorption properties of a new weakly basic ion-exchange resin for Cr(Ⅵ)[J].Environmental Science and Technology, 2008,31(10): 9?12.
[20]李朝麗, 周立祥.黃棕壤不同粒級組分對鎘的吸附動力學與熱力學研究[J].環境科學, 2008,29(5): 1406?1411.LI Zhao-li, ZHOU Li-xiang.Kinetics and thermodynamics of Cd(Ⅱ)adsorption onto particle-sized fractions of yellow-brown soil[J].Environmental Science, 2008, 29(5): 1406?1411.
[21]唐嘉英, 李 鑫, 應漢杰.離子交換樹脂吸附TP5的熱力學和動力學研究[J].南京工業大學學報: 自然科學版, 2006, 28(5):79?83.TANG Jia-ying, LI Xin, YING Han-jie.Kinetics and thermodynamics for ion exchange of TP5 on NH1-resin[J].Journal of Nanjing University of Technology: Natural Science Edition, 2006, 28(5): 79?83.

